Contents
- 0.1 美国乙型肝炎病毒感染的预防:免疫实践咨询委员会的建议
- 0.2 Prevention of Hepatitis B Virus Infection in the United States: Recommendations of the Advisory Committee on Immunization Practices
- 1 总结
- 2 介绍
- 3 新的或更新的建议
- 4 方法
- 5 HBV背景
- 6 预防HBV感染
- 7 建议
- 8 未来方向
- 8.0.0.1 方框1.本报告中使用的缩略语
- 8.0.0.2 图1.乙型肝炎病毒感染的发生率—美国国家法定传染病监测系统,1980-2015 年
- 8.0.0.3 方框2.在美国消除HBV传播的策略*
- 8.0.0.4 表1.乙型肝炎病毒感染检测结果的典型解释
- 8.0.0.5 图2.急性乙型肝炎病毒感染恢复
- 8.0.0.6 框注3.按国家分列的慢性乙型肝炎病毒感染流行率*
- 8.0.0.7 表2.乙型肝炎疫苗的推荐剂量,按组别和疫苗类型分列
- 8.0.0.8 表3.按婴儿出生体重和母体HBsAg状态划分的婴儿乙型肝炎疫苗接种时间表
- 8.0.0.9 表4.儿童、青少年和成人的乙型肝炎疫苗接种时间表
- 8.0.0.10 框注4.建议接种乙型肝炎疫苗的人士
- 8.0.0.11 表5.医护人员职业性经皮或粘膜暴露于血液或体液后对医护人员进行暴露后管理,由医护人员进行HepB疫苗接种和反应状态
- 8.0.0.12 图3.对既往接种过完整的≥3剂HepB疫苗系列但未进行疫苗接种后血清学检测的医护人员进行暴露前评估*
- 8.0.0.13 框注5.对过去接种过疫苗的医护人员(HCP)进行抗乙型肝炎检测
- 8.0.0.14 表6.非职业性经皮或黏膜暴露于血液或体液后的暴露后管理
- 8.0.0.15 框注6.建议在接种疫苗前接受血清学检测的人*
- 8.0.0.16 框注7.建议在完成一系列乙肝疫苗接种后接受疫苗接种后血清学检测*的人
- 8.0.1 引用
美国乙型肝炎病毒感染的预防:免疫实践咨询委员会的建议
Prevention of Hepatitis B Virus Infection in the United States: Recommendations of the Advisory Committee on Immunization Practices
莎拉·席利,医学博士1;克劳迪娅·韦洛齐(ClaudiaVellozzi),医学博士1;亚瑟·雷因戈尔德,医学博士2;亚伦·哈里斯,医学博士1;佩尼娜·哈伯(PeninaHaber),公共卫生硕士3;约翰·沃德,医学博士1;NoeleP.Nelson,医学博士1 (查看作者单位)
本页内容
介绍
方法
建议
未来方向
总结
乙型肝炎病毒(HBV)通过血液或性接触传播。慢性乙型肝炎病毒感染者患肝硬化和肝癌的风险增加,需要医疗护理。本报告更新并总结了免疫实践咨询委员会(ACIP)和CDC之前发表的关于预防美国HBV感染的建议。ACIP建议对所有孕妇进行乙型肝炎表面抗原(HBsAg)检测,对HBsAg阳性孕妇进行乙型肝炎病毒脱氧核糖核酸(HBV DNA)检测;HBV感染妇女出生后12小时内所生的婴儿接种乙肝疫苗和乙型肝炎免疫球蛋白(HBIG),然后完成疫苗系列和疫苗接种后血清学检测;在出生后24小时内接种通用乙型肝炎疫苗,然后完成疫苗系列接种;以及以前未接种过疫苗的<19岁儿童和青少年的疫苗接种。ACIP建议对有HBV感染风险的成年人进行疫苗接种,包括在高比例有HBV感染危险因素的环境中对成年人进行普遍疫苗接种,以及在不承认特定危险因素的情况下对要求HBV防护的成年人进行疫苗接种。这些建议还为CDC提供了职业暴露和其他暴露后暴露后预防的指导。本报告还简要总结了先前发表的美国肝病研究协会关于母体抗病毒治疗以减少围产期HBV传播的指南。
介绍
乙型肝炎病毒(HBV)通过经皮(即皮肤穿刺)或黏膜(即直接接触粘膜)暴露于感染性血液或体液传播。HBV具有高度传染性,可在没有肉眼可见血液的情况下传播(1,2),并在环境表面上存活至少7天(3)。慢性感染者(例如,急性感染后血清中持续存在乙型肝炎表面抗原[HBsAg]的人)是HBV传播的主要宿主(4)。
本报告总结并整合了免疫实践咨询委员会(ACIP)和CDC先前发表的建议。它还包含对美国预防HBV感染建议的更新。提供了常用缩略语列表(框1)。
新的或更新的建议
以下建议是新增或更新的:
对于体重≥2000克的医学上稳定的婴儿,在出生后24小时内普遍接种乙型肝炎疫苗;
HBsAg阳性孕妇乙型肝炎病毒脱氧核糖核酸(HBV DNA)检测;
对母亲的HBsAg状态无限期未知的婴儿进行疫苗接种后血清学检测(例如,当父母或有合法监护权的人在婴儿出生后不久秘密交出婴儿时);
对初始疫苗系列无反应的HBsAg阳性妇女所生婴儿进行单剂再接种;
慢性肝病患者(包括但不限于丙型肝炎病毒、肝硬化、脂肪肝、酒精性肝病、自身免疫性肝炎、丙氨酸转氨酶[ALT]或天冬氨酸转氨酶[AST]水平大于正常上限两倍的人接种疫苗;和
删除将出生剂量推迟到出院后的允许性语言。
本报告还简要总结了之前发表的美国肝病研究协会(AASLD)关于母体抗病毒治疗以减少围产期HBV传播的指南(5)。美国传染病学会(InfectiousDiseasesSocietyofAmerica,IDSA)关于免疫功能低下宿主疫苗接种的建议详见其他专题(6)。
方法
ACIP的肝炎工作组由来自学术医学(儿科、家庭医学、内科、传染病、职业健康和预防医学专家)、联邦和州公共卫生机构以及医学会的专业人员组成。工作组在总结本文所载的预防乙型肝炎病毒感染的建议时,考虑了现有已发表的ACIP和CDC疫苗建议。
本报告更新并取代了之前发表的ACIP关于儿童和成人HepB疫苗接种的建议(7,8)。本报告纳入了ACIP和CDC之前发表的建议(9-11)。
AASLD的指南告知对HBV DNA升高的孕妇使用抗病毒治疗,以预防围产期HBV传播。监测数据来自国家法定传染病监测系统(NNDSS)(https://wwwn.cdc.gov/nndss/)。
根据2016年5月11日完成的文献检索结果,总结了为澄清建议提供信息的数据。使用两个检索词来确定有关透析患者最大剂量数和透析接种最小间隔的数据:“乙型肝炎疫苗*透析加强*”和“透析乙型肝炎疫苗*时间表”。审查了流行病学和疫苗覆盖率数据,以及关于弃婴和安全交出婴儿人数的公开数据。文献检索包括自2000年以来在世界范围内进行的临床试验和比较研究,并以英文发表。所有提供相关信息的研究均符合纳入条件。检索结果还得到了工作组主题专家确定的其他相关论文的补充。根据ACIP流程,预先确定,对现有建议的这些更新不需要对建议进行分级评估、制定和评估(GRADE)。
为了评估疫苗安全性,工作组检索了2005年至2015年的两个许可后不良事件监测系统:疫苗不良事件报告系统(VAERS)(https://vaers.hhs.gov)和疫苗安全数据链(VSD)(https://www.cdc.gov/vaccinesafety/ensuringsafety/monitoring/vsd)。VAERS是一个国家被动监测系统,VSD进行基于人群的疫苗安全性研究。VAERS可以生成疫苗安全性假设,但不能评估因果关系,并且受到一些限制,包括报告偏倚和数据质量不一致(12,13)。VSD可用于评估因医学文献综述、向VAERS报告、免疫计划的变化或新疫苗的引入而产生的假设(14)。
2016年2月至9月期间,工作组举行了五次电话会议。在2016年10月ACIP会议之前,工作组和ACIP成员还审查了该声明的草案并发表了意见。工作组讨论摘要已于2016年10月19日提交给ACIP。当时,ACIP成员投票批准了HepB疫苗建议声明草案,包括建议在出生后24小时内为体重≥2,000克的医学稳定的婴儿普遍接种HepB疫苗。2017年1月,工作组召开了一次电话会议,审查了HBsAg阳性妇女所生婴儿单剂再接种的经济分析结果。该分析的结果已于2017年2月22日提交给ACIP。建议未使用GRADE进行评估,但使用专家意见来制定建议。当时,ACIP成员投票批准了HBsAg阳性妇女所生婴儿(无论出生体重如何)单剂再接种的语言。在CDC随后的审查过程中,对ACIP声明进行了修改,以更新和澄清报告中的措辞。
HBV背景
流行病学
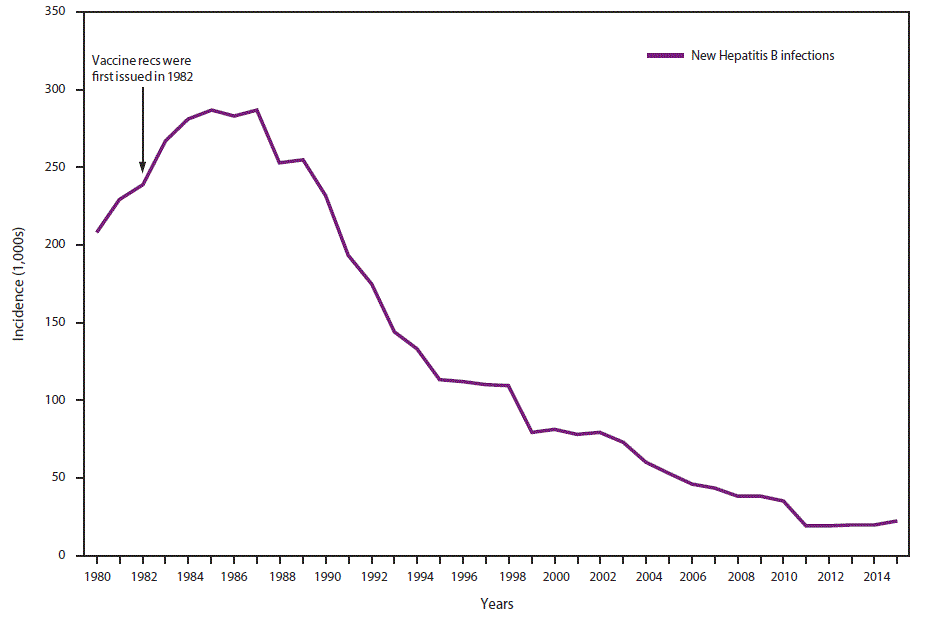
2015年,CDC共报告了3,370例急性HBV感染病例。据信,急性病例的实际数量是任何一年报告病例数的6.5倍。据估计,2015年有21,900例HBV新发病例,这些病例是由于考虑了确定不足和报告不足的情况(4)。自首次发布乙肝疫苗接种建议以来,报告的急性乙型肝炎病毒感染率下降了88.5%,从1982年的每10万人9.6例下降到2015年的每10万人1.1例(15),尽管急性乙型肝炎感染率在2010-2015年期间保持相当稳定(4)(图1)。2015年发病率最高的是30-39岁人群(每100,000人中有2.6人)。2015年,≤19岁人群的发病率最低(每10万人0.02例),这可能是常规婴儿疫苗接种的结果。虽然男性急性HBV感染的发生率高于女性,但差距已经缩小;2015年,男性的发病率约为女性的1.6倍(每10万人中分别为1.3例和0.8例)(4)。在2009-2013年期间,三个州(肯塔基州,田纳西州和西弗吉尼亚州)的急性HBV感染合并发病率增加了114%,并且与注射吸毒的增加有关[16]。
根据全国卫生调查数据,估计美国约有850,000人感染HBV(患病率)(17,18)。根据移民到美国的国家的数据和人口普查数据进行的研究表明,慢性乙型肝炎的总患病率可能高达220万人(19),这表明基于全国健康调查的估计可能是保守的。外国出生的人约占美国新报告的慢性感染的95%(20);在外国出生的人中,慢性HBV感染的患病率约为3.5%(19),而美国大多数慢性HBV感染者是亚洲/太平洋岛民。
消除乙型肝炎病毒的策略
1991年,美国通过了一项婴儿普遍接种乙肝疫苗的策略(21)。在随后的30年中,一项消除HBV传播的综合战略不断发展,包括:1)对所有孕妇进行HBsAg常规检测,并对HBsAg阳性母亲所生的婴儿进行预防,2)从出生开始对婴儿进行普遍疫苗接种,3)对以前未接种疫苗的儿童和青少年进行常规疫苗接种,以及4)对有HBV感染风险的成年人进行疫苗接种(7-11,第21-26页)。预防围产期传播依赖于对所有孕妇进行HBsAg检测,并对受感染母亲所生的婴儿进行及时预防(乙肝疫苗和乙型肝炎免疫球蛋白[HBIG])。从出生开始,所有婴儿就普遍接种乙肝疫苗,这为产前未发现的HBsAg阳性母亲所生的婴儿提供了重要的保障和预防感染(例如,在母亲未接受检测或发生检测、解释或转录错误的情况下)。建议为以前未接种过疫苗的儿童和青少年接种疫苗,并为有HBV感染风险的成年人接种疫苗(例如,通过性或经皮暴露以及前往某些国家的国际旅行者),以防止HBV在围产期环境之外传播(框2)。
乙型肝炎病毒预防策略已在美国成功实施,但挑战依然存在。大约88%的商业保险妇女和84%的医疗补助登记妇女在怀孕期间接受了HBsAg检测(27)。在一项针对北加州大型卫生系统的研究中,93%的HBsAg阳性孕妇接受了HBV DNA检测(28)。大多数(94.9%)受感染妇女所生的婴儿在出生后12小时内接受推荐的预防治疗(29)。通用乙肝疫苗出生剂量覆盖率(定义为在出生后3天内接种1剂疫苗)为71.1%(30),比2003-2005年期间的50.1%有所增加,此前ACIP建议出院前出生剂量(31),但低于2020年健康人85%的目标(32)。19-35个月和13-17岁儿童的乙肝疫苗覆盖率(≥3剂)分别为90.5%(30)和91.4%(33)。成人的疫苗覆盖率(≥3剂)较低:报告慢性肝病的成年人为27.4%;自1995年以来,在美国境外前往欧洲、日本、澳大利亚、新西兰或加拿大以外的国家的成年人中,这一比例为31.6%;在19-59岁的成人糖尿病患者中为24.4%,在≥60岁的成人糖尿病患者中为12.6%(34)。在医护人员中,≥3剂覆盖率为64.7%,比1992年《针刺安全与预防法》实施后不久的51%有所增加(35),但远低于2020年健康人群90%的目标(32,34)。
本报告中进一步减少HBV传播的新策略包括对HBsAg阳性孕妇进行HBV DNA检测,以识别感染风险最大的婴儿,并指导母体抗病毒治疗的使用[36,37]。已发表的证据表明,孕期母体抗病毒治疗可进一步减少围产期HBV传播;因此,当母体HBV DNA>200,000IU/mL时,AASLD建议进行抗病毒治疗 (5,38,39)。
病毒描述和传播
HBV是一种40-42nm包膜病毒,归类于 Hepadnaviridae 家族。HBV包含一个环状、部分双链DNA基因组,长度为3.2kb。易感人群接触后,病毒通过血液进入肝脏。肝脏是HBV复制的主要部位(40–43)。
HBV分为两个独立的系统:血清学亚型和基因型。最初根据HBsAg的异质性描述了9种血清学亚型:adrq+、adrq–、ayr、ayw1、ayw2、ayw3、ayw4、adw2和adw4(44,45)。已经描述了十种HBV基因型,命名为A-J。HBV血清型和基因型因地域而异。感染或接种一种基因型通常可对所有基因型产生免疫力(7,44,46,47)。
HBV具有高度传染性,可在没有可见血液的情况下传播(22),并且在环境表面保持传染性至少7天(2,3)。所有乙型肝炎抗原阳性者都具有传染性,但乙型肝炎病毒DNA升高或乙型肝炎e抗原(HBeAg)的乙型肝炎抗原(HBeAg)是乙型肝炎病毒的一种蛋白质,在血液中循环,是传染性的标志物,传染性最强。隐匿性HBV感染者(即HBsAg检测呈阴性但HBV DNA可检测到的人)也可能传播感染(48)。
HBV通过经皮、黏膜或非完整皮肤暴露于感染性血液或体液传播。乙型肝炎病毒在血液中的浓度最高,经皮暴露是一种有效的传播方式。精液和阴道分泌物具有传染性,唾液、眼泪和胆汁中也可检测到HBV。脑脊液、滑液、胸腔积液、腹膜液、心包积液和羊水也被认为具有潜在传染性。尿液、粪便、呕吐物、鼻咽冲洗液、痰液和汗液不是有效的传播媒介,除非它们含有少量传染性HBV,否则它们含有血液。在母乳中发现的HBsAg也不太可能导致传播,因此HBV感染不是母乳喂养的禁忌证(2,7,22)。
在成人中,HBV主要通过经皮血液暴露(例如注射吸毒)和性接触传播。乙型肝炎病毒通过异性恋者和男男性行为者(MSM)之间的性接触有效传播。异性恋者中性传播的危险因素包括与受感染的伴侣发生无保护的性行为、与多个伴侣发生无保护的性行为以及另一种性传播感染(STI)病史。与男男性行为者性传播相关的危险因素包括有多个性伴侣、另一种性传播感染史和。传播可能通过人际接触(例如,共用牙刷或剃须刀、接触皮肤病变的渗出物或接触HBsAg污染的表面)以及学校、托儿所和发育障碍者设施等环境中传播。由于献血者筛查和病毒灭活程序,通过输血或血液制品传播HBV的情况很少见。其他可能的感染源包括受污染的医疗或牙科器械、不安全的注射、针刺伤、器官移植和透析(49)。
临床特征和自然病程
HBV感染的临床表现从无症状感染到暴发性肝炎不等。从暴露到血清ALT水平异常发作的平均潜伏期为60天(范围:40-90天),从暴露到黄疸发作的平均潜伏期为90天(范围:60-150天)(8,42,43)。新获得HBV感染的婴儿、<5岁儿童和免疫抑制成人通常无症状,而30%-50%的年龄较大的儿童、青少年和成人有症状[7,8,44,50]。出现时,体征和症状包括恶心、呕吐、腹痛、发热、尿色深、粪便颜色改变、肝肿大、脾肿大和黄疸。不适和厌食可能在黄疸之前1-2周出现。暴发性HBV感染并不常见(<1%),但通常会导致死亡或肝衰竭,需要肝移植。也可能出现疾病的肝外表现(例如皮疹、关节痛和关节炎)[51]。报告急性乙型肝炎病毒感染病例的死亡率为<1.5%,其中≥55岁成年人的死亡率最高。由于大量感染者无症状,因此没有报告,因此所有HBV感染者的总体死亡率可能较低(8)。
80%-90%的婴儿期感染者、30%的6岁前感染者以及<1%-12%的年龄较大的儿童或成人感染者发生慢性感染(7,52-54)。在免疫功能正常的成人中,大约95%的原发性感染是自限性的,病毒会从血液中消除,并且通常对再感染具有免疫力。慢性感染在免疫抑制者(例如血液透析患者和人类免疫缺陷病毒[HIV]感染者)(54,55)和糖尿病患者(54)中更常见。慢性HBV感染可导致肝硬化、肝癌、肝衰竭和死亡。大约25%的儿童期慢性感染者和15%的儿童期后慢性感染者会过早死于肝硬化或肝癌(8,56-58)。
慢性HBV感染分为四个阶段:免疫耐受期、免疫活性期、免疫非活性期和再激活期。慢性感染者不一定以线性方式经历这些阶段。处于免疫耐受期的人没有或只有轻微的肝脏炎症或纤维化;大多数慢性感染的儿童将一直处于免疫耐受阶段,直到儿童晚期或青春期。免疫活性期的特征是活跃的免疫反应导致肝脏炎症,伴或不伴纤维化。长时间处于免疫活跃期的人患肝硬化和肝细胞癌的风险很高。处于免疫非活跃期的人肝脏炎症和纤维化有所改善。与免疫非活动期相比,处于免疫非活动期的人进展为肝细胞癌的风险较低。处于再激活期的人有活动性肝脏炎症,伴或不伴纤维化(44,59–61)。免疫抑制治疗或HCV治疗可能发生HBV再激活(62)。
急性HBV感染尚无特异性治疗方法;支持性治疗是治疗的主要手段。儿童和成人慢性HBV感染的管理指南,包括疾病监测和抗病毒治疗(5)。对于可能对治疗有反应且肝脏相关发病风险高的慢性HBV感染患者,通常应开始抗病毒治疗[5]。对于HBV DNA水平为>200,000IU/mL的HBsAg阳性孕妇,建议进行母体抗病毒治疗,以减少围产期传播(5)。
在乙型肝炎病毒高度流行的地区,乙型肝炎病毒经常在围产期从感染乙型肝炎病毒的孕妇传播给新生儿。大多数围产期HBV传播病例发生在分娩期间,极少数情况下是宫内传播(63)。HBV传播可能发生在生殖细胞系中,因为已在精子、卵母细胞和胚胎中检测到该病毒。现有数据不支持HBV DNA低的HBV感染孕妇需要剖宫产[63]。在广泛使用暴露后预防之前,HBsAg阳性妇女所生婴儿感染HBV的比例在HBeAg阴性母亲所生婴儿中约为30%,在HBeAg阳性母亲所生婴儿中为85%。在出生时进行暴露后预防,包括乙肝疫苗和血红蛋白,然后完成乙肝疫苗系列,0.7%-1.1%的婴儿发生感染(28,29,64);尽管接种了乙肝疫苗和乙型肝炎疫苗,但病毒载量高的母亲所生的婴儿感染风险最大(29)。未接种疫苗的婴儿和儿童也有从受感染的家庭和其他接触者那里横向传播的风险。
血清学标志物的解释
HBV感染的血清学标志物包括HBsAg、HBsAg抗体(抗HB)、乙型肝炎核心抗原免疫球蛋白M类(IgM)抗体(IgM抗HBc)和免疫球蛋白G类(IgG)抗HBc(IgG抗HBc)(49,65,66)。在感染的不同阶段至少存在一种血清学标志物。HBV DNA是病毒载量的量度,反映了病毒复制(49)(表1)。乙型肝炎e抗原(HBeAg)可在急性或慢性HBV感染者中检测到;HBeAg的存在与病毒复制和高传染性相关;HBeAg抗体(抗-HBe)与复制病毒的丢失相关,但也可能发生HBeAg阳性恢复(7)。
确诊的HBsAg阳性结果表明当前HBV感染,无论是急性还是慢性。所有HBsAg阳性者都具有传染性。如果HBsAg持续>6个月,则不太可能自发清除,并且认为感染是慢性的。在感染者中检测到HBsAg之前,可以检测到HBV DNA。当存在HBV DNA仍检测不到HBsAg时,就会发生隐匿感染(66–68)。短暂的HBsAg阳性可在接种疫苗后18天内发生(血液透析患者可达52天),临床意义不大(69)。
在急性HBV感染中,抗HBc(最初同时存在IgM和IgG)在HBsAg出现后1-2周出现(49)(图2)。抗HBc的IgM通常在6个月内检测不到,而抗HBc的IgG占主导地位,并且可在很长一段时间内保持可检测到,通常是终生的(65,66)。存在抗HBc的IgM提示急性感染,而抗HBc的IgG提示既往感染(65,66)。在HBV感染恢复者中,HBsAg从血液中消除,抗HBs通常在3-4个月内发生。抗HB的存在通常表明对HBV感染具有免疫力(8)。在HBIG接种后4-6个月内也可以检测到抗HB抗体(10)。从自然HBV感染中恢复的人通常同时具有抗HBs和抗HBc阳性,而对HepB疫苗有反应的人仅对抗HBs呈阳性。每年约有0.5%-2%的慢性感染者自发清除HBsAg;这些患者中的大多数会出现抗HBs(8)。
在某些人中,抗HBc是唯一检测到的血清学标志物。HBV感染后,在已康复但抗HBs水平减弱的人中可检测到孤立的抗HBc阳性;在HBV感染患病率高的人群中,孤立的抗HBc可能提示既往感染伴抗HB缺失。一些孤立性抗HBc阳性的慢性感染者有循环HBsAg,实验室检测无法检测到。在<10%的分离抗HBc患者中检测到HBV DNA(70,71),尽管可检测到HBV DNA的存在可能会波动(72)。这些人不太可能传播感染,除非他们是大量暴露源的情况,例如输血(8,73)。HBsAg阴性和抗HBc阳性者在化疗或免疫抑制治疗期间可能会出现感染再激活,并再次出现HBsAg(49)。突变型HBV菌株感染可导致HBsAg、总抗HBc、抗HBs和HBV DNA实验室检测呈阳性,抗HBcIgM呈阴性。
≤24月龄儿童围产期HBV感染通常无症状,但可发生暴发性肝炎;如果符合时机标准,HBsAg试验阳性、HBeAg试验阳性或可检测到的HBV DNA可被视为HBV感染母亲所生婴儿围产期HBV的实验室证据[74]。HBsAg阳性母亲所生且未感染的婴儿可能在出生后长达24个月内因被动获得的母体抗体而检测到抗HBc抗体(7)。
有HBV感染风险的成年人
2015年,CDC收到了3,370例急性HBV感染监测病例报告。在2,207例有风险信息的病例报告中,1,151例(52.2%)表示在发病前6周至6个月内没有HBV风险,其余病例表明至少有一个危险因素。注射吸毒和多个性伴侣是HBV传播的最常见来源(4)。
注射吸毒。在1,657例新报告的HBV病例中,有30.3%报告了注射吸毒,其中包括有关注射吸毒的信息(4)。自2009年以来,居住在非城市地区的30-39岁非西班牙裔白人的急性HBV感染有所增加,他们报告注射吸毒是一个危险因素(16)。在各种环境中,3.5%-20.0%(中点估计:11.8%)的注射吸毒者(PWID)中发现了慢性HBV感染(75%),22.6%的PWID有既往感染的证据(75)。在三个州(肯塔基州、田纳西州和西弗吉尼亚州),报告注射吸毒的HBV病例比例显著增加,从2006-2009年的53%增加到2010-2013年的75%(p<0.001,卡方)(16)。
性(异性恋和男男性行为者)暴露。在有HBV感染病例报告并提供有关性接触信息的人中,26.4%报告有两个或两个以上的性伴侣,3.3%报告与HBV感染者发生性接触,11.8%的男性报告与另一名男性发生性关系(4)。多达10%-40%在性传播感染诊所寻求治疗的成年人有当前或过去感染HBV的证据。在患有急性HBV感染的成年人中,39%的人在感染HBV之前接受了性传播感染的筛查或寻求治疗(76)。
家庭联系人。据估计,与其他慢性乙型肝炎病毒感染者同住的人中,有45%的人有既往乙型肝炎感染的血清学证据,16%的人有当前感染的证据(CDC,未发表的数据,2017年。在普遍接种婴儿疫苗之前,在家庭或大家庭环境中与慢性HBV感染者一起生活的未接种疫苗的儿童感染风险最大(67,77,78)。
长期护理机构中的发育障碍者。在住宅和非住宅设施中,发育障碍者历来慢性乙型肝炎病毒感染率高达20%。自这些地区实施常规乙肝疫苗接种以来,感染率已大幅下降(79-82)。
惩教设施。监狱囚犯中慢性HBV感染的患病率(1.0%-3.7%)高于一般人群(83,84),反映出进入有HBV感染风险的惩教设施(例如,注射吸毒和多个性伴侣史)的人数过多。
有职业暴露于乙型肝炎病毒风险的人群。在广泛实施乙肝疫苗接种之前,乙型肝炎病毒感染被认为是HCP的常见职业风险(85,86)。从1983年到2010年,HCP的常规HepB疫苗接种和标准预防措施的使用使HCP中的HBV感染率下降了98%(10)。职业安全与健康管理局要求雇主向所有有职业风险的员工提供乙肝疫苗接种,并在暴露后进行暴露后预防(10,87)。
血液透析患者。自从透析中心开始接种乙肝疫苗和采取额外的乙型肝炎感染控制预防措施以来,血液透析患者中HBV感染的发生率下降了约95%(88,89)。自1995年以来,年发病率一直稳定,HBsAg血清阳性率保持在1%(90)。<1%的急性HBV监测病例报告了透析,并向CDC报告了信息[4]。
丙型肝炎病毒感染者。2006-2012年,阿巴拉契亚四个州(肯塔基州、田纳西州、弗吉尼亚州和西弗吉尼亚州)报告的HCV病例数在≤30岁的人群中增加了364%,注射吸毒是最常见的报告危险因素(91)。丙型肝炎病毒感染的增加与阿巴拉契亚州农村社区年轻人乙型肝炎感染的增加同时发生。
慢性肝病患者。慢性肝病(例如肝硬化、脂肪肝、酒精性肝病和自身免疫性肝炎)患者发生HBV感染的风险不会增加,除非他们经皮或黏膜暴露于血液或体液。然而,并发慢性HBV感染可能会增加这些人患进行性慢性肝病的风险[92]。
前往乙型肝炎病毒流行国家的旅行者。前往乙型肝炎病毒感染高度或中度流行国家的短期旅行者(框注3)通常只有通过在医疗或救灾活动中接触血液、接受涉及肠外接触的医疗护理、性活动或吸毒才有感染风险。据报道,在前往该病流行国家的长期旅行者中,每月发病率为每10万名旅行者25-420例(93)。
艾滋病毒感染者。大约10%的HIV阳性者合并感染HBV(94-97)。在6%-14%的HIV阳性者中发现了慢性HBV感染,包括9%-17%的MSM和7%-10%的PWID(98)。合并感染者的肝硬化率和肝脏相关死亡率增加(99)。
糖尿病患者。与非糖尿病成人相比,成人糖尿病患者既往或现在感染HBV的患病率高出60%,患急性HBV的几率高出2倍。与辅助血糖监测相关的HBV感染反复暴发强调了该人群的持续风险(100-102)。数据还表明,与非糖尿病患者相比,急性感染HBV的糖尿病患者的病死率可能更高(9)。
预防HBV感染
乙型肝炎疫苗和乙型肝炎免疫球蛋白
乙肝疫苗接种是乙肝病毒预防工作的主要手段;HBIG通常用作HBsAg阳性母亲所生婴儿的乙肝疫苗的辅助手段,以及某些其他暴露后预防情况。第一批HepB疫苗由血浆来源的HBsAg组成。到1980年代后期,含有通过生化和生物物理分离技术纯化的酵母衍生HBsAg的重组HepB疫苗取代了美国的血浆衍生疫苗(64,103,104)。在美国推荐使用的HepB疫苗的配方中含有10-40 μg HBsAg蛋白/mL,并且不含硫柳汞作为防腐剂(105)。血红细胞增多蛋白可以增强保护作用,直到对疫苗接种产生反应。对于那些对乙肝疫苗接种没有反应的人,单独注射HBIG是HBV暴露后的主要保护手段。HBIG提供被动获得的抗HBs和临时保护(即3-6个月)。被动获得性抗HBs可在HBIG接种后4-6个月内检测到(10)。
乙肝疫苗可作为单一抗原制剂使用,也可与其他疫苗联合使用。在美国推荐使用的两种单抗原疫苗,Engerix-B(葛兰素史克生物制品公司,Rixensart,比利时)和RecombivaxHB(默克公司,新泽西州怀特豪斯站),用于从出生开始的人接种疫苗。在这两种联合疫苗中,Pediarix(葛兰素史克生物制品公司,Rixensart,比利时)用于6周-6岁人群的疫苗接种,含有重组HBsAg,白喉和破伤风类毒素以及无细胞百日咳吸附剂,灭活脊髓灰质炎病毒和Twinrix(葛兰素史克生物制品公司,Rixensart,比利时)用于≥18岁人群的疫苗接种,含有重组HBsAg和灭活甲型肝炎病毒(表2)。Comvax(Merck&Co.,Inc.,WhitehouseStation,NewJersey)以前用于6周-15个月大的人接种疫苗,含有重组HBsAg和嗜血杆菌b结合疫苗,自2015年1月1日起无法直接从默克公司购买。Comvax的停产与任何产品安全或制造问题无关。铝盐通常用作佐剂,以增强接种疫苗者的免疫反应。
两种HBIG产品已获准在美国使用:HepaGamB(CangeneCorporation,加拿大温尼伯)和Nabi-HB(BiotestPharmaceuticalsCorporation,佛罗里达州博卡拉顿)。HBIG是由具有高浓度抗HBs的供体血浆制备的。源血浆检测呈阴性,可检测HIV、HBV和HCV的证据。甲型肝炎病毒和细小病毒B19的研究性核酸检测也对源血浆的混合样本进行。制造过程包含两个步骤来灭活最终产品中的病毒:溶剂和洗涤剂步骤使包膜病毒失活,病毒过滤步骤根据病毒的大小去除病毒。在美国获准使用的HBIG产品不含防腐剂,仅供一次性使用(106)。
疫苗诱导的血清保护
抗-HBs的存在通常表明对HBV感染具有免疫力。免疫功能正常的儿童和成人在接受完整的HepB疫苗系列接种后1-2个月,疫苗诱导的抗HBs水平为≥10 mIU/mL,则被认为是血清保护者,并被视为疫苗应答者(107)。疫苗诱导的血清保护被认为是临床保护的替代物。接种疫苗后,抗乙型肝炎水平会随着时间的推移而减弱,这在一定程度上与接种疫苗的年龄有关。在<1岁时接种疫苗的人中,约有16%的人在接种疫苗后18年内抗体水平为≥10 mIU/mL,而在≥1岁时接种疫苗的人中,这一比例为74%(10)。然而,最初对完整的3剂HepB疫苗系列有反应的人,后来被发现患有抗HBs<10 mIU/mL的人仍然受到保护。大多数(88%)在儿童或成人接种乙肝疫苗30年后接受挑战剂量的乙肝疫苗后,抗体反应为≥10 mIU/mL,表明对HBV感染具有持续免疫力(108)。来自这项研究和其他研究的数据表明,在最初对HepB疫苗有反应的免疫功能正常者中,对急性症状和慢性HBV感染的保护作用持续30年或更长时间(108-110)。
3剂HepB疫苗系列在大约95%的健康婴儿中产生保护性抗体反应(抗HBs≥10 mIU/mL)(出生体重较低的婴儿反应较低)(64)和>90%的<40岁健康成年人(111,112)。在健康婴儿中,25%和63%的婴儿在第一剂和第二剂后分别达到抗HBs水平≥10 mIU/mL。在<40岁的健康成人中,30%-55%和75%在第一剂和第二剂后分别达到抗HBs水平≥10 mIU/mL(7,8,64)。体重<2000克的婴儿和老年人的疫苗反应降低。其他因素(例如吸烟、肥胖、衰老、慢性疾病、吸毒、糖尿病、男性、遗传因素和免疫抑制)导致对疫苗的反应降低(113-116)。尽管免疫功能低下人群的免疫原性较低,但在暴露于HBV之前达到并维持血清保护性抗体水平的人具有高水平的保护作用(8)。
出生剂量。出生剂量的乙肝疫苗可作为暴露后预防,以预防乙型肝炎感染母亲所生婴儿的围产期乙型肝炎感染。虽然需要暴露后预防的婴儿应通过母体HBsAg检测来识别,但对所有婴儿(即使没有HBIG)给予出生剂量,可以防止由于缺乏母体HBsAg检测或未能报告检测结果而未在产前发现的HBsAg阳性母亲所生婴儿的围产期传播。单独接种乙肝疫苗或乙肝免疫球蛋白在预防围产期HBV传播方面的有效性分别为75%和71%;它们的综合疗效为94%(29,52,117)。出生剂量还为围产期后有家庭暴露风险的婴儿提供保护(29,64)。
疫苗接种对98%的健康足月儿产生血清保护作用。出生体重<2000克(64)的婴儿的疫苗反应较低。一项针对低出生体重儿的研究表明,与出生后3天内相比,在1个月大时开始接种疫苗时,更多的婴儿达到血清保护性抗HBs水平(96%vs.68%,p<0.02)(118)。婴儿的疫苗反应不会因母体HBsAg状态或HBIG接种而有明显差异[64]。
青少年。大约95%的青少年在接种HepB疫苗后获得血清保护(7)。对于11-15岁的人,在0个月和4个月或0和6个月时使用2剂量压缩方案接种的成人(10 μg)剂量的RecombivaxHB产生的血清保护比例几乎与在0、1和6个月时以3剂量方案接种的5 μg标准方案获得的血清保护比例相当(99.2%对98.3%)(119,120).缺乏关于青少年在两剂方案中长期抗体持久性或保护的数据。
成年人。在<40岁的健康成年人中,接种完整系列疫苗可使>90%的人群具有血清保护作用。反应随着年龄的增长而降低,75%的60岁人群实现了血清保护(8)。
糖尿病。一项评估糖尿病患者乙肝疫苗反应的研究综述显示,糖尿病患儿的血清保护率为93.9%,而非糖尿病患儿的血清保护率为100%(112,121)。
在成人中,88.2%的糖尿病患者与93.6%的非糖尿病患者相比,实现了血清保护(112)。在血液透析/慢性肾病患者中,糖尿病患者的中位保护比例为60.1%,而非糖尿病患者的中位比例为75.1%(112)。
免疫功能低下的情况。免疫功能低下的儿童和成人(例如,造血干细胞移植受者、接受化疗的患者和HIV感染者)对HepB疫苗的体液反应降低(122,123)。改良接种方案,包括将标准抗原剂量加倍或给予额外剂量,可能会提高反应率。然而,关于对这些替代疫苗接种方案的反应的数据有限(6)。
疫苗安全性
在许可前试验中,HepB疫苗接种后的不良事件最常见的是注射部位反应和轻度全身反应(106)。上市后数据中常见的轻度不良事件包括疼痛(3%-29%)、红斑(3%)、肿胀(3%)、发烧(1%-6%)和头痛(3%)(124)。乙肝疫苗接种者的全身性过敏反应发生率估计为每百万剂疫苗1.1例(125)。2011年,医学研究所得出结论,证据令人信服地支持乙肝疫苗与酵母菌敏感人群的过敏反应之间存在因果关系,并且证据不足以接受或拒绝乙肝疫苗与几种神经系统,慢性和自身免疫性疾病之间的因果关系(126)。
在早期执照后监测期间,科学文献中描述了HepB疫苗接种后的几种不良事件,包括吉兰-巴利综合征(GBS)、慢性疲劳综合征、视神经炎、多发性硬化症和糖尿病;然而,多项研究表明,接种乙肝疫苗与这些疾病之间没有关联(126-129)。此外,没有证据表明类风湿性关节炎(130)、贝尔麻痹(131)、自身免疫性甲状腺疾病(132)、儿童溶血性贫血(133)、全身性过敏反应(134)、视神经炎(135)、格林-巴利综合征(136)、突发性感音神经性听力损失(137)或其他慢性疾病与接受HepB疫苗之间存在因果关系。
在2005-2015年期间,共有20,231份所有年龄段的HepB疫苗接种后不良事件报告提交给VAERS。大多数美国主要报告(20,231人中的15,787人,78%)在同一次就诊时接种了HepB疫苗和其他疫苗。其中,被归类为严重(即,如果报告了以下一项或多项:死亡、危及生命的疾病、住院或延长现有住院时间,或永久性残疾)†为16.7%,包括402例死亡,其中388例为6周-23个月的婴儿(138例)。联合接种疫苗最常报告的不良事件是发热(23%)、注射部位红斑(11%)和呕吐(10%)(138)。在4,444例单抗原HepB报告中,6.5%被归类为严重,包括43例死亡,其中27例为≤4周龄婴儿。单抗原HepB疫苗最常报告的不良事件是恶心/头晕(8%)和发烧/头痛(7%)。
疫苗接种时间表
疫苗接种计划是根据免疫原性数据确定的,对于婴儿和儿童,需要将乙肝疫苗纳入统一的免疫计划(表3和表4)。初次疫苗接种通常包括按0个月、1个月和6个月的时间表进行三次肌肉注射(表4)。对于使用成人制剂的11-15岁的人,RecombivaxHB可在0个月和4-6个月时以2剂方案接种。Pediarix在2、4和6个月大时接种;它不用于出生剂量。Twinrix可在旅行前或任何其他潜在暴露前以加速时间表在0、7和21-30天接种,然后在12个月时接种。成人血液透析患者的HepB疫苗接种包括以0、1和6个月的方案接种的高剂量(40 μg)RecombivaxHB或以0、1、2和6个月的方案接种的高剂量(40 μg)Engerix-B(106)。
替代疫苗接种方案(例如,0、1和4个月或0、2和4个月)已被证明可产生与0、1和6个月方案相似的剂量特异性和最终血清保护率。增加前2剂之间的间隔对免疫原性或最终抗体浓度几乎没有影响(139–141)。第三剂赋予最高水平的血清保护并提供长期保护(142)。最后2剂之间的间隔时间越长(例如,11个月)会导致最终抗体水平升高(142),但可能会增加对疫苗接种反应延迟的人感染HBV的风险。较高的几何平均滴度与可测量的抗HB持续时间越长有关。
对再接种的反应
使用挑战剂量的HepB疫苗可用于通过产生记忆删除反应来确定疫苗诱导的免疫记忆的存在。术语“加强剂量”已用于指在初次疫苗接种系列后接种的一剂乙肝疫苗,以提供针对重大感染(即感染导致血清学检测结果呈HBV阳性和/或具有临床意义的疾病)的快速保护性免疫。在1岁之前接种疫苗并在6-18年后发现抗HBs水平为<10 mIU/mL的人中,单次挑战剂量的HepB疫苗导致60%-97%的受测者的抗HBs水平为≥10 mIU/mL。在最初接种≥1岁疫苗的人中也发现了类似的结果(10)。攻击剂量后反应≥10 mIU/mL的免疫功能正常者被认为受到保护,无论随后抗HBs的下降如何(10,109)。
一项研究发现,在出生时未感染且对初级疫苗系列无反应的HBsAg阳性妇女所生的婴儿中,所有婴儿在接受3剂额外剂量后都出现了抗HBs的血清保护水平(143)。没有数据表明,接种6剂疫苗后没有可检测到抗体的儿童可以从额外剂量中受益。
预防围产期HBV传播的母体抗病毒治疗
抗病毒治疗(即拉米夫定、替比夫定和替诺福韦)已被研究作为一种干预措施,以减少HBV DNA水平高(例如,平均HBV DNA水平为7.6log10IU/mL)孕妇的围产期HBV传播(144)。母体抗病毒治疗在妊娠28-32周开始,作为分娩后不久给婴儿接种HepB疫苗和HBIG的辅助手段,与围产期HBV传播率显著降低有关(5)。拉米夫定和替比夫定的使用受到病毒耐药性和突变的限制。替诺福韦与耐药性无关,是首选药物(5)。现有数据支持替诺福韦在妊娠期间的安全性,但其使用可能与子宫内暴露婴儿的骨矿物质含量降低有关(5,39,63,144–146)。AASLD建议在母体HBV DNA>200,000IU/mL时进行抗病毒治疗以减少围产期HBV传播。母体治疗通常在出生时至产后3个月停止(5)。
成本效益考虑因素
针对围产期传播的乙型肝炎病毒预防策略被认为非常具有成本效益(即增加成本效益比<25,000美元)。目前对HBsAg阳性母亲所生的婴儿在出生后12小时内接种HepB疫苗和HBIG疫苗的策略,以及出院前普遍接种婴儿疫苗的策略,与单独出院前普遍接种婴儿HepB疫苗的策略相比,每质量调整生命年(QALY)可节省6,957美元的成本效益比(147)。CDC的美国围产期乙型肝炎预防计划(U.S.PerinatalHepatitisBPreventionProgram,https://www.cdc.gov/hepatitis/partners/perihepbcoord.htm)为HBsAg阳性妇女所生的婴儿提供病例管理服务,也已被证明可以减少感染,增加节省的QALYs,并具有成本效益地利用资源(148)。对HBsAg阳性孕妇进行HBV DNA检测,然后对HBV DNA高的妇女进行母体抗病毒预防的策略将额外花费300万美元,但将节省2,080个QALY并预防324例慢性HBV感染,因此将被认为是具有成本效益的,每节省一个QALY的增量成本效益比为1,583美元(36)。
还评估了围产期以外的乙型肝炎病毒预防策略的成本效益。为20-59岁的糖尿病成年人接种疫苗的费用为每节省QALY75,094美元;成本效益比随着疫苗接种年龄的增加而增加(149)。在先前接种过疫苗的当前HCP(包括正在接受培训的HCP)中,与不干预相比,暴露前抗HBs检测,然后重新接种疫苗和重新检测(如有必要,基于抗HBs水平)被认为不具有成本效益,第一年每QALY可节省3-400万美元的增量成本,10年内约为800,000美元(150)。
建议
本节包含预防乙型肝炎病毒感染的指南,包括ACIP对婴儿、儿童、青少年和成人的乙肝疫苗接种建议(框注4)以及CDC和ACIP对职业和非职业暴露后预防乙肝病毒的建议。
围产期HBV传播的预防
HBV感染孕妇的识别和管理
所有孕妇都应在每次妊娠的早期产前检查(例如,妊娠早期)进行HBsAg检测,即使她们之前接种过疫苗或接受过检测。对已知患有慢性乙型肝炎病毒的孕妇进行检测,可以证明怀孕期间获得的乙型肝炎表面抗原检测结果呈阳性,并有助于确保其婴儿被识别出来,以便及时进行预防。
o所有HBsAg阳性孕妇均应进行HBV DNA检测,以指导妊娠期母体抗病毒治疗预防围产期HBV传播(新推荐)。
o当母体HBV DNA>200,000IU/mL时,AASLD建议母体进行抗病毒治疗(新推荐)。
o所有HBsAg阳性孕妇都应转诊至其辖区的围产期乙型肝炎预防计划(PHBPP)进行病例管理,以确保其婴儿得到及时的预防和随访。应向计划分娩的医院或分娩机构以及照顾新生儿的医护人员提供表明孕妇乙肝表面抗原阳性状态的实验室报告原件副本。
o所有HBsAg阳性孕妇都应获得有关HBV的信息,其中讨论了抗病毒治疗的潜在用途、预防婴儿的重要性(出生后12小时内接种HepB疫苗和HBIG)、完成疫苗接种系列以及疫苗接种后血清学检测。
未进行产前检测的妇女、临床肝炎患者以及行为使她们面临HBV感染高风险的女性(例如,近期或当前使用注射吸毒者、过去6个月内有不止一个性伴侣或HBsAg阳性性伴侣、接受过STI评估或治疗)应在入院或分娩机构分娩时进行检测。
所有为孕妇提供HBsAg检测的实验室都应使用美国食品和药物管理局许可或批准的HBsAg检测,并应根据制造商的标签进行检测,包括使用许可的中和确认试验对最初反应性标本进行检测。当孕妇在入院分娩时接受HBsAg检测时,可以使用缩短的检测方案,并报告最初的反应性结果,以加快婴儿暴露后预防的实施。应鼓励商业实验室记录HBsAg检测妇女的妊娠状况,以帮助识别感染HBV的孕妇。
HBsAg阳性女性所生婴儿的管理
HBsAg阳性妇女所生的所有婴儿均应在出生后12小时内接种HepB疫苗和HBIG,在不同的注射部位(例如,分开的肢体)接种。出生剂量只能使用单抗原HepB疫苗(表3)。
对于妊娠期HBsAg检测结果不可用但存在其他提示母体HBV感染的证据(例如,存在HBV DNA、HBeAg阳性或已知患有慢性HBV的母亲)所生的婴儿,应像HBsAg阳性母亲所生一样进行管理(新推荐)。
对于HBsAg阳性母亲所生的婴儿,应按照推荐的时间表完成HepB疫苗系列接种。该系列的最后一剂不应在24周龄(164天)之前接种。虽然制造商的包装标签中没有标明,但Pediarix可用于HBsAg阳性母亲所生的≥6周龄婴儿,在接种出生剂量的单抗原HepB疫苗和HBIG后完成疫苗系列。
对于体重<2,000克的婴儿,出生剂量(即初始乙肝疫苗剂量)不应计入疫苗系列,因为乙肝疫苗在这些婴儿中的免疫原性可能会降低;当婴儿满1个月大时,应再接种3剂疫苗(共4剂)。该系列的最后一剂不应在24周龄(164天)之前接种。
抗HBs和HBsAg的疫苗接种后血清学检测应在9-12月龄完成疫苗接种系列后进行(通常在完成HepB疫苗系列后的下一次健康儿童访视时)。抗HBs检测应使用可检测抗HBs保护浓度(≥10 mIU/mL)的方法进行。不应在9个月大之前进行检测,以避免在出生时检测到HBIG的被动抗HBs,并最大限度地提高检测晚期HBV感染的可能性。不建议对婴儿进行抗HBc检测,因为在HBsAg阳性母亲所生的婴儿中可能会检测到被动获得性母体抗HBc,年龄不超过24个月。
o抗HBs水平≥10 mIU/mL的HBsAg阴性婴儿受到保护,无需进一步治疗。
o抗HBs<10 mIU/mL)的HBsAg阴性婴儿应重新接种单剂HepB疫苗,并在1-2个月后接受疫苗接种后血清学检测(新推荐)。单剂再接种后抗乙型肝炎仍<10 mIU/mL的婴儿应再接种两剂乙肝疫苗以完成第二剂系列接种,然后在最后一剂接种后1-2个月进行疫苗接种后血清学检测。
o根据临床情况或家庭偏好,抗HBs<10 mIU/mL)的HBsAg阴性婴儿可以改为重新接种第二剂完整的3剂系列疫苗,然后在最后一剂疫苗后1-2个月进行疫苗接种后血清学检测。
o现有数据并未表明,对于在接种两个完整的HepB疫苗系列后未达到抗HBs≥10 mIU/mL)的婴儿,接种额外的HepB疫苗剂量有益。
oHBsAg阳性婴儿应转诊进行适当的随访。
HBsAg阳性母亲所生并接受暴露后预防的婴儿可在出生后立即开始母乳喂养。
对于出生后转移到其他机构(例如,新生儿护理水平较高的医院)的婴儿,转移和接收机构的工作人员应就婴儿的HepB疫苗接种和HBIG接收状态进行沟通,以确保及时进行预防(新建议)。
HBsAg状态不明女性所生婴儿的管理
对于妊娠期HBsAg检测结果不可用但存在其他提示母体HBV感染的证据(例如,存在HBV DNA、HBeAg阳性或已知患有慢性HBV的母亲)所生的婴儿,应像HBsAg阳性母亲所生一样进行管理(新推荐)。婴儿应在出生后12小时内同时接种乙肝疫苗和乙型肝炎疫苗。
在没有HBsAg检测结果的情况下入院分娩的妇女应尽快抽血和检测。
虽然孕产妇HBsAg检测结果尚未公布,但出生体重≥2,000克的婴儿,HBsAg状态未知的妇女应在出生后12小时内接种第一剂HepB疫苗(不含HBIG)。出生剂量只能使用单抗原HepB疫苗(表3)。
o如果确定母亲为HBsAg阳性,婴儿应尽快接受HBIG,但不迟于7日龄,并且应按照HBsAg阳性母亲所生婴儿的推荐时间表完成疫苗接种系列。该系列的最后一剂不应在24周龄(164天)之前接种。如果确定母亲为HBsAg阴性,则应按照HBsAg阴性母亲所生婴儿的推荐时间表完成疫苗接种。该系列的最后一剂不应在24周龄(164天)之前接种。
由于疫苗对体重<2,000克的婴儿的免疫原性可能降低,如果母亲在出生后12小时内无法确定其HBsAg状态,则这些婴儿应同时接种单抗原HepB疫苗和HBIG,在不同的注射部位(例如,单独的肢体)接种。疫苗的出生剂量不应计入完成疫苗系列所需的3剂疫苗的一部分;应根据母亲的乙肝表面抗原检测结果,按照推荐的时间表再接种3剂疫苗(共4剂)。该系列的最后一剂不应在24周龄(164天)之前接种。
o如果无法确定母亲的HBsAg状态(例如,当父母或合法监护权人在婴儿出生后不久安全地秘密交出婴儿时),应根据HBsAg阳性母亲所生婴儿的推荐时间表完成疫苗接种系列(新推荐)。该系列的最后一剂不应在24周龄(164天)之前接种。这些婴儿应在9-12月龄时接受疫苗接种后血清学检测,必要时应再次接种疫苗(新推荐)。
抗HBs检测应使用可检测抗HBs保护浓度(≥10 mIU/mL)的方法进行。不应在9个月大之前进行检测,以避免在出生时检测到HBIG的被动抗HBs,并最大限度地提高检测晚期HBV感染的可能性。不建议对婴儿进行抗HBc检测,因为在HBsAg阳性母亲所生的婴儿中可能会检测到被动获得性母体抗HBc,年龄不超过24个月。
o抗HBs水平≥10 mIU/mL的HBsAg阴性婴儿受到保护,无需进一步治疗。
o抗HBs<10 mIU/mL)的HBsAg阴性婴儿应重新接种单剂HepB疫苗,并在1-2个月后接受疫苗接种后血清学检测(新推荐)。单剂再接种后抗乙型肝炎仍<10 mIU/mL的婴儿应再接种两剂乙肝疫苗以完成第二剂系列接种,然后在最后一剂接种后1-2个月进行疫苗接种后血清学检测。
o根据临床情况或家庭偏好,抗HBs<10 mIU/mL)的HBsAg阴性婴儿可以改为重新接种第二剂完整的3剂系列疫苗,然后在最后一剂疫苗后1-2个月进行疫苗接种后血清学检测。
o现有数据并未表明,对于在接种两个完整的HepB疫苗系列后未达到抗HBs≥10 mIU/mL)的婴儿,接种额外的HepB疫苗剂量有益。
oHBsAg阳性婴儿应转诊进行适当的随访。
HBsAg状态不明的母亲所生的婴儿可在出生后立即开始母乳喂养。
对于出生后转移到其他机构(例如,新生儿护理水平较高的医院)的婴儿,转移和接收机构的工作人员应就婴儿的HepB疫苗接种和HBIG接收状态进行沟通,以确保及时进行预防(新建议)。
推荐接种乙肝疫苗的人士
婴儿普遍接种疫苗
所有婴儿都应接种乙肝疫苗系列疫苗,作为推荐的儿童免疫计划的一部分,从出生开始作为安全网(框注4;表3)。
对于出生时体重≥2,000克且由HBsAg阴性母亲所生的所有医学稳定的婴儿,应在出生后24小时内接种第一剂疫苗(新建议)。出生剂量只能使用单抗原HepB疫苗。
体重<2,000克且由HBsAg阴性母亲所生的婴儿应将其第一剂疫苗推迟到出院时或1个月大时(即使体重仍为<2,000克)。对于这些婴儿,应将原始实验室报告的副本放在婴儿的病历中,表明母亲在怀孕期间是HBsAg阴性。出生时体重<2,000克的婴儿对1个月前接种的HepB疫苗的反应降低(118)。
对于出生后转移到其他机构(例如,新生儿护理水平较高的医院)的婴儿,转移和接收机构的工作人员应就婴儿的HepB疫苗接种和HBIG接收状态进行沟通,以确保及时进行预防(新建议)。
疫苗系列的最后一剂不应在24周龄(164天)之前接种。
在目前或以前儿童HBV感染率较高的人群中(例如,阿拉斯加原住民;太平洋岛民;以及来自亚洲、非洲和中度或高地方性感染率国家的移民家庭),第一剂乙肝疫苗应在出生时接种,最后一剂应在6-12个月大时接种。
儿童和青少年的疫苗接种
建议所有未接种疫苗的<19岁儿童和青少年接种乙肝疫苗(框注4)。
以前未接种过乙肝疫苗的儿童和青少年应在任何年龄常规接种疫苗(即建议儿童和青少年进行补种接种)(表4)。
成人疫苗接种
建议所有有HBV感染风险的未接种疫苗的成年人以及所有要求预防HBV感染的成年人接种乙肝疫苗。承认特定危险因素不应成为接种疫苗的必要条件(框注4)。
建议接种乙肝疫苗的成年人:
o有性暴露感染风险的人(例如,HBsAg阳性者的性伴侣、非一夫一妻制关系的性活跃者[例如,在过去6个月内有一个以上性伴侣的人]、寻求性传播感染评估或治疗的人,以及MSM)。
o有当前或近期注射吸毒史的人感染HBV的风险增加。美国农村社区年轻人中HBV发病率的增加与注射吸毒的增加有关。
o其他因经皮或黏膜暴露于血液而有感染风险的人(HBsAg阳性者的家庭接触者;发育障碍者设施的居民和工作人员;有合理预期接触血液或血液污染体液风险的卫生保健和公共安全人员,血液透析患者和透析前,腹膜透析和家庭透析患者;<60岁的糖尿病患者和糖尿病患者年龄≥60岁,由治疗临床医生自行决定)。
o其他(前往高水平或中等水平国家的国际旅行者[HBsAg患病率为≥2%][框3]地方性HBV感染者、HCV感染者、慢性肝病患者[包括但不限于肝硬化、脂肪肝、酒精性肝病、自身免疫性肝炎以及ALT或AST水平大于正常上限两倍的人][新推荐],艾滋病毒感染者、被监禁者、所有其他寻求保护免受乙肝病毒感染而未承认特定危险因素的人)。
孕妇疫苗接种
在妊娠期间被确定为有HBV感染风险的孕妇(例如,在过去6个月内有不止一个性伴侣、接受过STI评估或治疗、近期或当前注射吸毒,或有HBsAg阳性性伴侣)应接种疫苗。
对于妊娠期有乙型肝炎病毒感染风险的孕妇,应告知其预防乙型肝炎病毒感染的其他方法。
实施策略
分娩医院政策和程序
所有分娩医院和分娩设施都应实施政策和程序,确保识别乙型肝炎表面抗原阳性母亲所生的婴儿和乙型肝炎表面抗原状态不明的母亲所生的婴儿,开始对这些婴儿进行预防治疗,并在出生后24小时内对体重≥2000克的医学稳定婴儿进行常规分娩剂量。此类政策和程序应包括常规订单和电子病历提醒或提示。
预防围产期HBV感染的病例管理计划
各州和地方应制定病例管理计划,包括适当的政策、程序、法律和法规,以确保所有孕妇在每次怀孕期间都接受HBsAg检测,并确保HBsAg阳性的孕妇接受HBV DNA检测,以指导母体抗病毒治疗。HBsAg阳性女性和HBsAg状态未知的女性所生的婴儿也应接受病例管理。
为成人提供服务的设置
在高比例人群有乙肝病毒感染危险因素的环境中(例如,针对注射吸毒者服务的卫生保健机构、惩教设施、机构和发育障碍者的非寄宿日托设施),应假定所有成年人都有乙肝病毒感染的风险,如果他们以前没有完成疫苗接种,则应接种乙肝疫苗。
医护人员应执行常规命令,将乙肝疫苗作为未完成疫苗系列的成人常规服务的一部分,并将乙肝疫苗接种作为性传播感染和艾滋病毒/艾滋病评估和治疗的标准组成部分。
在可行的情况下,应在外展和其他向有HBV感染风险的人提供服务的环境中(例如,针头交换计划、HIV检测点、HIV预防计划和无家可归者收容所)提供乙肝疫苗接种。
在医疗环境中,医护人员应执行常规命令,以识别建议接种乙肝疫苗的成年人,并将疫苗接种作为常规服务的一部分。
暴露后预防
本节为在职业和非职业环境中通过明显、可识别的血液或含血体液暴露于乙型肝炎病毒的人提供管理建议。
与血液或体液接触过的伤口和皮肤部位应用肥皂和水清洗;粘膜应用水冲洗。使用防腐剂(例如2%-4%氯己定)进行伤口护理或通过进一步挤压伤口挤出液体尚未被证明可以降低HBV传播的风险;但是,使用防腐剂不是禁忌症。不建议在伤口内使用腐蚀性物质(例如漂白剂)或注射防腐剂或消毒剂。
职业设置
接种疫苗的医护人员
对于已接种疫苗的HCP(具有完整HepB疫苗系列的书面文件)以及随后记录的抗HBs≥10 mIU/mL),无需对源患者进行HBsAg检测。无论源患者的HBsAg状态如何,都不需要对HBV进行暴露后预防(表5)。表5卫生保健人员职业经皮或黏膜暴露于血液或体液后暴露后管理,按卫生保健人员划分乙肝疫苗接种和反应状态
对于已接种疫苗的医护人员(有完整乙肝疫苗系列的书面文件)之前没有进行过抗乙型肝炎检测,应对医护人员进行抗乙型肝炎检测,并且应在接触后尽快对源患者(如果已知)进行乙肝表面抗原检测。抗HBs检测应使用可检测抗HBs保护浓度(≥10 mIU/mL)的方法进行。源患者和医护人员应同时进行检测;在等待HCP抗HBs检测结果时不应延迟对源患者的检测,同样,在等待源患者的HBsAg结果时也不应延迟对HCP的检测(表5)。
o如果医护人员的抗乙型肝炎<10 mIU/mL,而源患者为乙型肝炎表面抗原阳性或乙型肝炎表面抗原状态未知,则医护人员应接种1剂乙型肝炎,并在暴露后尽快重新接种。HepB疫苗可与HBIG在单独的解剖注射部位(例如,单独的肢体)同时接种。然后,医护人员应根据疫苗接种时间表接种第二剂乙肝疫苗以完成第二剂乙肝疫苗(如果算上原来的系列,可能总共接种6剂)。因此,可以记录HCP的疫苗反应状态以备将来接触,抗HBs检测应在最后一次疫苗接种后1-2个月进行。
o如果医护人员的抗乙型肝炎<10 mIU/mL,而源患者为乙型肝炎表面抗原阴性,则医护人员应再接种一剂乙肝疫苗,然后在1-2个月后再次进行抗乙型肝炎检测。抗HB仍为<10 mIU/mL的HCP应再接种两剂(如果算上原始系列,可能总共接种6剂)。因此,可以记录HCP的疫苗反应状态以备将来接触,抗HBs检测应在最后一剂疫苗后1-2个月进行。
o如果HCP在暴露时具有抗HBs≥10 mIU/mL,则无论来源患者的HBsAg状态如何,都无需进行暴露后HBV管理。
对于接种了两剂完整的乙肝疫苗系列后接种抗乙型肝炎疫苗的医护人员<10 mIU/mL),应在暴露后尽快对源患者进行乙肝表面抗原检测。如果源患者为HBsAg阳性或HBsAg状态未知,则HCP应接受2剂HBIG(1,10)。第一剂应在暴露后尽快接种,第二剂应在1个月后接种。不建议之前已接种过两个乙肝疫苗系列的暴露的医护人员接种乙肝疫苗。如果源患者为HBsAg阴性,则不需要注射HBIG和HepB疫苗(表5)。
未接种疫苗的医护人员
对于未接种疫苗或未完全接种疫苗的医护人员,应在接触后尽快对源患者进行HBsAg检测。对未接种疫苗或未完全接种疫苗的HCP进行抗HBs检测是没有必要的,并且可能具有误导性,因为抗HBs≥10 mIU/mL作为疫苗诱导保护的相关性,仅针对已完成批准的疫苗接种系列的人确定(107)(表5)。
如源病人为乙肝表面抗原阳性或乙肝表面抗原状态不明,医护人员应在接触后尽快接种1剂乙型肝炎疫苗及1剂HBIG。HepB疫苗可与HBIG在单独的解剖注射部位(例如,单独的肢体)同时接种。医护人员应根据疫苗接种时间表完成乙肝疫苗系列。为了记录医护人员对未来暴露的疫苗反应状态,应在最后一剂疫苗后约1-2个月进行抗HBs检测。抗HBs检测应使用可检测抗HBs保护浓度(≥10 mIU/mL)的方法进行。由于接受HBIG的HCP的抗HBs检测应在不再检测到HBIG的抗HBs后(接种后6个月)进行,因此在这些情况下,可能需要将抗HBs检测推迟到最后一剂疫苗后1-2个月以上(表5)。
o接种初次疫苗系列后抗HBs≥10 mIU/mL的HCP被认为具有免疫力。免疫功能正常的人具有长期保护作用,不需要进一步的定期检测来评估抗HBs水平。
o在接受初级系列接种后,抗HBs<10 mIU/mL的HCP应重新接种疫苗。对于这些医护人员,在适当的时间内进行第二次完整系列接种,然后在最后一剂疫苗后1-2个月进行抗乙型肝炎检测,通常比在每剂额外接种疫苗后进行血清学检测更实用。因此,可以记录HCP的疫苗反应状态以备将来接触,抗HBs检测应在最后一次疫苗接种后1-2个月进行。
如源病人为乙肝表面抗原阴性,医护人员应按接种计划完成乙肝疫苗系列接种。因此,可以记录HCP的疫苗反应状态以备将来暴露,抗HBs检测应在最后一剂疫苗后约1-2个月进行(表5)。
o接种初次疫苗系列后抗HBs≥10 mIU/mL的HCP被认为具有免疫力。免疫功能正常的人具有长期保护作用,不需要进一步的定期检测来评估抗HBs水平。
o在接受初级系列接种后,抗HBs<10 mIU/mL的HCP应重新接种疫苗。对于这些医护人员,在适当的时间内进行第二次完整系列接种,然后在最后一剂疫苗后1-2个月进行抗乙型肝炎检测,通常比在每剂额外接种疫苗后进行血清学检测更实用。因此,可以记录HCP的疫苗反应状态以备将来接触,抗HBs检测应在最后一次疫苗接种后1-2个月进行。
暴露式HCP的临床管理
患有抗HBs<10 mIU/mL(或未接种疫苗或未完全接种疫苗)并持续暴露于HBsAg阳性或HBsAg状态未知的源患者的HCP应在暴露后尽快接受HBV感染基线检测,并在大约6个月后进行随访检测。暴露后立即进行检测时应包括总抗HBc抗体,约6个月后的随访检测应包括HBsAg和总抗HBc抗体(表5)。
暴露于HBsAg阳性或HBsAg状态未知的源患者的HCP在随访期间无需采取特殊预防措施以防止继发传播;但是,他们应该避免捐献血液、血浆、器官、组织或精液(10)。暴露的HCP不需要改变性行为或避免怀孕(10)。如果暴露的HCP正在母乳喂养,则不需要停止母乳喂养(7,10)。无需修改暴露的HCP的患者护理责任,以防止仅因暴露于HBsAg阳性或HBsAg状态未知的源患者而传播给患者。
既往接种过疫苗的医护人员
提供者应仅接受注明日期的书面记录作为HepB疫苗接种的证据(151)。
越来越多的医护人员在儿童时期接受了常规的乙肝疫苗接种。不建议在常规婴儿或青少年接种乙肝疫苗后进行疫苗接种后血清学检测。由于疫苗诱导的抗乙型肝炎会随着时间的推移而减弱,因此在接种疫苗数年后对医护人员进行抗乙型肝炎检测可能无法区分疫苗无反应者与反应者。在录用或入学时对当前或过去的抗乙型肝炎结果进行暴露前评估,然后为含有抗乙型肝炎的医护人员接种一剂或多剂乙肝疫苗<10 mIU/mL,并在必要时重新检测抗乙型肝炎疫苗,有助于确保医护人员在接触含乙型肝炎的血液或体液时得到保护(框注5;图3)。
o无法提供3剂乙肝疫苗文件的医护人员应被视为未接种疫苗,并应完成疫苗接种系列。建议在接种第三剂疫苗后1-2个月进行抗HB的疫苗接种后血清学检测。在接种3剂HepB疫苗之前无意中接受过检测且抗HBs≥10 mIU/mL的HCP不应被视为免疫,因为抗HBs≥10 mIU/mL仅在检测遵循记录的3剂系列时才是已知的保护相关性。鼓励卫生保健机构尝试查找医护人员的疫苗记录,并在其州免疫信息系统中输入所有疫苗剂量。
非职业设置
HBsAg阳性来源
本节为在非职业环境中通过明显、可识别的血液或含血体液暴露于HBV的人提供管理建议(表6)。暴露者不需要在接种疫苗后仅根据暴露进行疫苗接种后血清学检测。
有完整乙肝疫苗系列的书面文件且未接受疫苗接种后检测的接触者应接种单剂乙肝疫苗。
正在接种疫苗但尚未完成疫苗系列的接触者应接种一剂HBIG并完成HepB疫苗系列(无需重新开始HepB疫苗系列)。HepB疫苗可与HBIG在单独的解剖注射部位(例如,单独的肢体)同时接种。
未接种疫苗的人士应在接触后尽快接种乙肝和乙肝疫苗(最好在24小时内)。乙肝疫苗可以与HBIG同时在单独的解剖注射部位(例如,单独的肢体)接种。关于暴露后暴露后预防有效的最大间隔的研究有限,但经皮暴露的间隔不太可能超过7天,性暴露的间隔不太可能超过14天。乙肝疫苗系列应根据疫苗接种计划完成。
HBsAg-未知来源
具有完整乙肝疫苗系列书面文件的暴露者不需要进一步治疗。
正在接种疫苗但未完全接种疫苗的接触者应完成乙肝疫苗系列(无需重新开始接种系列)。
未接种疫苗的暴露者应在接触后尽快接种第一剂乙肝疫苗系列,最好在24小时内接种。关于暴露后暴露后预防有效的最大间隔的研究有限,但经皮暴露的间隔不太可能超过7天,性暴露的间隔不太可能超过14天。疫苗系列应根据疫苗接种计划完成。
免疫管理问题
疫苗接种前检测
对因当前或既往感染而免疫HBV的人接种疫苗或接种乙肝疫苗不会增加不良事件的风险(8)。然而,在既往乙型肝炎病毒感染率较高的人群中,疫苗接种前检测可能会避免对已经具有免疫力的人进行疫苗接种,从而降低成本。疫苗接种前检测包括HBsAg、抗-HBs和抗-HBc检测。血清学检测不应成为易感人群接种疫苗的障碍,尤其是在难以接触的人群中。检测不是接种疫苗的必要条件,在无法检测的情况下,应继续为推荐人员接种疫苗。
第一剂乙肝疫苗通常应在采集血液进行血清学检测后立即接种。建议对以下人士进行疫苗接种前检测(框注6):
oHBsAg阳性者的家庭接触者、性接触者或共用针头接触者;
o艾滋病毒阳性者;
o病因不明的丙氨酸转氨酶(ALT)/天冬氨酸转氨酶(AST)升高者;
o血液透析患者(更多信息参见2001年CDC建议[88]);
o男男性行为者;和
o过去或现在的注射吸毒者。
HBV感染检测
还建议对以下人员进行HBV感染检测(包括HBsAg、抗HBs和抗HBc检测):
o出生在HBV高流行和中度流行国家的人(HBsAg患病率≥2%);
o美国出生的婴儿未接种疫苗,其父母出生在乙型肝炎病毒高流行国家(≥8%);
o需要免疫抑制治疗的人,包括化疗、与器官移植相关的免疫抑制以及风湿病或胃肠病的免疫抑制;和
o血液、血浆、器官、组织或精液的供体。
所有孕妇在每次妊娠期间都应接受HBsAg检测。HBsAg检测呈阳性的孕妇应进行HBV DNA检测。
疫苗接种后血清学检测
婴儿、儿童或成人常规接种疫苗后,无需进行血清学免疫检测。
建议以下人士在接种疫苗后进行抗乙型肝炎检测,其后续临床管理取决于对其免疫状况的了解(框注7):
oHBsAg阳性女性所生的婴儿和HBsAg状态未知的女性所生的婴儿(例如,出生后不久安全投降的婴儿)。疫苗接种后血清学检测应包括抗乙型肝炎和乙型肝炎表面抗原检测;
o有血液或体液暴露风险的医护人员和公共安全工作者;
o血液透析患者(以及其他可能需要门诊血液透析的人)、HIV感染者和其他免疫功能低下者(例如,造血干细胞移植受者或接受化疗的人),以确定是否需要再次接种疫苗和后续检测的类型;和
oHBsAg阳性者的性伴侣,以确定是否需要重新接种疫苗和其他预防HBV感染的方法。
应在接种最后一剂疫苗后1-2个月进行检测,使用可测定抗HBs保护浓度(≥10 mIU/mL)的方法。
o在接种初次疫苗系列后发现抗HBs浓度为≥10 mIU/mL的人被认为具有免疫力。
o免疫功能正常的人具有长期保护作用,不需要进一步的定期检测来评估抗HBs水平。
o免疫功能低下者可能需要每年进行一次检测,以评估抗HBs浓度(重新接种疫苗)。
o在接种初次疫苗系列后发现抗HBs浓度为<10 mIU/mL的人应重新接种疫苗。按照适当的时间表接种第二剂疫苗中的所有剂量,然后在最后一剂疫苗后1-2个月进行抗HBs检测,通常比接种一剂或多剂疫苗后的血清学检测更实用(HBsAg阳性母亲所生婴儿重新接种时除外)。
o再次接种后抗乙型肝炎保护浓度未达到的人应进行乙型肝炎表面抗原检测。
o如果HBsAg检测结果呈阳性,则应接受适当的管理,并应识别任何家庭、性接触者或共用针头的接触者并接种疫苗。建议对HBsAg阳性者的家庭接触者、性接触者或共用针头接触者进行疫苗接种前检测(包括抗HBc、HBsAg和抗HBs)以识别感染者;血清学检测不应成为疫苗接种的障碍,应在采集血液进行血清学检测后立即接种第一剂乙肝疫苗。
oHBsAg检测呈阴性的人应被视为HBV感染的易感者,应告知预防HBV感染的预防措施,以及针对任何已知或可能暴露于HBsAg阳性源的暴露后预防HBIG的必要性(10)。
在雇用或入学时,使用完整的HepB抗HB疫苗接种文件对HCP进行检测(即,对先前对HepB疫苗接种的反应进行暴露前评估),然后额外接种一剂或多剂针对HCP的抗HB疫苗<10 mIU/mL),有助于确保HCP在接触含HBV的血液或体液时得到保护。
抗HBs水平为≥10 mIU/mL通常被认为具有血清保护作用;然而,不同的检测具有不同的检测临界值,根据这些临界值,报告的抗HBs水平可能因所使用的检测而异。请参阅测试的包装说明书,以确定抗HBs抗体的实际/正确水平。
再接种
对于在婴儿、儿童、青少年或成人时期接种过疫苗的免疫状态正常的人,通常不建议再次接种(即加强剂量、激发剂量或完整系列疫苗的重新接种)。现有数据并未表明加强剂量的最大数量。当抗HBs为<10 mIU/mL时,建议对以下人群重新接种疫苗:
oHBsAg阳性母亲所生的婴儿。抗乙型肝炎<10 mIU/mL的HBsAg阴性婴儿应重新接种单剂HepB疫苗,并在1-2个月后重新检测。单剂再接种后抗乙型肝炎仍<10 mIU/mL的婴儿应按疫苗接种时间表再接种两剂乙肝疫苗,以完成第二批疫苗,然后在1-2个月后进行抗乙型肝炎检测。或者,这些婴儿可以重新接种第二剂3剂系列疫苗,并在最后一剂疫苗后1-2个月重新检测(HBsAg和抗HBs)。
o医护人员。完全接种抗乙型肝炎疫苗的医护人员<10 mIU/mL)应再接种一剂乙肝疫苗,然后在1-2个月后进行抗乙型肝炎检测。抗HB仍为<10 mIU/mL的HCP应完成第二批(通常总共6剂),然后在最后一次接种后1-2个月重复进行抗HBs检测。或者,对于最近接种抗HBs疫苗的HCP<10 mIU/mL,接受第二个完整系列(通常总共6剂),然后在最后一次接种后1-2个月进行抗HBs检测可能更实用。
o血液透析患者。对于在门诊中心接受治疗的血液透析患者,应通过年度抗HBs检测来评估是否需要加强剂量。当抗HBs水平降至<10 mIU/mL时,应给予加强剂量。不建议在加强剂量后1-2个月进行抗HBs检测以评估反应。
o其他免疫功能低下的人。对于其他免疫功能低下者(例如,HIV感染者、造血干细胞移植受者和接受化疗的人),尚未确定是否需要加强剂量。对于有持续暴露风险的人群,应考虑每年进行抗乙型肝炎检测和加强剂量。
中断的时间表和最短接种间隔
对于所有年龄段,当乙肝疫苗接种计划中断时,不需要重新启动疫苗系列。如果在第一次接种后中断系列,应尽快给予第二剂,并且第二剂和第三剂应间隔至少8周。如果仅延迟了第三剂,则应尽快接种。最后一剂疫苗必须在第二剂后至少8周接种,并应在第一剂后至少16周接种;第一剂和第二剂之间的最短间隔为4周。乙肝疫苗剂量不足或接种间隔短于推荐剂量后接受的剂量应使用正确的剂量或时间表重新接种。
在最短间隔或年龄前≤4天接种的疫苗剂量被认为是有效的。由于Twinrix独特的加速时间表,因此4天指南不适用于以0天、7天、21-30天和12个月的时间表接种该疫苗的前3剂(新推荐)。
在婴儿中,不建议在24周龄之前给予最后一剂。
其他免疫管理问题
当一个制造商生产的一剂或两剂HepB疫苗之后再接种另一制造商的剂量时,没有观察到免疫原性差异(8)。在可行的情况下,后续剂量应使用相同的疫苗;但是,如果使用不同品牌的剂量,则应认为该剂量有效,无需重复。
提供者应仅接受注明日期的记录作为乙肝疫苗接种的证据。
虽然如果找不到记录,不应推迟疫苗接种,但应通过联系以前的医疗保健提供者、审查州或地方免疫信息系统以及搜索个人持有的记录来尝试查找缺失的记录。如果无法在合理时间内找到记录,则应将这些人视为易感人群,并按照适合年龄的疫苗接种计划开始接种。抗HBs≥10 mIU/mL仅在遵循记录在案的完整系列病例时才具有保护作用的血清学相关性。
在所有情况下,即使可能无法确保完成系列疫苗接种,也应开始接种疫苗。
接种任何疫苗后发生的不良事件都应报告给VAERS。报告应在线、传真或邮寄提交给VAERS。有关VAERS的更多信息,请致电1-800-822-7967(免费)或在线https://vaers.hhs.gov.
未来方向
ACIP和CDC将审查这些建议,作为与HepB疫苗(包括其他含HepB疫苗的许可)、HepB疫苗不良事件相关的新流行病学或其他信息,并在实施这些建议中获得的经验。将根据需要制定经修订的建议。
通讯作者:SarahSchillie,疾病预防控制中心国家艾滋病毒/艾滋病、病毒性肝炎、性病和结核病预防中心病毒性肝炎科。电话:404-718-8608;电子邮件: Ggi1@cdc.gov.
1疾病预防控制中心国家艾滋病毒/艾滋病、病毒性肝炎、性病和结核病预防中心病毒性肝炎科;2加州大学伯克利分校公共卫生学院,加州伯克利;3美国疾病预防控制中心国家新兴和人畜共患传染病中心医疗质量促进司
关系披露:2016-2017年ACIP肝炎疫苗工作组成员希望披露,他们与商业产品制造商或与乙型肝炎(HepB)疫苗相关的商业服务供应商没有经济或竞争利益。内容将不包括对产品或研究用途产品的无标签使用的任何讨论,但以下情况除外:•乙型肝炎表面抗原(HBsAg)阳性母亲或HBsAg状态未知的母亲在收到出生剂量的单抗原HepB疫苗和乙型肝炎免疫球蛋白(HBIG)后完成疫苗系列;•注意最低限度的替代3剂疫苗接种时间表第一剂和第二剂之间的间隔为4周,第二剂和第三剂之间的间隔为8周,第一剂和第三剂之间的间隔为16周;•在某些情况下(例如,对于免疫功能低下的人)修改接种方案(例如,将标准剂量增加一倍并给予额外剂量);•妊娠期抗病毒治疗,预防围产期乙型肝炎病毒(HBV)传播。
方框1.本报告中使用的缩略语
AASLD美国肝病研究协会
ACIP免疫实践咨询委员会
anti-HBc 抗乙型肝炎核心抗原的抗体
anti-HBe 抗乙型肝炎e抗原的抗体
anti-HBs抗乙型肝炎表面抗原的抗体
HBeAg乙型肝炎e抗原
HBIG乙型肝炎免疫球蛋白
HBsAg乙型肝炎表面抗原
HBV乙型肝炎病毒
HBV DNA乙型肝炎病毒脱氧核糖核酸
HCP医护人员
HC丙型肝炎病毒
HepB乙型肝炎
HIV人类免疫缺陷病毒
IDSA美国传染病学会
IDU注射吸毒
IgM免疫球蛋白M
IgG免疫球蛋白G
MSM男男性行为者
NNDSS法定传染病监测系统
PHBPP中期乙型肝炎预防计划
PWID注射吸毒者
QALY质量调整生命年
STI性传播感染
VAERS疫苗不良事件报告系统
VSD安全数据链
图1.乙型肝炎病毒感染的发生率—美国国家法定传染病监测系统,1980-2015 年
方框2.在美国消除HBV传播的策略*
对所有孕妇进行HBsAg筛查
o对HBsAg阳性孕妇进行HBV DNA检测,当HBV DNA>200,000IU/mL时,建议母体进行抗病毒治疗以减少围产期传播
o预防(乙肝疫苗和乙型肝炎免疫球蛋白)HBsAg阳性所生婴儿†女人
从出生开始就为所有婴儿普遍接种疫苗§,¶作为未在产前发现乙型肝炎病毒感染母亲所生婴儿的保障措施
以前未接种疫苗的<19岁儿童的常规疫苗接种
为有HBV感染风险的成年人接种疫苗,包括那些在未承认特定危险因素的情况下要求预防HBV的成年人
*来源:MastEE、MargolisHS、FioreAE等。消除乙型肝炎病毒感染在美国传播的综合免疫策略:免疫实践咨询委员会(ACIP)的建议。第1部分:婴儿、儿童和青少年的免疫接种。MMWRRecommRep2005;54(编号。RR-16):1-31;MastEE、WeinbaumCM、FioreAE等。消除乙型肝炎病毒感染在美国传播的综合免疫策略:免疫实践咨询委员会(ACIP)的建议。第二部分:成人免疫接种。MMWRRecommRep2006;55(否。RR-16):1-33。
†HBsAg状态不明的女性所生婴儿的预防建议见表3。
§体重≥2,000克的医学稳定婴儿出生后24小时内。
¶有关体重<2,000克的婴儿的出生剂量建议,请参阅表3。
表1.乙型肝炎病毒感染检测结果的典型解释
| HBsAg | Total anti-HBc | IgM anti-HBc | Anti-HBs | HBV DNA | 解释 |
| – | – | – | – | – | 从未感染 |
| + | – | – | – | +或– | 早期急性感染;接种疫苗后短暂(最多18天) |
| + | + | + | – | + | 急性感染 |
| – | + | + | +或– | +或– | 急性消退感染 |
| – | + | – | + | – | 从既往感染中恢复并免疫 |
| + | + | – | – | + | 慢性感染 |
| – | + | – | – | +或– | 假阳性(即易感);既往感染;“低水平”慢性感染;或将抗HBc被动转移至HBsAg阳性母亲所生的婴儿 |
| – | – | – | + | – | 如果疫苗系列完成后抗HBs浓度为≥10 mIU/mL,则具有免疫力;乙型肝炎免疫球蛋白接种后的被动转移 |
缩写: –=负数;+=正数;抗-HBc=乙型肝炎核心抗原抗体;抗-HBs=乙型肝炎表面抗原抗体;HBsAg=乙型肝炎表面抗原;HBV DNA=乙型肝炎病毒脱氧核糖核酸;IgM=免疫球蛋白M类。
图2.急性乙型肝炎病毒感染恢复
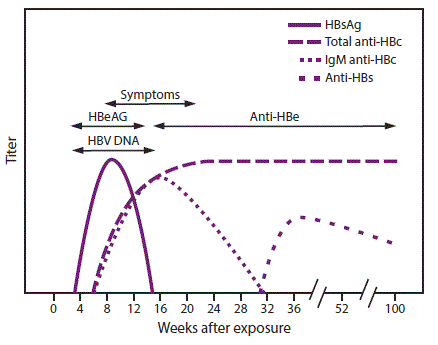
缩写:抗-HBc=乙型肝炎核心抗原抗体;抗-HBe=乙型肝炎e抗原抗体;抗-HBs=乙型肝炎表面抗原抗体;HBeAg=乙型肝炎e抗原;HBsAg=乙型肝炎表面抗原;HBV DNA=乙型肝炎病毒脱氧核糖核酸;IgM=免疫球蛋白M类。
框注3.按国家分列的慢性乙型肝炎病毒感染流行率*
高(患病率≥8%): 安哥拉、贝宁、布基纳法索、布隆迪、喀麦隆、中非共和国、刚果、科特迪瓦、吉布提、赤道几内亚、加蓬、冈比亚、加纳、几内亚、海地、基里巴斯、吉尔吉斯斯坦、老挝、利比里亚、马拉维、马里、毛里塔尼亚、蒙古、莫桑比克、纳米比亚、瑙鲁、尼日尔、尼日利亚、纽埃、巴布亚新几内亚、塞内加尔、塞拉利昂、所罗门群岛、索马里、南苏丹、苏丹、斯威士兰、多哥、汤加、乌干达、瓦努阿图、越南、也门和津巴布韦。
中度(患病率为5%–7.9%): 阿尔巴尼亚、不丹、佛得角、中国、刚果民主共和国、埃塞俄比亚、哈萨克斯坦、肯尼亚、马绍尔群岛、摩尔多瓦、阿曼、罗马尼亚、卢旺达、萨摩亚、南非、塔吉克斯坦、坦桑尼亚、泰国、突尼斯、图瓦卢、乌兹别克斯坦和赞比亚。
中低(患病率为2%–4.9%): 阿尔及利亚、阿塞拜疆、孟加拉国、白俄罗斯、伯利兹、文莱达鲁萨兰国、保加利亚、柬埔寨、哥伦比亚、塞浦路斯、多米尼加共和国、厄瓜多尔、厄立特里亚、密克罗尼西亚联邦、斐济、格鲁吉亚、意大利、牙买加、科索沃、利比亚、马达加斯加、缅甸、新西兰、巴基斯坦、帕劳、菲律宾、秘鲁、俄罗斯、沙特阿拉伯、新加坡、韩国、斯里兰卡、苏里南、叙利亚、塔希提岛和土耳其。
低(患病率为≤1.9%): 阿富汗、阿根廷、澳大利亚、奥地利、巴林、巴巴多斯、比利时、玻利维亚、波斯尼亚和黑塞哥维那、巴西、加拿大、智利、哥斯达黎加、克罗地亚、古巴、捷克共和国、丹麦、埃及、法国、德国、希腊、危地马拉、匈牙利、冰岛、印度、印度尼西亚、伊朗、伊拉克、爱尔兰、以色列、日本、约旦、科威特、黎巴嫩、立陶宛、马来西亚、墨西哥、摩洛哥、尼泊尔、荷兰、尼加拉瓜、挪威、巴勒斯坦、巴拿马、波兰、葡萄牙、卡塔尔、塞尔维亚、塞舌尔、斯洛伐克、斯洛文尼亚、西班牙、瑞典、瑞士、乌克兰、英国、阿拉伯联合酋长国、美利坚合众国和委内瑞拉。
暂无数据: 安道尔、安提瓜和巴布达、亚美尼亚、巴哈马、博茨瓦纳、乍得、科摩罗、库克群岛、多米尼克、萨尔瓦多、芬兰、格林纳达、几内亚比绍、圭亚那、洪都拉斯、拉脱维亚、莱索托、立陶宛、卢森堡、马其顿、马尔代夫、马耳他、毛里求斯、摩纳哥、黑山、朝鲜、巴拉圭、圣基茨和尼维斯、圣卢西亚、圣文森特和格林纳丁斯、圣马力诺、圣多美和普林西比、东帝汶、特立尼达和多巴哥、土库曼斯坦、和乌拉圭。
* 源:旅行者健康:与旅行有关的传染病。佐治亚州亚特兰大:美国卫生与公众服务部,CDC;2017.
表2.乙型肝炎疫苗的推荐剂量,按组别和疫苗类型分列
| 年龄组别(岁) | 单抗原疫苗 | 联合疫苗 | ||||||||
| Recombivax | Engerix | Pediarix* | Twinrix† | |||||||
| 剂量(μg) | 体积(mL) | 剂量(μg) | 体积(mL) | 剂量(μg) | 体积(mL) | 剂量(μg) | 体积(mL) | |||
| 出生–10 | 5 | 0.5 | 10 | 0.5 | 10* | 0.5 | 不适用 | 不适用 | ||
| 11–15 | 10§ | 1 | 不适用 | 不适用 | 不适用 | 不适用 | 不适用 | 不适用 | ||
| 11–19 | 5 | 0.5 | 10 | 0.5 | 不适用 | 不适用 | 不适用 | 不适用 | ||
| ≥20 | 10 | 1 | 20 | 1 | 不适用 | 不适用 | 20† | 1 | ||
| 血液透析患者和其他免疫功能低下的人 | ||||||||||
| <20 | 5 | 0.5 | 10 | 0.5 | 不适用 | 不适用 | 不适用 | 不适用 | ||
| ≥20 | 40 | 1 | 40 | 2 | 不适用 | 不适用 | 不适用 | 不适用 | ||
缩写:N/A=不适用。
*Pediarix被批准用于6周至6岁(7岁生日之前)的人。
†Twinrix被批准用于≥18岁的人群。
成人制剂按2剂方案接种。§
表3.按婴儿出生体重和母体HBsAg状态划分的婴儿乙型肝炎疫苗接种时间表
| 出生体重 | 母体HBsAg状态 | 单抗原疫苗 | 单抗原+复方疫苗 | ||
| 剂量 | 年龄 | 剂量 | 年龄 | ||
| ≥2,000克 | 阳性 | 1 | 出生(≤12小时) | 1 | 出生(≤12小时) |
| HBIG§ | 出生(≤12小时) | HBIG | 出生(≤12小时) | ||
| 2 | 1–2个月 | 2 | 2个月 | ||
| 3 | 6个月¶ | 3 | 4个月 | ||
| 4 | 6个月¶ | ||||
| 未知* | 1 | 出生(≤12小时) | 1 | 出生(≤12小时) | |
| 2 | 1–2个月 | 2 | 2个月 | ||
| 3 | 6个月¶ | 3 | 4个月 | ||
| 4 | 6个月¶ | ||||
| 阴性 | 1 | 出生(≤24小时) | 1 | 出生(≤24小时) | |
| 2 | 1–2个月 | 2 | 2个月 | ||
| 3 | 6–18个月¶ | 3 | 4个月 | ||
| 4 | 6个月¶ | ||||
| <2,000克 | 阳性 | 1 | 出生(≤12小时) | 1 | 出生(≤12小时) |
| HBIG | 出生(≤12小时) | HBIG | 出生(≤12小时) | ||
| 2 | 1个月 | 2 | 2个月 | ||
| 3 | 2–3个月 | 3 | 4个月 | ||
| 4 | 6个月¶ | 4 | 6个月¶ | ||
| 未知 | 1 | 出生(≤12小时) | 1 | 出生(≤12小时) | |
| HBIG | 出生(≤12小时) | HBIG | 出生(≤12小时) | ||
| 2 | 1个月 | 2 | 2个月 | ||
| 3 | 2–3个月 | 3 | 4个月 | ||
| 4 | 6个月¶ | 4 | 6个月¶ | ||
| 阴性 | 1 | 出院或年龄1个月 | 1 | 出院或年龄1个月 | |
| 2 | 2个月 | 2 | 2个月 | ||
| 3 | 6–18个月¶ | 3 | 4个月 | ||
| 4 | 6个月¶ | ||||
缩写:HBIG=乙型肝炎免疫球蛋白;HBsAg=乙型肝炎表面抗原。
*母亲入院分娩后应尽快抽血并检测乙型肝炎表面抗原;如果发现母亲是HBsAg阳性,婴儿应尽快接受HBIG,但不迟于7日龄。
†Pediarix不应在6周龄之前使用。
血红细胞瘤应在与疫苗分开的解剖部位接种。
疫苗系列的最后一剂不应在24周龄(164天)之前接种。§¶
表4.儿童、青少年和成人的乙型肝炎疫苗接种时间表
| 年龄组 | 时间表*(间隔表示从第一次接种开始的时间(以月为单位) |
| 儿童(1-10岁) | 0、1和6个月 |
| 0、1、2和12个月 | |
| 青少年(11-19岁) | 0、1和6个月 |
| 0、12和24个月 | |
| 0和4–6个月† | |
| 0、1、2和12个月 0、7天、21–30天、12个月§ | |
| 成人(≥20岁) | 0、1和6个月 |
| 0、1、2和12个月0、1、2和6个月 0、7天、21–30天、12个月¶§ |
*有关详细信息,请参阅包装说明书。对于所有年龄段,当乙肝疫苗接种计划中断时,不需要重新启动疫苗系列。如果在第一次接种后中断系列,应尽快给予第二剂,并且第二剂和第三剂应间隔至少8周。如果仅延迟了第三剂,则应尽快接种。最后一剂疫苗必须在第二剂后至少8周接种,并应在第一剂后至少16周接种;第一剂和第二剂之间的最短间隔为4周。乙型肝炎疫苗剂量不足或在短于推荐的接种间隔后接种的剂量应使用正确的剂量或时间表进行重新接种。在最短间隔或年龄前≤4天接种的疫苗剂量被认为是有效的。由于Twinrix独特的加速时间表,当以0天、7天、21-30天和12个月的时间表接种时,4天指南不适用于该疫苗的前三剂(新推荐)。
†Recombivax成人制剂(10μg)的2剂方案已获准用于11-15岁的青少年。当计划接受第二剂时,>15岁的青少年应改用3剂系列,第2剂和第3剂由儿科制剂组成,按适当的时间表接种。
Twinrix被批准用于≥18岁的人群,并可加速接种,剂量分别在0、7、21-30天和12个月接种。
对于成年血液透析患者,建议在0、1、2和6个月的方案中分两次1mL剂量(40μg)接种Engerix,共4剂。§¶
框注4.建议接种乙型肝炎疫苗的人士
•所有婴儿
•<19岁未接种疫苗的儿童
•有性接触感染风险的人
乙型肝炎表面抗原(HBsAg)阳性者的性伴侣
没有长期一夫一妻制关系的性活跃者(例如,在过去6个月内有不止一个性伴侣的人)
寻求性传播感染评估或治疗的人
男男性行为者
o经皮或粘膜暴露于血液有感染风险的人
当前或最近的注射吸毒者
乙肝表面抗原阳性者的家庭接触者
发育障碍者设施的居民和工作人员
有合理预期接触血液或血液污染体液风险的卫生保健和公共安全人员
血液透析患者和透析前患者、腹膜透析患者和家庭透析患者
19-59岁的糖尿病患者;年龄≥60岁的糖尿病患者,由主治临床医生自行决定
o别人
前往乙型肝炎病毒(HBV)感染(HBsAg患病率为≥2%)高或中等水平的国家的国际旅行者
丙型肝炎病毒感染者
慢性肝病患者(包括但不限于肝硬化、脂肪肝、酒精性肝病、自身免疫性肝炎、丙氨酸转氨酶[ALT]或天冬氨酸转氨酶[AST]水平大于正常上限两倍的人)
爱滋病病毒感染者
被监禁者
所有其他寻求保护免受乙型肝炎病毒感染的人
表5.医护人员职业性经皮或粘膜暴露于血液或体液后对医护人员进行暴露后管理,由医护人员进行HepB疫苗接种和反应状态
| HCP状态 | 暴露后测试 | 暴露后预防 | 接种疫苗后血清学检测 | |||
| 源患者(HBsAg) | HCP检测(抗HBs) | HBIG | 接种疫苗 | |||
| 完成系列后记录在案的响应者 | 无需执行任何操作 | |||||
| 两个完整系列后记录的无反应者 | 阳性/未知 | –* | HBIGx2间隔1个月 | – | 不适用 | |
| 阴性 | 无需执行任何操作 | |||||
| 完成系列后响应未知 | 阳性/未知 | <10毫IU/毫升 | 大x1 | 开始重新接种疫苗 | 阳性 | |
| 阴性 | <10毫IU/毫升 | – | 开始重新接种疫苗 | 阳性 | ||
| 任何结果 | ≥10毫IU/毫升 | – | – | – | ||
| 未接种疫苗/未完全接种疫苗或拒绝接种疫苗的人 | 阳性/未知 | – | 大x1 | 完成疫苗接种 | 阳性 | 阳性 |
| 阴性 | – | 无 | 完成疫苗接种 | 阳性 | ||
缩写:抗HBs=乙型肝炎表面抗原抗体;HBIG=乙型肝炎免疫球蛋白;HBsAg=乙型肝炎表面抗原;HCP=医护人员;N/A=不适用。
*未注明。
图3.对既往接种过完整的≥3剂HepB疫苗系列但未进行疫苗接种后血清学检测的医护人员进行暴露前评估*
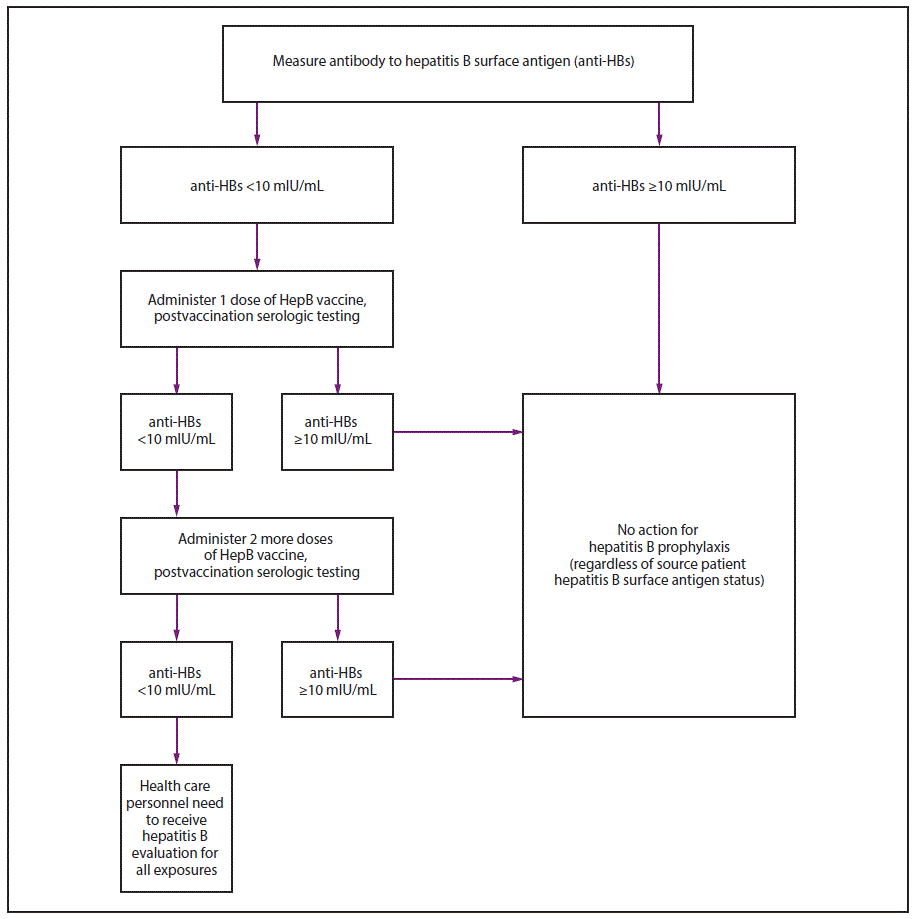
*应在最后一剂疫苗后1-2个月使用可检测抗HBs保护浓度(≥10 mIU/mL)的定量方法(例如酶联免疫吸附测定[ELISA])进行。
上图显示了一种算法,该算法描述了对先前接种过完整、大于或等于3剂乙型肝炎疫苗系列但未进行疫苗接种后血清学检测的医护人员进行暴露前评估的程序。此类检测应在最后一剂疫苗后1-2个月进行,使用可检测抗HBs保护浓度(≥10 mIU/mL)的定量方法(例如酶联免疫吸附测定[ELISA])。
框注5.对过去接种过疫苗的医护人员(HCP)进行抗乙型肝炎检测
问题:越来越多的医护人员在儿童时期接受了常规乙型肝炎(HepB)疫苗接种。不建议在常规婴儿或青少年接种乙肝疫苗后进行疫苗接种后血清学检测。由于疫苗诱导的乙型肝炎表面抗原抗体(抗-HBs)会随着时间的推移而减弱,因此在接种疫苗数年后检测HCP的抗-HBs抗体可能无法区分疫苗无反应者与反应者。
卫生保健机构指南:卫生保健机构可以在雇用或入学时对过去有完整HepB疫苗系列记录的HCP进行抗HB检测(例如,作为常规婴儿或青少年疫苗接种的一部分)。抗乙型肝炎<10 mIU/mL)的医护人员应再接种一剂或多剂乙肝疫苗并重新检测(图3)。如果机构决定在雇用或入学时不测量抗HBs,如果过去有完整的HepB疫苗系列文件,应确保在暴露后及时进行评估和暴露后预防(表5)。
考虑:在某些情况下,接种疫苗的医护人员感染职业性HBV的风险可能足够低,因此在暴露于潜在传染性血液或体液时应评估抗HBs状态并进行适当的随访。这种方法依赖于HCP识别和报告血液和体液暴露,因此可以根据记录在案的低风险、实施和成本考虑来应用。某些HCP职业的职业血液和体液暴露风险较低(例如,涉及咨询与执行程序的职业),非受训者血液和体液暴露的风险低于受训者。在某些环境中,所服务的患者群体中的HBV感染率也低于其他环境,这将影响HCP暴露于HBsAg阳性血液和体液的风险。
表6.非职业性经皮或黏膜暴露于血液或体液后的暴露后管理
| 暴露* | 管理 | |
| 未接种疫苗的人 | 以前接种过疫苗的人 | |
| HBsAg阳性来源 | 乙肝疫苗系列和血红蛋白 | 乙肝疫苗剂量 |
| 来源的HBsAg状态未知 | 乙肝疫苗系列 | 没有管理 |
缩写:乙肝=乙型肝炎;HBsAg=乙型肝炎表面抗原;HBIG=乙型肝炎免疫球蛋白。
*暴露包括经皮(例如咬伤或针刺)或粘膜暴露于血液或体液、性接触或共用针头接触,或性侵犯/虐待的受害者。
框注6.建议在接种疫苗前接受血清学检测的人*
乙型肝炎表面抗原(HBsAg)阳性者的家庭、性接触或针头接触者†
爱滋病病毒阳性者†
病因不明的丙氨酸转氨酶/天冬氨酸转氨酶升高的人†
血液透析患者†
男男性行为者†
过去或现在注射毒品的人†
出生在乙型肝炎病毒(HBV)高流行和中度(HBsAg患病率≥2%)国家的人
美国出生的婴儿未接种疫苗,其父母出生在HBV高流行国家(≥8%)
需要免疫抑制治疗的人,包括化疗、与器官移植相关的免疫抑制以及风湿病或胃肠病的免疫抑制
血液、血浆、器官、组织或精液的捐献者
*血清学检测包括乙型肝炎表面抗原(HBsAg)、乙型肝炎表面抗原抗体和乙型肝炎核心抗原抗体检测。
†表示也被推荐接种乙型肝炎疫苗的人。接种前应进行血清学检测。血清学检测不应成为易感人群接种疫苗的障碍。第一剂疫苗通常应在采集血液进行血清学检测后立即接种。
框注7.建议在完成一系列乙肝疫苗接种后接受疫苗接种后血清学检测*的人
•乙型肝炎表面抗原(HBsAg)阳性母亲或HBsAg状态仍然未知的母亲所生的婴儿(例如,当父母或合法监护权人在出生后不久安全地秘密交出婴儿时,婴儿在出生时或出生后不久安全交出婴儿)†
•医护人员和公共安全工作者
•血液透析患者和其他可能需要门诊血液透析的患者(例如透析前、腹膜透析和家庭透析)
•艾滋病毒感染者
•其他免疫功能低下的人(例如,造血干细胞移植受者或接受化疗的人)
•HBsAg阳性者的性伴侣
*对HBsAg阳性(或HBsAg未知)母亲所生婴儿以外的人进行的疫苗接种后血清学检测包括抗HBs。
†对HBsAg阳性(或HBsAg未知)母亲所生婴儿的疫苗接种后血清学检测包括抗HBs和HBsAg。接种初次疫苗后抗乙型肝炎患者<10 mIU/mL)应重新接种。HBsAg阳性母亲或HBsAg状态未知的母亲所生的婴儿应重新接种单剂HepB疫苗,并在1-2个月后接受疫苗接种后血清学检测。单剂再接种后抗乙型肝炎仍<10 mIU/mL的婴儿应再接种两剂乙肝疫苗,然后在最后一剂后1-2个月进行接种后血清学检测。根据临床情况或家庭偏好,抗HBs<10 mIU/mL)的HBsAg阴性婴儿可以改为重新接种第二剂完整的3剂系列疫苗,然后在最后一剂疫苗后1-2个月进行疫苗接种后血清学检测。对于初次接种后抗HBs<10 mIU/mL的患者,在适当时间再接种3剂HepB疫苗,然后在最后一剂后1-2个月进行抗HBs检测,通常比接种≥1剂疫苗后的血清学检测更实用。
引用
1.更新了美国公共卫生服务局关于HBV、HCV和HIV职业暴露管理的指南,以及暴露后预防的建议。MMWRRecommRep2001;50(编号。RR-11):1-52。PubMed的
2.PrebothM.PHSHBV、HCV和HIV职业暴露管理指南:职业性血液暴露管理。2001年AmFam医师;64:2012–4.PubMed的
3.邦德WW、法韦罗MS、新泽西州彼得森、GravelleCR、EbertJW、梅纳德JE。乙型肝炎病毒干燥和储存一周后的存活率。柳叶刀1981;317:550–1.交叉参考 PubMed的
4.疾病预防控制中心。病毒性肝炎——统计和监测。佐治亚州亚特兰大:美国卫生与公众服务部,CDC;2017. https://www.cdc.gov/hepatitis/statistics/
5.TerraultNA、BzowejNH、ChangKM、HwangJP、JonasMM、MuradMH;美国肝病研究协会。AASLD慢性乙型肝炎治疗指南,肝病学2016;63:261–83.交叉参考 PubMed的
6.RubinLG、LevinMJ、LjungmanP等;美国传染病学会。2013年IDSA免疫功能低下宿主疫苗接种临床实践指南。2014年临床感染病;58:E44-100。交叉参考 PubMed的
7.MastEE、MargolisHS、FioreAE等;免疫实践咨询委员会(ACIP)。消除乙型肝炎病毒感染在美国传播的综合免疫策略:免疫实践咨询委员会(ACIP)的建议。第1部分:婴儿、儿童和青少年的免疫接种。MMWRRecommRep2005;54(编号。RR-16):1-31。PubMed的
8.MastEE、WeinbaumCM、FioreAE等;免疫实践咨询委员会(ACIP)疾病控制与预防中心(CDC)。消除美国乙型肝炎病毒感染传播的综合免疫战略:免疫实践咨询委员会(ACIP)的建议第二部分:成人免疫接种。MMWRRecommRep2006;55(否。RR-16):1-33,测验CE1-4。PubMed的
9.疾病预防控制中心。成人糖尿病患者使用乙型肝炎疫苗接种:免疫实践咨询委员会(ACIP)的建议。MMWRMorbMortalWklyRep2011年;60:1709–11.PubMed的
10.SchillieS,MurphyTV,SawyerM,etal.CDC关于评估医护人员乙型肝炎病毒保护和管理暴露后管理的指南。MMWRRecommRep2013;62(否。RR-10):1-19。PubMed的
11.席利S、墨菲电视台、芬隆N、KoS、沃德JW。更新:缩短了乙型肝炎感染母亲所生婴儿接种疫苗后血清学检测的间隔。MMWRMorbMortalWklyRep2015年;64:1118–20.交叉参考 PubMed的
12.ShimabukuroTT,NguyenM,MartinD,DeStefanoF.疫苗不良事件报告系统(VAERS)中的安全性监测。疫苗2015;33:4398–405.交叉参考 PubMed的
13.周W,PoolV,伊斯坎德尔JK,等.免疫接种后安全性监测:疫苗不良事件报告系统(VAERS)——美国,1991-2001年。MMWRSurveillSumm2003;52(编号。SS-1):1-24。PubMed的
14.McNeilMM、GeeJ、WeintraubES等人。疫苗安全数据链:监测疫苗安全性的成功与挑战。疫苗2014;32:5390–8.交叉参考 PubMed的
15.美国疾病预防控制中心急性病毒性肝炎监测数据——美国,2008年。佐治亚州亚特兰大:美国卫生与公众服务部,CDC;2010. https://www.cdc.gov/hepatitis/statistics/2008surveillance/index.htm
16.HarrisAM、IqbalK、SchillieS等人。急性乙型肝炎病毒感染的增加——肯塔基州、田纳西州和西弗吉尼亚州,2006-2013年。MMWRMorbMortalWklyRep2016年;65:47–50.交叉参考 PubMed的
17.RobertsH、Kruszon-MoranD、LyKN等人。美国家庭慢性乙型肝炎病毒(HBV)感染率:1988-2012年全国健康和营养检查调查(NHANES)。肝病学2016;63:388–97.交叉参考 PubMed的
18.WasleyA、Kruszon-MoranD、KuhnertW等人。疫苗接种时代美国乙型肝炎病毒感染的流行率。J感染Dis2010;202:192–201.交叉参考 PubMed的
19.KowdleyKV,WangCC,WelchS,RobertsH,BrosgartCL.按原籍国划分的居住在美国的外国出生者的慢性乙型肝炎患病率。肝病学2012;56:422–33.交叉参考 PubMed的
20.米切尔T,阿姆斯特朗GL,胡DJ,瓦斯利A,画家JA。输入性慢性乙型肝炎负担的增加——美国,1974-2008年。PLoSOne2011年;6:e27717。交叉参考 PubMed的
21.乙型肝炎病毒:通过普遍的儿童疫苗接种消除美国传播的综合策略。免疫实践咨询委员会(ACIP)的建议。MMWRRecommRep1991年;40(编号。RR-13):1-25。PubMed的
22.疾病预防控制中心(CDC)免疫实践咨询委员会(ACIP)的建议。灭活乙型肝炎病毒疫苗。MMWRMorbMortalWklyRep1982年;31:317–22,327–8.PubMed的
23.美国乙型肝炎高危人群模式的变化。MMWRMorbMortalWklyRep1988年;37:429–32,437.PubMed的
24.CDC最新消息:预防人类免疫缺陷病毒、乙型肝炎病毒和其他血源性病原体在卫生保健环境中传播的通用预防措施。MMWRMorbMortalWklyRep1988年;37:377–82,387–8.PubMed的
25.预防乙型肝炎病毒围产期传播:对所有孕妇进行乙型肝炎表面抗原的产前筛查。MMWRMorbMortalWklyRep1988年;37:341–6,351.PubMed的
26.CDC更新:预防乙型肝炎病毒传播的建议——美国。MMWRMorbMortalWklyRep1999年;48:33–4.PubMed的
27.KolasaMS,TsaiY,XuJ,FenlonN,SchillieS.孕妇乙型肝炎表面抗原检测,美国2014年。儿科感染杂志2017;36:E175-80。交叉参考 PubMed的
28.KuboA、ShlagerL、MarksAR等。预防乙型肝炎垂直传播:一项观察性研究。AnnInternMed2014年;160:828–35.交叉参考 PubMed的
29.SchillieS、WalkerT、VeselskyS等人。感染乙型肝炎的妇女所生婴儿的结果。儿科2015;135:E1141-7。交叉参考 PubMed的
30.HillHA,Elam-EvansLD,YankeyD,SingletonJA,KangY.19-35个月儿童的疫苗接种覆盖率——美国,2016年。MMWRMorbMortalWklyRep2017年;66:1171–7.交叉参考 PubMed的
31.2003年1月至2005年6月出生的儿童的新生儿乙型肝炎疫苗接种覆盖率——美国。MMWRMorbMortalWklyRep2008年;57:825–8.PubMed的
32.美国卫生与公众服务部疾病预防和健康促进办公室。健康人2020。华盛顿特区:美国卫生与公众服务部;2014.https://www.healthypeople.gov/
33.WalkerTY、Elam-EvansLD、SingletonJA等人。13-17岁青少年的国家、地区、州和选定的地方疫苗接种覆盖率——美国,2016年。MMWRMorbMortalWklyRep2017年;66:874–82.交叉参考 PubMed的
34.WilliamsWW、LuPJ、O’HalloranA等人。成年人群疫苗接种覆盖率监测——美国,2015年。MMWRSurveillSumm2017;66(编号SS-11):1-28。交叉参考 PubMed的
35.AgertonTB、MahoneyFJ、波兰语LB、ShapiroCN。血源性病原体标准对医护人员接种乙型肝炎疫苗的影响。感染控制医院流行病学1995;16:287–91.交叉参考 PubMed的
36.范L、Owusu-EduseiKJr、SchillieSF、墨菲电视台。检测乙型肝炎阳性孕妇乙型肝炎e抗原或病毒载量的成本效益。ObstetGynecol2014年;123:929–37.交叉参考 PubMed的
37.疾病预防控制中心;美国妇产科医师学会。对孕妇进行乙型肝炎病毒(HBV)感染筛查。佐治亚州亚特兰大:美国卫生与公众服务部,CDC;2015.https://www.cdc.gov/hepatitis/hbv/pdfs/prenatalhbsagtesting.pdf
38.PanCQ,DuanZP,BhamidimarriKR,etal.乙型肝炎病毒母婴传播风险评估和干预的算法。临床胃肠醇肝2012;10:452–9.交叉参考 PubMed的
39.潘CQ,HanGR,江HX,等.替比夫定可防止患有慢性乙型肝炎的HBeAg阳性女性的垂直传播。ClinGastroenterolHepatol2012;10:520–6.交叉参考 PubMed的
40.乙型肝炎病毒感染的免疫发病机制.免疫细胞生物学2007;85:16–23.交叉参考 PubMed的
41.GishRG、GivenBD、LaiCL等。慢性乙型肝炎:病毒学、自然病程、当前治疗和对未来机遇的一瞥。抗病毒研究2015;121:47–58.交叉参考 PubMed的
42.HoofnagleJH,DiBisceglieAM.急性和慢性病毒性肝炎的血清学诊断。SeminLiverDis1991年;11:73–83.交叉参考 PubMed的
43.KrugmanS,OverbyLR,MushahwarIK,LingCM,FrösnerGG,DeinhardtF.病毒性肝炎,B型。重新检查了关于自然史和预防的研究。NEnglJMed1979年;300:101–6.交叉参考 PubMed的
44.LongSS,ProberCG,FischerM.儿科传染病的原理和实践。第5版。荷兰阿姆斯特丹:爱思唯尔;2017.
45.MagniusLO,NorderH.乙型肝炎病毒的亚型、基因型和分子流行病学,由S基因的序列变异性反映。Intervirology1995年;38:24–34.交叉参考 PubMed的
46.KramvisA.乙型肝炎病毒的基因型和遗传变异性。Intervirology2014年;57:141–50.交叉参考 PubMed的
47.克拉姆维斯A.乙型肝炎病毒基因型和HBeAg在儿科中的临床意义。RevMedVirol2016年;26:285–303.交叉参考 PubMed的
48.阿兰太平绅士。隐匿性乙型肝炎病毒感染。TransfusClinBiol2004年;11:18–25.交叉参考 PubMed的
49.TrépoC,ChanHL,LokA.乙型肝炎病毒感染。柳叶刀2014;384:2053–63.交叉参考 PubMed的
50.McMahonBJ、AlwardWL、HallDB等。急性乙型肝炎病毒感染:年龄与疾病临床表现和随后携带者状态发展的关系。J感染Dis1985;151:599–603.交叉参考 PubMed的
51.DienstagJL.乙型肝炎病毒感染肝外表现的免疫发病机制。SpringerSeminImmunopathol1981;3:461–72.交叉参考 PubMed的
52.BeasleyRP、HwangLY、LeeGC等。使用乙型肝炎免疫球蛋白和乙型肝炎疫苗预防围产期传播的乙型肝炎病毒感染。柳叶刀1983;322:1099–102.交叉参考 PubMed的
53.埃德蒙兹WJ、MedleyGF、NokesDJ、HallAJ、WhittleHC。年龄对乙型肝炎携带者状态发展的影响。ProcBiolSci1993;253:197–201.交叉参考 PubMed的
54.急性乙型肝炎病毒感染后慢性病的风险:综述。临床感染Dis1995;20:992–1000.交叉参考 PubMed的
55.HadlerSC、JudsonFN、O’MalleyPM等。同性恋男性乙型肝炎病毒感染的结果及其与既往人类免疫缺陷病毒感染的关系。J感染Dis1991;163:454–7.交叉参考 PubMed的
56.BeasleyRP,LinCC,HwangLY,ChienCS.肝细胞癌和乙型肝炎病毒。一项针对台湾22707名男性的前瞻性研究。柳叶刀1981;318:1129–33.交叉参考 PubMed的
57.GoldsteinST,周F,HadlerSC,BellBP,MastEE,MargolisHS.估计全球乙型肝炎疾病负担和疫苗接种影响的数学模型。国际流行病学杂志2005;34:1329–39.交叉参考 PubMed的
58.McMahonBJ,AlbertsSR,WainwrightRB,BulkowL,LanierAP.乙型肝炎相关后遗症。对1400名乙型肝炎表面抗原阳性阿拉斯加本地携带者的前瞻性研究。ArchInternMed1990;150:1051–4.交叉参考 PubMed的
59.JonasMM、LokAS、McMahonBJ等人。儿童慢性乙型肝炎病毒感染治疗中的抗病毒治疗:系统评价和荟萃分析。肝病学2016;63:307–18.交叉参考 PubMed的
60.LokAS、McMahonBJ、BrownRSJr等。成人慢性乙型肝炎病毒感染的抗病毒治疗:系统评价和荟萃分析。肝病学2016;63:284–306.交叉参考 PubMed的
61.麦克马洪BJ。慢性乙型肝炎病毒感染。MedClinNorthAm2014年;98:39–54.交叉参考 PubMed的
62.WangC,JiD,ChenJ,等.在接受直接抗病毒药物治疗的丙型肝炎患者中,乙型肝炎病毒在流行地区再激活引起的肝炎。临床胃肠醇肝2017;15:132–6.交叉参考 PubMed的
63.尼尔森NP、JamiesonDJ、墨菲电视台。预防围产期乙型肝炎病毒传播。JPediatricInfectDisSoc2014;3(增刊1):S7–12。交叉参考 PubMed的
64.席利SF,墨菲电视台。新生儿重组乙型肝炎疫苗接种后的血清保护:综述。疫苗2013;31:2506–16.交叉参考 PubMed的
65.庞德RA。乙型肝炎病毒感染的非典型血清学特征。EurJ临床微生物感染Dis2013;32:461–76.交叉参考 PubMed的
66.庞德RA、卡多佐DD、费罗MO。“单独抗-HBc”血清学特征的潜在机制。ArchVirol2010年;155:149–58.交叉参考 PubMed的
67.FranksAL,BergCJ,KaneMA,etal.在美国出生的东南亚难民儿童的乙型肝炎病毒感染。NEnglJMed1989年;321:1301–5.交叉参考 PubMed的
68.MortensenE、KamaliA、SchirmerPL等人。目前对慢性乙型肝炎病毒感染的筛查方案是否足够?诊断微生物感染Dis2016;85:159–67.交叉参考 PubMed的
69.CalistiG,HermanO,PowleyM,HaqueT.慢性血液透析患者在疫苗接种加强后血液中乙型肝炎表面抗原的持续存在。BMJ案例代表2014;2014(6月10日1):BCR2013202191.交叉参考 PubMed的
70.GrobP、JilgW、BornhakH等人。血清学模式“单独抗HBc”:研讨会报告。JMedVirol2000年;62:450–5.交叉参考 PubMed的
71.席尔瓦AE、麦克马洪BJ、帕金森AJ、SjogrenMH、HoofnagleJH、DiBisceglieAM。乙型肝炎病毒DNA在随后接种乙型肝炎疫苗的乙型肝炎核心抗原分离抗体的人中。临床感染Dis1998;26:895–7.交叉参考 PubMed的
72.CandottiD、LinCK、BelkhiriD等。东南亚献血者隐匿性乙型肝炎感染:分子特征和潜在发生机制。肠道2012;61:1744–53.交叉参考 PubMed的
73.德费奥TM,波利F,莫齐F,莫雷蒂MP,斯卡拉莫尼亚M;合作肾脏、肝脏和心脏北意大利移植计划研究小组。抗HBC阳性尸体器官捐献者传播乙型肝炎病毒的风险:一项合作研究。移植过程2005;37:1238–9.交叉参考 PubMed的
74.州和地区流行病学家委员会。乙型肝炎,围产期病毒感染2017年病例定义。佐治亚州亚特兰大:州和地区流行病学家委员会;2017. https://wwwn.cdc.gov/nndss/conditions/hepatitis-b-perinatal-virus-infection/case-definition/2017/
75.NelsonPK、MathersBM、CowieB等人。注射吸毒者乙型肝炎和丙型肝炎的全球流行病学:系统评价结果。柳叶刀2011;378:571–83.交叉参考 PubMed的
76.病毒性肝炎——CDC针对特定人群和环境的建议。佐治亚州亚特兰大:美国卫生与公众服务部,CDC;2015. https://www.cdc.gov/hepatitis/populations/stds.htm
77.HurieMB,MastEE,DavisJP.乙型肝炎病毒感染在美国出生的苗族难民儿童的水平传播。儿科1992;89:269–73.PubMed的
78.乔杜里RK、佩里E、克利里TE。智障机构居民中乙型肝炎感染的患病率。AmJ流行病学1977;105:123–6.交叉参考 PubMed的
79.ThompsonND,PerzJF,MoormanAC,HolmbergSD.非医院卫生保健相关的乙型和丙型肝炎病毒传播:美国,1998-2008年。AnnInternMed2009年;150:33–9.交叉参考 PubMed的
80.WilliamsRE,SenaAC,MoormanAC,etal.乙型肝炎爆发期间长期护理机构的易感老年居民接种乙型肝炎疫苗。疫苗2012;30:3147–50.交叉参考 PubMed的
81.WoodruffBA,VazquezE.发育障碍者机构中肝炎病毒感染的患病率。AmJMentRetard2002年;107:278–92.交叉参考 PubMed的
82.RosenbergSD、GoodmanLA、OsherFC等。严重精神疾病患者中HIV、乙型肝炎和丙型肝炎的患病率。美国公共卫生杂志2001;91:31–7.交叉参考 PubMed的
83.WeinbaumCM、WilliamsI、MastEE等。慢性乙型肝炎病毒感染者的识别和公共卫生管理建议。MMWRRecommRep2008;57(编号。RR-8):1-20。PubMed的
84.温鲍姆C、莱尔拉R、马戈利斯HS。在惩教环境中预防和控制肝炎病毒感染。MMWRRecommRep2003;52(编号。RR-1):1-36,测验CE1-4。PubMed的
85.DienstagJL,RyanDM.医院人员职业暴露于乙型肝炎病毒:感染还是免疫?AmJ流行病学1982;115:26–39.交叉参考 PubMed的
86.HadlerSC、DotoIL、MaynardJE等。医院工作人员感染乙型肝炎的职业风险。感染控制1985;6:24–31.交叉参考 PubMed的
87.美国劳工部。职业安全与健康管理局。OSHA法律和法规。https://www.osha.gov/law-regs.html
88.预防慢性血液透析患者感染传播的建议。MMWRRecommRep2001;50(编号。RR-5):1-43。PubMed的
89.阿尔特MJ、法韦罗女士、梅纳德JE。感染控制策略对美国透析相关性肝炎发病率的影响。JInfectDis1986年;153:1149–51.交叉参考 PubMed的
90.FinelliL、MillerJT、TokarsJI、AlterMJ、ArduinoMJ。2002年美国透析相关疾病全国监测。SeminDial2005年;18:52–61.交叉参考 PubMed的
91.ZibbellJE、IqbalK、PatelRC等。2006-2012年肯塔基州、田纳西州、弗吉尼亚州和西弗吉尼亚州≤30岁人群中与注射吸毒有关的丙型肝炎病毒感染增加。MMWRMorbMortalWklyRep2015年;64:453–8.PubMed的
92.慢性肝病患者的甲型肝炎和乙型肝炎疫苗接种。比利时胃肠学报2000;63:359–63.PubMed的
93.JohnsonDF,LederK,TorresiJ.国际旅行者的乙型肝炎和丙型肝炎感染。JTravelMed2013年;20:194–202.交叉参考 PubMed的
94.KellermanSE,HansonDL,McNaghtenAD,FlemingPL.人类免疫缺陷病毒感染受试者中慢性乙型肝炎的患病率和急性乙型肝炎感染的发生率。J感染Dis2003;188:571–7.交叉参考 PubMed的
95.ChunHM,FiebergAM,HullsiekKH,etal.;传染病临床研究计划HIV工作组。过去20年美国HIV感染者队列中乙型肝炎病毒感染的流行病学。临床感染Dis2010;50:426–36.交叉参考 PubMed的
96.霍曼C、克罗格斯加德K、佩德森C、安德森P、尼尔森JO。晚期HIV感染患者乙型肝炎感染的高发病率和慢性乙型肝炎感染的演变。JAcquir免疫缺陷Syndr1991;4:416–20.PubMed的
97.人类免疫缺陷病毒感染患者的乙型肝炎:流行病学、自然病程和治疗。SeminLiverDis2003年;23:125–36.交叉参考 PubMed的
98.改变MJ。病毒性肝炎和HIV合并感染的流行病学。JHepatol2006年;44(增刊):S6–9。交叉参考 PubMed的
99.ThioCL、SeabergEC、SkolaskyRJr等;多中心艾滋病队列研究。HIV-1、乙型肝炎病毒和多中心队列研究(MACS)中肝脏相关死亡风险。柳叶刀2002;360:1921–6.交叉参考 PubMed的
100.ReillyML、SchillieSF、SmithE等人。诊断为糖尿病的成人患急性乙型肝炎的风险增加。J糖尿病科学技术2012;6:858–66.交叉参考 PubMed的
101.席莉SF,XingJ,墨菲TV,胡DJ。1999-2010年美国确诊糖尿病患者乙型肝炎病毒感染率。J病毒性肝病2012;19:674–6.交叉参考 PubMed的
102.波兰语LB、ShapiroCN、BauerF等。乙型肝炎病毒的院内传播与使用弹簧式指尖装置有关。NEnglJMed1992年;326:721–5.交叉参考 PubMed的
103.埃米尼EA、埃利斯RW、米勒WJ、麦卡利尔WJ、斯科尼克EM、GeretyRJ。重组乙型肝炎疫苗的生产及免疫学分析。J感染1986;13(增刊A):3-9。交叉参考 PubMed的
104.StephenneJ.重组酵母衍生乙型肝炎疫苗的开发和生产方面。疫苗1990;8(增刊):S69-73,讨论S79-80。
105.CDC更新:扩大无硫柳汞防腐剂乙型肝炎疫苗的供应。MMWRMorbMortalWklyRep2000;49:642–51
106.美国食品和药物管理局。附有证明文件的持牌生物制品。马里兰州银泉市:美国卫生与公众服务部、食品和药物管理局;2017.https://www.fda.gov/biologicsbloodvaccines/ucm133705.htm
107.杰克AD、霍尔AJ、缅因州N、门迪M、惠特尔HC。什么水平的乙型肝炎抗体具有保护作用?JInfectDis1999年;179:489–92.交叉参考 PubMed的
108.BruceMG、BrudenD、HurlburtD等。乙型肝炎疫苗后的抗体水平和保护:30年随访研究的结果和对加强剂量的反应。J感染Dis2016;214:16–22.交叉参考 PubMed的
109.LeuridanE,VanDammeP.乙型肝炎和加强剂量的必要性。2011年临床感染Dis;53:68–75.交叉参考 PubMed的
110.SimonsBC、SpradlingPR、BrudenDJ等。纵向乙型肝炎疫苗队列显示出持久的乙型肝炎病毒(HBV)细胞免疫力,尽管针对HBV表面抗原的抗体丢失。J感染Dis2016;214:273–80.交叉参考 PubMed的
111.安德烈·菲。酵母源性乙型肝炎疫苗的安全性和有效性数据摘要。美国医学杂志1989;87(3a):S14-20。交叉参考 PubMed的
112.SchillieSF、SpradlingPR、MurphyTV。乙型肝炎疫苗在糖尿病患者中的免疫反应:文献系统评价。糖尿病护理2012;35:2690–7.交叉参考 PubMed的
113.AverhoffF,MahoneyF,ColemanP,SchatzG,HurwitzE,MargolisH.乙型肝炎疫苗的免疫原性。对有乙型肝炎病毒感染职业风险的人的影响。美国医学杂志1998;15:1–8.交叉参考 PubMed的
114.ShawFEJr、GuessHA、RoetsJM等。解剖注射部位、年龄和吸烟对乙型肝炎疫苗接种免疫反应的影响。疫苗1989;7:425–30.交叉参考 PubMed的
115.BowmanS,GrauLE,SingerM,ScottG,HeimerR.通过美国三个城市的注射器交换计划,在一项针对注射吸毒者的随机试验中,与乙型肝炎疫苗系列完成相关的因素。BMC公共卫生2014;14:820。交叉参考 PubMed的
116.DrachmanR,IsacsohnM,RudenskyB,DrukkerA.透析儿童和青少年患者接种乙型肝炎疫苗。NephrolDial移植1989;4:372–4.交叉参考 PubMed的
117.LeeC,GongY,BrokJ,BoxallEH,GluudC.乙型肝炎免疫接种对乙型肝炎表面抗原阳性母亲新生儿的影响:系统评价和荟萃分析。英国医学杂志2006;332:328–36.交叉参考 PubMed的
118.PatelDM,ButlerJ,FeldmanS,GravesGR,RhodesPG.乙型肝炎疫苗在健康极低出生体重儿中的免疫原性。JPediatr1997年;131:641–3.交叉参考 PubMed的
119.MarsanoLS、WestDJ、ChanI等。两剂乙型肝炎疫苗方案:年轻人启动和记忆反应的证据。疫苗1998;16:624–9.交叉参考 PubMed的
120.卡西迪WM、沃森B、伊奥利VA、威廉姆斯K、伯德S、韦斯特DJ。青少年替代两剂和三剂乙型肝炎疫苗接种方案的随机试验:抗体反应、安全性和免疫记忆。儿科2001;107:626–31.交叉参考 PubMed的
121.FabriziF,DixitV,MessaP,MartinP.慢性肾病中的乙型肝炎病毒疫苗:佐剂提高免疫原性?随机试验的荟萃分析。疫苗2012;30:2295–300.交叉参考 PubMed的
122.HoviL、ValleM、SiimesMA、JalankoH、SaarinenUM。接受抗癌化疗的儿童对乙型肝炎疫苗的反应受损。PediatrInfectDisJ1995年;14:931–4.交叉参考 PubMed的
123.ZuinG、PrincipiN、TornaghiR等人。HIV感染儿童对乙型肝炎疫苗的反应受损。疫苗1992;10:857–60.交叉参考 PubMed的
124.世界卫生组织。信息表观察到的疫苗反应率:乙型肝炎疫苗。瑞士日内瓦:世界卫生组织;2012.http://www.who.int/vaccine_safety/initiative/tools/Hep_B_Vaccine_rates_information_sheet.pdf
125.BohlkeK、DavisRL、MarcySM等人;疫苗安全数据链团队。儿童和青少年接种疫苗后发生过敏反应的风险。儿科2003;112:815–20.交叉参考 PubMed的
126.斯特拉顿K、福特A、鲁施E、克莱顿EW,编辑。疫苗的不良反应:证据和因果关系。华盛顿特区:国家学院出版社;2012.
127.StrattonK、AlmarioD、McCormickMC,编辑。免疫安全性评价:乙型肝炎疫苗和脱髓鞘神经系统疾病。华盛顿特区:国家科学院出版社;2002.
128.哈尔西NA、杜克洛斯P、范达姆P、马戈利斯H;病毒性肝炎预防委员会。乙型肝炎疫苗和中枢神经系统脱髓鞘疾病。PediatrInfectDisJ1999年;18:23–4.交叉参考 PubMed的
129.DeStefanoF,WeintraubES,ChenRT.乙型肝炎疫苗和多发性硬化症的风险。药典流行病学药物Saf2007;16:705-7,作者回复707-8。交叉参考 PubMed的
130.RayP、BlackS、ShinefieldH等人;疫苗安全数据链团队。15-59岁人群接种破伤风、流感和乙型肝炎疫苗后患类风湿性关节炎的风险。疫苗2011;29:6592–7.交叉参考 PubMed的
131.Rowhani-RahbarA、KleinNP、LewisN等人。儿童免疫接种和贝尔麻痹:以病例为中心的分析。AmJ流行病学2012;175:878–85.交叉参考 PubMed的
132.YuO,BohlkeK,HansonCA,etal.乙型肝炎疫苗和自身免疫性甲状腺疾病的风险:疫苗安全数据链研究。药典流行病学药物Saf2007;16:736–45.交叉参考 PubMed的
133.NalewayAL、BelongiaEA、DonahueJG、KiekeBA、格兰仕JM;疫苗安全数据链。儿童免疫接种后发生免疫性溶血性贫血的风险。疫苗2009;27:7394–7.交叉参考 PubMed的
134.McNeilMM、WeintraubES、DuffyJ等人。儿童和成人接种疫苗后发生过敏反应的风险。过敏临床免疫学杂志2016;137:868–78.交叉参考 PubMed的
135.巴克斯特R、刘易斯E、消防员B、德斯特凡诺F、吉J、克莱因NP。以病例为中心的疫苗接种后视神经炎分析。临床感染Dis2016;63:79–81.交叉参考 PubMed的
136.BaxterR、BakshiN、FiremanB等人。吉兰-巴雷综合征与疫苗接种缺乏关联。临床感染Dis2013;57:197–204.交叉参考 PubMed的
137.巴克斯特R、刘易斯N、BohrerP、哈灵顿T、奥克斯L、克莱因NP。免疫接种后突发性感音神经性听力损失:以病例为中心的分析。耳鼻喉头颈外科2016;155:81–6.交叉参考 PubMed的
138.138.HaberP,MoroPL,NgC,等.美国目前获得许可的乙型肝炎表面抗原疫苗的安全性,疫苗不良事件报告系统(VAERS),2005-2015年。疫苗2017.http://www.sciencedirect.com/science/article/pii/S0264410X1731722X
139.HadlerSC,deMonzonMA,LugoDR,PerezM.乙型肝炎疫苗剂量时间对尤卡印第安人疫苗反应的影响。疫苗1989;7:106–10.交叉参考 PubMed的
140.HalseyNA、MoultonLH、O’DonovanJC等人每年对儿童和青少年接种乙型肝炎疫苗。儿科1999;103:1243–7.交叉参考 PubMed的
141.WiströmJ,AhlmC,LundbergS,SettergrenB,TärnvikA.在接种一剂疫苗四年后接种重组乙型肝炎疫苗加强接种。疫苗1999;17:2162–5.交叉参考 PubMed的
142.JilgW,SchmidtM,DeinhardtF.乙型肝炎疫苗接种:三种不同疫苗接种时间表的比较。J感染Dis1989;160:766–9.交叉参考 PubMed的
143.重组酵母衍生乙型肝炎疫苗在围产期免疫无反应者中的免疫原性。美国医学会杂志1994;271:859–61.交叉参考 PubMed的
144.BrownRSJr、McMahonBJ、LokAS等人。妊娠期慢性乙型肝炎病毒感染的抗病毒治疗:系统评价和荟萃分析。肝病学2016;63:319–33.交叉参考 PubMed的
145.JourdainG、Ngo-Giang-HuongN、CresseyTR等人。预防乙型肝炎病毒母婴传播:一项III期、安慰剂对照、双盲、随机临床试验,旨在评估富马酸替诺福韦二吡呋酯短期治疗乙型肝炎病毒e抗原女性的疗效和安全性。BMC感染Dis2016;16:393。交叉参考 PubMed的
146.HanGR,江HX,岳旭,等.替比夫定治疗的有效性和安全性:一项针对孕妇的开放标签前瞻性研究,用于预防乙型肝炎病毒感染的围产期传播。J病毒性肝病2015;22:754–62.交叉参考 PubMed的
147.范L、Owusu-EduseiKJr、SchillieSF、墨菲电视台。妊娠期主动-被动预防和抗病毒预防预防围产期乙型肝炎病毒感染的成本效益。肝病学2016;63:1471–80.交叉参考 PubMed的
148.BarbosaC、SmithEA、HoergerTJ等人。国家围产期乙型肝炎预防规划的成本效益分析。儿科2014;133:243–53.交叉参考 PubMed的
149.HoergerTJ、SchillieS、WittenbornJS等。乙型肝炎疫苗接种对确诊为糖尿病的成人的成本效益。糖尿病护理2013;36:63–9.交叉参考 PubMed的
150.HoergerTJ、布拉德利C、席利SF、赖利M、墨菲电视台。确保为先前接种疫苗的医护人员提供乙型肝炎保护的成本效益。2014年传染病控制医院流行病学;35:845–54.交叉参考 PubMed的
151.CDC.关于免疫接种的一般建议——免疫接种实践咨询委员会(ACIP)的建议。MMWRRecommRep2011;60(编号RR-2):1-64。PubMed的
建议引用本文:SchillieS、VellozziC、ReingoldA等人。美国乙型肝炎病毒感染的预防:免疫实践咨询委员会的建议。MMWRRecommRep2018;67(编号。RR-1):1-31。DOI:http://dx.doi.org/10.15585/mmwr.rr6701a1.
上次审核日期: 2018年5月22 日
资料来源:美国疾病控制与预防中心
Hits: 47

