Contents
第28章:风疹
2013年1月
风疹 应呈报
疾病
风疹是一种由披膜病毒引起的轻微疾病。可能有轻度前驱疾病,包括低烧、不适、鼻炎和轻度结膜炎。涉及耳后和枕下腺体的淋巴结病可能先于皮疹出现。皮疹通常是短暂的,呈红斑状,主要见于耳后、面部和颈部。临床诊断是不可靠的,因为皮疹可能是短暂的,并不是风疹所特有的。
风疹通过飞沫传播。潜伏期为14至21天,大多数人在接触后14至17天出现皮疹。风疹患者在症状出现前一周至皮疹出现后四天具有传染性。
并发症包括血小板减少症(发病率可高达3000例感染中的一例)和感染后脑炎(6000例中的一例)(Lokletz and Reynolds, 1965; Plotkin and Orenstein, 2004)。在成人中,风疹感染后偶尔会出现关节炎和关节痛;慢性关节炎很少被报道(Plotkin and Orenstein, 2004)。
孕妇在怀孕期间感染风疹可能导致流产或先天性风疹综合征(CRS)。CRS呈现以下一种或多种情况:
- 白内障和其他眼睛缺陷
- 聋
- 心脏异常
- 头小畸型
- 子宫内生长迟缓
- 脑、肝、肺和骨髓的炎性病变。
怀孕前八到十周的感染会导致高达90%的存活婴儿受损;多种缺陷是常见的。当感染发生在妊娠11至16周之间时,损伤的风险下降至约10%至20%(Miller et al., 1982)。在妊娠16周后感染的胎儿损伤是罕见的,只有在妊娠20周后感染后报告耳聋。一些受感染的婴儿可能在出生时表现正常,但感知性耳聋可能在以后被发现(Miller et al., 1982; Plotkin and Orenstein, 2004)。
疾病的历史和流行病学
在引入风疹免疫接种之前,风疹通常发生在儿童中,超过80%的成人有既往风疹感染的证据(Morgan Capner et al., 1988)。
风疹免疫接种于1970年在英国引入,用于青春期前的女孩和非免疫育龄妇女,以防止怀孕期间感染风疹。这一战略的目的不是阻断风疹的循环,而是通过增加风疹抗体的比例来直接保护育龄妇女;这一比例从1970年前的85%至90%上升到1987年的97%至98%(Vyse et al., 2002)。先天性风疹监测于1971年建立,以监测疫苗接种计划的影响。在1971-1975年期间,英国每年平均有48例CRS分娩和742例终止妊娠(Tookey and Peckham, 1999)(见图28.1)。
尽管选择性免疫接种政策有效地减少了CRS和终止妊娠的数量,但妊娠期风疹病例仍在发生。这主要是因为少数仍易患风疹的妇女仍可能从自己和/或朋友的孩子那里感染风疹。
1988年10月开始使用麻疹、流行性腮腺炎和风疹疫苗进行风疹全面免疫接种。这项政策的目的是阻断风疹在幼儿中的传播,从而保护易感的成年妇女免受感染。与此同时,风疹被列为法定传染病。引入MMR后,幼儿风疹发病率显著下降,孕妇风疹感染率也随之下降——从1987年的167例降至2003年的1例。
1989年的一项血清流行率研究表明,学龄儿童,尤其是男孩对风疹的易感性很高(Miller et al., 1991)。1993年,风疹的通报和实验室确认病例都有大幅增加。许多受影响的人没有资格接种MMR或风疹疫苗。为此原因,1994年11月在学校运动中使用了麻疹-风疹联合疫苗(见第一章)
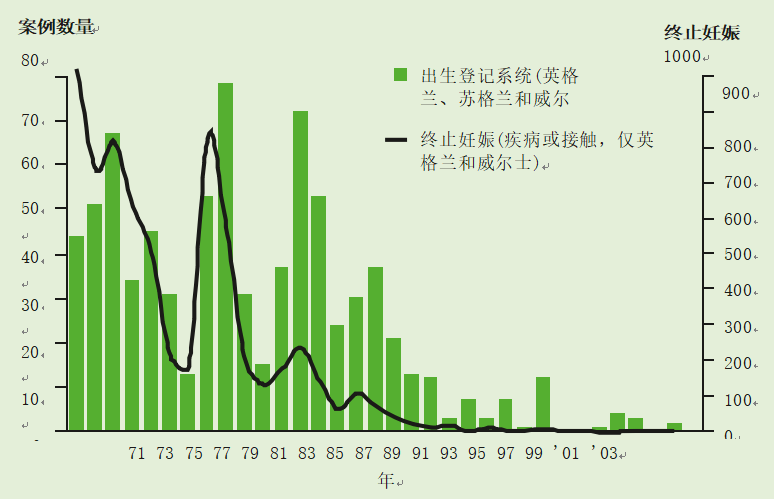
图28.1先天性风疹综合征分娩(资料来源:1971-2004年国家先天性风疹监测方案)和风疹相关终止妊娠(资料来源:1971-2003年国家统计局)
21).当时,MMR库存不足,无法为所有这些儿童接种腮腺炎疫苗。超过800万5至16岁的儿童接种了MR疫苗。
1996年10月,实行了两剂混合疫苗接种计划,停止了对少女的选择性疫苗接种政策。在英国使用的单剂量含风疹的疫苗提供了大约95-100%的风疹保护(Plotkin and Orenstein, 2004)。
在芬兰,1982年引入了两剂MMR方案;每剂药物的高覆盖率始终如一。自1994年以来,本土麻疹、腮腺炎和风疹已被消灭(Peltola et al., 1994)。美国于1989年引入了两剂方案,并于2000年宣布已经阻断了地方性传播(Plotkin and Orenstein, 2004,第20章)。目前,包括欧盟、北美和澳大拉西亚在内的100多个国家例行提供MMR。
1996年,风疹在英国再次出现。这些病例大多发生在大专院校,男性在1994年MR运动之前就已经离开学校(Vyse et al., 2002)。从那时起,就报告了散发性风疹病例,主要与输入性病例有关(健康保护局网站)。
自1991年以来,只有大约三分之一的出生于在英国的感染CRS新生儿是英国妇女。其余三分之二的婴儿是出生在海外的母亲所生。其中,大约一半是在海外感染的,主要是在怀孕早期,在他们的原籍国。其余的妇女在英国被感染,通常是在到达后的两年内(Rahi et al., 2001; Tookey and Peckham, 1999; Tookey et al., 2002; Tookey, 2004)。后一种观察结果可以用英国一些少数民族群体中较高的易感性来解释,这些人在来英国之前没有被感染或免疫(Tookey et al., 2002)。
MMR疫苗
MMR疫苗是冻干制剂,含有麻疹、腮腺炎和风疹病毒的减毒活毒株。将三种减毒病毒株在合适的培养基中分别培养,并在冻干前混合。这些疫苗包含以下成分:
Priorix®
每0.5毫升剂量的复溶疫苗含有:
不低于103.0的半数细胞培养感染量 (CCID50) Schwarz麻疹病毒
不少于103.7 CCID50的RIT 4385腮腺炎病毒
不少于103.0 CCID50的Wistar RA 27/3风疹病毒株。
MMRVaxPRO®
每0.5毫升剂量在复溶时含有不少于相当于:
100050%组织细胞感染量 (TCID50)的更减毒的麻疹病毒埃德蒙斯顿株恩德斯系
20,000 TCID50的腮腺炎病毒(Jeryl Lynn级毒株)
1000 TCID50的风疹病毒(Wistar RA 27/3株)。
MMR疫苗不含硫柳汞或任何其他防腐剂。该疫苗含有已经减毒(修饰)的活生物体。当需要预防麻疹、腮腺炎和/或风疹时,建议使用MMR。
储存
未配制的疫苗及其稀释液应储存在+2℃至+8℃的原包装中,并避光保存。所有疫苗在某种程度上都对冷热敏感。高温加速了大多数疫苗效力的下降,从而缩短了它们的保质期。除非储存在正确的温度下,否则无法保证疫苗的有效性。冷冻可能导致某些疫苗的反应原性增加和效力丧失。它还会在容器中产生细小的裂纹,导致内容物被污染。
疫苗应使用制造商提供的稀释剂复溶,并在一小时内使用或丢弃。
剂型
风疹疫苗仅作为联合产品(MMR)的一部分提供。
Priorix®以白色至淡粉色冻干疫苗颗粒的形式提供,用于与所提供的稀释剂复溶。必须充分摇动复溶疫苗,直到颗粒完全溶解在稀释剂中。
MMRVaxPRO®以冻干粉的形式提供,可与所提供的稀释剂复溶。必须轻轻摇动复溶疫苗,以确保充分混合。复溶疫苗为黄色,只有在透明且无颗粒物质的情况下才能使用。
剂量和时间表
在推荐的时间间隔内服用两剂0.5毫升(见下文)。
接种
疫苗通常通过上臂或大腿前外侧肌肉注射。然而,对于患有出血性疾病的个体,应通过深层皮下注射来接种疫苗,以降低出血的风险。
MMR疫苗可与其他疫苗(如DTaP/ IPV、Hib/MenC和乙型肝炎疫苗)同时接种。疫苗应在单独的部位接种,最好是在不同的肢体。如果给药在同一个肢体,它们应该至少分开2.5厘米(美国儿科学会,2003)。参见第11章常规儿童免疫接种计划。如果MMR不能与灭活疫苗同时注射,可以在之前的任何间隔时间注射
或者之后。应该在孩子的记录中注明接种每种疫苗的地点。
MMR最好与其他活疫苗(如卡介苗)同时接种。如果同时给予活疫苗,那么每种疫苗病毒将开始复制,并对每种疫苗产生适当的免疫反应。接种活疫苗后,会产生天然干扰素作为对疫苗的反应。如果在这种反应期间给予第二种活疫苗,干扰素可以防止第二种疫苗病毒的复制。这可能会减弱对第二种疫苗的反应。基于MMR疫苗可导致水痘疫苗反应减弱的证据((Mulloolyand Black, 2001),目前推荐的活疫苗间隔为4周。因此,如果不能同时接种活疫苗,建议间隔四周。
在接种MMR疫苗和进行结核菌素试验之间应间隔四周。MMR的麻疹疫苗成分可以降低迟发型超敏反应。由于这是阳性结核菌素试验的基础,这可能会产生假阴性反应。
当在接受血液制品(如免疫球蛋白)后的三个月内给予MMR时,对麻疹成分的反应可能会降低。这是因为这种血液制品可能含有大量的麻疹特异性抗体,这可能会阻止疫苗病毒的复制。在可能的情况下,MMR应推迟到收到此类产品后的三个月。如果最近接受过血液制品的人需要立即获得麻疹保护,仍应接种MMR疫苗。为了提供更长期的保护,MMR应该在三个月后重复。
如果需要对已经接受抗D免疫球蛋白的产后妇女进行风疹保护,则没有必要延期,因为对风疹成分的反应通常是足够的(Edgar and Hambling, 1977; Black et al., 1983)。分娩时输血可能会抑制风疹反应,因此,应在接种疫苗后6至8周进行风疹抗体检测。如有必要,应重复接种疫苗。
处理
用于接种疫苗的设备,包括用过的小瓶或安瓿,应在每次接种结束后,密封在一个合适的防刺穿“锐器”盒中进行处置(未批准,BS 7320)。
疫苗使用建议
免疫接种计划的目标是在适当的时间间隔为所有符合条件的个人提供两剂MMR疫苗。
在英国目前使用的MMR疫苗的第一剂后,超过90%的个体将血清转化为麻疹、腮腺炎和风疹抗体(Tischer and Gerike, 2000)。然而,许可前研究的抗体反应可能高于常规使用下的临床保护。有证据表明,单剂量的含麻疹的疫苗在约90%的个体中提供麻疹保护(Morse et al., 1994;医学研究委员会,1977年)。单剂含风疹的疫苗可提供约95%至100%的保护(Plotkin and Orenstein, 2004)。在英国使用的单剂量含腮腺炎疫苗可提供61%至91%的腮腺炎保护作用(Plotkin and Orenstein, 2004)。最近在英国进行的一项研究表明,单剂量MMR对流行性腮腺炎的有效性约为64%(Harling et al., 2005)。
因此,需要两剂MMR才能对麻疹、腮腺炎和风疹产生令人满意的保护作用。
当需要预防麻疹、腮腺炎和/或风疹时,建议使用MMR。不管是否有麻疹、腮腺炎或风疹感染史,都可以接种MMR疫苗。对这些人进行免疫接种不会产生不良影响,因为他们已经具有抑制疫苗病毒复制的免疫力。
十岁以下的儿童
第一剂MMR应在12至13个月大时(即第一个生日的一个月内)注射。一岁前的免疫接种在麻疹风险较高的地区提供了早期保护,但残留的母体抗体可能会降低对疫苗的反应率。因此,为计划生育选择的最佳年龄是疾病风险和保护水平之间的折衷。
如果在第一个生日之前注射了一剂MMR,无论是因为去流行国家旅行,还是因为当地疫情爆发,都应忽略该剂量,并在12至13个月大(即第一个生日的一个月内)和3岁4个月至5岁大(见第11章)的推荐时间再注射两剂。
第二次注射通常在入学前进行,但也可以在第一次注射后三个月内的任何时间进行常规注射。允许两次给药之间间隔三个月可能使应答率最大化,特别是在18个月以下的幼儿中,其中母体抗体可能降低对疫苗接种的应答(Orenstein et al., 1986; Redd et al., 2004; de Serres et al., 1995)。当迫切需要麻疹疫苗时,可在第一剂疫苗注射后一个月注射第二剂疫苗(ACIP,1998年)。如果儿童在第一剂疫苗接种后不到三个月且不到18个月时接种第二剂疫苗,则应接种常规学龄前疫苗(第三剂)以确保充分保护。
十岁或十岁以上的儿童和成人
所有儿童在离开学校前都应接种两剂MMR疫苗。青少年(离校)强化课程或预约是确保未免疫或部分免疫儿童获得MMR的机会。如果需要两剂MMR,则应在第一剂后一个月注射第二剂。
MMR疫苗可以给任何年龄的人接种。进入学院、大学或其他高等教育机构、监狱或军队服役提供了检查个人免疫史的机会。应该为那些没有接受过MMR的人提供适当的MMR免疫。
应向所有需要预防风疹的血清反应阴性的育龄妇女提供MMR疫苗。令人满意的保护证据将包括接受过两剂含风疹疫苗或风疹抗体检测呈阳性的证明文件。
在决定何时为其他成人接种疫苗时,需要考虑过去的疫苗接种史、个体保持易感的可能性以及未来的暴露和疾病风险:
- 1980年至1990年间出生的人可能无法预防腮腺炎,但有可能接种麻疹和风疹疫苗。他们可能从未接种过含腮腺炎成分的疫苗
或仅服用一剂MMR,暴露于天然腮腺炎的机会有限。他们应该被召回并接种MMR疫苗。如果这是他们的第一剂,一个月后应再注射一剂MMR。
- 1970年至1979年间出生的人可能已经接种了麻疹疫苗,许多人在童年时期会接触到腮腺炎和风疹。然而,只要可行,这个年龄组应该提供MMR,特别是如果他们被认为有高暴露风险。如果这些成年人因为被证明对至少一种疫苗成分易感而接受疫苗接种,则应给予两剂疫苗,或者应该
成为相关抗原血清转化的证据。
- 1970年之前出生的人很可能已经感染了所有三种自然感染,并且不太可能易感。MMR疫苗应根据请求提供给这些人,或者如果他们被认为具有高暴露风险。如果这些成年人因为被证明对至少一种疫苗成分易感而接受疫苗接种,则应给予两剂疫苗或应存在相关抗原血清转化的证据。
有未知或不完整疫苗接种史的个人
来自发展中国家的儿童可能在其原籍国接种过含麻疹成分的疫苗,但可能没有接种过腮腺炎或风疹疫苗(www-nt.who.int/immunization_monitor ing/en/global summary/country profile select . cfm)。除非有可靠的适当免疫史,否则应假定个人未免疫,并应遵循上述建议。18个月及以上未接受MMR的个体应至少间隔一个月接受两剂。已经接受一剂MMR的个体应该接受第二剂以确保他们受到保护。
医护人员
鉴于医护人员有能力将麻疹或风疹传染给弱势群体,对他们的保护尤为重要。虽然他们可能出于自身利益需要接种MMR疫苗,但基于上述原因,他们也应该对麻疹和风疹免疫,以保护他们的患者。
令人满意的保护证据将包括以下文件:
- 接受了两剂MMR,或
- 麻疹和风疹抗体检测呈阳性。
正在旅行或打算出国居住的个人
所有前往流行地区或流行地区的旅行者都应确保他们按照英国的时间表完全接种疫苗(见上文)。
禁忌症
极少数人不能接种MMR疫苗。如有疑问,应向儿科顾问、免疫协调员或传染病控制顾问寻求适当的建议,而不是拒绝接种疫苗。
疫苗不应用于:
- 免疫抑制者(详见第6章)
- 对先前剂量的麻疹、腮腺炎或风疹疫苗有过敏反应的人
- 对新霉素或明胶有过敏反应的人
- 孕妇。
MMR后的过敏反应极为罕见(每百万剂量3.5至14.4)(Bohlke et al., 2003; Patja et al., 2000; Pool et al., 2002; D’Souza et al., 2000)。可能会出现轻微的过敏症状,但不是MMR或其他疫苗进一步免疫的禁忌症。对这些事件的详细病史通常会区分过敏反应和其他不是由疫苗引起的或不危及生命的事件。在后一种情况下,有可能继续免疫过程。必须寻求专家对疫苗和接种环境的建议。必须考虑到不免疫对个人的终身风险。
预防措施
没有发烧或全身不适的小病不是推迟免疫接种的正当理由。如果个人急性不适,应推迟免疫接种,直到他们完全康复。这是为了避免由于错误地将任何体征或症状归因于疫苗的副作用而混淆任何急性疾病的鉴别诊断。
特发性血小板减少性紫癜
接种MMR疫苗后,特发性血小板减少性紫癜(ITP)很少发生,通常在首剂疫苗接种后6周内。
MMR疫苗接种后发生ITP的风险远低于感染野生麻疹或风疹病毒后发生ITP的风险。
如果在接种第一剂MMR后的六周内出现ITP,则应在接种第二剂MMR前采集血液并检测麻疹、腮腺炎和风疹抗体。血清应送至健康保护局(HPA)病毒参考实验室(Colindale),该实验室为此类儿童提供免费的专业血清学检测。如果结果表明对麻疹、腮腺炎或风疹的免疫力不完全,则建议接种第二剂MMR。
鸡蛋过敏
所有鸡蛋过敏的儿童都应该接受MMR疫苗接种,作为初级保健的常规程序(Clark et al., 2010)。最近的数据表明,对MMR疫苗的过敏反应与对鸡蛋抗原的超敏反应无关,而是与疫苗的其他成分(如明胶)的超敏反应有关(Fox and Lack, 2003)。在总共超过1000名鸡蛋过敏患者的三项大型研究中,在MMR疫苗接种后没有报道严重的心肺反应(Fasano et al., 1992; Freigang et al.,1994; Aickin et al., 1994; Khakoo and Lack, 2000)。对疫苗本身有过敏反应记录的儿童应由过敏症专科医生进行评估(Clark et al .,2010)。
怀孕和母乳喂养
没有证据表明含风疹的疫苗是致畸的。在美国、英国和德国,对661名妇女进行了积极监测,其中293名妇女在高危期(即末次月经后6周)接种了疫苗(主要是单一风疹疫苗)。只有16名婴儿有感染的证据,没有一个婴儿有符合CRS的永久性异常(Best et al .,2004)。然而,作为预防措施,MMR疫苗不应用于已知怀孕的妇女。如果给成年妇女接种MMR疫苗,应建议她们避孕一个月。
不建议在意外接种疫苗后终止妊娠(Tookey et al., 1991)。应向潜在父母提供怀孕期间接种疫苗无风险证据的信息。HPA免疫部门正在对怀孕期间意外服用MMR进行监测,并应向其报告此类情况(电话:020 8200 4400)。
被发现易患风疹的孕妇应在分娩后接种MMR疫苗。
母乳喂养不是MMR免疫接种的禁忌症,MMR疫苗可以给母乳喂养的母亲,对她们的婴儿没有任何风险。极少数情况下,在母乳中发现风疹疫苗病毒,但这并未导致婴儿出现任何症状(Buimovici-Klein et al., 1997; Landes et al., 1980; Losonsky et al., 1982)。口服疫苗不起作用。没有证据表明在母乳中发现腮腺炎和麻疹疫苗病毒。
早产儿
根据时间表,早产儿在适当的年龄接种疫苗是很重要的(见第11章)。
免疫抑制和艾滋病毒
MMR疫苗不推荐用于严重免疫抑制的患者(见第6章)(Angel et al., 1996)。MMR疫苗可用于无或中度免疫抑制的HIV阳性患者(定义见表28.1)。
表28.1 CD4计数/升(占淋巴细胞总数的%)
| 年龄 | 少于12个月 | 1-5岁 | 6至12岁 | 超过12岁 |
| 无抑制 | ≥1500 (≥25%) | ≥1000 (15–24%) | ≥500 (≥25%) | ≥500 (≥25%) |
| 中度抑制 | 750–1499 | 500–999 | 200–499 | 200–499 |
| (15–24%) | (15–24%) | (15–24%) | (15–24%) | |
| 严重抑制 | <750 | <500 | <200 | <200 |
| (<15%) | (<15%) | (<15%) | (<15%) |
皇家儿科和儿童健康学院(www.rcpch.ac.uk)、英国艾滋病毒协会(BHIVA)艾滋病毒感染成人免疫指南(BHIVA,2006年)和英国和爱尔兰儿童艾滋病毒协会(CHIVA)免疫指南提供了进一步的指导(www.bhiva.org/chiva)。
神经疾病
神经疾病的存在不是免疫接种的禁忌症。如果有证据表明目前的神经恶化,包括控制不良的癫痫,应推迟免疫接种,直到病情稳定。有个人或密切家族史的儿童应该注射MMR疫苗。应给出关于任何发热的可能时间和发热管理的建议。医生和护士应该寻求儿科专家的建议,而不是拒绝免疫接种。
不良反应
MMR疫苗后的不良反应(过敏反应除外)是由于疫苗病毒的有效复制以及随后的轻微疾病。这种情况在某些人身上是可以预料的。麻疹成分引起的事件发生在接种疫苗后6至11天。腮腺炎和风疹成分引起的事件通常发生在疫苗接种后2-3周,但也可能发生在疫苗接种后6周。这些事件仅发生在对该成分易感的个体中,因此在第二次和后续剂量后不太常见。出现疫苗相关症状的个体不会传染给他人。
常见事件
接种第一剂MMR疫苗后,可能会出现不适、发热和/或皮疹,最常见的是在免疫接种后约一周,持续约两到三天。在一项对6000多名1至2岁儿童的研究中,所报告的症状在性质、频率、发病时间和持续时间方面与单独接种麻疹疫苗后通常报告的症状相似(Miller et al., 1989)。大约1%的4岁以下儿童出现腮腺肿大,通常发生在第三周。
接种第二剂MMR疫苗后的不良反应比接种第一剂疫苗后少得多。一项研究表明,与未接种疫苗的对照组相比,大学生再次接种疫苗后,发热或皮疹没有增加(Chen et al., 1991)。对1991-1993年通过美国疫苗不良事件报告系统报告的过敏反应进行的分析表明,6-19岁儿童(被认为是第二剂受试者)的过敏反应少于1-4岁儿童(被认为是第一剂受试者)(Chen et al., 1991)。在一项超过8000名儿童的研究中,在4至6岁之间接种第二剂MMR疫苗后的几个月内,惊厥、皮疹或关节痛的风险没有增加(Davis et al., 1997)。
罕见和更严重的事件
热性惊厥是麻疹免疫接种后最常报告的神经系统事件。接种MMR疫苗的1000名儿童中有1名在第6-11天发生癫痫发作——这一比率与接种麻疹疫苗后同期报告的比率相似。MMR后的热性惊厥率低于麻疹感染后的热性惊厥率(Plotkin and Orenstein, 2004)有充分证据表明,与其他原因引起的热性惊厥相比,MMR免疫接种后的热性惊厥不会增加继发癫痫的风险(Vestergaard et al., 2004)。
先前在英国使用的MMR疫苗中的一株腮腺炎病毒(Urabe)与无菌性脑膜炎的风险增加有关(Miller et al., 1993)。该疫苗于1992年被替换(卫生部,1992年),并且不再在英国获得许可。在芬兰进行的一项研究使用了含有不同流行性腮腺炎毒株(Jeryl Lynn)的MMR,类似于目前在英国MMR中使用的MMR,但没有发现MMR和无菌性脑膜炎之间有任何联系(Makela et al., 2002)。
因为MMR疫苗含有减毒活病毒,所以从生物学角度看,它可能导致脑炎。最近在芬兰进行的一项大规模记录关联研究观察了50多万1至7岁的儿童,没有发现MMR和脑炎之间的任何联系(Makela et al., 2002)。
ITP是MMR后可能出现的一种情况,很可能是由风疹成分引起的。这通常发生在六周内,并自行解决。在出生后第二年接受第一剂MMR的儿童中,每22,300名中约有一名出现ITP(Miller et al., 2001)。如果在接种第一剂MMR后6周内出现ITP,则应在接种第二剂疫苗前采血检测麻疹、腮腺炎和风疹抗体(见上文)。
关节病(关节痛或关节炎)也很少在MMR免疫接种后发生,可能是由于风疹成分。如果是由疫苗引起的,应在免疫接种后14至21天出现。如果它发生在其他时间,它极不可能是由疫苗接种引起的。几项对照流行病学研究表明,女性没有患慢性关节炎的额外风险(Slater,1997)。
所有疑似疫苗不良反应发生在儿童身上,或任何年龄的人在接种了标有黑三角(▼)的疫苗后,应使用黄卡计划向人类药物委员会报告。成人对疫苗的严重、可疑不良反应应通过黄卡计划报告。
接种含麻疹、腮腺炎和风疹的疫苗后报告的其他情况
在1994年11月MR免疫接种运动之后,只报告了三例格林-巴利综合征(GBS)。从背景率来看,在此期间该人群中预计会出现1-8例病例。因此,这三个病例很可能是巧合,不是由疫苗引起的。对美洲世卫组织地区急性弛缓性麻痹监测中的GBS报告率进行的分析表明,在开展麻疹免疫接种运动后,8000万儿童接受了免疫接种,GBS发病率没有增加(da Silveira et al., 1997)。在接受900,000剂MMR的人群中,在接种疫苗后的任何时间,GBS的风险都没有增加(Patja et al., 2001)。这一证据驳斥了MMR导致GBS的说法。
尽管有报道称MMR后出现步态障碍,但最近的一项流行病学研究显示,没有证据表明MMR和步态障碍之间存在因果关系(Miller et al., 2005)。
近年来,麻疹疫苗和肠道疾病之间的假设联系已得到调查。与对照组相比,接种含麻疹疫苗的受试者炎症性肠病的发生率没有增加(Gilat et al., 1987;Feeney et al., 1997)。自从芬兰(Pebody et al., 1998)或英国(Seagroatt,2005)引入MMR疫苗接种以来,炎症性肠病的发病率没有增加。
有压倒性的证据表明MMR不会导致自闭症(www.iom. edu/report.asp?id=20155)。在过去的七年里,已经发表了大量关于这个问题的研究。这些研究表明:
- 与未接种MMR的儿童相比,接种MMR的儿童患自闭症的风险没有增加((Farrington et al., 2001; Madsen and Vestergaard, 2004)
在接种MMR疫苗后的时期内,自闭症症状的发作没有聚集性(Taylor et al., 1999; De Wilde et al., 2001; Makela et al., 2002)
- 在英国,报告的自闭症发病率的增加先于MMR的使用(Taylor et al., 1999)
- 1993年后,尽管日本撤销了MMR,自闭症的发病率仍持续上升(Honda et al., 2005)
- 在英国或美国,自闭症发病率和MMR疫苗覆盖率之间没有相关性(Kaye et al., 2001;Dales et al., 2001)
- 接种MMR后出现自闭症的儿童与未接种疫苗的儿童相比,出现自闭症的比例没有差异(Kaye et al., 2001; Dales et al., 2001)
- MMR后出现肠道症状的儿童与未接种疫苗的儿童相比,出现自闭症的比例没有差异(Fombonne, 2001; Taylor et al., 2002; Gillberg and Heijbel, 1998)
- 使用最敏感的方法也无法在自闭症儿童中检测到疫苗病毒(Afzal et al., 2006)。
最新的证据见卫生部网站: www.dh.gov.uk/en/Publichealth/Healthprotection/Immunisation/Keyvaccineinformation/DH_103952
有人认为,MMR联合疫苗可能会使免疫系统超负荷。从出生的那一刻起,人类就在日常生活环境中暴露于无数的外来抗原和传染因子。对MMR中的三种病毒作出反应将仅使用婴儿免疫系统总能力的很小一部分(Offit et al., 2002)。MMR中的三种病毒以彼此不同的速率复制,并且预期在不同的时间达到高水平。
一项检查免疫超负荷问题的研究发现,与其他时间段相比,MMR疫苗接种后不久,严重细菌感染的入院率较低。这表明MMR不会引起免疫系统的任何普遍抑制(Miller et al., 2003)。
病例、接触和暴发的管理
诊断
需要将麻疹、腮腺炎和风疹迅速通知当地卫生保护单位(HPU ),以确保能够迅速采取公共卫生行动。通知应基于临床怀疑,不应等待实验室确认。自1994年以来,很少有临床诊断病例
后来证实是真的麻疹、腮腺炎或风疹。然而,在疾病爆发和流行期间,确诊率确实会增加。
麻疹、流行性腮腺炎和风疹的诊断可以通过无创手段得到确认。理想地,在皮疹或腮腺肿胀发作后的1-6周内检测口腔液(唾液)样品中的特异性IgM,已经显示出对于确认这些感染是高度敏感和特异的(Brown et al., 1994; Ramsay et al., 1991; Ramsay et al., 1998)。建议从所有已通报的病例中获取口腔液样本,大规模流行期间除外。可以从当地的HPU获得有关该程序的建议。
应直接向儿童健康研究所(电话:020 7905 2604)或通过英国儿科监测单位(电话:020 7323 7911)向国家先天性风疹监测计划报告疑似先天性风疹感染的婴儿。
用MMR保护接触
暴露于疑似风疹后,对MMR疫苗风疹成分的抗体反应发展得不够快,不足以提供有效的预防。即使在为MMR提供有效的暴露后预防为时已晚的情况下,疫苗也可以为未来暴露于所有三种感染提供保护。因此,与疑似麻疹、腮腺炎或风疹的接触为以前未接种过MMR疫苗的个体提供了一个很好的机会。如果个人已经在潜伏麻疹、腮腺炎或风疹,接种MMR疫苗不会加剧症状。在这些情况下,应告知个人,接种疫苗后不久发生的风疹样疾病可能是由于自然感染。如果对一个人的疫苗接种状况有疑问,MMR仍然应该进行,因为对已经免疫的人进行疫苗接种不会产生不良影响。
免疫球蛋白接触的保护
人类正常免疫球蛋白通常不用于风疹的暴露后保护,因为没有证据表明它是有效的。不建议用于保护暴露于风疹的孕妇。只有在终止妊娠不可接受的情况下才应考虑。对受者进行血清学随访至关重要。
要防止或减弱攻击:
剂量:750毫克
供应
- MMRVaxPRO®–由赛诺菲巴斯德MSD公司制造。
- Priorix®由葛兰素史克公司生产。
这些疫苗由医疗物流(电话:0870 871 1890)提供,作为国家儿童免疫规划的一部分。
在苏格兰,应该从当地的儿童疫苗储备中心获得供应。详情可从苏格兰保健用品公司(电话:0131 275 6154)获得。
在北爱尔兰,应该从当地的儿童疫苗储备中心获得供应。详情可向区域药品采购处索取(电话:02890 552368)。
人类正常免疫球蛋白
英格兰和威尔士:
健康保护局,传染病中心(电话:020 8200 6868)。
苏格兰:
输血服务(电话:0141 3577700)。
北爱尔兰:
贝尔法斯特市立医院公共卫生实验室(电话:01232 329241)。0
参考
ACIP (1998) Measles, mumps, and rubella – vaccine use and strategies for elimination of
measles, rubella, and congenital rubella syndrome and control of mumps: recommendations
of the Advisory Committee on Immunization Practices (ACIP). MMWR 47(RR-8): 1–57.
www.cdc.gov/mmwr/preview/mmwrhtml/00053391.htm.
Afzal MA, Ozoemena LC, O’Hare A et al. (2006) Absence of detectable measles virus
genome sequence in blood of autistic children who have had their MMR vaccination during
the routine childhood immunisation schedule of the UK. J Med Virol 78: 623–30.
Aickin R, Hill D and Kemp A (1994) Measles immunisation in children with allergy to egg.
BMJ 308: 223–5.
American Academy of Pediatrics (2003) Active immunization. In: Pickering LK (ed.) Red
Book: 2003 Report of the Committee on Infectious Diseases, 26th edition. Elk Grove Village,
IL: American Academy of Pediatrics.
Angel JB, Udem SA, Snydman DR et al. (1996) Measles pneumonitis following measlesmumps-rubella vaccination of patients with HIV infection, 1993. MMWR 45: 603–6.
Best JM, Cooray S and Banatvala JE (2004) Rubella. In: Mahy BMJ and ter Meulen V (eds)
Topley and Wilson’s Virology, 10th edition. London: Hodder Arnold.
Black NA, Parsons A, Kurtz JB et al. (1983) Post-partum rubella immunisation: a controlled
trial of two vaccines. Lancet 2(8357): 990–2.
Bohlke K, Davis RL, Moray SH et al. (2003) Risk of anaphylaxis after vaccination of
children and adolescents. Pediatrics 112: 815–20.
British HIV Association (2006) Immunisation guidelines for HIV-infected adults. BHIVA.
www.bhiva.org/pdf/2006/Immunisation506.pdf
Brown DW, Ramsay ME, Richards AF and Miller E (1994) Salivary diagnosis of measles:
a study of notified cases in the United Kingdom, 1991–3. BMJ 308(6935): 1015–17.
Buimovici-Klein E, Hite RL, Byrne T and Cooper LR (1997) Isolation of rubella virus in
milk after postpartum immunization. J Pediatr 91: 939–43.
Chen RT, Moses JM, Markowitz LE and Orenstein WA (1991) Adverse events following
measles-mumps-rubella and measles vaccinations in college students. Vaccine 9: 297–9.
Clark AT, Skypala I, Leech SC, et al. (2010). British Society for Allergy and Clinical
Immunology guidelines for the management of egg allergy. Clin Exp Allergy 40(8):1116-
29.
Dales L, Hammer SJ and Smith NJ (2001) Time trends in autism and in MMR
immunization coverage in California. JAMA 285(22): 2852–3.
da Silveira CM, Salisbury DM and de Quadros CA (1997) Measles vaccination and
Guillain-Barré syndrome. Lancet 349(9044): 14–16.
Davis RL, Marcuse E, Black S et al. (1997) MMR2 immunization at 4 to 5 years and 10 to
12 years of age: a comparison of adverse clinical events after immunization in the Vaccine
Safety Datalink project. Pediatrics 100: 767–71.
Department of Health (1992) Changes in supply of vaccine. Circular (PL/CMO(92)11).
de Serres G, Boulianne N, Meyer F and Ward BJ (1995) Measles vaccine efficacy during
an outbreak in a highly vaccinated population: incremental increase in protection with age
at vaccination up to 18 months. Epidemiol Infect 115: 315–23.
De Wilde S, Carey IM, Richards N et al. (2001) Do children who become autistic consult
more often after MMR vaccination? Br J General Practice 51: 226–7.
D’Souza RM, Campbell-Lloyd S, Isaacs D et al. (2000) Adverse events following
immunisation associated with the 1998 Australian Measles Control Campaign. Commun
Dis Intell 24: 27–33.
Edgar WM and Hambling MH (1977) Rubella vaccination and anti-D immunoglobulin
administration in the puerperium. Br J Obstet Gynaecol 84(10): 754–7.
Farrington CP, Miller E and Taylor B (2001) MMR and autism: further evidence against a
causal association. Vaccine 19: 3632–5.
Fasano MB, Wood RA, Cooke SK and Sampson HA (1992) Egg hypersensitivity and
adverse reactions to measles, mumps and rubella vaccine. J Pediatr 120: 878–81.
Feeney M, Gregg A, Winwood P and Snook J (1997) A case-control study of measles
vaccination and inflammatory bowel disease. The East Dorset Gastroenterology Group.
Lancet 350: 764–6.
Fombonne E (1998) Inflammatory bowel disease and autism. Lancet 351: 955.
Fombonne E (2001) Is there an epidemic of autism? Pediatrics 107: 411–12.
Fox A and Lack G (2003) Egg allergy and MMR vaccination. Br J Gen Pract 53(495):
801–2.
Freigang B, Jadavji TP and Freigang DW (1994) Lack of adverse reactions to measles,
mumps and rubella vaccine in egg-allergic children. Ann Allergy 73: 486–8.
Gilat T, Hacohen D, Lilos P and Langman MJ (1987) Childhood factors in ulcerative
colitis and Crohn’s disease. An international co-opreative study. Scan J Gastroenterology
22: 1009–24.
Gillberg C and Heijbel H (1998) MMR and autism. Autism 2: 423–4.
Harling R, White JM, Ramsay ME et al. (2005) The effectiveness of the mumps component
of the MMR vaccine: a case control study. Vaccine 23(31): 4070–4.
Health Protection Agency (2006) Measles deaths, England and Wales, by age group, 1980-
2004. www.hpa.org.uk/infections/topics_az/measles/data_death_age.htm
Honda H, Shimizu J and Rutter M (2005) No effect of MMR withdrawal on the incidence
of autism: a total population study. J Child Psychol Psychiatry 46(6): 572–9.
Kaye JA, del Mar Melero-Montes M and Jick H (2001) Mumps, measles and rubella
vaccine and the incidence of autism recorded by general practitioners: a time trend
analysis. BMJ 322(7284): 460–3.
Khakoo GA and Lack G (2000) Recommendations for using MMR vaccine in children
allergic to eggs. BMJ 320: 929–32.
Landes RD, Bass JW, Millunchick EW and Oetgen WJ (1980) Neonatal rubella following
postpartum maternal immunisation. J Pediatr 97: 465–7.
Lokletz H and Reynolds FA (1965) Post-rubella thrombocytopaenic purpura. Report of nine
new cases and review of published cases. Lancet 85: 226–30.
Losonsky GA, Fishaut JM, Strussenberg J and Ogra PL (1982) Effect of immunization
against rubella on lactation products. Development and characterization of specific immunologic reactivity in breast milk. J Infect Dis 145: 654–60.
Madsen KM and Vestergaard M (2004) MMR vaccination and autism: what is the evidence
for a causal association? Drug Saf 27: 831–40.
Makela A, Nuorti JP and Peltola H (2002) Neurologic disorders after measles-mumpsrubella vaccination. Pediatrics 110: 957–63.
Medical Research Council (1977) Clinical trial of live measles vaccine given alone and live
vaccine preceded by killed vaccine. Fourth report of the Medical Research Council by the
measles sub-committee on development of vaccines and immunisation procedures. Lancet
ii: 571–5.
Miller C, Miller E, Rowe K et al. (1989) Surveillance of symptoms following MMR
vaccine in children. Practitioner 233(1461): 69–73.
Miller E, Cradock-Watson JE and Pollock TM (1982) Consequences of confirmed maternal
rubella at successive stages of pregnancy. Lancet 2: 781–4.
Miller EM, Waight P, Vurdein JE et al. (1991) Rubella surveillance to December 1990: a
joint report from the PHLS and National Congenital Rubella Surveillance Programme.
CDR Review 1(4): R33–37.
Miller E, Goldacre M, Pugh S et al. (1993) Risk of aseptic meningitis after measles,
mumps, and rubella vaccine in UK children. Lancet 341(8851): 979–82.
Miller E, Waight P, Farrington P et al. (2001) Idiopathic thrombocytopaenic purpura and
MMR vaccine. Arch Dis Child 84: 227–9.
Miller E, Andrews N, Waight P and Taylor B (2003) Bacterial infections, immune overload,
and MMR vaccine. Measles, mumps, and rubella. Arch Dis Child 88(3): 222–3.
Miller E, Andrews N, Grant A et al. (2005) No evidence of an association between MMR
vaccine and gait disturbance. Arch Dis Child 90(3): 292–6.
Morgan Capner P, Wright J, Miller CL and Miller E (1988) Surveillance of antibody to
measles, mumps and rubella by age. BMJ 297: 770–2.
Morse D, O’Shea M, Hamilton G et al. (1994) Outbreak of measles in a teenage school
population: the need to immunize susceptible adolescents. Epidemiol Infect 113: 355–65.
Mullooly J and Black S (2001) Simultaneous administration of varicella vaccine and other
recommended childhood vaccines – United States, 1995–1999. MMWR 50(47): 1058–61.
Offit PA, Quarles J, Gerber MA et al. (2002) Addressing parents’ concerns: do multiple
vaccines overwhelm or weaken the infant’s immune system? Pediatrics 109(1): 124–9.
Orenstein WA, Markowitz L, Preblud SR et al. (1986) Appropriate age for measles
vaccination in the United States Dev Biol Stand 65: 13–21.
Patja A, Davidkin I, Kurki T et al. (2000) Serious adverse events after measles-mumpsrubella vaccination during a fourteen-year prospective follow-up. Pediatr Infect Dis J19: 1127–34.
Patja A, Paunio M, Kinnunen E et al. (2001) Risk of Guillain-Barré syndrome after measles-mumps-rubella vaccination. J Pediatr 138: 250–4.
Pebody RG, Paunio M and Ruutu P (1998) Measles, measles vaccination, and Crohn’s
disease has not increased in Finland. BMJ 316(7146): 1745–6.
Peltola H, Heinonen OP and Valle M (1994) The elimination of indigenous measles, mumps
and rubella from Finland by a 12-year two-dose vaccination program. NEJM 331(21):
1397–402.
Plotkin SA and Orenstein (eds) (2004) Vaccines, 4th edition. Philadelphia: WB Saunders
Company, Chapters 19, 20 and 26.
Pool V, Braun MM, Kelso JM et al. (2002) Prevalence of anti-gelatin IgE antibodies in
people with anaphylaxis after measles-mumps-rubella vaccine in the United States.
Pediatrics 110(6):e71. www.pediatrics.org/cgi/content/full/110/6/e71
Rahi K, Adams G, Russell-Eggitt I and Tookey P (2001) Epidemiological surveillance of
rubella must continue (letter). BMJ 323: 112.
Ramsay ME, Brown DW, Eastcott HR and Begg NT (1991) Saliva antibody testing and
vaccination in a mumps outbreak. CDR (Lond Engl Rev) 1(9): R96–8).
Ramsay ME, Brugha R, Brown DW et al. (1998) Salivary diagnosis of rubella: a study of
notified cases in the United Kingdom, 1991–4. Epidemiol Infect 120(3): 315–19.
Redd SC, King GE, Heath JL et al. (2004) Comparison of vaccination with measlesmumps-rubella at 9, 12 and 15 months of age. J Infect Dis 189: S116–22.
Seagroatt V (2005) MMR vaccine and Crohn’s disease: ecological study of hospital
admissions in England, 1991 to 2002. BMJ 330: 1120–1.
Slater PE (1997) Chronic arthropathy after rubella vaccination in women. False alarm?
JAMA 278: 594–5.
Taylor B, Miller E, Farrington CP et al. (1999) Autism and measles, mumps and rubella: no
epidemiological evidence for a causal association. Lancet 353(9169): 2026–9.
Taylor B, Miller E, Langman R et al. (2002) Measles, mumps and rubella vaccination and
bowel problems or developmental regression in children with autism; population study.
BMJ 324(7334): 393–6.
Tischer A and Gerike E (2000) Immune response after primary and re-vaccination with
different combined vaccines against measles, mumps, rubella. Vaccine 18(14): 1382–92.
Tookey PA, Jones G, Miller BH and Peckham CS (1991) Rubella vaccination in pregnancy.
CDR London Engl Rev 1(8): R86–8.
Tookey PA and Peckham CS (1999) Surveillance of congenital rubella in Great Britain,
1971–96. BMJ 318: 769–70.
Tookey PA, Cortina-Borja M and Peckham CS (2002) Rubella susceptibility among
pregnant women in North London, 1996–1999. J Public Health Med 24(3): 211–16.
Tookey PA (2004) Rubella in England, Scotland and Wales. Euro Surveill 9: 21–2.
Vestergaard M, Hviid A, Madsen KH et al. (2004) MMR vaccination and febrile seizures.
Evaluation of susceptible subgroups and long-term prognosis. JAMA 292: 351–7.
Vyse AJ, Gay NJ, White JM et al. (2002) Evolution of surveillance of measles, mumps, and
rubella in England and Wales: Providing the platform for evidence based vaccination
policy. Epidemiologic Reviews 24(2): 125–36.
WHO (2005) Vaccine Preventable Diseases Monitoring System. Global summary.
www-nt.who.int/immunization_monitoring/en/globalsummary/countryprofileselect.cfm
Hits: 65

