Nirsevimab预防进入第一个呼吸道合胞病毒季节的婴儿呼吸道合胞病毒相关住院的有效性的早期评估—新的疫苗监测网络,2023年10月至2024年2月
Nirsevimab effectiveness was 90% against RSV-associated hospitalization in infants in their first RSV season
Weekly / March 7, 2024 / 73(9);209–214
总结
关于这个话题已经知道什么?
呼吸道合胞病毒(RSV)是美国婴儿住院的主要原因。2023年8月,CDC推荐长效单克隆抗体nirsevimab用于保护<8个月大的婴儿在第一个RSV季节免受RSV相关的下呼吸道感染。
这份报告增加了什么?
Nirsevimab对第一个RSV季节婴儿RSV相关住院的有效性为90%。从接受nirsevimab到症状发作的中位时间为开始突出显示45天(IQR=19–76)。
对公共卫生实践有何影响?
摘要
呼吸道合胞病毒(RSV)是美国婴儿住院的主要原因。2023年8月,CDC免疫实践咨询委员会建议<8个月大的婴儿在第一个RSV季节和8-19个月大的儿童使用长效单克隆抗体nirsevimab,以预防RSV相关的下呼吸道感染,以预防RSV相关下呼吸道感染。在3期临床试验中,nirsevimab在收到后150天内对住院时RSV相关下呼吸道感染的疗效为81%(95%CI=62%–90%);美国尚未评估引入后的有效性。在这项分析中,新疫苗监测网络评估了nirsevimab对2023年10月1日至2024年2月29日期间第一个RSV季节婴儿RSV相关住院治疗的有效性。在699例因急性呼吸系统疾病住院的婴儿中,59例(8%)在症状出现前≥7天接受了nirsevimab。Nirsevimab对RSV相关住院治疗的有效性为90%(95%CI=75%-96%),从收到到出现症状的中位时间为45天(IQR=19-76天)。接受nirsevimab治疗的婴儿数量太少,无法按接受治疗后的持续时间进行分层;然而,由于抗体衰变,预计Nirsevimab的有效性会随着接受后时间的增加而降低。尽管在本分析中,nirsevimab的摄取和接受nirsevimab的间隔有限,但这一早期估计支持了目前nirsevimab预防婴儿严重RSV疾病的建议。婴儿应通过母体RSV疫苗接种或婴儿接受nirsevimab来保护。
介绍
呼吸道合胞病毒(RSV)是美国婴儿住院的主要原因,每年导致50,000-80,000例<5岁儿童住院(1,2)。住院率最高,发生在出生后的头几个月,随着婴儿期和儿童早期年龄的增长,风险下降(3)。2023年8月,CDC免疫实践咨询委员会(ACIP)建议将长效单克隆抗体nirsevimab用于所有在第一个RSV季节出生或进入RSV季节的<8个月大的婴儿,以及8-19个月大且患严重RSV疾病风险增加并进入第二个RSV季节的儿童(4)。在对许可前随机安慰剂对照临床试验数据的汇总分析中,在<8月龄时给予1剂nirsevimab对就诊的RSV相关下呼吸道感染的有效率为79%,对注射后150天内住院治疗的RSV相关下呼吸道感染的有效率为81%(4).2023年9月,母体RSV疫苗也可用于预防幼儿RSV疾病。ACIP建议使用nirsevimab或母体RSV疫苗,以保护在RSV季节或进入第一个RSV季节出生的婴儿(5)。2023年10月,为应对nirsevimab短缺,CDC建议nirsevimab供应有限的医疗机构优先将nirsevimab用于<6个月大的婴儿和患有严重疾病风险最高的基础疾病的婴儿(6)。2024年1月,更多剂量的nirsevimab上市,CDC建议提供充足nirsevimab供应的医疗机构恢复到ACIP对nirsevimab使用的原始建议(7)。该分析首次在美国婴儿的第一个RSV季节中对nirsevimab引入后的有效性进行了估计。
方法
数据收集和纳入标准
新疫苗监测网络(NVSN)是一个基于人群的前瞻性<18岁婴儿、儿童和青少年急性呼吸道疾病(ARI)监测平台,在美国七个儿科学术医疗中心监测儿科呼吸道病毒,以评估免疫效果。†人口统计学、临床和免疫数据是通过父母/监护人访谈、病历提取和州免疫信息系统地收集的。从入组儿童中收集呼吸道标本,并通过实时逆转录-聚合酶链反应检测RSV和其他常见呼吸道病毒。nirsevimab的接收是通过家长报告确定的,并通过州免疫信息系统、出生医院或初级保健提供者记录进行验证。§¶
如果婴儿在2023年10月1日或2023年10月1日之后出生<8个月,在2023年10月1日至2024年2月29日期间因ARI**住院,并且已验证nirsevimab状态、报告出生时胎龄和病历审查以评估潜在的医疗状况,则他们有资格进行此分析。如果婴儿在nirsevimab在其站点可用之前就已入组,则被排除在外,††接受过任何剂量的帕利珠单抗,在怀孕期间报告了母体RSV疫苗接种,或不确定或未知的RSV检测结果。对于纳入该分析的部位,至少有五名在该部位登记的婴儿必须在症状出现前≥7天接受过nirsevimab。
数据分析
Nirsevimab对RSV相关住院的有效性使用检测阴性的病例对照设计进行估计。病例患者为RSV检测结果呈阳性的婴儿。对照组患者是RSV检测结果为阴性的婴儿。如果婴儿在症状出现前≥7天接受nirsevimab,以考虑RSV潜伏期和达到峰值抗体浓度的时间,则认为婴儿是nirsevimab接受者。在症状出现前<7天接受nirsevimab治疗的婴儿被排除在外。Pearson的卡方检验用于比较病例患者和对照患者以及nirsevimab状态的人口统计学特征。使用多变量logistic回归模型估计有效性,比较病例患者和对照患者接受nirsevimab的几率。回归模型控制了入组时的年龄(以月、患病月份、入组地点为单位)以及存在一种或多种严重RSV疾病的高危医疗条件。早产状态(<28、28-31、32-33、34-36和≥37周出生)和保险类型被评估为潜在的混杂因素,但没有改变估计值,也没有纳入最终模型。有效性计算为(1−调整后的比值比)×100%。使用SAS软件(版本9.4;SAS研究所)。此活动已由CDC审查,被视为非研究,并且根据适用的联邦法律和CDC政策进行。§§¶¶
结果
在1,036名符合条件的婴儿中,四个地点的699名婴儿符合纳入标准,†††包括407例(58%)病例患者和292例(42%)对照患者(表)。与没有这些疾病的婴儿相比,患有高危疾病的婴儿接受nirsevimab的频率更高(46% vs 6%,p<0.001)。按早产状态或保险类型,接受nirsevimab的频率没有差异。从接受nirsevimab到ARI症状出现的时间从7天到127天不等,中位时间为45天(IQR=19-76天)(图)。总体而言,6例(1%)病例患者和53例(18%)对照患者接受了nirsevimab治疗;在所有纳入的婴儿中,按部位划分,Nirsevimab的接受率为4%至12%。Nirsevimab对RSV相关住院治疗的有效性为90%(95%CI=75-96)。
讨论
在这项对699名在第一个RSV季节因ARI住院的婴儿进行的多中心分析中,在接受nirsevimab到ARI症状发作的中位时间为45天时,接受nirsevimab对RSV相关住院治疗的有效率为90%。这一早期有效性估计支持了在婴儿的第一个RSV季节预防严重RSV疾病的现有建议。
这项对美国引入后nirsevimab有效性的首次估计的优势包括使用标准化ARI定义招募婴儿、系统RSV检测以及接受所有婴儿的州免疫信息系统或医疗记录的nirsevimab验证。然而,需要注意的是,在整个RSV季节中,nirsevimab的有效性预计将低于此处报告的估计值,因为被动免疫的抗体水平会随着时间的推移而减弱。在这项分析中,接受nirsevimab的中位间隔为45天,而COVID-19大流行之前美国RSV季节的中位持续时间为189天(8)。在临床试验中,nirsevimab在接受nirsevimab后150天内对婴儿的RSV相关下呼吸道感染仍然非常有效,与延长的半衰期63-73天一致(9)。
在真实世界条件下,评估RSV季节整个持续时间的有效性,以及建议在第二个RSV季节之前接受nirsevimab治疗的8-19个月重症RSV疾病高风险儿童的有效性仍然很重要。因此,CDC将继续监测nirsevimab的有效性。
局限性
本报告中的调查结果至少受到五项限制。首先,只有一小部分患有ARI的住院婴儿接受了nirsevimab,部分原因可能是在引入的第一个季节延迟供应和间歇性供应短缺,并且接受nirsevimab的婴儿更有可能患有基础疾病。因此,结果可能无法完全推广到所有有资格在第一个RSV季节接受nirsevimab的婴儿。其次,接受nirsevimab治疗的病例患者数量较少,因此无法按接受nirsevimab治疗后的时间进行分层估计。第三,由于nirsevimab在美国的大多数地点都是在季节性RSV传播开始后才开始可用的,因此本分析中的一些婴儿可能在接受nirsevimab之前已经感染了RSV,这可能会影响估计的疗效。第四,由于无法确定nirsevimab的剂量,因此没有通过剂量(体重<5公斤的婴儿为50mg或体重≥5公斤的婴儿为100mg)来估计nirsevimab的有效性。最后,本报告中的有效性估计仅限于预防RSV相关住院治疗。婴儿中的呼吸道合众神经病毒(RSV)也会导致门诊和急诊就诊人数大幅增加;有必要进行其他研究来评估Nirsevimab对这些结局的有效性。§§§
对公共卫生实践的影响
在进入第一个RSV季节的婴儿中,接受单剂量的nirsevimab对RSV相关住院非常有效。这一发现支持了目前CDC的建议,即所有婴儿都应通过母体RSV疫苗接种或婴儿接受nirsevimab来保护,以降低RSV相关住院风险(4,6)。
新的疫苗监测网络产品有效性合作者
美国疾病预防控制中心国家免疫和呼吸系统疾病中心冠状病毒和其他呼吸道病毒部门RuthLink-Gelles;AmandaPayne,CDC国家免疫和呼吸系统疾病中心冠状病毒和其他呼吸道病毒部门;RyanWiegand,CDC国家免疫和呼吸系统疾病中心冠状病毒和其他呼吸道病毒部门;XimenaAguileraCorrea,范德比尔特大学医学中心儿科;克劳迪娅·格瓦拉·普利多(ClaudiaGuevaraPulido),范德比尔特大学医学中心儿科;汉娜·格里奥尼(HannaGrioni),西雅图儿童医院儿科;BonnieStrelitz,西雅图儿童医院儿科;VasanthiAvadhanula,贝勒医学院;FlorM.Munoz,德克萨斯儿童医院和贝勒医学院;WendeFregoe,罗切斯特大学医学中心和罗切斯特大学戈利萨诺儿童医院儿科;SaranyaPeri,堪萨斯城儿童慈善院病理学和检验医学系;AnjanaSasidharan,堪萨斯城儿童慈善院病理学和检验医学系;莫妮卡·约翰逊(MonikaJohnson),儿科,匹兹堡大学医学院;KlancieDauer,匹兹堡大学医学院儿科系。
通讯作者:HeidiL.Moline, ick6@cdc.gov.
*这些资深作者对本报告的贡献同样大。
†密苏里州堪萨斯城儿童慈善医院;俄亥俄州辛辛那提市辛辛那提儿童医院医疗中心;纽约州罗切斯特市戈利萨诺儿童医院;华盛顿州西雅图市西雅图儿童医院;德克萨斯州休斯顿德克萨斯儿童医院;宾夕法尼亚州匹兹堡匹兹堡UPMC儿童医院;范德比尔特大学医学中心,田纳西州纳什维尔。
§所有登记的儿童都接受了以下病毒检测:腺病毒、SARS-CoV-2、鼻病毒/肠道病毒、RSV、人类偏肺病毒、肠道病毒-D68、副流感病毒、人类冠状病毒和流感病毒。
¶初级保健提供者记录验证是在未强制向州免疫信息系统报告nirsevimab给药的地点进行的。
**ARI定义为在入组前<14天内出现以下一种或多种体征或症状:发烧、咳嗽、耳痛、鼻塞、流鼻涕、喉咙痛、咳嗽后呕吐、喘息、呼吸急促、呼吸急促或呼吸浅、呼吸暂停、明显的危及生命的事件或短暂的无法解释的事件。
††2023年:德克萨斯州休斯顿,10月5日;田纳西州纳什维尔,10月8日;华盛顿州西雅图,10月8日;俄亥俄州辛辛那提,10月10日;密苏里州堪萨斯城,11月1日;宾夕法尼亚州匹兹堡,11月2日;纽约州罗切斯特,11月6日。
§§在临床试验中,成人在肌肉注射后第6天达到峰值中和抗体浓度水平。https://www.accessdata.fda.gov/drugsatfda_docs/label/2023/761328s000lbl.pdf
¶¶高危疾病被定义为早产儿慢性肺病(支气管肺发育不良、闭塞性细支气管炎、慢性呼吸衰竭伴持续气道正压通气/双水平气道正压通气/呼吸机、肺动脉高压或间质性肺病)(11);血流动力学显着的先天性心脏病(主动脉弓异常、左心发育不良综合征、肺动脉闭锁、三尖瓣闭锁、法洛四联症、大动脉转位、部分或全部肺静脉回流异常、心脏瓣膜其他异常、右心室双出口或其他严重先天性心脏畸形)(21);严重免疫功能低下(1例);严重囊性纤维化(2例);神经肌肉疾病(自主神经功能障碍、不稳定或自主神经功能障碍、胼胝体发育不全或发育不全、肌营养不良或脊髓性肌萎缩症、张力障碍或其他神经肌肉疾病)(11);或先天性肺部异常,损害清除分泌物的能力(无)。
45C.F.R.第46部分、21C.F.R.第56部分;42U.S.C.第241(d)条;5U.S.C.第552a条;44U.S.C.Sect.3501etseq.
†††在被排除在该分析之外的337名婴儿中,排除的原因包括在接受nirsevimab治疗的婴儿少于5名的地点入组(来自罗切斯特、辛辛那提和堪萨斯城的296名)、在症状发作前7天接受nirsevimab<20)、RSV检测结果缺失或不确定(20)、母亲在怀孕期间接受RSV疫苗(22)、以及帕利珠单抗的接受(10);排除的原因并不相互排斥。
§§§ https://www.cdc.gov/vaccines/imz-managers/coverage/rsvvaxview/index.html(2024年1月30日访问)。
引用
1.SuhM,MovvaN,江X,etal.呼吸道合胞病毒是2009-2019年美国婴儿住院的主要原因:全国(全国)住院患者样本研究。J感染Dis2022;226(增刊2):S154–63。https://doi.org/10.1093/infdis/jiac120 PMID:35968878
2.HallCB、WeinbergGA、IwaneMK等。幼儿呼吸道合胞病毒感染的负担。NEnglJMed2009年;360:588–98.https://doi.org/10.1056/NEJMoa0804877 PMID:19196675
3.CurnsAT、RhaB、LivelyJY等。呼吸道合胞病毒相关儿童<5岁住院:2016年至2020年。儿科2024;153:e2023062574。https://doi.org/10.1542/peds.2023-062574 PMID:38298053
4.JonesJM、Fleming-DutraKE、PrillMM等。使用nirsevimab预防婴幼儿呼吸道合胞病毒病:免疫实践咨询委员会的建议——美国,2023年。MMWRMorbMortalWkly代表2023;72:920–5.https://doi.org/10.15585/mmwr.mm7234a4 PMID:37616235
5.Fleming-DutraKE、JonesJM、RoperLE等。怀孕期间使用辉瑞呼吸道合胞病毒疫苗预防婴儿呼吸道合胞病毒相关下呼吸道疾病:免疫实践咨询委员会的建议——美国,2023年。MMWRMorbMortalWkly代表2023;72:1115–22.https://doi.org/10.15585/mmwr.mm7241e1 PMID:37824423
6.CDC.应急准备和响应:nirsevimab在美国的供应有限——CDC在2023-2024年呼吸道病毒季节保护婴儿免受呼吸道合胞病毒(RSV)侵害的临时建议。佐治亚州亚特兰大:美国卫生与公众服务部,CDC;2023. https://emergency.cdc.gov/han/2023/han00499.asp
7.CDC.COCANow:在2023-2024年呼吸道病毒季节,为增加nirsevimab供应以保护幼儿免受严重呼吸道合胞病毒(RSV)的侵害,更新了医疗保健提供者指南。佐治亚州亚特兰大:美国卫生与公众服务部,CDC;2024. https://emergency.cdc.gov/newsletters/coca/2024/010524a.html
8.哈米德S、温恩A、帕里克R等人。呼吸道合胞病毒的季节性——美国,2017-2023年。MMWRMorbMortalWkly代表2023;72:355–61.https://doi.org/10.15585/mmwr.mm7214a1 PMID:37022977
9.HammittLL,DaganR,YuanY,etal.;MELODY研究小组。Nirsevimab用于预防健康晚期早产儿和足月儿的RSV。NEnglJMed2022;386:837–46.https://doi.org/10.1056/NEJMoa2110275 PMID:35235726
表.根据呼吸道合胞病毒检测结果和接受nirsevimab,在第一个呼吸道合胞病毒季节出生或进入第一个呼吸道合胞病毒季节并因急性呼吸道疾病住院的婴儿的特征*,†—新的疫苗监测网络,2023年10月至2024年2月
| 特征 | 总人数(%) | RSV检测结果 | 使用nirsevimab | ||||
|---|---|---|---|---|---|---|---|
| 阳性数(%) | 阴性数 (%) | p值§ | 是(%) | 不 (%) | p值§ | ||
| 所有儿童 | 699 | 407(58) | 292(42) | — | 59(8) | 640(92) | — |
| 入组时的年龄,月龄 | |||||||
| <1 | 111(16) | 51(13) | 60(21) | <0.001 | 10(9) | 101(91) | 0.028 |
| 1–2 | 214(31) | 144(35) | 70(24) | 18(8) | 196(92) | ||
| 3–4 | 131(19) | 90(22) | 41(14) | 9(7) | 122(93) | ||
| 5–6 | 121(17) | 67(16) | 54(18) | 6(5) | 115(95) | ||
| 7–8 | 96(14) | 49(12) | 47(16) | 9(9) | 87(91) | ||
| 9–10 | 23(3) | 6(1) | 17(6) | 6(26) | 17(74) | ||
| 11–12 | 3(0) | 0(—) | 3(1) | 1(33) | 2(67) | ||
| 胎龄 | |||||||
| 早产儿(<37周)¶ | 146(21) | 77(19) | 69(24) | 0.129 | 15(10) | 131(90) | 0.377 |
| 期限(≥37周) | 551(79) | 329(81) | 222(76) | 44(8) | 507(92) | ||
| 未知 | 2(0) | 1(0) | 1(0) | 0(—) | 2(100) | ||
| 高危医疗状况** | |||||||
| 没有 | 660(94) | 396(97) | 264(90) | <0.001 | 41(6) | 619(94) | <0.001 |
| ≥1 | 39(6) | 11(3) | 28(10) | 18(46) | 21(54) | ||
| 性 | |||||||
| 女性 | 293(42) | 182(45) | 111(38) | 0.076 | 28(10) | 265(90) | 0.367 |
| 雄 | 406(58) | 225(55) | 181(62) | 31(8) | 375(92) | ||
| 种族和民族†† | |||||||
| 美洲印第安人或阿拉斯加原住民 | 1(0) | 1(0) | 0(—) | 0.002 | 0(—) | 1(100) | 0.511 |
| 亚裔 | 47(7) | 27(7) | 20(7) | 3(6) | 44(94) | ||
| 黑人或非裔美国人 | 89(13) | 41(10) | 48(16) | 8(9) | 81(91) | ||
| 夏威夷原住民或其他太平洋岛民 | 225(32) | 126(31) | 99(34) | 23(10) | 202(90) | ||
| 白 | 30(4) | 12(3) | 18(6) | 5(17) | 25(83) | ||
| 西班牙裔或拉丁裔 | 8(1) | 3(1) | 5(2) | 0(—) | 8(100) | ||
| 多种族或其他非指定 | 280(40) | 188(46) | 92(32) | 18(6) | 262(94) | ||
| 未知 | 19(3) | 9(2) | 10(3) | 2(11) | 17(89) | ||
| 保险状况 | |||||||
| 公共 | 385(55) | 198(49) | 187(64) | <0.001 | 37(10) | 348(90) | 0.296 |
| 私人 | 233(33) | 155(38) | 78(27) | 17(7) | 216(93) | ||
| 公共和私人 | 4(1) | 2(0) | 2(1) | 1(25) | 3(75) | ||
| 自费(无) | 51(7) | 31(8) | 20(7) | 4(8) | 47(92) | ||
| 未知 | 26(4) | 21(5) | 5(2) | 0(—) | 26(100) | ||
| 网站 | |||||||
| 德克萨斯州休斯顿 | 195(28) | 110(27) | 85(29) | 0.050 | 24(12) | 171(88) | 0.013 |
| 田纳西州纳什维尔 | 93(13) | 47(12) | 46(16) | 9(10) | 84(90) | ||
| 宾夕法尼亚州匹兹堡 | 235(34) | 153(38) | 82(28) | 9(4) | 226(96) | ||
| 华盛顿州西雅图 | 176(25) | 97(24) | 79(27) | 17(10) | 159(90) | ||
| 呼吸道合胞病毒检测结果 | |||||||
| 阳性 | 407(58) | NA | NA | — | 6(1) | 401(99) | <0.001 |
| 阴性 | 292(42) | NA | NA | 53(18) | 239(82) | ||
缩写:BPAP=双水平气道正压通气;CPAP=持续气道正压通气;NA=不适用;RSV=呼吸道合胞病毒。
*总体而言,在分析期间登记的337名婴儿被排除在外。排除原因包括在接受nirsevimab治疗的婴儿少于5名的地点入组(来自罗切斯特、辛辛那提和堪萨斯城的296名)、在症状发作前<7天接受nirsevimab治疗(20例)、RSV检测结果缺失或不确定(20例)、母亲在怀孕期间接受RSV疫苗(22例)和接受帕利珠单抗治疗(10例);排除的原因并不相互排斥。
†登记处或提供者记录的当季nirsevimab接收(654:94%)或仅记录(45:6%)。
Pearson的卡方检验用于比较病例患者和对照患者的人口统计学特征,以及接受nirsevimab。
<28周(12:2%);28-31周(12:2%);32-33周(48:7%);34-36周(74:11%)。
**高危医疗状况被定义为早产儿慢性肺病(支气管肺发育不良、闭塞性细支气管炎、CPAP/BIPAP/呼吸机慢性呼吸衰竭、肺动脉高压[新生儿、原发性或继发性]或间质性肺病)(12);血流动力学显着的先天性心脏病(主动脉弓异常、左心发育不良综合征、肺动脉闭锁、三尖瓣闭锁、法洛四联症、大动脉转位、部分或全部肺静脉回流异常、心脏瓣膜、右心室双出口或其他先天性心脏畸形)(21);严重免疫功能低下(1例);严重囊性纤维化(2例);神经肌肉疾病(自主神经功能障碍、不稳定或自主神经功能障碍、胼胝体发育不全或发育不全、肌肉萎缩症或脊髓性肌萎缩症、张力障碍或其他神经肌肉疾病)(12);或先天性肺部异常,损害清除分泌物的能力(无)。§¶
††西班牙裔或拉丁裔(西班牙裔)血统的人可能属于任何种族,但被归类为西班牙裔;所有种族群体都是非西班牙裔。
图.根据呼吸道合胞病毒检测结果,在第一个呼吸道合胞病毒季节出生或进入第一个呼吸道合胞病毒季节并因急性呼吸道疾病住院的婴儿从接受nirsevimab*到出现症状的时间—新疫苗监测网络,2023年10月至2024年2月
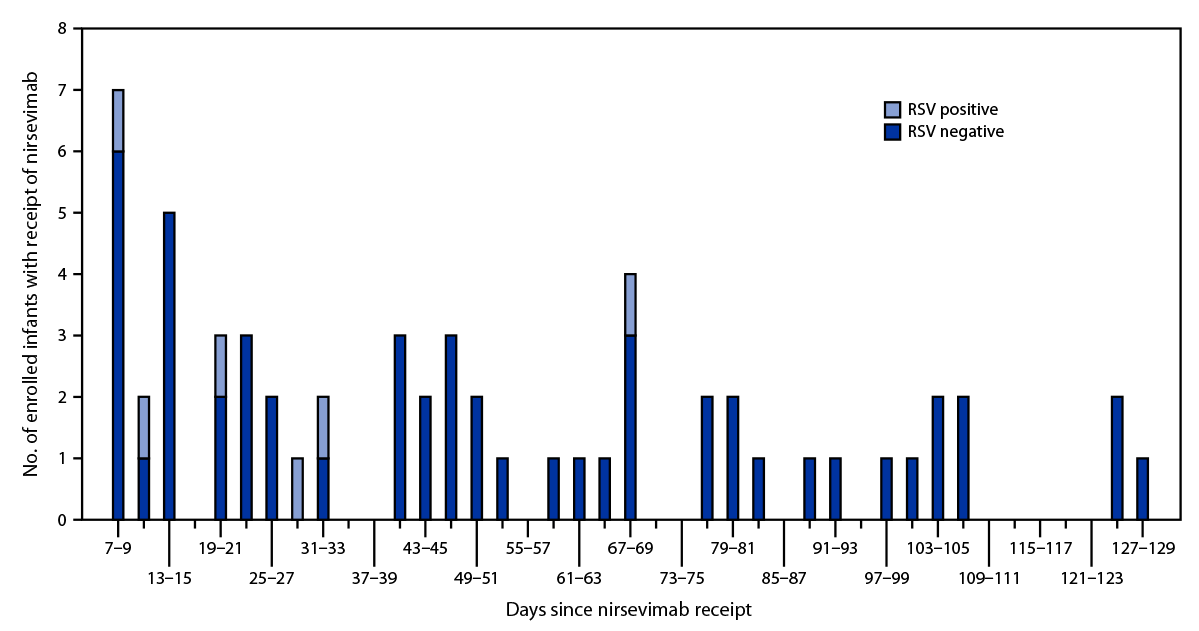
缩写:RSV=呼吸道合胞病毒。
*不包括第0-6天,因为在症状出现后7天内接受nirsevimab的婴儿被排除在该分析之外。
本文的建议引用:Moline HL, Tannis A, Toepfer AP, et al. Early Estimate of Nirsevimab Effectiveness for Prevention of Respiratory Syncytial Virus–Associated Hospitalization Among Infants Entering Their First Respiratory Syncytial Virus Season — New Vaccine Surveillance Network, October 2023–February 2024. MMWR Morb Mortal Wkly Rep 2024;73:209–214. DOI: http://dx.doi.org/10.15585/mmwr.mm7309a4.
最后审核日期:2024年3月7日
资料来源:美国疾病控制与预防中心
Hits: 35
