The hepatitis E virus: New insights into targeted treatment and diagnosis
2月 16, 2024
戊型肝炎病毒:靶向治疗和诊断的新见解
戊型肝炎病毒(HEV)引起的肝脏炎症的常见症状包括发烧、腹痛、大便苍白、恶心和黄疸。有这种感染风险的个体包括免疫系统较弱(免疫功能低下)的人以及孕妇。免疫功能低下的患者经常患有慢性感染,这对全球北方来说是一个更大的问题。
孕妇经常患有严重病例(暴发性肝炎)。这种类型的肝炎与高达30%的死亡率有关,主要发生在全球南方。地理差异可以解释为人畜共患的食源性戊型肝炎病毒株(基因型3和4)主要在北部传播,而主要在水传播的基因型1和2分布在南部。
到目前为止,欧洲尚未批准针对戊型肝炎病毒的疫苗。尽管有用于治疗感染的药物,但治疗选择仍然有限,并且与强烈的副作用或耐药性的发展有关。这也是由于缺乏对病毒生命周期的大部分了解。
病毒多蛋白 pORF1——病毒基因组产生的核心,但几乎不为人知
HEV遗传信息的复制(基因组复制)是通过病毒多蛋白pORF1介导的。该蛋白质由多个结构域组成。蛋白质结构域是蛋白质内的稳定折叠结构,在功能和结构上独立于相邻的蛋白质片段。
pORF1是复制(复制酶)的中心蛋白,这意味着它负责病毒遗传信息的繁殖。然而,人们对pORF1知之甚少,包括其在感染细胞中的确切位置。
由Mirco Glitscher博士领导的研究人员在Paul-Ehrlich研究所病毒学部门负责人Eberhard Hildt教授的工作组中专注于这种重要的未知HEV元素。在他们的研究中,他们使用共聚焦激光扫描显微镜来分析pORF1及其各个结构域的亚细胞定位,这些结构域是在病毒复制酶的结构预测的基础上生成和克隆的。
使用超速离心分离从细胞中释放的外泌体,并通过等密度(根据相同密度分离)密度梯度离心进行分析。然后通过荧光法、蛋白质印迹分析或RT-qPCR更仔细地检查分离的颗粒。
囊泡系统是病毒繁殖的基石
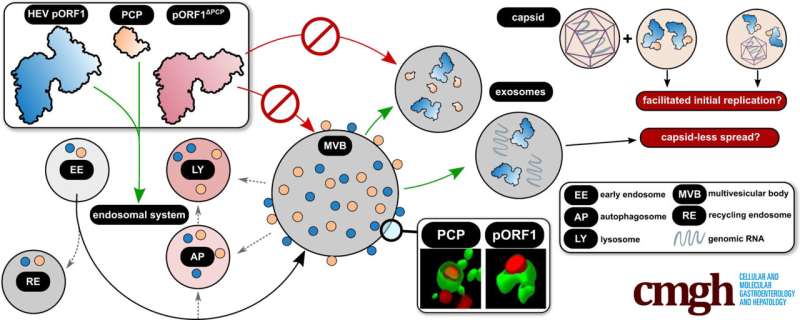
研究小组发现,pORF1在细胞的囊泡系统(内体系统)中积累,主要在多囊泡体(MVB)中积累。这些结构是外泌体形成的核心,迄今为止仅被视为释放病毒HEV颗粒的宿主结构。这里病毒复制酶的存在被鉴定为依赖于 pORF1 结构域,即 PCP(木瓜蛋白酶样半胱氨酸蛋白酶)。
因此,研究小组发现病毒复制酶也通过外泌体释放。该过程由作为复制酶一部分的病毒蛋白酶介导。因此,即使在没有病毒颗粒的情况下,病毒基因组也会通过这种途径释放。
研究结果表明,pORF1以PCP依赖性方式进入MVB,随后释放外泌体。因此,病毒的释放和复制,遗传信息的繁殖,可能在空间上是耦合的。这可能会促进病毒感染的传播,因为在再次感染期间进入细胞的基因组可以迅速遇到外泌体传播的pORF1并被复制。此外,收集的数据表明,衣壳不一定是遗传物质释放所必需的。
外泌体和相关蛋白质结构可能是治疗HEV的合适靶标,因为这可能会阻止病毒复制和病毒释放。HEV基因组的衣壳非依赖性释放肯定会对诊断产生影响,因为迄今为止一直认为病毒颗粒和病毒基因组的数量存在相关性。
然而,当涉及到诊断程序时,仍然必须研究没有衣壳的外泌体中存在基因组RNA的相关性。
该研究发表在《细胞和分子胃肠病学和肝病学》杂志上。
更多信息:Mirco Glitscher 等人,HEV pORF1 中的蛋白酶结构域介导复制酶对多泡小体的定位及其外泌体释放,细胞和分子胃肠病学和肝病学 (2024)。DOI: 10.1016/j.jcmgh.2024.01.001
Hits: 31
