Contents
Universal HepatitisB Vaccination in Adults Aged 19–59 Years:Updated Recommendations of the Advisory CommitteeonImmunization Practices—United States,2022
MarkK.Weng,医学博士1;莫娜·多沙尼,医学博士1;MohammedA.Khan,博士1;莎伦·弗雷,医学博士2;凯文·奥尔特,医学博士3;凯利·摩尔(KellyL.Moore),医学博士4;EricW.Hall,博士5;RebeccaL.Morgan,博士6;道格·坎波斯-奥特卡特,医学博士7;卡罗琳·韦斯特,医学博士1;NoeleP.Nelson,医学博士,博士1 (查看作者单位)
总结
关于这个话题已经知道什么?
接种乙型肝炎(HepB)疫苗显示出公认的安全性和有效性。然而,由于先前的疫苗接种建议中基于风险因素的方法,成人的覆盖率一直不理想。
此报告增加了哪些内容?
除了已经建议接种乙肝疫苗的人群外,免疫实践咨询委员会还建议所有19-59岁的成年人都应接种乙肝疫苗。
对公共卫生实践有何影响?
在59岁之前,普遍接种成人乙肝疫苗消除了对危险因素筛查和披露的需要,可以提高疫苗接种覆盖率并减少乙型肝炎病例。
乙型肝炎(HepB)疫苗在过去4年中已证明安全性、免疫原性和有效性(1,2)。然而,成人疫苗接种覆盖率一直不理想,限制了美国乙型肝炎病毒(HBV)感染的进一步减少。免疫实践咨询委员会(ACIP)的这项建议扩大了普遍接种HepB疫苗的指示年龄范围,现在包括19-59岁的成年人。取消先前建议用于确定该成人年龄组疫苗资格的危险因素评估(2)可以提高疫苗接种覆盖率并减少乙型肝炎病例。
背景
乙型肝炎是由乙型肝炎病毒引起的一种可通过疫苗预防的肝脏传染病。乙型肝炎病毒通过经皮(即穿刺皮肤)或黏膜(即直接接触粘膜)暴露于感染性血液或体液传播。自1982年推出乙肝疫苗以来,报告的乙型肝炎病例数已大幅下降。然而,尽管在过去四十年中乙型肝炎发病率有所下降,这是通过逐步扩大建议接种乙肝疫苗的群体来实现的,但近年来在进一步减少急性乙型肝炎病例方面的进展停滞不前(3)。乙型肝炎事件从1985年的26,654例报告病例(估计实际病例172,700例)下降到2014年的2,791例报告病例(估计实际病例18,100例)(3,4)。2019年,向CDC报告了3,192例急性乙型肝炎病例,相当于20,700例估计急性感染(95%CI=11,800–50,800)。最常报告的风险行为和暴露是注射吸毒(35%)、多个性伴侣(23%)和手术(10%),其次是其他性风险行为和血源性风险行为;37.1%的病例缺少风险行为和暴露信息。根据2013-2018年美国国家健康和营养检查调查数据,美国估计有880,000例(95%CI=580,000-1,170,000)流行的慢性HBV感染,模型估计为189万(范围=1.49-2.40万),这说明了非美国出生人口的代表性可能不足(5,6).2018年,≥19岁成年人报告的乙肝疫苗接种覆盖率(≥3剂)为30.0%,在过去40年中仅略有增加(7)。
方法
2019年9月至2021年10月期间,ACIP*肝炎工作组†(工作组)每月举行一次电话会议,审查和讨论与在普遍成人疫苗接种建议中使用HepB疫苗相关的科学证据。工作组确定了以下值得评估的结局:乙型肝炎发病率、乙型肝炎相关发病率、乙型肝炎相关死亡率以及与疫苗相关的严重不良事件。根据2020年9月10日完成的文献系统综述的结果,总结了关于普遍HepB疫苗接种结果和安全性的数据,并于2021年9月20日更新。工作组使用建议分级评估、开发和评估(GRADE)方法,评估了与美国许可的HepB疫苗相关的结果水平的证据质量,这些证据适用于所有以前未接种过HBV感染疫苗的成年人。方法和结果的详细说明可在GRADE证据概况(https://www.cdc.gov/vaccines/acip/recs/grade/hepb-adults.html)中找到。在GRADE评估之后,使用证据到建议(EtR)框架(https://www.cdc.gov/vaccines/acip/recs/grade/hepb-adults-etr.html)做出决定。
在2021年7月至2022年2月期间,工作组参加了三次电话会议,以审查PreHevbrio的血清保护和安全性证据,PreHevbrio是一种三抗原3剂HepB疫苗,于2021年获得美国食品和药物管理局(FDA)新批准。方法和结果的描述可用于GRADE证据(https://www.cdc.gov/vaccines/acip/recs/grade/prehevbrio-hepb.html)和EtR框架(https://www.cdc.gov/vaccines/acip/recs/grade/prehevbrio-hepb-etr.html)。
主要调查结果摘要
从2006年1月1日至2020年9月10日,使用PubMed、Medline、Embase、CINAHL和Cochrane图书馆数据库对科学文献进行了系统评价。搜索词包括“乙型肝炎疫苗”、“成人”、“常规”和“通用”。为了有资格被纳入该评价,一项研究必须讨论成人HepB疫苗接种。如果研究没有针对成年人群,是非英语语言的,讨论的乙肝疫苗未在美国获得许可,或者数据无法提取,则被排除在外。检索确定了3,226项研究,其中263项被认为是合格的,并为本综述提供了信息。报告的急性乙型肝炎发病率在10多年内没有明显下降,2019年估计有20,700例感染(3,4)。在比较普遍和基于风险的成人乙肝疫苗接种时,没有一项确定的研究报告乙型肝炎的发病率、发病率和死亡率。单抗原3剂HepB疫苗的安全性已经确定(1,2)。PreHevbrio于2021年获得FDA批准,并于2022年获得ACIP推荐。与3剂单抗原疫苗(Engerix-B)相比,PreHevbrio在血清保护或严重不良事件或轻度不良事件的发生率方面几乎没有差异(GRADE证据类型3;低质量证据),两种疫苗的严重不良事件都很少见。2剂HepB疫苗(Heplisav-B)于2017年获得FDA批准,并于2018年获得ACIP推荐。与3剂疫苗(Engerix-B)相比,Heplisav-B在严重不良事件的发生率(GRADE证据类型1;高质量证据)方面没有差异,两种疫苗的严重不良事件都很少见(8,9).
建议的理由
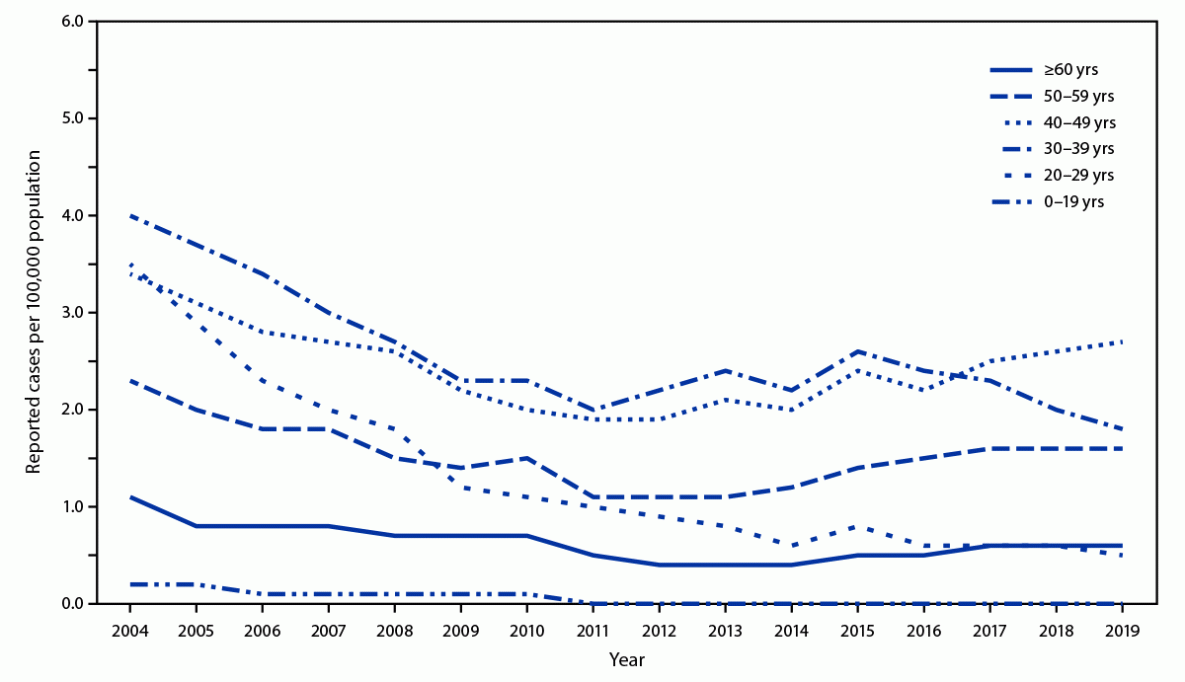
2019年报告的急性乙型肝炎病例中约有一半发生在30-49岁的人群中(图)。≥40岁成年人的急性乙型肝炎病例数有所增加,尤其是40-49岁的成年人,他们的报告病例率从2011年的每10万人1.9例增加到2019年的每10万人2.7例(图)。同期,50-59岁成年人的发病率增加了45.5%(从每10万人1.1例增加到1.6例),占2019年报告病例的22.2%。成人急性乙型肝炎病毒感染导致慢性乙型肝炎,估计有2%-6%的病例。
≥19岁成年人的乙肝疫苗接种覆盖率较低。2018年,≥19岁成年人自我报告的乙肝疫苗接种覆盖率(≥3剂)为30.0%(7)。19-49岁成人的乙肝疫苗接种覆盖率(≥3剂)为40.3%,≥50岁成人为19.1%。在2013-2018年期间,21.4%(95%CI=20.2%–22.6%)的≥25岁成年人具有疫苗诱导的乙型肝炎免疫力(5)。
在有危险因素的成年人中,乙肝疫苗接种覆盖率一直不理想。2018年,成人慢性肝病患者的自我报告覆盖率(≥3剂)为33.0%,自1995年以来前往乙型肝炎病毒感染流行的国家的旅行者为38.9%,19-59岁成人糖尿病患者为33.0%,医护人员为67.2%(7)。在一项针对433名家庭医学医生和420名内科医生的全国性调查中,68%的医生认为患者未披露风险因素是一个障碍,44%的医生认为没有足够的时间来常规评估患者的危险因素(10).
对乙肝疫苗接种的普遍建议可能会增加在慢性肝病和其他合并症(例如肥胖或糖尿病)发作之前接种疫苗的人数,这些合并症可能会降低疫苗接种的有效性。例如,已知慢性肝病患者对乙肝疫苗接种的免疫反应降低(11).
在CDC收到的2019年3,192例急性乙型肝炎病例报告中,有1,183例(37.1%)缺少风险行为和暴露数据。根据先前的HepB疫苗接种建议评估的危险因素包括潜在的犯罪或污名化行为(例如,注射吸毒、监禁或多个性伴侣),这限制了提供者风险评估的有效性[3,12,13]。普遍的疫苗接种建议消除了在接种疫苗前进行风险评估的需要。
乙型肝炎病毒感染者之间存在种族和民族差异。2005年,非西班牙裔美国黑人的急性乙型肝炎发病率大约是其他几个种族和族裔人群的两倍(3)。2019年,非西班牙裔黑人成年人的HBV感染率是亚洲或太平洋岛民成年人的三倍,大约是西班牙裔成年人的两倍(3)。在对该年龄组实施普遍疫苗接种策略后,所有种族和族裔的儿童和青少年的乙型肝炎发病率趋于较低(3)。
资源使用
使用经济模型来估计普遍成人乙肝疫苗接种有望带来的健康改善(14)。成本效益的一项衡量标准,即增量成本效益比(ICER),计算为所有≥19岁成年人每获得153,000美元的质量调整生命年(QALY)。对19-59岁的成年人进行的子分析得出,每增加一个QALY的ICER为117,000美元。通过模拟疫苗接种干预策略提高疫苗接种覆盖率,带来更好的健康结果;随着干预策略中疫苗接种覆盖率的增加,平均QALY的增加、生命年的增加、避免的急性HBV感染数量和避免的乙型肝炎相关死亡人数都有所增加(14)。在≥60岁人群中,乙型肝炎发病率明显较低(2019年每10万人0.6例);因此,该年龄组中可预防的HBV感染人数低于19-59岁的人。§
建议
建议19-59岁的成年人和≥60岁有乙型肝炎危险因素的成年人接种乙肝疫苗,没有已知乙型肝炎危险因素的≥60岁成年人也可以接种乙肝疫苗(盒)。已经建议婴儿和所有其他<19岁的人接种乙肝疫苗(2)。
临床指导
ACIP建议19-59岁的成年人和有乙型肝炎危险因素的≥60岁成年人应接种乙肝疫苗,而没有已知乙型肝炎危险因素的≥60岁成年人可以接种乙肝疫苗。在之前的HepB疫苗建议中,建议提供者为所有要求接种HepB疫苗的患者接种HepB疫苗。针对没有已知风险因素的≥60岁成年人的新语言旨在促使所有提供者为该队列中的患者提供HepB疫苗接种,而不是等待患者要求接种疫苗,从而将启动考虑HepB疫苗接种的责任从患者转移到提供者。
在任何时候完成乙肝疫苗接种系列或有乙肝病毒感染史的人不应接受额外的乙肝疫苗接种,尽管没有证据表明接受额外的疫苗剂量是有害的。然而,在某些情况下,可能需要按照2018年ACIP建议的规定进行再接种(例如,乙型肝炎表面抗原[HBsAg]检测呈阳性的人、医疗保健提供者和血液透析患者所生的无反应婴儿)(2)。提供者应仅接受注明日期的记录作为乙肝疫苗接种的证据。对因当前或既往感染而免疫HBV感染者接种疫苗或接种乙肝疫苗不会增加不良事件的风险。然而,在患者群体既往乙型肝炎病毒感染率较高的情况下,**可在接种第一剂疫苗的同时进行疫苗接种前检测,可能会避免对已经免疫的人进行完全疫苗接种,从而降低成本。疫苗接种前检测包括检测HBsAg、HBsAg抗体(抗-HBs)和乙型肝炎核心抗原抗体(抗-HBc)。HBsAg的存在提示当前HBV感染。抗-HBs的存在通常被解释为表明免疫力,无论是在完整的系列接种后或从HBV感染中恢复后,还是从HepB疫苗接种中恢复。总抗HBc的存在表明既往或正在进行的HBV感染。HBV感染的血清学标志物已有详细解释(2)。无法获得血清学检测不应成为易感人群接种疫苗的障碍,尤其是在难以接触的人群中。检测不是接种疫苗的必要条件,在检测不可行的情况下,应继续为建议接种疫苗的人接种疫苗(2)。¶
Heplisav-B和PreHevbrio在成人血液透析中的安全性和有效性尚未确定(表)。没有数据来评估Heplisav-B和PreHevbrio对母乳喂养婴儿或对产奶和排泄的影响。关于Heplisav-B和PreHevbrio的数据目前不足以告知妊娠期疫苗相关风险(8,15)。因此,医务人员应为需要接种HepB疫苗的孕妇接种Engerix-B、RecombivaxHB或Twinrix疫苗。
通讯作者:MarkK.Weng,mweng@cdc.gov,404-718-5498。
1疾病预防控制中心国家艾滋病毒、病毒性肝炎、性病和结核病预防中心病毒性肝炎司;2密苏里州圣路易斯大学医学院;3堪萨斯大学医学中心,堪萨斯州堪萨斯城;4Immunize.org,明尼苏达州圣保罗;5俄勒冈州波特兰市俄勒冈健康与科学大学公共卫生学院;6加拿大安大略省汉密尔顿麦克马斯特大学卫生研究方法、证据和影响系;7亚利桑那大学医学与公共卫生学院,亚利桑那州凤凰城。
*儿童、青少年和成人常规使用疫苗的建议由ACIP制定。ACIP被特许为联邦咨询委员会,向CDC主任提供关于使用疫苗和相关制剂控制美国平民疫苗可预防疾病的专家外部建议和指导。儿童和青少年常规使用疫苗的建议与美国儿科学会、美国家庭医师学会(AAFP)和美国妇产科医师学会(ACOG)的建议尽可能保持一致。成人常规使用疫苗的建议与AAFP、ACOG和美国内科医师学会的建议一致。CDC主任批准的ACIP建议在发病率和死亡率周报中公布的日期成为机构指南。https://www.cdc.gov/vaccines/acip
†ACIP肝炎疫苗工作组由来自学术医学(家庭医学、内科、儿科、产科、传染病、职业健康和预防医学专家)、联邦和州公共卫生实体以及医学会的专业人员组成。
§ https://www.cdc.gov/vaccines/acip/meetings/downloads/slides-2021-11-2-3/02-HepWG-weng-508.pdfpdf图标
¶ https://www.cdc.gov/vaccines/hcp/acip-recs/general-recs/index.html
** https://cdafound.org/polaris/externalicon(2021年11月19日访问)。
图.2004-2019年美国按年龄组报告的急性乙型肝炎病毒感染率
来源:https://www.cdc.gov/hepatitis/statistics/2019surveillance/Figure2.4.htm
盒. 建议接种乙型肝炎疫苗的人士
所有婴儿
<19岁人士
19-59岁的成年人
有乙型肝炎危险因素的≥60岁成人:
有性接触感染风险的人
oHBsAg检测呈阳性的人的性伴侣
o没有长期一夫一妻制关系的性活跃者(例如,在过去6个月内有不止一个性伴侣的人)
o寻求性传播感染评估或治疗的人
o男男性行为者
经皮或粘膜暴露于血液有感染风险的人
o当前或最近注射吸毒的人
o乙肝表面抗原检测呈阳性人士的家庭接触者
o发育障碍者设施的居民和工作人员
o有合理预期接触血液或血液污染体液风险的卫生保健和公共安全人员
o维持性透析(包括中心或家庭血液透析和腹膜透析)的人,以及透析前的人
o糖尿病患者由治疗临床医生自行决定
别人
o前往乙型肝炎病毒感染(HBsAg患病率为≥2%)高或中等水平的国家的国际旅行者
o丙型肝炎病毒感染者
o慢性肝病患者(包括但不限于肝硬化、脂肪肝、酒精性肝病、自身免疫性肝炎、丙氨酸转氨酶或天冬氨酸转氨酶水平大于正常上限两倍的人)
o爱滋病病毒感染者
o被监禁者
年龄≥60岁且没有已知乙型肝炎危险因素的成年人可以接种乙型肝炎疫苗
缩写:HBsAg=乙型肝炎表面抗原。
表.按疫苗类型和年龄组分列的≥18岁成人和11-19岁人群的乙型肝炎疫苗推荐剂量和时间表*
| 乙肝疫苗*/年龄组,岁 | 剂量(μg) | 体积(mL) | 附表 |
|---|---|---|---|
| Recombivax HB | |||
| 11–15 | 10 | 1 | 0个月和4-6个月接种2剂† |
| 11–19 | 5 | 0.5 | 0、1和6个月接种3剂† |
| ≥20 | 10 | 1 | |
| 接受血液透析的成年人和其他≥20岁免疫功能低下的成年人 | 40 | 1 | |
| Engerix-B | |||
| 11–19 | 10 | 0.5 | 0、1和6个月接种3剂 |
| ≥20 | 20 | 1 | |
| 接受血液透析的成年人和其他≥20岁免疫功能低下的成年人 | 40 | 2 | 0、1、2和6个月接种4剂§ |
| Heplisav-B | |||
| ≥18¶ | 20 | 0.5 | 0个月和1个月2剂 |
| Twinrix(HepA-HepB联合疫苗) | |||
| ≥18 | 20 | 1 | 0、1和6个月(标准)接种3剂,或0天、7天、21-30天和12个月(加速)接种4剂 |
| PreHevbrio(2022年ACIP推荐) | |||
| ≥18¶ | 10 | 1 | 0、1和6个月接种3剂 |
缩写:ACIP=免疫实践咨询委员会;甲型肝炎=甲型肝炎;HepB=乙型肝炎。*如果HepB疫苗接种计划中断,则不需要重新启动该系列。
如果在第一次给药后中断了3剂系列,则应尽快给予第二剂;第二剂和第三剂应间隔≥8周。如果仅延迟了第三剂,则应尽快接种。3剂系列的最后一剂必须在第二剂后≥8周和第一剂后≥16周给药;第一剂和第二剂之间的最短间隔为4周。乙型肝炎疫苗剂量不足或在短于推荐的给药间隔后接种的剂量应使用正确的剂量或时间表进行重新接种。在最短间隔或年龄前≤4天接种的疫苗剂量被认为是有效的。由于Twinrix独特的加速时间表(https://www.fda.gov/media/119351/downloadexternalicon),4天指南不适用于以0天、7天、21-30天和12个月的时间表接种该疫苗的前3剂。PreHevbrio(https://www.fda.gov/media/154561/downloadexternalicon)是2021年美国食品药品监督管理局批准、2022年ACIP推荐的三抗原HepB疫苗。
†RecombivaxHB成人制剂(10 μg)的2剂方案(https://www.fda.gov/media/74274/downloadexternalicon)适用于11-15岁的儿童和青少年。当计划接受第二剂时,≥16岁的人应改用3剂系列,其中第2剂和第3剂由儿科制剂组成,按适当的时间表给药。
§Engerix-B(https://www.fda.gov/media/119403/downloadexternalicon)用于接受血液透析的成人,分4剂(每剂2mL)作为单次2mL剂量或两次1mL剂量给药,每次0、1、2和6个月。RecombivaxHB用于成人透析是一个3剂量系列。
Heplisav-B和PreHevbrio的安全性和有效性尚未在血液透析成人中确定。没有数据来评估Heplisav-B和PreHevbrio对母乳喂养婴儿或母乳产生和排泄的影响。Heplisav-B(¶https://www.fda.gov/media/108745/downloadexternalicon)和PreHevbrio目前不足以告知妊娠期疫苗相关风险。因此,医务人员应为需要HepB疫苗的孕妇接种Engerix-B、RecombivaxHB或Twinrix疫苗。
引用
.
1.BruceMG、BrudenD、HurlburtD等。乙型肝炎疫苗初级系列接种后35年的保护和抗体水平以及对加强剂量的反应。肝病学2022;HEP.32474.https://doi.org/10.1002/hep.32474externalicon PMID:35320592externalicon
2.SchillieS、VellozziC、ReingoldA等人。美国乙型肝炎病毒感染的预防:免疫实践咨询委员会的建议。MMWRRecommRep2018;67:1–31.https://doi.org/10.15585/mmwr.rr6701a1externalicon PMID:29939980externalicon
3.疾病预防控制中心。病毒性肝炎。2019年病毒性肝炎监测报告。佐治亚州亚特兰大:美国卫生与公众服务部,CDC;2021. https://www.cdc.gov/hepatitis/statistics/SurveillanceRpts.htm
4.KlevensRM,LiuS,RobertsH,JilesRB,HolmbergSD.从全国报告的病例中估计急性病毒性肝炎感染。AmJ公共卫生2014;104:482–7.https://doi.org/10.2105/AJPH.2013.301601externalicon PMID:24432918externalicon
5.RobertsH,LyKN,YinS,HughesE,TeshaleE,JilesR.高危人群中HBV感染、疫苗诱导的免疫力和易感性:美国家庭,2013-2018年。肝病学2021;74:2353–65.https://doi.org/10.1002/hep.31991externalicon PMID:34097776externalicon
6.WongRJ、BrosgartCL、WelchS等人。对居住在美国的外国出生者的慢性乙型肝炎患病率的最新评估。肝病学2021;74:607–26.https://doi.org/10.1002/hep.31782externalicon PMID:33655536externalicon
7.LuPJ,HungMC,SrivastavA,etal.成年人群疫苗接种覆盖率监测——美国,2018年。MMWRSurveillSumm2021;70:1–26.https://doi.org/10.15585/mmwr.ss7003a1externalicon PMID:33983910externalicon
8.SchillieS,HarrisA,Link-GellesR,RomeroJ,WardJ,NelsonN.免疫实践咨询委员会关于使用乙型肝炎疫苗和新型佐剂的建议。MMWRMorbMortalWklyRep2018;67:455–8.https://doi.org/10.15585/mmwr.mm6715a5externalicon PMID:29672472externalicon
9.BruxvoortK、SlezakJ、QianL等。2剂与3剂乙型肝炎疫苗与急性心肌梗死之间的关联。美国医学会杂志2022;327:1260–8.https://doi.org/10.1001/jama.2022.2540externalicon PMID:35333303externalicon
10.DaleyMF、HennesseyKA、WeinbaumCM等。医生关于成人乙型肝炎疫苗接种的做法:一项全国性调查。美国医学杂志2009;36:491–6.https://doi.org/10.1016/j.amepre.2009.01.037externalicon PMID:19362798externalicon
11.RoniDA,PathapatiRM,KumarAS,NihalL,SridharK,TumkurRajashekarS.乙型肝炎疫苗接种在肝硬化中的安全性和有效性。高级病毒2013;2013:196704。https://doi.org/10.1155/2013/196704externalicon PMID:23840211externalicon
12.TaylorJEB,SureyJ,MacLellanJ,FrancisM,AbubakarI,StaggHR.伦敦难以覆盖的人群的乙型肝炎疫苗接种率:一项横断面研究。BMC感染Dis2019;19:372。https://doi.org/10.1186/s12879-019-3926-2externalicon PMID:31046683externalicon
13.MokayaJ、McNaughtonAL、BurbridgeL等人。盲点?面对乙型肝炎病毒(HBV)感染的耻辱感——系统评价。惠康开放分辨率2018;3:29。https://doi.org/10.12688/wellcomeopenres.14273.1externalicon PMID:30483598externalicon
14.霍尔EW、WengMK、HarrisAM等。评估成人普遍接种乙型肝炎疫苗的成本效用。J感染Dis2022;JIAC088.https://doi.org/10.1093/infdis/jiac088externalicon PMID:35260904externalicon
15.美国食品和药物管理局。PREHEVBRIO[包装说明书]。马里兰州银泉:美国卫生与公众服务部,食品和药物管理局,2021年。https://www.fda.gov/media/154561/downloadexternalicon
建议引用本文:WengMK,DoshaniM,KhanMA,etal.19-59岁成人普遍接种乙型肝炎疫苗:免疫实践咨询委员会的最新建议—美国,2022年。MMWRMorbMortalWklyRep2022;71:477–483.DOI:http://dx.doi.org/10.15585/mmwr.mm7113a1externalicon.
页面上次审核: 2022年4月15日
内容来源:美国疾病控制与预防中心
Hits: 19

