Contents
Hepatitis B
CDC Yellow Book 2024
传染因子:乙型肝炎病毒
风土性
全世界的
非洲和西太平洋的高流行率
暴露和感染风险最高的旅行者类别
预防方法
确保无菌医疗和牙科技术
使用安全注射方法
乙型肝炎是一种疫苗可预防的疾病
诊断支持
病原体
乙型肝炎病毒(HBV)是家族中的一种小的环状部分双链DNA病毒嗜肝病毒科.
传播
HBV通过接触受污染的血液、血液制品和其他体液(如精液)传播。旅行者可能通过牙科或医疗程序中不良的感染控制、接受血液制品、注射毒品、纹身或针灸或无保护的性行为暴露于HBV。
流行病学
HBV是全世界慢性肝炎、肝硬化和肝细胞癌的主要原因。2015年,全球估计有2.57亿人患有慢性HBV感染;那一年,HBV造成了大约887,000人死亡。然而,HBV感染可能被低估了,因为许多国家缺乏准确的数据(地图5-07)。
缺乏证明旅行者面临特定风险的数据;然而,关于旅行者感染乙型肝炎的报道很少,没有高风险行为或暴露的旅行者的风险很低。在慢性HBV感染流行率≥2%的国家(如西太平洋和非洲地区),HBV感染的风险可能更高;这些地区的外籍人士、传教士和长期发展工作者感染HBV病毒的风险可能会增加。所有旅行者都应该知道HBV是如何传播的,并采取措施尽量减少接触。
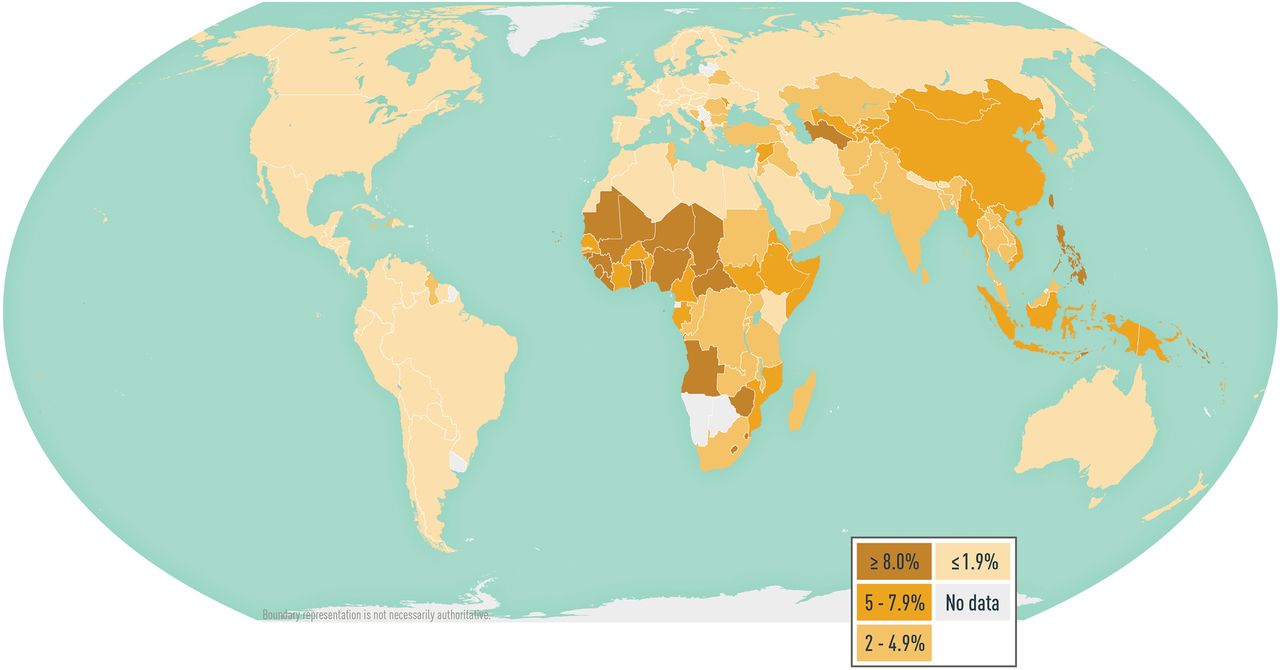
地图5-07乙型肝炎病毒感染的全球流行率
疾病数据来源:2021年乙型肝炎病毒疾病负担估计。CDA基金会北极星天文台。可从以下位置获得:https://cdafound.org/polaris-countries-distribution/.
临床表现
HBV感染主要影响肝脏。通常,乙型肝炎的潜伏期为90天(范围为60-150天)。新获得的急性HBV病毒感染有时只会引起症状,并且症状和体征因年龄而异。大多数小于5岁的儿童和免疫抑制的成人在新感染时无症状,而30%–50%的年龄≥5岁的新感染者有症状和体征。急性感染的典型体征和症状包括腹痛、厌食、疲劳、发热、黄疸、关节痛、不适、恶心和呕吐、浅色(粘土色)大便和深色尿液。急性乙型肝炎的总病死率约为1%。
一些急性HBV感染会自行消失,但一些会发展成慢性感染。急性乙型肝炎发展为慢性HBV病毒感染的风险取决于初次感染时的年龄,如下所示:> 90%的新生儿和婴儿,25%-50%的1-5岁儿童,以及< 5%的较大儿童和成人。大多数慢性HBV病毒感染者没有症状,也没有肝病的迹象。然而,15%至40%的慢性HBV感染患者将发展为肝硬化、肝细胞癌或肝衰竭,并且25%的慢性感染者过早死于这些并发症。感染HBV病毒的人容易感染丁型肝炎病毒;混合感染会增加暴发性肝炎和快速进展性肝病的风险。
诊断
乙型肝炎是一种全国性的传染病。急性HBV感染的临床诊断基于与病毒性肝炎和肝转氨酶升高一致的体征或症状,不能与急性肝炎的其他原因相区别。乙型肝炎特异性血清学标记对于诊断HBV感染和适当的临床管理是必要的(表5-11)。这些标记可以区分急性、消退性和慢性感染。
请参阅以下信息如何获得乙型肝炎诊断支持来自美国疾病控制和预防中心(CDC)传染病实验室,包括联系方式,送哪些样本,如何送样本。选择仅用于研究的乙型肝炎基因分型,如果需要临床实验室改进修正案规定的检测,则选择乙型肝炎血清学和定量PCR。
表5-11乙型肝炎病毒感染血清学检测结果的解释1
| 临床状态 | 乙型肝炎表面抗原 | 总抗-HBs | 总抗HBc | 行为 |
|---|---|---|---|---|
| 慢性感染 | 积极的 | 否定的;消极的;负面的;负的 | 积极的 | 链接到乙型肝炎指导的护理2 |
| 急性传染 | 积极的 | 否定的;消极的;负面的;负的 | 阳性(HBc IgM) | 链接到乙型肝炎指导的护理2 |
| 已解决的感染 | 否定的;消极的;负面的;负的 | 积极的 | 积极的 | 咨询,安慰 |
| 免疫(免疫) | 否定的;消极的;负面的;负的 | 积极的3 | 否定的;消极的;负面的;负的 | 再保证 |
| 易感(从未感染且无免疫证据) | 否定的;消极的;负面的;负的 | 否定的;消极的;负面的;负的 | 否定的;消极的;负面的;负的 | 接种疫苗 |
| 分离的核心抗体4 | 否定的;消极的;负面的;负的 | 否定的;消极的;负面的;负的 | 积极的 | 视情况而定 |
治疗
没有药物可用于治疗急性HBV感染;治疗是支持的。有几种抗病毒药物可供慢性HBV病毒感染者使用。慢性HBV病毒感染者应接受健康专家的护理,并接受全面的身体检查和实验室检测,以确定是否需要抗病毒治疗,并持续监测肝细胞癌和肝损伤。参见美国肝病研究协会(AASLD)的实践慢性HBV感染治疗指南.
预防
疫苗
使用适应症
对所有前往慢性HBV感染中度到高度流行地区(即HBV表面抗原阳性流行率≥2%的国家)的未接种疫苗的人接种乙肝疫苗(地图5-07)。查看完整美国疫苗接种信息和建议.
管理
有几种乙型肝炎疫苗(表5-12)。乙型肝炎疫苗可在0个月和1个月时分两个剂量系列给药(Heplisav-B[dyna VAX Technologies Corporation]),也可在0个月、1个月和6个月时分三个剂量系列给药(Engerix-B [GlaxoSmithKline]、Recombivax HB [Merck]、PreHevbrio [VBI]以及甲型肝炎和乙型肝炎联合疫苗Twinrix [GlaxoSmithKline])。Heplisav-B获准用于18岁以上成人的2剂方案;第二次给药应在第一次给药后≥1个月。
Engerix B和Recombivax HB也已根据替代疫苗接种计划获得使用许可。Engerix-B可采用4剂方案给药,前3剂在2个月内给药,第12个月加强给药(剂量分别为0、1、2和12个月)。Recombivax HB可用于11-15岁儿童的2剂方案。Twinrix可用于加速4剂方案(0、7和21-30天,12个月时加强注射)以促进长期免疫。
使用替代方案和配方时,请务必查阅处方信息。只要可行,使用同一制造商的疫苗来完成患者的疫苗系列;但是,如果不知道先前注射剂量的制造商,或者无法从同一制造商处获得疫苗,则不要推迟接种。2剂Heplisav-B疫苗系列仅适用于系列中的两剂疫苗均由Heplisav-B组成的情况。由1剂Heplisav-B和来自不同制造商的疫苗组成的系列应遵循3剂方案。
标准疫苗接种系列的保护是强有力的,超过95%的健康人在完成疫苗接种系列后获得免疫力。不建议已接种过疫苗的具有免疫能力的成年人在旅行前进行血清学检测和加强疫苗接种。然而,对于随后的临床管理依赖于对其免疫状态的了解的人,包括面临血液或体液暴露风险的卫生保健人员和公共安全工作者,考虑进行疫苗接种后血清学检测;需要(或可能需要)门诊血液透析者;艾滋病毒感染者;HBsAg阳性者的性伴侣;和其他免疫受损的人(例如,造血干细胞移植接受者或接受化疗的人)。
表5-12乙型肝炎疫苗
| 疫苗 | 商品名称(制造商) | 年龄(年) | 剂量和途径 | 日程安排 | 加强剂 |
|---|---|---|---|---|---|
| 含新型佐剂的重组乙型肝炎疫苗(1018) | Heplisav-B (Dynavax技术公司) | ≥18 | 0.5毫升(20克HBsAg和3000克1018)肌注 | 剂量1: ≥18岁 第2剂:第1剂后1个月 | 没有人 |
| 乙型肝炎疫苗,重组1 | Engerix-B(葛兰素史克) | 0–19 | 0.5毫升(10克乙型肝炎表面抗原)肌肉注射 | 标准 剂量1:0-19岁 第2剂:第1剂后1个月 第3剂:第1剂后6个月 | 没有人 |
| 乙型肝炎疫苗,重组1 | Engerix-B(葛兰素史克) | 0–10 | 0.5毫升(10克乙型肝炎表面抗原)肌肉注射 | 加速 剂量1:0-10岁 第2剂:第1剂后1个月 第3剂:第1剂后2个月 | 第1剂后12个月 |
| 乙型肝炎疫苗,重组1 | Engerix-B(葛兰素史克) | 11–19 | 1毫升(20克乙型肝炎表面抗原)肌肉注射 | 加速 剂量1:11-19岁 第2剂:第1剂后1个月 第3剂:第1剂后2个月 | 第1剂后12个月 |
| 乙型肝炎疫苗,重组1 | Engerix-B(葛兰素史克) | ≥20 | 1毫升(20克乙型肝炎表面抗原)肌肉注射 | 标准 剂量1: ≥20岁 第2剂:第1剂后1个月 第3剂:第1剂后6个月 | 没有人 |
| 乙型肝炎疫苗,重组1 | Engerix-B(葛兰素史克) | ≥20 | 1毫升(20克乙型肝炎表面抗原)肌肉注射 | 加速 剂量1: ≥20岁 第2剂:第1剂后1个月 第3剂:第1剂后2个月 | 没有人 |
| 乙型肝炎疫苗,重组1 | Recombivax HB(默克) | 0–19 | 0.5毫升(5克乙型肝炎表面抗原)肌肉注射 | 标准 剂量1:0-19岁 第2剂:第1剂后1个月 第3剂:第1剂后6个月 | 没有人 |
| 乙型肝炎疫苗,重组1 | Recombivax HB(默克) | 11–15 | 1毫升(10克乙型肝炎表面抗原)肌肉注射 | 青春期,加速 剂量1:11-15岁 第2剂:第1剂后4-6个月 | 没有人 |
| 乙型肝炎疫苗,重组1 | Recombivax HB(默克) | ≥20 | 1毫升(10克乙型肝炎表面抗原)肌肉注射 | 标准 剂量1: ≥20岁 第2剂:第1剂后1个月 第3剂:第1剂后6个月 | 没有人 |
| 乙型肝炎疫苗,重组1 | PreHevbrio(VBI) | ≥18 | 1毫升(10克乙型肝炎表面抗原)肌肉注射 | 剂量1: ≥18岁 第2剂:第1剂后1个月 第3剂:第1剂后6个月 | 没有人 |
| 甲型和乙型肝炎联合疫苗 | Twinrix(葛兰素史克) | ≥18 | 1毫升(720 ELU HAV + 20克乙肝表面抗原)肌肉注射 | 标准 剂量1: ≥18岁 第2剂:第1剂后1个月 第3剂:第1剂后6个月 | 没有人 |
| ≥18 | 1毫升(720 ELU HAV + 20克乙肝表面抗原)肌肉注射 | 加速 剂量1: ≥18岁 第2剂:第1剂后7天 第3剂:第1剂后21–30天 | 第1剂后12个月 |
缩写:HBsAg,乙肝表面抗原;IM,肌内;ELU,ELISA单位灭活HAV;HAV,甲型肝炎病毒。
1请查阅处方信息,了解接受血液透析患者和其他免疫功能低下患者的剂量差异。
特殊情况
加速Twinrix疫苗接种计划(0、7和21-30天,加上12个月的加强免疫)可用于面临迫在眉睫的HBV暴露的短期旅行人员或灾区的紧急救援人员。或者,Heplisav-B可在第0周和第4周作为2剂系列使用,以单独预防乙型肝炎。理想情况下,Heplisav-B疫苗接种应在旅行前至少1个月开始,以便在出发前完成整个疫苗系列。当使用Heplisav-B以外的疫苗时,在预定旅行前≥6个月开始接种疫苗。因为一些保护是由1或2剂提供的,如果有指示,开始疫苗系列,即使该系列不能在出发前完成。然而,在系列研究完成之前,疫苗不会提供最佳的保护;建议旅行者在返回时完成疫苗系列。
安全性和不良反应
所有年龄的人都可以接种安全的乙肝疫苗,严重的不良反应很少发生。最常见的不良反应是注射部位疼痛(3%–29%)和低烧(体温> 99.9°F[37.7°C];1%–6%)。乙型肝炎疫苗不应用于对任何疫苗成分(包括酵母)有过敏史的人。该疫苗包含非感染性重组蛋白(乙型肝炎表面抗原)和佐剂(1018[Heplisav-B的小合成免疫刺激性胞苷-磷酸-鸟苷寡脱氧核苷酸基序]或铝[Engerix-B、Recombivax HB、PreHevbrio、Twinrix])。
影响孕妇的HBV感染可导致母亲的严重疾病和新生儿的慢性感染。有限的数据表明,母亲接种Engerix-B、Recombivax HB或Twinrix疫苗后,母亲(或发育中的胎儿)不良事件的风险没有明显增加;尚无关于孕妇或哺乳期妇女使用Heplisav-B或PreHevbrio的数据。因此,在获得Heplisav-B和PreHevbrio的安全性数据之前,需要接种乙肝疫苗的孕妇或哺乳者应接种Engerix-B、Recombivax HB或Twinrix疫苗。
个人防护措施
作为旅行前教育过程的一部分,教育所有旅行者乙肝和其他血源性病原体的暴露风险,包括涉及刺穿皮肤或粘膜的活动或程序;接受血液制品;美容(如纹身或穿孔)、牙科或医疗过程中使用的污染设备;注射吸毒;以及无保护的性行为。告诫旅行者不要让供应商使用消毒或灭菌不充分的设备、重复使用受污染的设备或不使用安全注射方法(如重复使用一次性针头和注射器)。
如果医疗设备没有消毒,或者工作人员没有遵循适当的感染控制程序,HBV病毒和其他血源性病原体也可能传播。旅行者在海外接受牙科或医疗护理时应考虑健康风险;美国大使馆特定国家的网站可能有关于医疗问题的信息。建议旅行者在前往可能不具备或不实行充分的消毒或杀菌程序的目的地旅行时,在进行身体穿孔或纹身之前,充分考虑健康风险。
疾控中心网站:乙型肝炎
以下作者对本章的前一版本有贡献:亚伦·m·哈里斯
Hits: 92
- 甲型肝炎 CDC黄皮书2024
- 基孔肯亚 CDC黄皮书2024
- 疫苗接种和免疫预防-一般原则 CDC黄皮书2024
- 乙型肝炎 CDC黄皮书2024
- 脑膜炎球菌病, CDC黄皮书,2024
- 沙特阿拉伯:朝觐和朝圣 CDC黄皮书2024
- 登革热 CDC 黄皮书 2024
- 蚊子、扁虱和其他节肢动物 CDC黄皮书2024
- 乙型脑炎 CDC黄皮书2024
- 动物传染病暴露:咬伤、螫伤、抓伤和其他危险 CDC黄皮书2024
- 狂犬病 CDC黄皮书2024
- 观点:狂犬病免疫 CDC黄皮书2024
- 蜱传脑炎 CDC黄皮书2024
- 伤寒和副伤寒 CDC黄皮书2024
- 黄热病 CDC黄皮书2024
- 按国家或地区分列的黄热病疫苗和疟疾预防信息 CDC黄皮书2024
- 婴儿和儿童疫苗建议 CDC黄皮书2024
- 游轮旅行 CDC黄皮书2024
- 病毒性出血热 CDC黄皮书2024
- 疟疾 2024 年 CDC 黄皮书
- 黄热病和疟疾信息,按国家划分(埃塞俄比亚)
- 旅行者的疾病模式 2024 年 CDC 黄皮书
- 天花和其他正痘病毒相关感染 2024 年 CDC 黄皮书
- 黄皮书 -脊髓灰质炎