Contents
- 1 储存
- 1.0.0.1 剂型
- 1.0.0.2 接种
- 1.0.0.3 处理
- 1.0.0.4 疫苗使用建议
- 1.0.0.5 初级免疫接种
- 1.0.0.6 加强免疫
- 1.0.0.7 免疫状态未知或不完全的儿童接种疫苗
- 1.0.0.8 禁忌症
- 1.0.0.9 预防措施
- 1.0.0.10 先前免疫接种后的全身和局部反应
- 1.0.0.11 怀孕和母乳喂养
- 1.0.0.12 早产儿
- 1.0.0.13 免疫抑制和艾滋病毒感染
- 1.0.0.14 神经疾病
- 1.0.0.15 图16.2免疫程序流程图(如果在免疫前有神经疾病的证据)
- 1.0.0.16 免疫接种后的神经异常
- 1.0.0.17 推迟免疫接种
- 1.0.0.18 不良反应
- 1.0.0.19 Hib/MenC结合疫苗
- 1.0.0.20 病例和联系人的管理
- 1.0.0.21 疫苗
- 1.0.0.22 参考
第16章:b型流感嗜血杆菌(Hib)
2011年3月
疾病
流感嗜血杆菌可导致严重的侵袭性疾病,尤其是在幼儿中。侵袭性疾病通常是由被包裹的有机体菌株引起的。已知六种可分型的荚膜血清型(a-f)可导致疾病;不可分型的包膜菌株偶尔会引起侵袭性疾病。在引入疫苗接种之前,b型(Hib)是流行菌株。可分型菌株与不可分型菌株的比例很大程度上取决于b型菌株的流行程度。无包膜菌株主要与呼吸道感染有关,如慢性支气管炎和中耳炎的恶化。
侵袭性Hib疾病最常见的表现是脑膜炎,通常伴有菌血症。这种表现约占所有病例的60%(Anderson et al., 1995)。15%的病例表现为会厌炎,这是一种潜在的危险疾病,表现为气道阻塞。10%的病例会出现菌血症,但不伴有任何其他感染。其余由化脓性关节炎、骨髓炎、蜂窝组织炎、肺炎和心包炎组成。Hib脑膜炎的后遗症可能包括耳聋、癫痫和智力障碍。在威尔士和牛津进行的研究中,8-11%有永久性神经后遗症(Howard et al., 1991; Tudor-Williams et al., 1989)。Hib脑膜炎的病死率为4-5%。
个人可以在没有表现出疾病迹象的情况下在他们的鼻子和喉咙中携带Hib细菌。在引入Hib疫苗之前,每100名学龄前儿童中约有4名携带Hib病菌;疫苗引入后,携带率下降到检测水平以下(McVernon et al., 2004)。Hib通过咳嗽、打喷嚏或与带菌者或感染者密切接触传播。
疾病的历史和流行病学
在引入Hib免疫接种之前,五岁以下儿童的侵袭性Hib疾病年发病率估计为每100,000名儿童中有34例。在五岁生日前,每600名儿童中就有一名患上某种形式的侵袭性Hib疾病(Booy et al., 1994)。这种疾病在3个月以下的儿童中很少见,但发病率在第一年内逐渐上升,在10至11个月大时达到高峰。此后,发病率稳步下降至4岁,此后感染并不常见。
针对Hib的疫苗最初是在20世纪70年代早期生产的,它们含有纯化的荚膜多糖。这些疫苗对18个月以上的儿童有效,但不能保护更小的儿童,因为他们患病的风险最高。结合Hib疫苗的发展克服了这个问题。在结合疫苗中,荚膜多糖与蛋白质相连,提高了疫苗的免疫原性,特别是在一岁以下的儿童中。1992年,Hib结合疫苗被引入英国常规免疫接种计划。Hib结合疫苗最初是作为单独的疫苗施用的。1996年,联合疫苗(DTwP/ Hib)问世,2004年,由DTaP和IPV联合制成的Hib疫苗(DTaP/IPV/Hib)问世。
结合Hib疫苗的效力和安全性已经在芬兰、美国和英国的大型临床试验中得到证实,效力范围为83-100%(Black et al., 1991a; Black et al., 1991b; Eskola et al., 1990)。使用目前英国主要方案比较不同疫苗的研究表明,90%至99%的儿童在接种三剂疫苗后产生了保护性抗体水平(Booy et al., 1994)。包括英国在内的一些国家报告了完全接种疫苗的儿童出现侵袭性疾病(疫苗失败)的病例((Heath and McVernon, 2002)。此类病例中有一小部分有潜在的疾病,如免疫球蛋白缺乏,使儿童易患疫苗失败。
自从在英国引入Hib免疫接种以来,发病率已经下降(见图16.1)。1998年,英格兰和威尔士五岁以下儿童中仅报告了21例侵袭性Hib(每100,000人0.65例),而1991年为803例(每100,000人20.5例)。一岁以下的婴儿是疾病的最高风险年龄组,报告的病例下降了95%以上(从300例下降到7例)。同期流感嗜血杆菌脑膜炎的通报从485起下降至29起。1998年,到第二个生日时,覆盖率为95%。
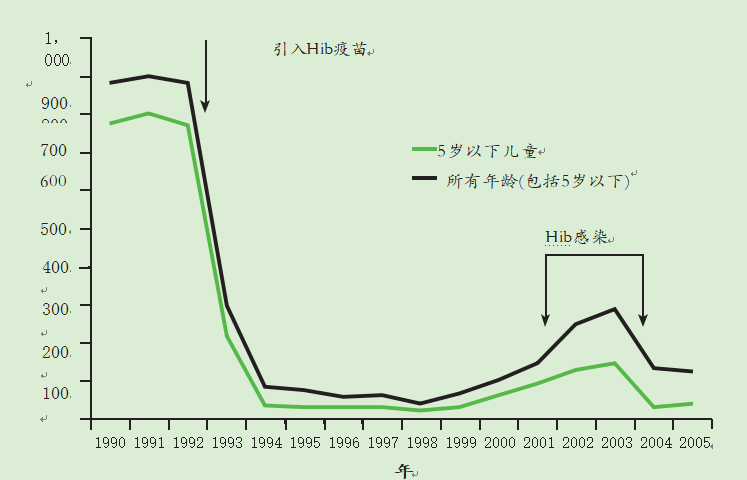
图16.1英格兰和威尔士Hib疾病的实验室报告(1990-2005年)
自1999年以来,报告的Hib病例数量有小幅但逐渐增加,主要发生在4岁以下的儿童中。然而,这一增长在2000年和2001年出生的儿童中最为显著(McVernon et al., 2003)。疫苗失败增加的原因被认为包括当时使用的DTaP/Hib联合疫苗的影响,以及引入疫苗时追赶计划影响的减弱。在后一组中,在较大年龄免疫,其效力高于婴儿时期常规接种的儿童。
2003年,实施了一项加强运动,召回6个月至4岁的儿童(Chief Medical Officer et al., 2004)。运动之后,病例开始恢复到以前的低水平(见图16.1)。2006年,在研究表明对Hib的保护在生命的第二年减弱(Trotter et al., 2003)后,引入了加强剂量(与MenC结合作为Hib/MenC)。
Hib疫苗接种
含Hib的疫苗由从Hib细菌培养物中提取的荚膜多糖制成。根据制造商的方法,多糖与蛋白质连接(结合)。在英国,使用的Hib疫苗已经与以下两者之一结合
CRM197(白喉毒素的无毒变种)或破伤风类毒素。结合增加了免疫原性,特别是在幼儿中,因为普通多糖疫苗没有免疫原性。
与DTwP/Hib组合相比,一些DTaP/Hib组合疫苗已被证明可减弱Hib反应(Trotter et al., 2003)。在英国计划中选择用于初级免疫接种的含Hib的疫苗(Pediacel)已被证明没有这个问题(Miller et al., 2003)。
Hib疫苗作为组合产品的一部分提供:
- 白喉/破伤风/无细胞百日咳/灭活脊髓灰质炎疫苗/Hib疫苗
(DTaP/IPV/Hib),或
- Hib/MenC联合疫苗。
Hib/MenC结合疫苗由下列荚膜多糖制成,Hib荚膜多糖和C型脑膜炎奈瑟球菌荚膜多糖与破伤风类毒素结合。当在婴儿时期接种过Hib和MenC结合疫苗的儿童在出生后第二年接种该疫苗时,该疫苗已被证明能引发对Hib和MenC的加强应答。
上述疫苗不含硫柳汞。它们是灭活的,不含活的有机体,不会引起它们所保护的疾病。
储存
疫苗应储存在+2℃至+8℃的原包装中,并避光保存。所有疫苗在某种程度上都对冷热敏感。高温加速了大多数疫苗效力的下降,从而缩短了它们的保质期。除非储存在正确的温度下,否则无法保证疫苗的有效性。冷冻可能导致某些疫苗的反应原性增加和效力丧失。它还会在容器中产生细小的裂纹,导致内容物被污染。
剂型
Hib疫苗作为联合产品DTaP/IPV/Hib或Hib/MenC的一部分提供。DTaP/IPV/Hib组合产品以混浊的白色混悬液的形式提供,装在单剂量安瓿或预装注射器中。混悬剂在储存过程中可能会沉淀,在接种前应摇动混悬剂使其均匀分布。
Hib/MenC以一小瓶白色粉末和0.5ml溶剂的形式提供,装在预装注射器中。疫苗必须通过将预填充注射器的全部内容物添加到含有粉末的小瓶中来复溶。加入溶剂后,应充分摇动混合物,直到粉末完全溶解。重新配制后,应立即接种疫苗,或在+2℃和+8℃之间放置,并在24小时内使用。
剂量和时间表
对于一岁以下的儿童:
- 首剂0.5ml含Hib疫苗。
- 第二剂0.5ml,第一剂后一个月。
- 第三剂0.5ml,第二剂后一个月。
- 第四次加强剂量的0.5ml含Hib的疫苗应在推荐的时间间隔内注射(见下文)。
对于1岁以上10岁以下未接种过白喉、破伤风、百日咳或脊髓灰质炎疫苗或未完成初级疗程的儿童,应接种DTaP/IPV/Hib疫苗。完成白喉、破伤风、百日咳或脊髓灰质炎初级课程的一岁以上十岁以下儿童应接种Hib/MenC。
接种
疫苗通常通过上臂或大腿前外侧肌肉注射。这是为了降低局部反应的风险,局部反应在皮下注射疫苗时更常见(Mark et al., 1999; Diggle and Deeks, 2000; Zuckerman, 2000)。然而,对于患有出血性疾病的个体,应通过深层皮下注射来接种疫苗,以降低出血的风险。
含Hib的疫苗可以与MMR、MenC、乙型肝炎和肺炎球菌等其他疫苗同时接种。疫苗应该在不同的部位注射,最好是在不同的肢体。如果给药在同一个肢体,它们应该至少分开2.5厘米(American Academy of Pediatrics, 2003)。每种疫苗的注射部位应在患者记录中注明。
处理
用于接种疫苗的设备,包括用过的小瓶或安瓿,应在每次接种结束后,密封在一个合适的防刺穿“锐器”盒中进行处置(未批准,BS 7320)。
疫苗使用建议
免疫接种计划的目的是保护10岁以下的人,以及10岁以上的人,他们可能有患侵袭性Hib疾病的高风险。
为了实现这一目标,每个年龄组的适当疫苗也取决于保护个人免受白喉、破伤风、百日咳、Hib和脊髓灰质炎的需要。
初级免疫接种
10岁以下的婴儿和儿童
婴儿接种Hib疫苗的主要过程包括三剂含Hib的产品,每剂之间间隔一个月。DTaP/IPV/Hib推荐给所有两个月到十岁的儿童。虽然一剂Hib疫苗从一岁开始有效,但为了充分预防白喉、破伤风、百日咳和脊髓灰质炎,未接种疫苗或未完成初级课程的儿童应接种三剂DTaP/IPV/Hib疫苗。如果第一疗程中断,应重新开始,但不能重复,允许剩余剂量之间有一个月的间隔。
已完成白喉、破伤风、百日咳和脊髓灰质炎初级疗程但尚未接种含Hib疫苗的1至10岁儿童应接种一剂Hib/MenC疫苗。
加强免疫
对于接受了三次含Hib疫苗注射的完整初级疗程的儿童,建议在12个月时进行Hib/MenC的强化(加强)剂量。Hib/MenC疫苗可与肺炎球菌结合疫苗和MMR疫苗同时接种。
免疫状态未知或不完全的儿童接种疫苗
如果在英国出生的儿童有不充分的免疫接种史,应尽一切努力澄清他们可能接种过哪些疫苗(参见第11章,免疫接种时间表)。未完成初级疗程的儿童应每月注射一次剩余剂量。
来到英国的儿童,如果有在原籍国完成免疫接种的历史,可能无法获得针对目前在英国使用的所有抗原的保护。他们可能没有收到含Hib原产国的疫苗(www-nt.who.int/immunization_monitor ing/en/global summary/country profile select . cfm)。
来自发展中国家、冲突地区或难以接触到的人群的儿童可能没有完全免疫。如果没有可靠的既往免疫史,则应假设他们未免疫,并应遵循完整的英国建议(见第11章)。
患有无脾症、脾功能障碍或补体缺乏的儿童和成人
患有无脾症或脾功能障碍的儿童和成人可能会增加侵袭性Hib感染的风险。患有早期补体缺乏症(例如C1、2、3或4种缺乏症)的儿童和成人也可能具有增加的侵袭性Hib感染风险(Figueroa et al., 1991)。
鉴于风险增加,建议患有无脾症或脾功能障碍的个人或根据年龄和疫苗接种史诊断为补体缺乏的个人额外接种Hib疾病疫苗。有关这些群体的完整免疫列表,请参见第7章中的表7.1。
两岁以下的儿童
这些人应根据英国常规儿童期计划接种疫苗,包括在12个月大时接种Hib/MenC和PCV的加强剂。应在Hib/MenC和PCV加强免疫后至少一个月接种一剂MenACWY结合疫苗。
在第二个生日后,应给予额外剂量的Hib/MenC。如果患者接受了常规肺炎球菌加强剂量的pcv 7(2010年4月前),应同时给予额外剂量的PCV13,两个月后再给予一剂PPV。如果儿童常规接种了PCV13疫苗(2010年4月后),应同时接种一剂PPV疫苗和Hib/MenC疫苗。
两岁以上五岁以下完全接种疫苗的人
这些人应该接受一次额外剂量的Hib/MenC和PCV13(因为他们已经接受了PCV7)。
一个月后,他们应该注射一剂MenACWY结合疫苗。应在最后一剂PCV13后至少两个月注射PPV。
两岁以上五岁以下以前未接种疫苗的人
这些人应该接受一次额外剂量的Hib/MenC和PCV13(因为他们已经接受了PCV7)。一个月后,他们应该接受一剂MenACWY结合疫苗。应在最后一剂PCV13后至少两个月注射PPV。
五岁以上的个人,无论其疫苗接种状况如何
这些人应接种一剂Hib/MenC疫苗和一剂PPV疫苗。一个月后,应注射一剂MenACWY结合疫苗。
禁忌症
极少数人不能接种含Hib的疫苗。如有疑问,应向儿科顾问、免疫协调员或传染病控制顾问寻求适当的建议,而不是拒绝接种疫苗。
疫苗不应注射给患有以下疾病的人:
- 对先前剂量的含Hib疫苗的确认过敏反应,或
- 对疫苗的任何成分产生过敏反应。
确诊的过敏反应极少发生。来自英国、加拿大和美国的数据表明,每100万剂疫苗中发生0.65至3次过敏反应事件(Bohlke et al., 2003; Canadian Medical Association, 2002)。其他过敏情况可能更常见,但不是进一步免疫的禁忌症。仔细的事件史通常会区分过敏反应和其他不是由疫苗引起的或不威胁生命的事件。在后一种情况下,有可能继续免疫过程。必须寻求专家对疫苗和接种环境的建议。必须考虑到个人未接种疫苗的风险。
预防措施
没有发烧或全身不适的小病不是推迟免疫接种的正当理由。如果个人急性不适,免疫接种可能会推迟,直到他们康复。这是为了避免由于错误地将任何体征或症状归因于疫苗的副作用而混淆任何急性疾病的鉴别诊断。
先前免疫接种后的全身和局部反应
本节给出了对在接种疫苗后72小时内有严重或轻度全身或局部反应史的儿童进行免疫接种的建议。应在以下病史后继续接种含Hib的疫苗:
- 发烧,不论其严重程度
- 低渗-低反应性发作(HHE)
- 持续哭闹或尖叫超过三小时,或
- 严重的局部反应,与程度无关。
在加拿大,对DTaP/IPV/Hib的严重全身或局部反应不是进一步接种疫苗的禁忌症(Canadian Medical Association,1998)。加拿大对儿童免疫接种后的不良事件进行了仔细监测(Le Saux et al., 2003),他们的经验表明,进一步的剂量与之前事件的复发或恶化无关(S Halperin and R Pless, pers. comm., 2003)。
怀孕和母乳喂养
当需要保护时,可以立即给孕妇接种含Hib的疫苗。没有证据表明给孕妇或哺乳期妇女接种灭活病毒或细菌疫苗或类毒素有风险(Plotkin and Orenstein, 2004)。
早产儿
根据时间表,早产儿在适当的年龄接种疫苗是很重要的。接种疫苗后窒息的发生率在早产婴儿中特别高。
住院的非常早产儿(出生≤妊娠28周)在第一次免疫接种时应进行48-72小时的呼吸监测,特别是那些以前有呼吸不成熟史的人。如果儿童在第一次免疫接种后出现呼吸暂停、心动过缓或不饱和,第二次免疫接种也应在医院进行,并进行48-72小时的呼吸监测
(Pfister et al., 2004; Ohlsson et al., 2004; Schulzke et al., 2005; Pourcyrous et al., 2007; Klein et al., 2008)。
由于这一组婴儿接种疫苗的益处很大,因此不应停止或推迟接种疫苗。
免疫抑制和艾滋病毒感染
免疫抑制和HIV感染的个体(无论CD4计数如何)应根据上述建议接种含Hib的疫苗。这些人可能不会产生完全的抗体反应。在治疗结束并痊愈后,应考虑重新免疫。可能需要专家的建议。
皇家儿科和儿童健康学院(RCPCH)提供进一步的指导(www.rcpch.ac.uk),英国艾滋病毒协会(BHIVA)艾滋病毒感染成人免疫指南(BHIVA,2006)和英国和爱尔兰儿童艾滋病毒协会(CHIVA)免疫指南(www.bhiva.org/chiva)。
神经疾病
原有的神经疾病
神经疾病的存在不是免疫接种的禁忌症。如果有证据表明儿童患有神经疾病,应遵循图16.2流程图中给出的建议。
如果儿童有稳定的先存神经异常,如脊柱裂、先天性大脑异常或围产期缺氧缺血性脑病,他们应根据建议的时间表进行免疫接种。当有记录的新生儿期脑损伤史时,应进行免疫接种,除非有证据表明出现了神经异常。
如果有证据表明目前的神经系统恶化,包括控制不佳的癫痫,应推迟免疫接种,并应将儿童转介给儿童专家进行调查,以确定潜在的原因。如果没有确定病因,应推迟免疫接种,直到病情稳定。如果确定了病因,免疫接种应该照常进行。
癫痫家族史不是免疫接种的禁忌症。当有热性惊厥的个人或家族病史时,在任何发热(包括由免疫接种引起的发热)后发生热性惊厥的风险会增加。
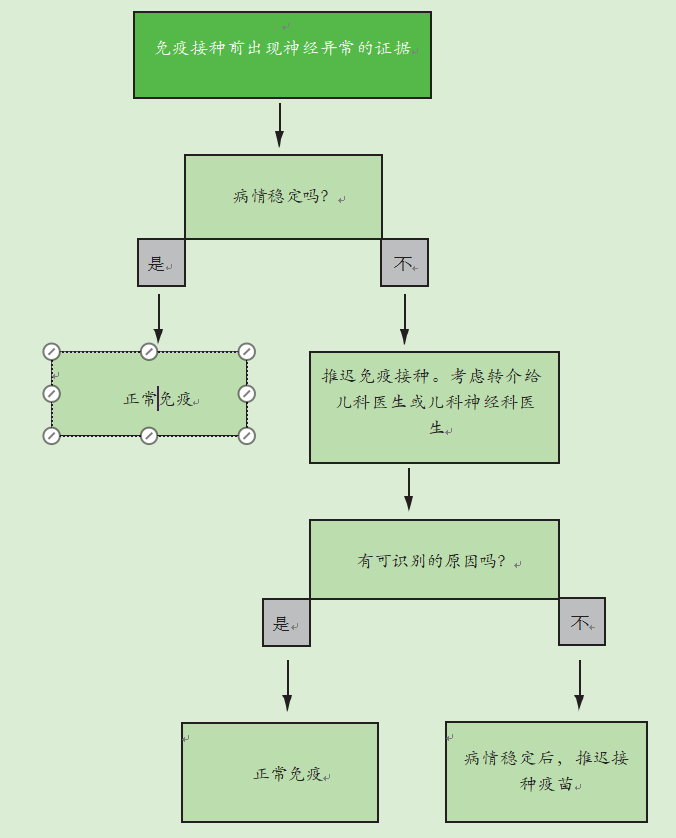
图16.2免疫程序流程图(如果在免疫前有神经疾病的证据)
与发热相关的癫痫发作在出生后的前六个月很少见,在出生后的第二年最常见。过了这个年龄,频率下降,五岁以后就很少了。
当儿童在过去有过与发热相关的癫痫发作,没有神经恶化的证据时,应按照建议进行免疫接种。接种疫苗前应提供预防和控制发烧的建议。
当儿童出现与发热无关的癫痫发作,并且没有神经恶化的迹象时,应按照建议进行免疫接种。当接种百白破疫苗时,有癫痫发作家族史或个人史的儿童没有明显的不良事件,他们的发育进程是正常的(Ramsay et al., 1994)。
免疫接种后的神经异常
如果儿童在免疫接种后7天内出现脑病或脑炎,应遵循图16.3流程图中的建议。这些情况不太可能是由疫苗引起的,应该由专家进行调查。如果没有发现潜在病因,并且儿童在7天内没有完全康复,则应推迟免疫接种,直到病情稳定。如果确定了病因或儿童在七天内康复,应按照建议进行免疫接种。
如果在免疫接种后72小时内出现与发烧相关的癫痫发作,如果没有找到潜在原因,并且儿童在24小时内没有完全康复,则应推迟进一步的免疫接种,直到病情稳定。如果查明了病因或儿童在24小时内康复,应按照建议继续进行免疫接种。
推迟免疫接种
需要推迟免疫接种的情况很少(见上文)。延期使孩子得不到保护;应尽量缩短延期时间,以便尽快开始免疫接种。如果专家建议推迟,应明确告知全科医生,一旦孩子适合接种,必须立即告知他或她。
不良反应
注射部位的疼痛、肿胀或发红是常见的,并且可能在后续剂量后更频繁地发生。注射部位可能会形成一个小而无痛的结节;这通常会消失,没有任何后果。破伤风疫苗联合无细胞百日咳疫苗的局部反应发生率低于全细胞百日咳疫苗,与白喉(DT)疫苗后的局部反应发生率相似(Miller, 1999; Tozzi and Olin, 1997)。
接种DTaP和DT疫苗后,发烧、抽搐、高声尖叫、苍白、发绀和无力(HHE)的发生频率相同(Tozzi and Olin, 1997)。
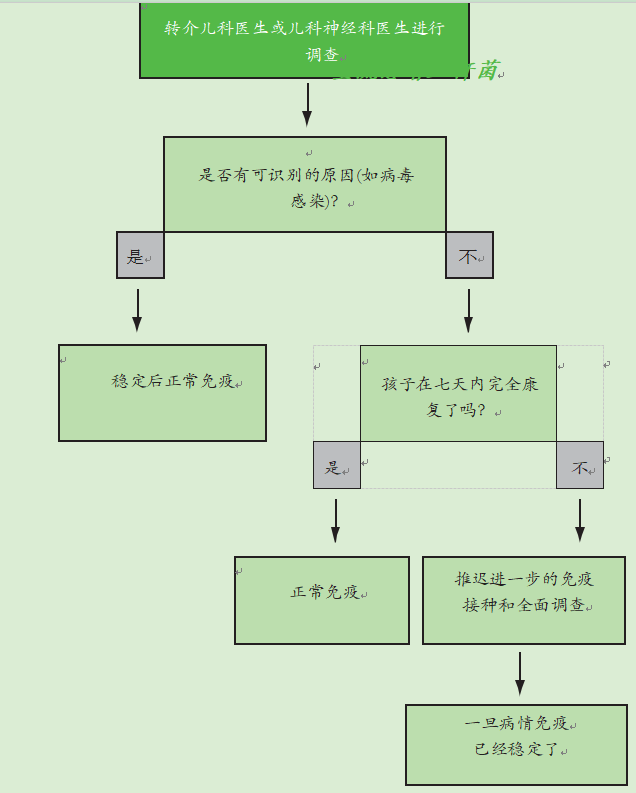
图16.3免疫接种后七天内发生的脑炎或脑病的流程图
确诊的过敏反应极少发生。来自英国、加拿大和美国的数据表明,每100万剂疫苗中发生0.65至3次过敏反应事件(Bohlke et al., 2003; Canadian Medical Association, 2002)。其他过敏情况可能更常见,但不是进一步免疫的禁忌症。
Hib/MenC结合疫苗
通常会出现轻微的副作用,如过敏、食欲不振、疼痛、肿胀、注射部位发红以及轻微的体温升高。
据报告,有不太常见的哭闹、腹泻、呕吐、特应性皮炎、不适和超过39.5℃的发烧。
所有疑似疫苗不良反应发生在儿童身上,或任何年龄的人在接种了标有黑三角(▼)的疫苗后,应使用黄卡计划向人类药物委员会报告。成人对疫苗的严重疑似不良反应应通过黄卡计划进行报告。
病例和联系人的管理
10岁以下的未免疫病例在感染痊愈后,应根据其适龄计划进行免疫接种。以前接种过疫苗的病例应测量其恢复期的抗体水平,并建议加强疫苗接种。在不可能进行抗体检测的情况下,应在感染恢复后给予额外剂量的含Hib的疫苗。
侵袭性Hib病例的家庭接触者感染该疾病的风险增加。10岁以下未接种疫苗的儿童面临巨大风险。应按照当地健康保护单位的建议管理病例接触者,如下所示:
- 从未接种过任何疫苗的儿童,如果年龄在10岁以下,应接种三剂DTaP/IPV/Hib疫苗。
- 从未接种过Hib疫苗但接种过白喉、破伤风、百日咳和脊髓灰质炎疫苗的儿童,如果不满一岁,应接种三剂Hib/MenC疫苗,如果年龄在一岁至十岁之间,应接种一剂。
- 1至10岁的儿童在婴儿期接种过Hib疫苗,但在12个月后没有接种含Hib疫苗的加强剂量,应接种一剂Hib/ MenC疫苗。
如果一个病例的家庭中有任何个人也处于危险中,则指示病例和所有家庭接触者都应给予利福平预防。家庭中的高危人群包括所有10岁以下的儿童和任何年龄的脆弱人群(如免疫抑制或无脾症患者),无论其免疫状况如何。该建议的目的是防止Hib传播给家庭中的脆弱个体。更多信息请访问:
www . HPA . org . uk/Topics/infectious diseases/infection az/Haemophilus influenza etype b/Guidance/
当病例发生在幼儿园、托儿所、托儿所或学校时,应抓住机会识别任何10岁以下未接种疫苗的儿童并为其接种疫苗。当120天内在幼儿园、托儿所、托儿所或学校发生两起或更多Hib病例时,应向所有室内接触者——教师和儿童——提供化学预防。这是一项预防措施,因为几乎没有证据表明,在这种环境下的儿童患Hib疾病的风险明显高于同龄普通人群。
疫苗
- Pediacel(白喉/破伤风/五组分无细胞百日咳/灭活脊髓灰质炎疫苗/b型流感嗜血杆菌(DTaP/IPV/Hib)-由赛诺菲巴斯德MSD公司生产。
- menitorix(Hib/MenC)-由葛兰素史克公司生产。
这些疫苗由医疗物流(电话:0870 871 1890)提供,作为国家儿童免疫规划的一部分。
在苏格兰,应该从当地的儿童疫苗储备中心获得供应。详情可从苏格兰保健用品公司(电话:0141 282 2240)获得。
参考
American Academy of Pediatrics (2003) Active immunization. In: Pickering LK (ed.) Red Book: 2003 Report of the Committee on Infectious Diseases, 26th edition. Elk Grove Village, IL: American Academy of Pediatrics, p 33.
Anderson EC, Begg NT, Crawshaw SC et al. (1995) Epidemiology of invasive Haemophilus influenzae infections in England and Wales in the pre-vaccination era (1990–2). Epidemiol Infect 115: 89–100.
British HIV Association (2006) Immunisation guidelines for HIV-infected adults: www.bhiva.org/pdf/2006/Immunisation506.pdf.
Black SB, Shinefield HR, Fireman B et al. (1991a) Efficacy in infancy of oligosaccharide conjugate Haemophilus influenzae type b (HbOC) vaccine in a United States population of 61,080 children. Pediatr Infect Dis J 10: 97–104.
Black SB, Shinefield H, Lampert D et al. (1991b) Safety and immunogenicity of oligosaccharide conjugate Haemophilus influenzae type b (HbOC) vaccine in infancy. Pediatr Infect Dis J 10: 2.
Bohlke K, Davis RL, Marcy SH et al. (2003) Risk of anaphylaxis after vaccination of children and adolescents. Pediatrics 112: 815–20.
Booy R, Hodgson S, Carpenter L et al. (1994) Efficacy of Haemophilus influenzae type b conjugate vaccine PRP-T. Lancet 344 (8919): 362–6.
Canadian Medical Association (1998) Pertussis vaccine. In: Canadian Immunization Guide. 5th edition. Canadian Medical Association, p 133.
Canadian Medical Association (2002) General considerations. In: Canadian Immunization Guide, 6th edition. Canadian Medical Association, p 14.
Chief Medical Officer, Chief Nursing Officer and Chief Pharmaceutical Officer (2004) Planned Hib vaccination catch-up campaign – further information. www.dh.gov. uk/ cmo/letters/cmo0302.htm
Department of Health (2001) Health information for overseas travel, 2nd edition. London: The Stationery Office.
Diggle L and Deeks J (2000) Effect of needle length on incidence of local reactions to routine immunisation in infants aged 4 months: randomised controlled trial. BMJ
321: 931–3.
Eskola J, Kayhty H, Takala AK et al. (1990) A randomised, prospective field trial of a conjugate vaccine in the protection of infants and young children against invasive Haemophilus influenzae type b disease. NEJM 323 (20): 1381–7.
Heath PT and McVernon J (2002) The UK Hib vaccine experience. Arch Dis Child 86:396–9.
Howard AJ, Dunkin KT, Musser JM and Palmer SR (1991) Epidemiology of Haemophilusinfluenzae type b invasive disease in Wales. BMJ 303: 441–5.
Klein NP, Massolo ML, Greene J et al. (2008) Risk factors for developing apnea after immunization in the neonatal intensive care unit. Pediatrics 121(3): 463-9.
McVernon J, Andrews N, Slack MPE and Ramsay ME (2003) Risk of vaccine failure after Haemophilus influenzae type b (Hib) combination vaccines with acellular pertussis. Lancet 361: 1521–3.
McVernon J, Howard AJ, Slack MP and Ramsay ME (2004) Long-term impact of vaccination on Haemophilus influenzae type b (Hib) carriage in the United Kingdom. Epidemiol Infect 132 (4): 765–7.
Mark A, Carlsson RM and Granstrom M (1999) Subcutaneous versus intramuscular injection for booster DT vaccination in adolescents. Vaccine 17: 2067–72
Miller E (1999) Overview of recent clinical trials of acellular pertussis vaccines. Biologicals 27: 79–86.
Miller E, Southern J, Kitchin N et al. (2003) Interaction between different meningococcal C conjugate vaccines and the Hib component of concomitantly administered diphtheria/ tetanus/pertussis/Hib vaccines with either whole-cell or acellular pertussis antigens. 21st Annual Meeting of the European Society for Paediatric Infectious Diseases, Sicily.
Ohlsson A and Lacy JB (2004) Intravenous immunoglobulin for preventing infection in preterm and/or low-birth-weight infants. Cochrane Database Syst Rev(1): CD000361.
Pfister RE, Aeschbach V, Niksic-Stuber V et al. (2004) Safety of DTaP-based combined immunization in very-low-birth-weight premature infants: frequent but mostly benign cardiorespiratory events. J Pediatr 145(1): 58-66.
Plotkin SA and Orenstein WA (eds) (2004) Vaccines, 4th edition. Philadelphia: WB Saunders Company, Chapter 8.
Pourcyrous M, Korones SB, Arheart KL et al. (2007) Primary immunization of premature infants with gestational age <35 weeks: cardiorespiratory complications and C-reactive protein responses associated with administration of single and multiple separate vaccines simultaneously. J Pediatr 151(2): 167-72.
Ramsay M, Begg N, Holland B and Dalphinis J (1994) Pertussis immunisation in children with a family or personal history of convulsions: a review of children referred for specialist advice. Health Trends 26: 23–4.
Le Saux N, Barrowman NJ, Moore D et al. (2003) Canadian Paediatric Society/Health Canada Immunization Monitoring Program – Active (IMPACT). Decrease in hospital admissions for febrile seizures and reports of hypotonic-hyporesponsive episodes presenting to hospital emergency departments since switching to acellular pertussis vaccine in Canada: a report from IMPACT. Pediatrics 112 (5): e348.
Schulzke S, Heininger U, Lucking-Famira M et al. (2005 ) Apnoea and bradycardia in preterm infants following immunisation with pentavalent or hexavalent vaccines. Eur J Pediatr 164(7): 432-5.
Tozzi AE and Olin P (1997) Common side effects in the Italian and Stockholm 1 Trials. Dev Biol Stand 89: 105–8.
Trotter CL, Ramsay ME and Slack MPE (2003) Rising incidence of Haemophilus influenzae type b disease in England and Wales indicates a need for a second catch-up vaccination campaign. Commun Dis Public Health 6: 55–8.
Tudor-Williams G, Frankland J, Isaacs D et al. (1989) Haemophilus influenzae type b disease in the Oxford region. Arch Dis Child 64: 517–19.
Zuckerman JN (2000) The importance of injecting vaccines into muscle. BMJ 321: 1237–8.
Hits: 85


