Contents
ASPR/CDC Mpox 疫苗接种操作规划指南 – HHS Mpox 疫苗接种计划
ASPR/CDC Mpox Vaccination Operational Planning Guide – HHS Mpox Vaccination Program
感染高危人士疫苗接种资料
更新时间:2024 年 4 月 4 日
修订包括截至 2024 年 4 月 4 日通过 HHS 和商业渠道更新 JYNNEOS mpox 疫苗的可用性。
2024 年 4 月 1 日,Bavarian Nordic 商业化推出了他们的 JYNNEOS 疫苗。在商业化后的一段时间内,HHS将继续根据需要提供JYNNEOS疫苗。HHS 提供的 JYNNEOS 仅作为商业可用性增加时的补充供应,以支持在尚无法获得商业产品的情况下的访问。
提供本业务规划指南是为了帮助州、部落、地方和地区卫生官员进行规划和应对工作。请注意,有关巴伐利亚北欧公司将JYNNEOS疫苗用于管理猴痘(原猴痘)的商业化以及逐步从美国政府(USG)卫生与公众服务部(HHS)JYNNEOS分发过渡到整个文件的新信息。为清晰度和一致性,还进行了其他更新。
2022 年 6 月 28 日,HHS 宣布了一项加强的全国疫苗接种策略,以减轻猴痘的传播。该战略描述了为有猴痘感染风险的人接种疫苗。根据这一战略,美国卫生与公众服务部(HHS)的机构,包括战略准备和应对管理局(ASPR)、美国疾病控制与预防中心(CDC)和食品药品监督管理局(FDA)合作,迅速扩大了从国家战略储备(SNS)中获得数十万剂JYNNEOS疫苗的机会,用于预防性使用猴痘。这些努力使 HHS 能够更快、更公平地向全国各地的司法管辖区分发疫苗。
HHS 于 2022 年 8 月 4 日宣布猴痘为突发公共卫生事件 (PHE)。PHE声明扩大了权力,促进了HHS对蔓延的猴痘疫情做出更有力的反应。尽管 PHE 已于 2023 年 1 月 31 日到期,但 HHS 仍致力于确保美国境内可能接触或有接触猴痘风险的人能够获得 JYNNEOS 疫苗,以防止或尽量减少国内猴痘病例的死灰复燃,包括在 JYNNEOS 向商业市场过渡期间。
随着更多信息的出现,本指导文件将继续更新。
目录
疫苗
ASPR/CDC Mpox 疫苗接种操作规划指南 – HHS Mpox 疫苗接种计划
两种经 FDA 批准的天花疫苗(JYNNEOS 和 ACAM2000)已从 SNS 获得,用作猴痘的暴露后预防 (PEP) 或暴露前预防 (PrEP)(在适当的监管机制下,如适用)。
JYNNEOS 疫苗已获得 FDA 批准用于预防天花和猴痘疾病。2023 年 10 月,免疫实践咨询委员会 (ACIP) 建议 18 岁及以上有猴痘风险的人接种 JYNNEOS:1) 在猴痘暴发期间和 2) 因某些性行为而有猴痘风险,扩大了资格标准。除了 FDA 批准的 JYNNEOS 商业销售的 mpox 适应症外,JYNNEOS 还被授权紧急用于其他年龄组和替代给药途径。医务人员和医疗保健从业者的重要临床考虑因素包括:
- JYNNEOS应分两次注射(两剂系列)给药。
- 两剂应间隔 28 天(范围 24-35 天)。
- 如果在推荐的间隔内未给予第二剂,则应尽快给予。
- 预计在第二剂后 14 天达到峰值免疫力。
- JYNNEOS 适用于被确定为天花或猴痘感染高风险人群。FDA 许可的给药途径是皮下注射(标准方案),适用于 18 岁或以上的人。根据 2022 年 8 月 9 日开始的紧急使用授权 (EUA):
- 未满 18 岁被确定为猴痘病高风险人群可以通过皮下 (SC) 给药(标准方案)接受 JYNNEOS。
- 18 岁或以上被确定为猴痘感染高风险人群也可以通过皮内 (ID) 给药(替代方案)接受 JYNNEOS。
- 即使PHE已过期,JYNNEOS的EUA仍然有效。
- 2023 年 10 月,ACIP/CDC 建议 18 岁及以上有猴痘风险的人群接种 2 剂 JYNNEOS 疫苗系列。
- 评估JYNNEOS疫苗安全性和有效性的早期数据 没有发现任何新的安全问题,并观察到与未接种疫苗的人相比,接种2剂疫苗的人的猴痘发病率降低了9.6倍,接种1剂猴痘的人的猴痘发病率降低了7.4倍。 两剂系列疫苗的有效性为66-89%,一剂后为36-75%。
- JYNNEOS对HIV感染者或特应性皮炎患者是安全的。
- JYNNEOS 在 -20°C 下运输,需要冷链管理。
- 在 -20°C 下储存时,标示有效期适用。
- 有效期在纸箱上,但在小瓶本身上没有。
- 到期日期也可以在 ASPR 网站上找到 HHS 分销的产品。
- 当在2°C-8°C的温度下解冻和冷藏时,根据FDA发布的JYNNEOS的EUA情况说明书,未开封的小瓶可以储存长达8周(然而,这与FDA批准的包装说明书不同,后者将2°C-8°C的储存限制为4周)。
- JYNNEOS用针头/注射器给药;SNS不提供辅助用品。
ACAM2000疫苗已获得 FDA 批准用于预防天花疾病,并被允许根据 CDC 持有的扩大准入 IND 用于预防猴痘病,特别是针对免疫实践咨询委员会建议中概述的正痘病毒感染职业风险人群。
有关这些疫苗的更多信息,请访问:2022 年美国猴痘疫情期间使用 JYNNEOS 和 ACAM2000 疫苗的临时临床注意事项。
JYNNEOS疫苗商业化转型
ASPR/CDC Mpox 疫苗接种操作规划指南 – HHS Mpox 疫苗接种计划
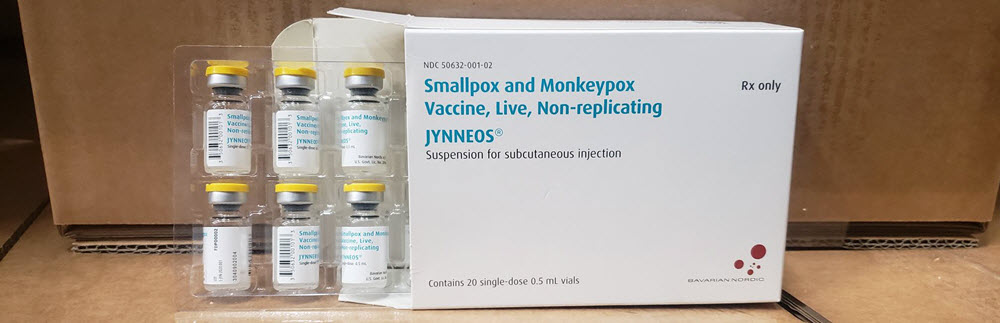
截至 2024 年 4 月 1 日,JYNNEOS mpox 疫苗已上市。作为ACIP推荐的针对18岁及以上高危人群的疫苗接种,该疫苗由Medicare和Medicaid承保,预计将由私人付款人承保。JYNNEOS 的商业分销是以 10 个单剂量小瓶的纸箱(纸箱 NDC 编号:50632-001-03)的形式。这与HHS目前分发的20包单剂量小瓶(纸箱NDC编号:50632-001-02)不同。
在向商业供应过渡期间,随着商业可用性的增加,供应商可以继续获得 HHS JYNNEOS 供应,特别是在尚无法获得商业供应的情况下支持访问。卫生部门应继续利用以前分发的任何剩余的 HHS 提供的库存来支持访问。将根据需要继续通过 HPOP 订购 HHS 供应。2024 年 4 月 30 日上午 9:00,所有当前阈值将设置为零。如果在此之后需要额外的供应,司法管辖区和联邦实体合作伙伴可以使用已建立的 OOC 请求流程。在 2024 年 8 月 1 日或附近,HHS 预计 USG 采购的 JYNNEOS 的请求和订购将完全关闭。
HHS分发的任何猴痘疫苗都不能提交购置费用报销。我们的 SLTT 和联邦实体合作伙伴以及各个供应商都有责任确保不要求从 HHS 免费获得的供应付款。
分销背景
ASPR/CDC Mpox 疫苗接种操作规划指南 – HHS Mpox 疫苗接种计划
2022 年 8 月 1 日实施了数字订购门户,即健康合作伙伴订购门户 (HPOP),使司法管辖区能够下订单、跟踪分发和协调联邦 JYNNEOS 供应的分发。
HSAP培训可从ASPR获得。向免疫规划管理人员、PHEP主任、注册用户、ASPR RECS和辖区注册用户发出了HPOP培训邀请。
迄今为止,HHS 已向 63 个司法管辖区和多个联邦实体合作伙伴提供了大约 110 万瓶 JYNNEOS,并订购了超过 835,000 瓶。
| 阶段 | 启动日期 | 分配给 司法管辖区的小瓶 | 路线 | 地位 |
|---|---|---|---|---|
| 1 | 2022 年 6 月 | 56,000 | SC | 完成 |
| 2 | 2022 年 7 月 | 144,000 | SC | 完成 |
| 3 | 2022年7月/8月 | 383,856 | ID 或 SC | 完成 |
| 4 | 2022 年 8 月 | 360,000 | ID 或 SC | 过渡到 2023 年 1 月的门槛 |
| 5 | 4月 30, 2024 | 0(仅限非周期请求) | SC 或 ID | 从 HHS 分销过渡到商业供应 |
| 总计 = 943,856 瓶 | ||||
- FDA 于 2022 年 8 月 9 日根据 EUA 批准了 JYNNEOS 疫苗。这种变化发生在第 3 阶段,除了 SC 之外,还允许通过 ID 途径给药。 考虑到途径的变化,ASPR 估计在第 3a 阶段分发了大约 313,500 剂仅限 SC 的剂量,在第 3b 和 3c 阶段每瓶最多分发了 5 剂 ID。
- 在下达第 3 阶段订单之前,司法管辖区必须签署数据使用协议 (DUA),并应继续在 HPOP 中输入其总库存和管理计数,以便 HHS 分布式供应,直到所有交付的库存都得到核对。
- HHS 从分阶段分配过渡到管辖阈值方法,类似于用于 COVID-19 疫苗和 TPOXX 分配的阈值方法。
- 阈值计算基于每个司法管辖区目前建议接种 JYNNEOS 疫苗的全国人口的估计百分比。例如,如果推荐人口中有 5% 居住在特定司法管辖区,则该司法管辖区的阈值为该阈值下可用小瓶总数的 5%。
疫苗接种策略
ASPR/CDC Mpox 疫苗接种操作规划指南 – HHS Mpox 疫苗接种计划
截至 2022 年 10 月,大多数 (99%) 猴痘病例为男性,94% 报告在症状出现前 3 周内发生过男性对男性的性接触或密切亲密接触。很大一部分病例(57%)发生在艾滋病毒感染者中。据报道,种族和民族之间存在健康差异,黑人和西班牙裔的病例数量不成比例。
猴痘可以通过密切的、个人的、通常是皮肤对皮肤的接触传播给任何人。
人们在接触猴痘后可以接种疫苗,以帮助预防疾病。
为了达到最有效的目的,在暴露前使用猴痘疫苗的策略应成为更大规模预防工作的一部分,同时考虑受影响的社区、当地流行病学、人口需求以及基于可用疫苗供应的可行性。这种努力应以健康公平原则为基础,并包括社区外展、教育工作和行为策略沟通等策略,以最大限度地降低风险。在与受影响不成比例的社区和群体合作设计和实施疫苗之前使用疫苗的策略可能最有效。例如,成功的HIV PrEP运动是建立在高水平的社区参与之上的,并建立了高度的信任。随着疫情流行病学的发展和新数据的出现,将更新关于暴露前使用猴痘疫苗的临时指南。
有关疫苗接种的更多信息,请参阅:CDC|美国国家猴痘疫苗接种战略的组成部分
健康公平考虑因素
ASPR/CDC Mpox 疫苗接种操作规划指南 – HHS Mpox 疫苗接种计划
在制定疫苗接种计划时,请考虑以下方法,以确保公平分配给所有高危人群:
- 让受影响社区的人们参与疫苗计划的规划,并作为有关猴痘病和疫苗接种的可靠信息来源
- 在所有形式的交流(例如,印刷材料和面对面交流)中以个人的首选语言使用非污名化的通俗语言
- 通过允许个人自我证明符合在接触前接受猴痘疫苗接种的标准(即提供疫苗而不要求个人说明他们符合哪个标准)来减少疫苗接种的障碍
- 以个人的首选语言提供有关所有可用疫苗接种选项的通俗语言详细信息以及支持这些选项的数据
- 重申信息隐私、数据的使用方式以及谁有权访问
- 让已经与受影响人群合作的不同合作伙伴参与进来
- 通过在受影响人群的社区和街区便利地开展弹出式活动和移动外展活动,将疫苗带到受影响人群生活和工作的地方
- 提供多种接种疫苗的机会和时间,包括晚上和周末,以提高可及性
- 利用临床场所为历史上获得初级保健的机会较少的人提供服务,包括性健康诊所、跨性别健康诊所和药房
- 使用多种渠道,例如社交媒体、网站、电视/广播公告或传单来宣传和预约
- 尽量减少使用先到先得的系统;即使采用先到先得的模式,也应实施优先考虑无法获得疫苗能力较差的人群(例如低收入或农村社区)的公平干预措施
通过 HPOP 订购 HHS 提供的 JYNNEOS
ASPR/CDC Mpox 疫苗接种操作规划指南 – HHS Mpox 疫苗接种计划
产品订购
JYNNEOS 目前的门槛将持续到 2024 年 4 月 30 日,使司法管辖区能够通过 HPOP 订购产品,以便在无法获得商业产品的情况下方便访问。美国东部时间 2024 年 4 月 30 日上午 9:00,HHS 将通过将所有阈值设置为零来关闭当前的阈值排序机制。如果在该日期之后在商业供应不可用或无法获得的情况下需要额外的供应,JYNNEOS 将使用既定的非周期请求流程根据请求提供。HHS 采购的 JYNNEOS 的订购预计将于 2024 年 8 月 1 日或接近 2024 年 8 月 1 日完全结束。预计将于2024年8月1日或前后通过CDC的常规疫苗计划提供疫苗。
- 订购少量样品将有助于司法管辖区,将样品瓶用于最需要的地方,并最大限度地减少浪费。这将有助于司法管辖区减少重新分配小瓶的需要,以纠正整个司法管辖区的不太理想的放置。
- 辖区应随时计划和安排疫苗分发、诊所、第二剂和活动,因为您知道,当您继续按照 CDC 的建议使用供应时,完整的阈值将保持可用。
- SNS履行订单以提供这些医疗对策。请将有关订单状态、货件交付更新和温度验证的任何问题直接提交给 SNS sns.ops@hhs.gov。
- USG 提供的 JYNNEOS 的最小起订量 (MOQ) 为 20 瓶。所有订单必须以 20 为增量下单。
通过HPOP订购JYNNEOS需要满足以下条件:
- 报告 IIS 系统中的管理数据。
- HPOP 中的库存报告。
- P产品规格(HHS 分布式电源):
- 标记为单剂量小瓶 (0.5mL),每盒 20 瓶,包装盒尺寸为 5.5 x 1.5 x 4 英寸。每个小瓶的实际填充体积为 6.4mL。
- 最小起订量(MOQ)为1盒,20瓶。
为了继续减缓猴痘的传播,各辖区应重点下令在传播率最高的地区分发疫苗。如果持续的传播很少,疫苗接种工作应侧重于提高有猴痘暴露风险人群的疫苗接种覆盖率,重点是缩小差距。
超过阈值的补充订单(周期外请求)
如果司法管辖区预计超过其设定的阈值,并且必须在 2024 年 4 月 30 日美国东部时间上午 9:00 之后使用 OOC 请求流程,则可以申请额外的小瓶。对疫苗的要求应包括充分证明承诺使用以前分发的和商业供应作为主要选择。在商业供应和报销系统增加的同时,只应要求提供额外的JYNNEOS疫苗,以提高推荐人群的疫苗接种率,并且只在无法获得或无法获得商业产品的情况下支持获取。
司法管辖区可以通过提比略中既定的 OOC 请求流程发起额外小瓶的请求。该请求应包括说明为什么需要额外的疫苗,包括为什么预期的接受者无法获得市售的JYNNEOS疫苗。有关OOC请求流程的更多信息,请联系 SPD_AdminOMT@hhs.gov。
每个准备和管理注射剂的提供者,或监督准备和管理注射剂的提供者都有责任确保患者接受正确的药物并且不会暴露于危及生命的感染。提供者应遵守标准预防措施和安全注射实践原则,包括每次注射使用无菌、一次性、一次性针头和注射器,以及防止注射设备和药物污染。
产品转移
鼓励司法管辖区共享/转让已根据其规格储存的多余产品。如果需要,产品可以在一个司法管辖区内转让,也可以根据州和地方法规转移到其他司法管辖区。我们要求司法管辖区保留有关在各自转让和接收实体的文件中共享的任何产品的库存记录。
交货地点
ASPR/CDC Mpox 疫苗接种操作规划指南 – HHS Mpox 疫苗接种计划
接受 HHS 分发疫苗的地点需要准备好维持冷链并满足其他储存和处理要求。辖区应与当地卫生部门和其他合作伙伴协调制定分配计划,并仔细确定哪些地点将获得疫苗产品,并纳入下列考虑因素。
- 订购地点必须在 HPOP 中注册。
- 司法管辖区可以根据需要指定任意数量的分发地点。接收者应与熟悉处理和储存温控药品的工作人员协调。
- 收件人必须打开运输集装箱并按照随附的说明立即停止临时运输,以验证持续的运输温度范围。
- HPOP mpox MCM订单和发货:
- 温度偏差信息/图片必须发回 sns.ops@hhs.gov。
- SNS 将评估临时图片(是否有偏差),并通过电子邮件批准该产品可用。
- 使用提供的运输标签立即将装运集装箱和临时装运返回 SNS。
- 如果收到的产品有任何问题或疑虑,请立即 sns.ops@hhs.gov 通知 SNS。
- JYNNEOS 应作为 2 剂疫苗系列接种。提供者负责适当管理第二剂 JYNNEOS 所需的打开的 JYNNEOS 小瓶。
- HHS 和制造商提供额外的培训,以准备提供者接种ACAM2000疫苗;提供者将需要接受培训。
- CDC为医护人员和疫苗管理人员提供了解如何使用多次穿刺技术和分叉针头接种ACAM2000天花疫苗所需的信息: 接种ACAM2000天花疫苗视频 |天花 |疾病预防控制中心
报告
ASPR/CDC Mpox 疫苗接种操作规划指南 – HHS Mpox 疫苗接种计划
辖区应继续提供如下所述的库存和管理报告,直到所有 HHS 分发的剂量得到核对。
如果符合以下任何一项,则可以考虑使用小瓶:
- 即使只进行一次注射,也会打开小瓶
- 保留一小瓶用于第二剂
- 由于明显的损坏、明显的篡改或以任何方式掺假(例如颗粒物),整个小瓶无法使用;此外,小瓶应在 HPOP 中报告为浪费
所有其他小瓶都应计入该司法管辖区的可用库存,包括已重新分配到接收直接装运地点之外的小瓶。
下表显示了每个报告要求中应捕获的指标。
| 报告要求 | 小瓶/施用剂量 | 浪费的小 瓶 | 重新分配的小 瓶 | 第一剂小瓶 | 第二剂小瓶 |
|---|---|---|---|---|---|
| 管理(IIS 或 IZDL) | X(剂量) | ||||
| 库存 (HPOP) | X(小瓶) | X | X | X | X |
请确保 HPOP 中的库存数据是最新且准确的。
在HPOP中报告的发明数据应反映:
- 按站点直接装运或按司法管辖区重新分配或汇总的站点上的所有小瓶。
- 与 2022 年猴痘疫情应对相关的库存(即,从 USG 收到的 JYNNEOS 疫苗,无论订购/接收的 HHS 阶段如何)
- 主订单站点中剩余现有库存的库存
- 以小瓶(即非纸箱或剂量)报告的库存
- 请注意:库存报告旨在捕获可用于管理的总库存,包括第一剂和第二剂的小瓶。
为便于参考,猴痘疫苗库存和浪费指南如下表所示。
| 产品 标签 | 授权 | 授权 用于 | 方案 | 样品瓶体积 | 每 瓶剂量 | 最大可报告库存(仅限未开封的小瓶) | 最大 可报告浪费 (仅限样品瓶) |
|---|---|---|---|---|---|---|---|
| JYNNEOS公司 | FDA批准 | 18+ 岁 | 0.5 mL 皮下注射 | 0.5毫升 | 1 | 1 | 1 |
| 紧急使用授权 | <18 岁 | 0.5 mL 皮下注射 | 0.5毫升 | 1 | 1 | 1 | |
| 18+ 岁 | 0.1 mL 皮内注射 | 0.5毫升 | 最多 5 个 | 1 | 1 |
疫苗管理应报告给辖区免疫信息系统(IIS),并包含在辖区向CDC提交的季度常规免疫数据中。有关 IIS 报告的问题可直接向 疫苗管理应报告给辖区免疫信息系统(IIS),并包含在辖区向CDC提交的季度常规免疫数据中。有关 IIS 报告的问题可直接发送至 提出。
供应商协议
ASPR/CDC Mpox 疫苗接种操作规划指南 – HHS Mpox 疫苗接种计划
所有接受 HHS 分发的猴痘疫苗剂量的实体,包括直接接受猴痘疫苗的实体和重新分发疫苗的当地站点,都必须遵守 HHS Mpox 疫苗接种计划提供者协议对 HHS Mpox 疫苗计划的要求。
提供者协议对同时担任疫苗接种者时 HPOP 订购实体的适用性
所有通过 HPOP 命令直接从 SNS 获得猴痘疫苗剂量的实体,如果打算作为疫苗接种提供者直接接种任何这些剂量,都必须遵守 HHS Mpox 疫苗接种计划提供者协议的要求。在使用美国政府免费提供的 JYNNEOS 疫苗时,提供者和提供者的组织将同意遵守提供者协议的要求,包括任何更新。
过期JYNNEOS的处置
ASPR/CDC Mpox 疫苗接种操作规划指南 – HHS Mpox 疫苗接种计划
猴痘的医疗对策一旦部署完毕,就不能返回给SNS。这适用于 HHS 作为 mpox 响应的一部分部署的所有产品,包括 JYNNEOS、ACAM2000 和 TPOXX。
- 目前,JYNNEOS 没有预期的约会延期,一些 JYNNEOS 在 2023 年到期。一旦这些产品过期,司法管辖区可以使用自己制定的处置协议处置产品。医疗废物处理要求可能因州而异,因为它们是由州环境机构制定的。司法管辖区应联系免疫计划或州环境机构寻求指导,以确保疫苗处置程序符合州和联邦法规。
- 要求各司法管辖区保留被销毁产品的批号和数量的记录。浪费记录应输入HPOP。
- 虽然目前没有 JYNNEOS 的预期日期延期,但如果司法管辖区选择这样做,他们可以自由地将过期产品隔离。
准备情况清单
ASPR/CDC Mpox 疫苗接种操作规划指南 – HHS Mpox 疫苗接种计划
以下清单旨在促进 HHS 分布式供应的司法管辖区准备。
- 确定适当的提供者网络,以确保在感染高风险人群中公平扩展:
- 确定提供者并促进他们的参与,特别是能够填补地理或代表性不足的人口差距的提供者。
- 包括为历史上获得初级保健机会较少的人提供服务的临床场所,例如性健康或性病诊所、LGBTQ+ 健康诊所和药房。
- 确定并促进经常照顾残疾人或特殊医疗保健需求(例如 HIV+)的提供者的注册。
- 确定并促进经常照顾残疾人或特殊医疗保健需求(例如 HIV+)的提供者的注册。
- 与各自地区内的部落国家联系,参与规划工作。
- 准备确定的提供者接受 JYNNEOS 疫苗:
- 制定计划,以确定是否或何时可能需要额外的站点,尤其是在疫苗接种计划的最初几周,此时需求可能很高。
- 向医疗保健提供者传播培训和沟通材料(例如,情况说明书、在线视频)。
- 提醒已注册的提供商准备调度系统,并根据需要增加其呼叫中心和网站的容量,以处理额外的数量。
- 确保及时申请第二剂,以完成两剂 JYNNEOS 系列。
- 确保提供者或其他现场工作人员配备和培训,以应对可能的严重过敏反应。
- 各辖区应将交付地点与扩大的配送能力保持一致。
- 将未使用的疫苗剂量保持在适当的温度下,以最大限度地延长储存寿命。
- 加强提供者必须向疫苗不良事件报告系统 (VAERS) 报告接种疫苗后的某些不良事件。
- 定期评估提供者网络的充分性,确定差距以及是否需要额外的疫苗接种地点(例如,地方公共卫生部门、联邦合格医疗保健中心 [FQHC]、其他项目诊所,如 STD/HIV 诊所)以进一步增加公平获取并确保疫苗公平。
Hits: 48