Contents
- 0.1 天花疫苗 ACAM2000 FDA
- 0.2 ACAM2000, (Smallpox (Vaccinia) Vaccine, Live)
- 0.3 Lyophilized preparation for percutaneous scarification
- 0.4 Initial U.S. Approval: 2007
- 1 完整的处方信息
- 1.1 警告:
- 1.2 1 适应症和用法
- 1.3 2 剂量和用法
- 1.4 3 剂型和强度
- 1.5 4 禁忌症
- 1.6 5 警告和注意事项
- 1.7 6 不良反应
- 1.8 7 药物相互作用纳秒
- 1.9 8 用于特定人群使用
- 1.10 12临床药理学
- 1.11 14临床的研究
- 1.12 15参考文献
- 1.13 16如何供应/储存和搬运
- 1.14 17患者咨询信息
天花疫苗 ACAM2000 FDA
ACAM2000, (Smallpox (Vaccinia) Vaccine, Live)
Lyophilized preparation for percutaneous scarification
Initial U.S. Approval: 2007
处方信息要点
这些亮点并不包括所有信息需要使用ACAM2000安全有效。查看完整的处方信息对于ACAM2000。
ACAM2000,(天花(牛痘)疫苗,活着)
用于经皮划痕的冻干制剂
最初的US批准: 2007
| 警告: 看见全部处方信息为完整的方框警告 •心肌炎和心包炎(观察疑似病例的比率为每1000名初级疫苗接种者5.7例 (95% CI: 1.9-13.3)),脑炎,脑脊髓炎、脑病、进行性牛痘、全身性牛痘、严重的牛痘皮肤感染、多形红斑主要(包括史蒂文斯-约翰逊综合征)、湿疹导致永久性后遗症或死亡的疫苗接种,视觉的出现了失明和胎儿死亡等并发症跟随用活痘苗病毒进行初次接种或再次接种天花疫苗。这些风险是有限的在一定程度上增加个人并可能导致严重残疾、永久性残疾神经病学的后遗症和/或死亡【参见警告和预防措施用途(5)]. |
———适应症和使用————
ACAM2000适用于被确定为天花感染高危人群的天花主动免疫接种。
———剂量和管理———
•只有在接受过经皮途径(割)安全有效接种疫苗的培训后,才能接种ACAM2000。(2.3)
•一滴ACAM2000通过使用15针分叉针头的经皮途径(划痕)接种。ACAM2000不应通过皮内、皮下、肌肉或静脉途径注射。(2.3)
•通过将针头浸入ACAM2000小瓶中,用分叉针头吸取复溶疫苗液滴(0.0025 mL)。(2.3)
•参见完整的处方信息,了解疫苗制备说明(2.2)、接种说明,包括为接种者提供用药指南和接种部位护理说明(2.3)以及对疫苗接种反应的解释。(2.4)
•可能会建议重新接种疫苗(例如每3年一次)。(2.5)
———剂量形式和强项———
•用包装稀释剂复溶的冻干粉。复溶后,每瓶约有100剂0.0025毫升的活痘苗病毒,含有2.5–12.5 x105个噬斑形成单位。(3)
———禁忌症———
•预计不会从疫苗中受益的严重免疫缺陷者。这些人可能包括正在接受骨髓移植的人或患有需要隔离的原发性或获得性免疫缺陷症的人(4)。
———警告信息和预防措施———
•心肌炎和/或心包炎、缺血性心脏病和非缺血性扩张型心肌病。(5.1,5.2)
•脑炎、脑脊髓炎、脑病、进行性牛痘(坏死性牛痘)、泛发性牛痘、严重牛痘性皮肤感染、多形性红斑(包括史蒂文斯-约翰逊综合征)、牛痘性湿疹、胎儿牛痘和胎儿死亡。(5.1)
•眼部牛痘和失明。(5.3)
•在以下情况下,这些风险(包括严重残疾和/或死亡的风险)会增加:
•心脏病(5.2)。
•局部类固醇治疗眼疾。(5.3)
•先天性或获得性免疫缺陷疾病。(5.4)
•湿疹和其他皮肤病的历史或存在。(5.5)
•小于12个月的婴儿。(5.6)
•怀孕(5.7)
•ACAM2000是一种活痘苗病毒,可传播给与疫苗接种者密切暴露的人,暴露的风险与疫苗接种者相同。(5.10)
———不良反应———
常见的不良事件包括接种部位体征和症状、淋巴结炎和全身症状,如不适、疲劳、发热、肌痛和头痛(6.1)。与首次接种疫苗的人相比,再次接种疫苗的人发生这些不良事件的频率较低。
在其他部位不慎接种是牛痘疫苗接种最常见的并发症。最常见的受累部位是面部、鼻子、嘴巴、嘴唇、生殖器和肛门。
接种疫苗后可能出现与痘苗在皮肤中复制无关的自限性皮疹,包括荨麻疹和毛囊炎。
报告疑似不良反应,联系急诊生物溶液在1-877-246-8472或者VAERS在800-822-7967和https://vaers.hhs.g观测速度(observed velocity).
———在特定人群中使用———
•ACAM2000可能很少引起胎儿感染,通常导致死胎或死亡。(8.1)
•ACAM2000活痘苗病毒可能会从哺乳期母亲传播给婴儿,从而因意外接种而导致婴儿并发症。(8.3)
•ACAM2000可能与儿童严重并发症风险增加有关,尤其是小于12个月的婴儿。(8.4)
参见17获取患者咨询信息和用药指南
修订日期:【2018年3月】
| 完整的处方信息:内容* | 6 不良反应 *完整处方信息中省略的章节或小节未列出。 |
完整的处方信息
警告:
| •在接受ACAM2000的健康成人初级疫苗接种者中观察到疑似心肌炎和/或心包炎病例(约为5.7/1000,95% CI: 1.9- 13.3)【参见警告和注意事项(5.1)】。 •初次接种或再次接种牛痘病毒天花活疫苗后出现脑炎、脑脊髓炎、脑病、进行性牛痘、泛发性牛痘、严重牛痘皮肤感染、多形红斑(包括史蒂文斯-约翰逊综合征)、导致永久性后遗症或死亡的牛痘性湿疹、眼部并发症、失明和胎儿死亡【参见警告和注意事项(5)】。 •患有以下疾病的疫苗接种者的这些风险会增加,并可能导致严重残疾、永久性神经后遗症和/或死亡: •心脏病或心脏病史 •使用局部类固醇治疗眼疾 •先天性或获得性免疫缺陷疾病,包括服用免疫抑制药物的患者 •湿疹和有湿疹或其他急性或慢性剥脱性皮肤病病史的人 •不到12个月的婴儿 •怀孕 ACAM2000是一种活的牛痘病毒,可传播给与受种者密切暴露的人,暴露的风险与受种者相同。 必须权衡经历严重疫苗接种并发症的风险和经历潜在致命天花感染的风险。 |
1 适应症和用法
ACAM2000®适用于被确定为天花感染高危人群的天花主动免疫接种。
2 剂量和用法
只有在接受过经皮途径(划痕)安全有效注射疫苗的培训后,才能注射ACAM2000。ACAM2000不应通过皮内、皮下、肌肉或静脉途径注射。在注射疫苗前,向每位患者提供FDA批准的用药指南。
2.1疫苗制备说明
2.1.1复溶
ACAM2000通过向含有冻干疫苗的小瓶中加入0.3 mL稀释剂而被复溶。注意:这0.3毫升的稀释液不是这的全部内容稀释剂瓶。ACAM2000只能用所提供的0.3毫升稀释剂进行复溶。在复溶前,应将疫苗小瓶从冷藏中取出并置于室温下。取下疫苗和稀释液瓶的翻盖密封,用异丙醇拭子擦拭每个橡胶塞,并让其彻底干燥。使用无菌技术和配有25号x 5/8 “针头的1 mL无菌注射器(已提供),吸取0.3 mL稀释剂,并将注射器中的全部内容物转移到疫苗瓶中。轻轻旋转混合,但尽量不要让产品粘在橡胶塞上。复溶疫苗应该是澄清至微混浊、无色至稻草色的液体,不含外来物质。接种前,应目视检查复溶疫苗是否有颗粒物质和变色。如果观察到颗粒物质或变色,则不应使用疫苗,小瓶应安全处置。[参见准备/处理注意事项和处置说明(2.2)]
2.1.2重新确认后的存储机构
复溶后,如果保存在室温(20-25℃,68-77℉)下,ACAM2000疫苗可在6至8小时内接种。未使用的复原ACAM2000疫苗可在冰箱(2-8℃,36- 46℉)中储存长达30天,之后应作为生物危险材料丢弃。[参见制备/处理注意事项和处置说明(2.2)]在疫苗接种期间,应通过在患者接种之间将其放置在冰箱或冰上,最大限度地减少复溶疫苗在室温下的暴露。
2.2准备/处理注意事项和处置说明
准备和注射疫苗的人员应戴上外科手套或防护手套,避免疫苗暴露皮肤、眼睛或粘膜。
疫苗瓶、其塞子、稀释剂注射器、用于复溶的通气针头、用于接种的分叉针头以及任何与疫苗暴露的纱布或棉花都应丢弃在防漏、防穿刺的生物危害容器中。然后这些容器应该被适当地处理掉。
2.3疫苗接种说明
在施用前,应使复溶疫苗达到室温。接种前,应目视检查药瓶内容物,以确认不含微粒,并轻轻旋动,不要让产品暴露橡胶塞,如果有必要,再溶解任何可能形成的沉淀物。
接种疫苗的部位是三角肌插入处上方的上臂。
除非预期接种部位的皮肤明显较脏,否则不应进行皮肤准备,在这种情况下,可使用酒精棉签清洁该区域。如果使用酒精,必须让皮肤彻底干燥,以防止活疫苗病毒被酒精灭活。
取下疫苗瓶盖。从独立包装中取出分叉针头。将针头分叉端浸没在复溶疫苗溶液中。针头将在分叉的分叉处拾取一滴疫苗(0.0025毫升)。使用无菌技术,即不要将与手指暴露过的针头上部插入疫苗瓶中,如果针头暴露过皮肤,也不要将针头再次浸入疫苗瓶中。
将疫苗滴在准备接种的干净、干燥的手臂皮肤上。针保持在拇指和食指之间,垂直于皮肤。接种员持针的手腕靠在病人的手臂上。将针头垂直于皮肤快速刺入15次,穿过疫苗液滴,在直径约5毫米的范围内刺穿皮肤。刺入的力度应足够大,以便在疫苗接种部位出现一滴血。
应使用干纱布垫擦去皮肤上任何多余的疫苗和血液液滴,并将其丢弃在生物危害容器中。将针头丢弃在生物危害尖锐物容器中。通过重新插入橡胶盖封闭疫苗瓶,并放回冰箱或冰上,除非它将立即用于接种另一受试者。[参见复溶后的储存(2.1.2)]
用纱布绷带松散地覆盖疫苗接种部位,使用急救胶带将其固定。这种绷带提供了防止痘苗病毒传播的屏障。如果受种者参与直接的病人护理,纱布应覆盖一层半透性(半封闭性)敷料作为额外的屏障。半透性敷料允许空气通过,但不允许液体通过。
在直接暴露疫苗接种部位、可能被疫苗接种部位病毒污染的绷带或衣服、毛巾或床单后,用肥皂和温水或含酒精的擦手剂(如凝胶或泡沫)洗手。这对于去除手上的病毒和防止暴露传播是至关重要的。
将污染的绷带放入密封的塑料袋中,然后扔进垃圾桶。
用含有洗涤剂和/或漂白剂的热水分别清洗可能直接暴露过疫苗接种部位或该部位排水系统的衣物、毛巾、被褥或其他物品。事后洗手。
不要使用阻挡空气进入疫苗接种部位的绷带。这可能会导致疫苗接种部位的皮肤变软并磨损。使用用医用胶带固定的松散纱布覆盖该部位。
不要将药膏或软膏放在接种部位。
2.4解释疫苗接种反应的说明
2.4.1主要的疫苗接种者
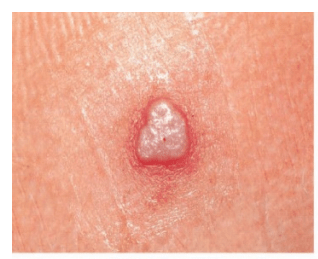
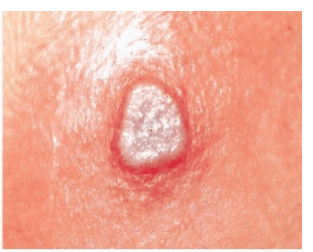
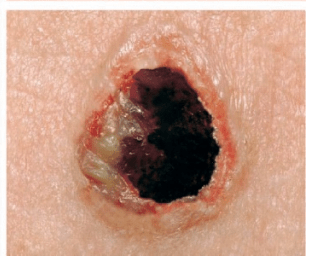
在第一次接种疫苗(初次接种)的个体中,对接种的预期反应是在接种部位出现主要的皮肤反应(以脓疱为特征)。病变逐渐发展,2-5天后在接种部位出现丘疹。丘疹变成水疱,然后是脓疱,在接种疫苗后8- 10天达到最大。脓疱干燥后形成痂,通常在14-21天内分离,留下凹陷的疤痕。(见图1)在第6-8天形成主要的皮肤反应是成功“接受”和获得保护性免疫的证据。可疑反应是任何不是主要反应的反应,并表明由于无效疫苗或不适当的疫苗接种技术而未接种(疫苗接种失败)。
2.4.2以前接种过疫苗的个体(再次接种)
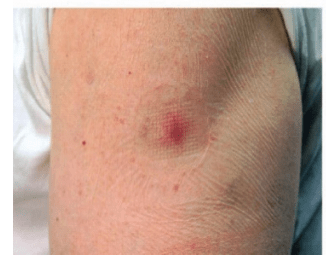
当在接种疫苗后6至8天观察到主要皮肤反应时,确认先前暴露过疫苗的个体接种成功【参见主要疫苗接种者(2.4.1)和图1】。然而,任何先前的疫苗接种可能会改变(减少)再次接种后的皮肤反应(图2),因此没有皮肤反应不一定表明疫苗接种失败。以前接种过疫苗的人在再次接种时没有皮肤反应,不需要再次接种疫苗来引起皮肤反应。
2.4.3疫苗接种失败
初次接种后未成功接种疫苗(即接种失败)的个体可以再次接种疫苗,以达到令人满意的效果。应检查疫苗接种程序,并使用另一小瓶或另一批疫苗重复接种,采用2.3中描述的相同技术【参见疫苗接种说明(2.3)】。
如果使用另一瓶疫苗或另一批疫苗进行重复接种未能产生重大反应,医疗保健提供者应在再次接种疫苗前咨询疾病控制和预防中心(CDC)紧急行动中心(EOC)770-488-7100及其州或地方卫生部门。
图1:初次接种疫苗后主要皮肤反应的进展1
| 5天
| 8天
|
| 10天
| 14天
|
图2:再次接种疫苗后主要皮肤反应的进展1
| 3天
| 7天
|
| 10天
| 14天
|
2.5加强时间表
持续暴露于天花的高风险人群(如处理天花病毒的研究实验室工作人员)应每三年重复接种一次ACAM2000疫苗。
2.6天花疫苗根据美国政府的建议代理
更多信息可从美国国防部获得(超文本传送协议(Hyper Text Transport Protocol的缩写)://万维网.(同Esdras)[圣经]以斯拉记.whs.密耳/门户网站/54/文档/直接伤害/发行/多德/620503p。可移植文档格式文件的扩展名(portable document format的缩写))和美国疾病控制和预防中心(CDC)关于天花疫苗的信息(https://www.cdc.gov/smallpox/clinicians/vaccination.html).
3 剂型和强度
冻干制剂复溶后,每瓶约含100剂0.0025毫升牛痘病毒(活),每剂含2.5- 12.5×105个噬斑形成单位。
4 禁忌症
对于天花高危人群来说,这种疫苗几乎没有绝对禁忌症。必须权衡经历严重疫苗接种并发症的风险与经历潜在致命天花感染的风险。看见警告和预防措施(5)对于经历严重疫苗接种并发症的风险较高的人。
严重免疫缺陷
免疫系统虚弱的人可能会发生严重的局部或全身性牛痘感染(进行性牛痘)。预计不会从疫苗中受益的严重免疫缺陷者不应接种ACAM2000。这些个体可以包括正在接受骨髓移植的个体或患有原发性或获得性免疫缺陷需要隔离的个体。
5 警告和注意事项
最有可能出现严重疫苗接种并发症的人往往是最有可能死于天花的人。必须权衡经历严重疫苗接种并发症的风险与经历潜在致命天花感染的风险。
5.1严重的并发症和死亡
初次牛痘天花疫苗接种或再接种后可能出现的严重并发症包括:心肌炎和/或心包炎、脑炎、脑脊髓炎、脑病、进行性牛痘(坏死性牛痘)、全身性牛痘、严重牛痘皮肤感染、多形性红斑(包括史蒂文斯-约翰逊综合征)、接种性湿疹、失明和孕妇胎儿死亡。这些并发症很少会导致严重残疾、永久性神经后遗症和死亡。根据临床试验,每1000次初级疫苗接种中有5.7次出现疑似心肌炎或心包炎的症状(如胸痛、肌钙蛋白/心肌酶升高或心电图异常)。这一发现包括急性症状性或无症状性心肌炎或心包炎或两者。历史上,接种活痘苗病毒后死亡是罕见的事件;接种活痘苗病毒后,大约每100万次初次接种中有1例死亡,每400万次复种中有1例死亡。死亡通常是心脏性猝死、接种后脑炎、进行性牛痘或接种性湿疹的结果。已接种疫苗的个人意外感染未接种疫苗的暴露者也有死亡报告。
5.1.1严重并发症的发生率1968年美国监控研究
根据常规推荐使用牛痘病毒天花活疫苗(即纽约市卫生局毒株Dryvax)时进行的安全性监测研究,初次接种和再次接种后发生严重并发症的风险估计如下:
表1A-与初次痘苗接种相关的并发症率(a)(病例/百万疫苗接种)(b)
| 年龄(岁) | <1 | 1-4 | 5-19 | ≥20 | 整体发生率(b) |
| 无意接种(c)§ | 507.0 | 577.3 | 371.2 | 606.1 | 529.2 |
| 全身性牛痘 | 394.4 | 233.4 | 139.7 | 212.1 | 241.5 |
| 痘痘湿疹 | 14.1 | 44.2 | 34.9 | 30.3 | 38.5 |
| 进行性牛痘(d) | –(g) | 3.2 | –(g) | –(g) | 1.5 |
| 疫苗接种后脑炎 | 42.3 | 9.5 | 8.7 | –(g) | 12.3 |
| 死亡(e) | 5 | 0.5 | 0.5 | 不知道 | — |
| 合计(f) | 1549.3 | 1261.8 | 855.9 | 1515.2 | 1253.8 |
a.关于并发症的描述见文章。
b.改编自莱恩·JM,鲁伯·弗洛里,内夫·JM,米勒法学博士。1968年天花疫苗接种的并发症:全州调查结果。感染疾病。1970;122:303-309.
c.被称为意外着床。
d.称为坏死牛痘。
e.死于各种并发症。
f.按年龄组划分的总体并发症发生率包括本表中未提供的并发症,包括严重的局部反应、疫苗接种部位的细菌双重感染和多形性红斑。
g.在1968年10个州的调查中没有发现这种并发症。
h.每种并发症的总发生率包括年龄未知的人。
表1B-与牛痘再接种相关的严重并发症率(a)(病例/百万疫苗接种)(b)
| 年龄(岁) | <1 | 1-4 | 5- 19 | ≥20 | 整体发生率(b) |
| 无意接种(c) | (g) | 109.1 | 47.7 | 25.0 | 42.1 |
| 普遍的牛痘 | (g) | (g) | 9.9 | 9.1 | 9.0 |
| 接种性湿疹 | (g) | (g) | 2.0 | 4.5 | 3.0 |
| 进行性牛痘(d) | (g) | (g) | (g) | 6.8 | 3.0 |
| 疫苗接种后脑炎 | (g) | (g) | (g) | 4.5 | 2.0 |
| 死亡(e) | — | — | — | — | — |
| 总数(f) | (g) | 200.0 | 85.5 | 113.6 | 108.2 |
参见表1A对脚注的解释。
5.1.2在2002-2005,严重并发症发生率阳离子和出现心肌炎和/或者心包炎
在2002年12月开始的疫苗接种计划期间,接种Dryvax(一种许可的活痘苗病毒天花疫苗)的美国军事人员和平民第一反应者的不良事件发生率数据如下表2所示。与20世纪60年代收集的数据相比,这些项目中可预防的不良事件(接种性湿疹、暴露传播和自体接种)的发生率明显较低;大概是因为更好的疫苗接种筛选程序和在接种部位常规使用保护绷带。20世纪60年代接种天花疫苗后,心肌炎和心包炎并不常见,但根据军事和民用项目中更积极的监测,心肌炎和心包炎成为更频繁的事件。
表2 –严重的不利的事件在2002-20055
| 不良事件 | Na | 发病率/百万 | Nb | 事故ce/百万 |
| 肌/心包炎 | 86 | 117.71 | 21 | 519.52 |
| 疫苗接种后脑炎 | 1 | 1.37 | 1 | 24.74 |
| 接种性湿疹 | 0 | 0.00 | 0 | 0.00 |
| 泛发性牛痘 | 43 | 58.86 | 3 | 74.22 |
| 进行性牛痘 | 0 | 0.00 | 0 | 0.00 |
| 胎儿牛痘 | 0 | 0.00 | 0 | 0.00 |
| 暴露传播 | 52 | 71.18 | 0 | 0.00 |
| 自动接种(非视觉) | 62 | 84.86 | 20 | 494.78 |
| 眼部牛痘 | 16 | 21.90 | 3 | 74.22 |
a.国防部计划(n=730,580)截至2005年1月,71%的初级疫苗接种;89%男性;平均年龄28.5岁
b.卫生与公众服务部计划(n=40,422)截至1月4日,36%的初级疫苗接种;36%为男性;平均年龄47.1岁
5.1.3ACAM2000临床试验中的心肌炎和心包炎经验
在涉及2983名接受ACAM2000治疗的受试者和868名接受Dryvax治疗的受试者的临床试验中,发现了十(10)例疑似心肌炎【0.2%(2983名受试者中的7名)接受ACAM2000治疗的受试者和0.3%(868名受试者中的3名)】。接种疫苗后出现疑似心肌炎和/或心包炎的平均时间为11天,范围为9至20天。所有经历这些心脏事件的受试者都没有接种过牛痘。在10名受试者中,有2名住院治疗。其余8例无需住院或药物治疗。在这10例病例中,8例为亚临床病例,仅通过伴有或不伴有心肌肌钙蛋白I升高的心电图异常发现。所有病例均在9个月内解决,Dryvax组的一名女性受试者除外,其超声心动图显示左心室射血分数持续临界异常。心肌炎和心包炎风险的最佳估计来自3期ACAM2000临床试验,其中对心肌炎和心包炎的可能性进行了积极监测。在未接种牛痘疫苗的接种者中,两个治疗组均发现8例疑似心肌炎和心包炎病例,总发病率为每1000名接种者6.9例(1,162例中有8例)。ACAM2000治疗组的比率相似:每1000名疫苗接种者中有5.7人(95% CI:1.9-13.3)(873名疫苗接种者中有5人),而Dryvax组的比率为每1000名疫苗接种者中有10.4人(95% CI:2.1-30.0)(289名疫苗接种者中有3人)。在1819名先前接种疫苗的受试者中未发现心肌炎和/或心包炎病例。接种ACAM2000疫苗后心肌炎和心包炎的长期结果目前未知。
5.2心脏的疾病
据报道,接种天花疫苗后会发生缺血性心脏事件,包括死亡;这些事件(如果有)与疫苗接种的关系尚未确定。此外,已有天花疫苗接种后出现非缺血性扩张型心肌病的病例报告;这些病例与天花疫苗接种的关系尚不清楚。
患有已知心脏病的人使用ACAM2000可能会增加不良事件的风险,包括先前诊断患有心肌梗死、心绞痛、充血性心力衰竭、心肌病、胸痛或活动时呼吸急促、中风或短暂性脑缺血发作或其他心脏疾病的人。此外,已被诊断患有以下3种或3种以上缺血性冠心病危险因素的受试者:1)高血压;2)血胆固醇升高;3)糖尿病或高血糖;4)50岁前患有心脏病的一级亲属(例如母亲、父亲、兄弟或姐妹);或者5)吸烟可能会增加风险。
5.3眼部并发症和失明海角
眼部意外感染(眼部牛痘)可能导致眼部并发症,包括角膜炎、角膜疤痕和失明。使用皮质类固醇滴眼液的患者使用ACAM2000可能会增加眼部并发症的风险。
5.4存在先天性或获得性免疫缺陷障碍
免疫系统虚弱的人可能会发生严重的局部或全身性牛痘感染(进行性牛痘),包括白血病、淋巴瘤、器官移植、全身恶性肿瘤、艾滋病毒/艾滋病、细胞或体液免疫缺陷、放射治疗或接受抗代谢药物、烷化剂、高剂量皮质类固醇(>10 mg泼尼松/天或等效剂量持续≥2周)或其他免疫调节药物治疗的患者。严重免疫缺陷者禁用该疫苗【参见禁忌症(4)】。有这些情况的密切暴露者接种疫苗可能会增加风险,因为活痘苗病毒可以脱落并传播给密切暴露者。
5.5有湿疹或病史和其他皮肤疾病
患有任何类型湿疹(如特应性皮炎、神经性皮炎和其他湿疹性疾病)的人(无论病情的严重程度如何)或在过去任何时候有这些疾病病史的人都有较高的风险患上疫苗性湿疹。与患有湿疹的密切暴露者一起接种疫苗可能会增加风险,因为活痘苗病毒可以脱落并传播给这些密切暴露者。患有其他急性、慢性或剥脱性皮肤病(包括烧伤、脓疱病、水痘带状疱疹、开放性皮损寻常痤疮、达里埃病、银屑病、脂溢性皮炎、红皮病、脓疱性皮炎等)的接种者。),或者与患有此类皮肤病的家庭暴露者的接种者也可能有更高的患疫苗性湿疹的风险。
5.6婴儿(<12个月大)和儿童
ACAM2000尚未在婴儿或儿童中进行研究。婴儿接种活痘苗病毒疫苗后发生严重不良事件的风险更高。与婴儿有密切暴露(例如母乳喂养)的接种者必须采取预防措施,以避免无意中将ACAM2000活痘苗病毒传播给婴儿。
5.7怀孕
ACAM2000尚未在孕妇中进行研究。牛痘病毒活疫苗可导致胎儿牛痘和胎儿死亡。如果在怀孕期间使用ACAM2000,应告知接种者其对胎儿的潜在危害【见特定人群用药(8.1)】。作为疫苗接种者的密切暴露者的孕妇可能面临更高的风险,因为活痘苗病毒可以脱落并传播给密切暴露者。
5.8对ACAM2000天花疫苗或其成分的过敏
ACAM2000含有新霉素和多粘菌素b .对这些成分过敏的人在接种疫苗后发生不良事件的风险可能更高。
5.9天花疫苗并发症的管理
疾病预防控制中心可以帮助医生诊断和管理疑似牛痘(天花)疫苗接种并发症的患者。牛痘免疫球蛋白(VIG)适用于接种牛痘病毒天花活疫苗的某些并发症。如果需要VIG和/或其他抗病毒药物或需要其他信息,医生应在东部标准时间周一至周五上午8点至下午4点30分拨打770-488-7100联系CDC EOC其他时间请拨打(404)639-2888。
5.10预防牛痘活病毒的传播
预防因接种牛痘疫苗而导致的无意自动接种和暴露传播的最重要措施是在更换绷带或与接种部位进行任何其他暴露后彻底洗手。
应识别易受痘苗病毒副作用影响的个体,即患有心脏病、眼疾、免疫缺陷状态(包括艾滋病毒感染、湿疹、孕妇和婴儿)的个体,并采取措施避免这些个体与疫苗接种后出现活动性病变的人暴露。
最近接种过疫苗的医护人员应避免与患者暴露,尤其是那些免疫缺陷患者,直到痂与接种部位的皮肤分离。然而,如果与患者的持续暴露不可避免,接种疫苗的医护人员应确保疫苗接种部位覆盖良好,并遵循良好的洗手技术。在这种情况下,可以使用更封闭的敷料。半透性聚氨酯敷料是预防牛痘脱落的有效屏障。然而,渗出物可能积聚在敷料下面,当更换敷料时,必须小心防止病毒传播。此外,敷料下液体的积聚可能会增加疫苗接种部位的皮肤浸渍。首先用干纱布覆盖疫苗,然后将敷料覆盖在纱布上,可以减少渗出物的积累。敷料应每1-3天更换一次[参见自我接种和传播至密切暴露者(17.3)和疫苗接种部位和潜在污染材料的护理(17.4)]。
5.11血液和器官捐献
接种ACAM2000疫苗后至少30天内应避免献血和捐献器官。
5.12疫苗有效性的局限性
ACAM2000天花疫苗可能无法保护所有暴露天花的人。
6 不良反应
以下不良反应将在标签的其他部分详细讨论:
•脑炎、脑脊髓炎、脑病、进行性牛痘(坏死性牛痘)、泛发性牛痘、严重牛痘皮肤感染、严重多形性红斑(包括史蒂文斯-约翰逊综合征)和牛痘性湿疹。可能出现严重残疾、永久性神经后遗症和/或死亡。与已接种疫苗的人有过暴露的未接种疫苗的人死亡。[参见警告和注意事项(5.1)]。
•心肌炎和/或心包炎、缺血性心脏病和非缺血性扩张型心肌病[参见警告和注意事项(5.1)]。
•眼部并发症和失明[见警告和注意事项(5.3)]。
6.1总体不良反应曲线
有关ACAM2000安全性的信息来自三个来源:1) ACAM2000临床试验经验(1、2和3期临床试验),2)在使用其他NYCBH牛痘疫苗进行常规天花疫苗接种的时代收集的数据,以及3)在使用Dryvax(一种经许可的活牛痘病毒天花疫苗)的军用和民用天花疫苗接种计划(2002-2005年)期间获得的不良事件数据。
•一般疾病和管理地点条件:在ACAM2000临床研究中,97%和92%的未接种牛痘疫苗和以前接种过牛痘疫苗的受试者分别经历了一个或多个不良事件。常见事件包括注射部位反应(红斑、瘙痒、疼痛和肿胀)和全身症状(疲劳、不适、发热、寒战和运动耐量下降)。在所有ACAM2000研究中,10%的未接种过牛痘疫苗的受试者和3%的先前接种过牛痘疫苗的受试者经历了至少一次严重不良事件(定义为干扰正常日常活动)。
•神经系统疾病:在ACAM2000研究中,总体而言,50%和34%的未接种过牛痘疫苗的受试者和先前接种过牛痘疫苗的受试者报告了头痛。有报道称接种天花疫苗后出现头痛,需要住院治疗。尽管ACAM2000项目中不到1%的受试者出现严重头痛,但没有人需要住院治疗。
在2002-2005年军队(n=590,400)和DHHS(n = 64,600)项目中评估的与天花疫苗接种暂时相关的神经系统不良事件包括头痛(95例)、非严重肢体感觉异常(17例)或疼痛(13例)以及头晕或眩晕(13例)。严重的神经系统不良事件包括13例疑似脑膜炎、3例疑似脑炎或脊髓炎、11例贝尔麻痹、9例癫痫发作(包括1例死亡)和3例格林-巴利综合征。在这39起事件中,27起(69%)发生在初次接种者中,除2起事件外,其余均发生在接种后12天内。接种天花疫苗后也出现过畏光的病例,其中一些需要住院治疗。
•肌肉骨骼和结缔组织疾病:在ACAM2000的所有研究中,1%的未接种过牛痘的受试者和<1%的先前接种过牛痘的受试者出现了严重的疫苗相关肌痛。其他不良事件包括背痛、关节痛和四肢疼痛,在未接种过牛痘疫苗或先前接种过牛痘疫苗的人群中,发生频率均不超过2%。
血液和淋巴系统疾病:ACAM2000研究中发生率≥5%的唯一不良事件是淋巴结疼痛和淋巴结病。严重淋巴结疼痛和淋巴结病的发生率<1%。
胃肠道(GI)疾病:ACAM2000治疗受试者中常见的胃肠道疾病包括恶心和腹泻(14%)、便秘(6%)和呕吐(4%)。严重腹痛、恶心、呕吐、便秘、腹泻和牙痛占所有报告的严重不良事件,发生在<1%的受试者中。
皮肤和皮下组织异常:分别有18%和8%的受试者出现红斑和皮疹。在ACAM2000名受试者中,1%的牛痘初发受试者和<1%的既往接种受试者经历了至少一次严重不良事件。除一例暴露性皮炎和一例荨麻疹外,所有严重事件均为红斑和皮疹。
接种天花疫苗后出现全身皮疹(红斑性、丘疹性、荨麻疹性、毛囊炎性、非特异性)并不罕见,被认为是发生在无基础疾病的人群中的超敏反应。这些皮疹通常是自限性的,需要很少或不需要治疗,除非患者的病情似乎是毒性的或患有严重的基础疾病。
在身体其他部位的意外接种是牛痘疫苗接种最常见的并发症,通常是由从接种部位转移的疫苗病毒的自体接种引起的。最常见的受累部位是面部、鼻子、嘴巴、嘴唇、生殖器和肛门。眼部意外感染(眼部牛痘)可能导致眼部并发症,包括但不限于角膜炎、角膜疤痕和失明。
接种部位的主要皮肤反应以大面积红斑和硬结以及引流淋巴管的条痕炎症为特征,可能类似于蜂窝织炎。据报道,在天花疫苗接种部位发生了良性和恶性病变。
6.2ACAM2000临床的试验经验
两项随机、对照、多中心3期试验招募了2244名接受ACAM2000的受试者和737名接受对照许可的活痘苗病毒疫苗Dryvax的受试者。研究1在男性(ACAM2000和Dryvax分别为66%和63%)和女性(ACAM2000和Dryvax分别为34%和37%)受试者中进行,这些受试者以前没有接种过天花疫苗(即未接种过牛痘的受试者)。大多数受试者为高加索人(ACAM2000和Dryvax分别为76%和71%),两组的平均年龄为23岁,年龄范围为18-30岁。研究2在男性(ACAM2000和Dryvax分别为50%和48%)和女性(ACAM2000和Dryvax分别为50%和52%)受试者中进行,这些受试者在10年前接种过天花疫苗(即,以前接种过受试者)。大多数受试者为高加索人(两组均为78%),两组的平均年龄为49岁,年龄范围为31至84岁。
6.2.1ACAM2000临床项目中报告的常见不良事件
在3期研究中,ACAM2000或对照治疗组中≥5%的受试者报告的不良事件按不良事件类型、基线疫苗接种状态(初次接种牛痘疫苗与之前接种过牛痘疫苗)和治疗组列出。ACAM2000组和对照组分别有10%和13%的受试者报告了疫苗相关的严重不良事件(定义为干扰正常的日常活动)。在以前接种过疫苗的受试者中,ACAM2000组严重疫苗相关不良事件的发生率为4%,对照组为6%。
表3 -≥在ACAM2000或Dryvax®中有5%的受试者报告的不良事件
| ACAM2000 N=873(b) n (%) | Dryvax® N=289(b) n (%) | ACAM2000 N=1371(c) n (%) | Dryvax® N=448(c) n (%) | |
| 至少有1个不良事件 | 864(99) | 288 (100) | 1325(97) | 443(99) |
| 血液和淋巴系统混乱 | 515(59) | 204(71) | 302(22) | 133(30) |
| 淋巴结疼痛(a)* | 494(57) | 199(69) | 261(19) | 119(27) |
| 淋巴结病 | 72(8) | 35(12) | 78(6) | 29(6) |
| 胃肠的混乱 | 273(31) | 91(31) | 314(23) | 137(31) |
| 恶心(a) | 170(19) | 65(22) | 142(10) | 63(14) |
| 腹泻(a) | 144(16) | 34(12) | 158(12) | 77(17) |
| 便秘(a) | 49(6) | 9(3) | 88(6) | 31(7) |
| 呕吐(a) | 42(5) | 10(3) | 40(3) | 18(4) |
| 一般疾病和注射部位情况 | 850(97) | 288 (100) | 1280(93) | 434(97) |
| 注射部位瘙痒(a) | 804(92) | 277(96) | 1130(82) | 416(93) |
| 注射部位红斑(a) | 649(74) | 229(79) | 841(61) | 324(72) |
| 注射部位疼痛(a) | 582(67) | 208(72) | 505(37) | 209(47) |
| 乏力(a) | 423(48) | 161(56) | 468(34) | 184(41) |
| 注射部位肿胀 | 422(48) | 165(57) | 384(28) | 188(42) |
| 不舒服(a) | 327(37) | 122(42) | 381(28) | 147(33) |
| 感觉发热(a) | 276(32) | 97(34) | 271(20) | 114(25) |
| 僵直(a) | 185(21) | 66(23) | 171(12) | 76(17) |
| 运动耐受性降低(a) | 98(11) | 35(12) | 105(8) | 50(11) |
| 肌肉骨骼和结缔组织疾病 | 418(48) | 153(53) | 418(30) | 160(36) |
| 肌痛(a) | 404(46) | 147(51) | 374(27) | 148(33) |
| 神经系统混乱 | 444(51) | 151(52) | 453(33) | 174(39) |
| 头痛(a) | 433(50) | 150(52) | 437(32) | 166(37) |
| 呼吸系统、胸椎和纵隔系统疾病 | 134(15) | 40(14) | 127(9) | 42(9) |
| 气短(a) | 39(4) | 16(6) | 41(3) | 18(4) |
| 皮肤和皮下的组织紊乱 | 288(33) | 103(36) | 425(31) | 139(31) |
| 红斑(a) | 190(22) | 69(24) | 329(24) | 107(24) |
| 皮疹(a) | 94(11) | 30(10) | 80(6) | 29(6) |
a.事件被列入受试者日记中的检查表;因此应被视为被请求。除上述事件外,以下事件也包括在检查表中:胸痛和心悸,但这些事件在≥5%的受试者中未发生。
b.研究1未接种牛痘的受试者
研究2以前接种过疫苗的受试者
7 药物相互作用纳秒
7.1与其他疫苗同时接种
没有评估ACAM2000与其他疫苗同时接种的数据。
7.2对实验室测试的干扰
ACAM2000可能导致梅毒假阳性检测。阳性RPR试验结果应使用更特异的试验来确认,如FTA试验。
ACAM2000可能会导致结核菌素皮肤试验(纯化蛋白衍生物[PPD])和可能的结核病血液试验出现暂时性假阴性结果。如果可能,结核菌素试验应在接种天花疫苗后推迟1个月。
8 用于特定人群使用
8.1怀孕
妊娠类别D
ACAM2000尚未在孕妇中进行研究。活痘苗病毒疫苗在给孕妇使用时会对胎儿造成伤害。先天性感染,主要发生在妊娠早期,在接种牛痘天花活疫苗后观察到,尽管风险可能较低。已有胎儿泛发性牛痘、死产婴儿早产或围产期死亡高风险的报道。
只有在被认为有可能暴露于天花时,才应该考虑对孕妇进行疫苗接种。如果在怀孕期间使用该疫苗,或者如果接种者与孕妇生活在同一家庭或与孕妇有密切暴露,应告知接种者对胎儿的潜在危害。卫生保健提供者、州卫生部门和其他公共卫生工作人员应向国家妊娠天花疫苗登记处报告所有从受孕前42天开始接种ACAM2000或在之前28天内与接种ACAM2000的人有密切暴露的孕妇..平民妇女应联系他们的医疗保健提供者或国家卫生部门,以帮助注册。所有民事和军事案件都应报告给国防部,电话619 553-9255,国防交换网络(DSN) 553-9255,传真619 533-7601或电子邮件NHRC出生登记@med.navy.mil.
8.3哺乳的母亲
尚未对哺乳期妇女进行ACAM2000研究。尚不清楚疫苗病毒或抗体是否分泌到母乳中。活的痘苗病毒可以无意中从哺乳的母亲传染给她的婴儿。婴儿很容易因接种牛痘疫苗而出现严重的并发症。
8.4小儿科的使用
ACAM2000的安全性和有效性尚未在出生至16岁年龄组中确定。ACAM2000在所有儿科年龄组中的使用得到了来自ACAM2000在成人中的充分和良好对照研究的证据以及在儿科中使用活痘苗病毒天花疫苗的额外历史数据的支持。在根除天花疾病之前,所有儿科年龄组(包括新生儿和婴儿)都常规接种活痘苗病毒天花疫苗,这对于预防天花疾病是有效的。在此期间,活痘苗病毒偶尔与儿童的严重并发症有关,12个月以下婴儿的风险最高。[参见警告和注意事项(5.6)]。
8.5老人的使用
ACAM2000的临床研究没有包括足够数量的65岁及以上的受试者,以确定他们的反应是否与年轻受试者不同。没有已发表的数据支持在老年人群(年龄> 65岁)中使用这种疫苗。
11描述
ACAM2000,天花(牛痘)疫苗,活的,是从Dryvax (Wyeth Laboratories,Marietta,PA,小牛淋巴液疫苗,纽约市卫生局毒株)的噬斑纯化克隆衍生的活牛痘病毒,并且在非洲绿猴肾(Vero)细胞中生长,并且经测试不含外来因子。
ACAM2000作为纯化活病毒的冻干制剂提供,包含以下非活性赋形剂:6-8 mM HEPES (pH 6.5-7.5),2%人血清白蛋白USP,0.5-0.7%氯化钠USP,5%甘露醇USP,以及痕量新霉素和多粘菌素b。
ACAM2000稀释剂含有50% (v/v)甘油USP、0.25% (v/v)苯酚USP注射用水USP,装在3 mL透明玻璃小瓶中,内含0.6 mL稀释剂。
复溶后,每瓶ACAM2000疫苗包含约100剂(0.0025毫升/剂)。痘苗病毒的浓度为1.0-5.0×108噬斑形成单位(PFU)/毫升或2.5-12.5×105 PFU/剂量,通过Vero细胞中的噬斑测定法测定。ACAM2000通过经皮途径(划痕)施用,使用15针浸入疫苗中的不锈钢分叉针。
12临床药理学
天花疫苗不含天花病毒(天花),不会传播或导致天花。
12.1作用机理
痘苗病毒与天花病毒属于同一分类组(正痘属),由痘苗病毒诱导的免疫可针对天花病毒产生交叉保护。痘苗病毒导致接种部位的表皮、皮肤和皮下组织周围以及引流淋巴结的局部病毒感染。病毒可能短暂存在于血液中,并感染网状内皮组织和其他组织。表皮中的朗格汉斯细胞是病毒复制早期的特定目标。在接种部位形成脓疱(“痘坑”或“感染”)提供了保护性免疫的证据。病毒在细胞内复制,病毒抗原被呈递到免疫系统。中和抗体和B、T细胞提供长期记忆。预防天花的中和抗体水平尚不清楚,但超过95%的初次接种者产生了牛痘中和抗体或抑制血凝的抗体。
12.2药效学
12.2.1皮肤的反应
天花疫苗接种后的皮肤反应取决于个体的免疫状态、疫苗效力和接种技术。世卫组织天花专家委员会定义了两种类型的反应,免疫实践咨询委员会(ACIP)也对此进行了描述。反应包括:a)主要的皮肤反应,这表明病毒复制已经发生并且疫苗接种成功;或b)不明确的反应。可疑反应可能是预先存在的足以抑制病毒繁殖的免疫力、疫苗接种技术失败或使用无效疫苗或失效疫苗的结果。
初次接种天花疫苗的人的成功接种(称为初次接种)表现为主要的皮肤反应,定义为水泡或脓疱病变或中央病变周围明确可触及的硬结或充血区域,中央病变可能是结痂或溃疡。
与未接种过牛痘的受试者相比,先前已接种疫苗并再次接种疫苗的受试者可能表现出较低的皮肤反应,但仍表现出对疫苗的免疫反应。【参见剂量和接种(2.4)】
12.2.2中和抗体和细胞免疫反应
众所周知,中和抗体可以介导对天花的保护。初次接种后,超过95%的个体产生针对牛痘的中和抗体,抗体迅速升高(在接种后15-20天),并可能在再次接种时加强。抗体滴度变化很大。与初次接种疫苗相比,接种两次或两次以上疫苗后,滴度可能会在更长时间内保持高水平。初次接种后的中和抗体反应水平通常与皮肤反应的强度成比例。预防天花所需的中和抗体水平尚未明确确定,尽管一些研究表明抗体滴度>1:32的人受到保护。细胞免疫反应也可通过疫苗接种引发,并可能有助于保护和免疫记忆。
12.2.3病毒脱落
在丘疹开始形成期间(第2-5天),病毒从接种部位脱落;接种疫苗后约14-21天,当痂分离且损伤重新上皮化时,脱落停止。临床使用时应采取措施降低接种疫苗患者其他部位意外感染或暴露传播给其他个体的风险【参见疫苗接种说明(2.3)】。
14临床的研究
在两项随机、多中心活性对照临床试验中,通过比较ACAM2000与另一种美国许可的活痘苗病毒天花疫苗Dryvax的免疫应答来评估疫苗效力;一项研究针对以前未接种过天花疫苗的受试者(即未接种过牛痘的受试者),另一项研究针对10年前接种过天花疫苗的受试者(即以前接种过疫苗的受试者)。在两项试验中,共同主要疗效终点是第30天成功接种疫苗/再次接种疫苗的受试者比例和几何平均中和抗体滴度(GMT)。成功的初次疫苗接种被定义为在第7天或第10天(第6天至第11天,有允许的随访窗口)的主要皮肤反应。成功的再接种定义为在第7天(1天)出现可测量大小的任何皮肤损伤。一个专家小组审查了皮肤损伤的数码照片,确定了成功的再接种。
用于比较两个治疗组中成功接种疫苗的受试者比例的统计方法是ACAM2000相对于活性对照的非劣效性检验,旨在排除对照在成功初次接种疫苗(研究1)方面超过5%的优势范围,以及在成功再次接种疫苗(研究2)方面超过10%的优势范围。如果ACAM2000和对照之间的百分比差异的单侧97.5%置信区间(CI)的下限在未接种受试者中超过-5%,在先前接种过疫苗的受试者中超过-10%,则宣布非劣效性。
使用ACAM2000和对照疫苗之间的中和抗体滴度的非劣效性测试进行GMT分析,旨在确保ACAM2000:对照疫苗的GMT比率至少为0.5(相当于log10 (GMT)的差异至少为-0.301)。
在研究1中,共有1037名年龄在18至30岁(含)的男性和女性未接种过牛痘的受试者,主要是白种人(76%),以3:1的比例随机接受ACAM2000 (780名受试者)或对照(257名受试者)。ACAM2000受试者被进一步分层,以1:1:1的比例接受三个批次(批次A、B和C)中的一个(分别为258、264和258名受试者)。将评估所有受试者的皮肤反应,并随机选择一个子集来评估中和抗体反应。
在研究2中,共有1647名男性和女性先前接种过疫苗的受试者,年龄在31至84岁之间,主要是白种人(81%),以3:1的比例随机接受ACAM2000 (1242名受试者)或对照(405名受试者)。ACAM2000受试者进一步分层,以1:1:1的比例接受三个批次(批次A、B和C)中的一个(分别为411、417和414名受试者)。评估所有受试者的皮肤反应,并随机选择一个子集来评估中和抗体反应。
表4和表5显示了两项研究的主要疗效分析结果。
表4–受试者的皮肤反应(疫苗接种成功)接种ACAM2000对比较疫苗,研究1和2
| 研究1 ACAM2000 | 研究1 比较疫苗 | 研究2 ACAM2000 | 研究2 比较疫苗 | |
| 可评估人群的规模(a) | 776 | 257 | 1189 | 388 |
| 疫苗接种成功率(%) | 747 (96)(b) | 255(99) | 998 (84)(d) | 381(98) |
| 正常情况下97.5%单侧置信区间约为。ACAM2000-比较疫苗之间的百分比差异 | -4.67% (c) | — | –17%(e) | — |
| 非劣于比较者 | 是 | — | 否 | — |
a.接受研究疫苗接种并在方案指定的时间框架内接受局部皮肤反应评估的受试者被纳入疗效可评估(EE)人群。
b.结果对于疫苗批次,A、B和C分别为95%、98%和96%。
c.由于评估的临界值被宣布为-5%,ACAM2000被认为在这个参数上不次于比较器。
d.结果对于疫苗批次,A、B和C分别为79%、87%和86%。
e.由于评估的临界值被宣布为-10%,ACAM2000在这一参数上不逊于比较疫苗。
表5–中和抗体反应接受ACAM2000的受试者的反应对比疫苗,研究1和研究2
| 研究1 ACAM 2000年 | 研究1 比较疫苗 | 研究2 ACAM2000 | 研究2 比较疫苗 | |
| 可评估人群的规模(a) | 565 | 190 | 734 | 376 |
| GMT(b) | 166 | 255 | 286 | 445 |
| Log10平均值 | 2.2 | 2.4 | 2.5 | 2.6 |
| 97.5%单侧CI的差异方差分析,ACAM2000对比较疫苗 | -0.307(c) | — | -0.275(d) | — |
| 满足非劣效性 | 不 | — | 是 | — |
a.随机选择的受试者样本接受了研究疫苗,并在基线和治疗后指定时间点收集了中和抗体反应样本
抗体可评估群体。
b.GMT–通过牛痘50%空斑减少中和试验测量的几何平均中和抗体滴度。
c.因为评估的临界值被宣布为-0.301,
ACAM2000在这一参数上不逊于比较疫苗。
d.由于评估的临界值为-0.301,因此ACAM2000在这一参数上不逊于对比产品。
初次接种疫苗者有效免疫反应的主要决定因素是主要的皮肤反应。在引发主要皮肤反应方面,ACAM2000在该人群中并不劣于对照组。产生的抗体反应强度的测量结果相似,但不符合非劣效性的预定标准。在先前接种过牛痘疫苗的受试者中,再次接种牛痘疫苗后出现的主要皮肤反应可能无法准确衡量免疫反应的强度,因为预先存在的免疫力会改变皮肤反应的范围。在先前接种过疫苗的受试者中,ACAM2000在中和抗体免疫反应的强度方面不劣于对照者。因此,ACAM2000在未接种疫苗者的主要皮肤反应率以及先前暴露过牛痘天花疫苗者的中和抗体免疫反应强度方面并不劣于对照组。
15参考文献
1.弗吉尼亚州富基尼蒂,纸甲,巷JM,内夫JM,亨德森,DA。天花疫苗接种:综述,第1部分。背景、接种技术、正常接种和再接种以及预期的正常反应。临床感染疾病。2003;37:241-250.
2.疾病控制和预防中心。读者须知:事件前接种计划中天花疫苗后不良事件的补充建议:免疫实践咨询委员会的建议。2003年MMWR摩布世界周代表;52(13):282-284.
3.美国天花疫苗接种并发症的风险。流行病学杂志。1971;93:238-240.
4.莱恩,JM,鲁本佛罗里达州,奈夫JM,米勒JD。1968年天花疫苗接种并发症:全州调查结果。感染疾病。
1970;122(4):303-309.
5.波兰GA,GrabensteinJD,内夫JM。美国天花疫苗接种计划:一项大型现代天花疫苗接种实施计划的回顾。疫苗。2005;23:2078-2081.
6.卡塞伊格,伊斯坎德尔JK,罗珀MH,马斯特EE,温X-J,托罗克TJ等..2003年1-10月美国与天花疫苗接种相关的不良事件。贾马。2005;94(21):2734-2743.
7.疾病控制和预防中心。更新:2003年美国民间天花疫苗接种后的心脏和其他不良事件。2003年MMWR摩布世界周代表;52(27):639-42.
8.疾病控制和预防中心。天花疫苗接种后的心脏不良事件-美国,2003年。2003年MMWR摩布世界周代表;52(12):248-50.
9.疾病控制和预防中心。更新:天花疫苗接种后的不良事件-美国,2003年。2003年MMWR摩布世界周代表;52(13):278-282.
10.内夫杰姆,莱恩JM,珀斯JH,摩尔R,米勒JD,亨德森达。天花疫苗接种的并发症。1963年美国全国调查。英国医学博士。1967;276:125- 132.
11.疾病控制和预防中心。在赛前接种计划中使用天花疫苗的建议。免疫实践咨询委员会(ACIP)和医疗感染控制实践咨询委员会(HICPAC)的补充建议。MMWR 2003年;52(编号RR- 7)。
12.疾病控制和预防中心。读者注意。怀孕登记的国家天花疫苗。MMWR莫尔布凡人周刊代表2003;52(12):256.
13.疾病控制和预防中心。免疫实践咨询委员会的牛痘(天花)疫苗建议(ACIP)。2001.2001年Morb莫尔勃·莫勒代表;50 (RR10):1-25。
14.塞伊瓦、拉布塔·RJ、查普曼·勒、格拉本斯坦法学博士、伊斯坎德尔·莱恩·JM。2002-2004年美国与天花疫苗接种相关的神经系统不良事件。贾马。2005;294(24):2744-50.
15.接种痘苗病毒部位的NagaoS,Inaba S,Iijima S .朗格汉斯细胞。Arch Dermatol Res. 1976256(1):23-31.
16.痘病毒免疫学。英寸纳米亚斯AJ,奥雷利RJ,编辑综合免疫学,人类感染免疫学,第二部分,病毒和寄生虫。第9卷纽约,纽约:全会;1982:1- 19.
17.Mack TM,Noble J,ThomasDB。血清抗体与预防天花的前瞻性研究。我是。医学与卫生学。1972: 21(2):214-218.
18.国防部指令。编号6205.3国防部生物战防御免疫计划。1993.可向…购买超文本传送协议(Hyper Text Transport Protocol的缩写)://万维网.(同Esdras)[圣经]以斯拉记.whs.密耳/门户网站/54/文档/直接伤害/发行/多德/620503p。螺纹中径f.2018年2月28日接入。
- 疾病控制和预防中心。生物恐怖准备和反应用天花疫苗的使用建议。可向…购买https://www.cdc.gov/smallpox/bioterrorism-response-planning/index . html 2017年5月30日访问。
16如何供应/储存和搬运
16.1怎么提供
ACAM2000,天花(牛痘)活疫苗,装在多剂量3 mL透明玻璃小瓶中,内含冻干粉末(冻干疫苗)。用0.3毫升稀释剂复溶后,小瓶含有约100个标称剂量的0.0025毫升牛痘病毒(活),1.0–5.0×108 PFU/毫升或2.5-12.5×105 PFU/剂。
ACAM2000的稀释剂,50% (v/v)甘油USP,0.25% (v/v)苯酚USP的注射用水USP,装在3 mL透明玻璃小瓶中,内含0.6 mL稀释剂。
分叉针头装在装有100根针头的盒子(5 x 5 x 1 in)中。
配有25号x 5/8 “针头的1 mL结核菌素注射器用于疫苗复溶。
疫苗和稀释剂瓶塞都不是用天然橡胶制成的。
16.2储存;储备和处理
ACAM2000应储存在平均温度为–15℃至-25℃(温度为+5℉至–13℉)的冰箱中。
在复溶前,ACAM2000疫苗在+2-8℃ (36-46℉)的冷藏温度下储存至少18个月,每剂疫苗保持1.0×108 PFU或更高的效价。
在运输过程中,ACAM2000应保持在–10℃或更低的温度下。
复溶后,ACAM2000疫苗可在室温(20-25℃,68-77℉)下于6-8小时工作日进行接种。复溶ACAM2000疫苗可在冰箱(2-8℃,36-46℉)中储存不超过30天,30天后应丢弃[参见剂量和管理(2.3)].天花疫苗的稀释液,(Vero细胞)冻干,ACAM2000应在室温下保存(15-30℃,59- 86℉)。
ACAM2000含有可传播的活痘苗病毒,一旦药瓶被打开,应作为传染物处理。有关处理和处置的详细信息,请参见2.1[疫苗制备说明]和2.2[制备/处理注意事项和处置说明]。
17患者咨询信息
请患者参考FDA批准的ACAM2000天花疫苗用药指南。
17.1疫苗接种的严重并发症
必须告知患者与疫苗接种相关的主要严重不良事件,包括心肌炎和/或心包炎、免疫功能低下者的渐进性牛痘、皮肤病患者的牛痘湿疹、自身和意外接种、全身性牛痘、荨麻疹、重度多形性红斑(包括史蒂文斯-约翰逊综合征)和孕妇的胎儿牛痘。
17.2保护发生不良事件的风险最高的联系人
必须告知患者,他们应避免暴露具有痘苗病毒严重不良反应高风险的人,例如,过去或现在患有湿疹、免疫缺陷状态(包括HIV感染)、怀孕或小于12个月的婴儿。
17.3自我接种和传播到密切暴露者
必须告知患者,从大约第3天开始直到结痂发生,病毒从接种部位的皮肤损伤处脱落,通常在初次接种后的第14-21天。痘苗病毒可通过直接身体暴露传播。有意接种疫苗(自我接种)以外的部位的皮肤意外感染可能因外伤或抓伤而发生。暴露传播也可能导致家庭成员或其他密切暴露者意外接种。意外感染的结果是在疫苗接种者或暴露者不需要的部位出现痘坑病变,类似于疫苗接种部位。自体接种最常发生在面部、眼睑、鼻子和口腔,但创伤性接种的任何部位都可能发生病变。眼睛的自体接种可能会导致眼部牛痘,这是一种潜在的严重并发症。
17.4护理疫苗接种地点和潜在受污染的材料
必须向患者提供以下说明:
•接种部位必须用半透性绷带完全覆盖。保持覆盖部位,直到结痂自行脱落。
•接种部位必须保持干燥。可以继续正常洗澡,但洗澡时用防水绷带覆盖接种部位。网站不应该被擦洗。沐浴后用宽松的纱布绷带覆盖接种部位。
•不要抓伤接种部位。不要抓或抓结痂处。
•不要触摸病变或污染的绷带,然后触摸身体的其他部位,特别是眼睛、肛门和生殖器部位,这些部位容易发生意外(自动)接种。
•更换绷带或暴露伤口后,用肥皂和水或浓度大于60%的酒精擦手溶液彻底洗手。
•为防止传染给暴露者,必须避免与病变部位暴露的物体(如污染的绷带、衣物、手指)的物理暴露。
•使用含有洗涤剂和/或漂白剂的热水单独清洗可能直接暴露过疫苗接种部位或该部位排水系统的衣物、毛巾、被褥或其他物品。事后洗手。
•弄脏和污染的绷带必须放在塑料袋中处理。
•作为防止痘苗病毒传播的额外预防措施,疫苗接种者必须穿有袖子的衬衫覆盖接种部位。这在身体密切暴露的情况下尤其重要。
•疫苗接种者必须每1到3天更换一次绷带。这将使接种部位的皮肤保持完整,并最大限度地减少软化。
•不要在接种部位涂抹药膏或软膏。
•当痂脱落时,用密封塑料袋将其扔掉,然后洗手。
由紧急产品开发公司盖瑟斯堡制造。
美国马里兰州盖瑟斯堡20879
XXXX牌照号
任何和所有紧急生物解决方案公司的品牌、产品、服务和功能名称、徽标和口号都是紧急生物解决方案公司或其在美国或其他国家的子公司的商标或注册商标。保留所有权利。
Hits: 38