DNA vaccination induces sustained virus-specific CD8+ T cell immunity in AIDS monkey model
2月 1, 2024
DNA疫苗接种在艾滋病猴模型中诱导持续的病毒特异性CD8 + T细胞免疫
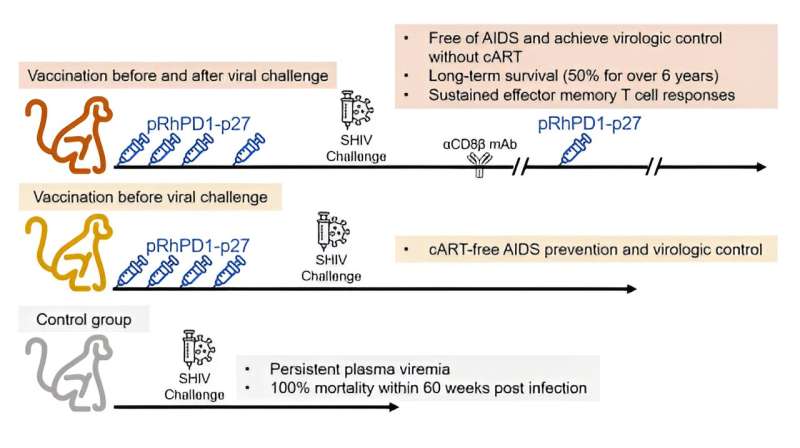
研究人员发现,PD-1增强的DNA疫苗接种可以在艾滋病猴子模型中诱导持续的病毒特异性CD8 T细胞免疫。接种疫苗的猴子在六年内没有艾滋病,并在不需要联合抗逆转录病毒疗法(cART)的情况下实现了病毒学控制,cART是一种用于抑制人类免疫缺陷病毒(HIV)感染者病毒复制的治疗方法。+
该研究还发现,多功能和广泛反应的效应记忆病毒特异性T细胞在受保护的实验猕猴中维持了六年以上。这些发现提供了支持证据,证明PD-1增强的DNA疫苗策略有望成为艾滋病预防和免疫治疗的第三代DNA疫苗。
该研究发表在《微生物学谱》上,由香港大学临床医学院微生物学系艾滋病研究所和李嘉诚医学院新发传染病国家重点实验室的研究人员与香港大学深圳医院、佛山大学和深圳市第三人民医院合作进行。
将 cART 用于暴露前预防 (PrEP) 和暴露后预防 (PEP) 有助于有效减少与艾滋病相关的死亡和 HIV-1 传播病例。尽管 cART 有效,但 HIV-1 可以在潜伏宿主中持续存在。自 1980 年代初发现艾滋病及其病原体 HIV-1 以来的过去 40 年中,这使得对 HIV-1 感染实现完全或持续的无 cART 病毒学控制具有挑战性。
此外,广泛的HIV-1遗传多样性促进了抗cART药物的突变逃逸变异的形成,导致病毒控制的临床失败。大量的病毒变种也阻碍了艾滋病疫苗的开发。确定新的疫苗接种策略,包括诱导强大的交叉反应性T细胞反应,将加强对抗艾滋病毒/艾滋病流行病的武器库。
研究人员开发了一种称为程序性死亡-1(PD-1)增强DNA疫苗策略的疫苗技术,该策略涉及使用DNA载体编码与PD-1蛋白可溶性结构域融合的特异性抗原。
该团队先前的小鼠研究发现,这种策略允许更有效地将抗原递送靶向专业抗原呈递细胞,称为树突状细胞。与常规疫苗相比,它具有免疫原性和对病毒感染和肿瘤发生的保护效力。值得注意的是,PD-1 增强的 DNA 疫苗会引起强烈的 CD8 T 细胞反应。+
2021 年,研究人员报告了一项恒河猴研究的结果,该研究评估了 PD-1 增强的 DNA 疫苗对抗猿猴人类免疫缺陷病毒 (SHIV) 的潜力。恒河猴接种了基于PD-1增强DNA疫苗策略设计的DNA疫苗pRhPD1-p27。
该疫苗导致了针对致病性SHIVSF162P3CN攻击的持续病毒学控制,该攻击是由强大的多功能疫苗诱导的效应记忆 CD8 T 细胞反应介导的。+
在一组四只接种了 pRhPD1-p27 疫苗的猕猴中,病毒血症状态(血液中没有可检测到的病毒)维持了两年,这表明使用 PD-1 增强 DNA 疫苗可以实现潜在的无 cART 病毒学控制。最近的随访研究表明,无 cART 病毒学控制已延长六年多。
更多信息:Xiaoen He 等人,一项后续研究:基于 PD-1 的 DNA 疫苗接种后恒河猴针对致病性 SHIV SF162P3CN挑战的 6 年无 cART 病毒学控制,Microbiology Spectrum (2023)。DOI: 10.1128/spectrum.03350-23
Hits: 36

孟博士您好
1.请问我在外面买东西,接对方给我的东西的时候发现对方手指上有几处伤口,看着都是新的伤口。我自己手指上也有一个刚划伤没多久的伤口,接东西的时候我的伤口和他的伤口碰到了两三次,会不会有感染艾滋的风险?
2.我买的东西是烤串,他的手必然是接触到烤串的签子过的,假如说他的手接触过签子和烤的肉有留下艾滋病毒。我在拿到这些东西后五分钟左右就拿来吃了,吃的时候手上的伤口和签子之间有过来回的摩擦,口腔内和烤肉的部分也会有摩擦行为,我的嘴里牙龈上有一点出血(是我自己的指甲划破的),这种情况会有感染艾滋风险吗?
3.在那之后我坐车回家,可能有个十几分钟的样子到家后我第一时间先用肥皂洗手了,是不是就可以断定我手上已经不可能会有艾滋病毒了?就算在回家的路途中我有将病毒擦在衣服上也早就失活,就算我洗了手再碰衣服也不可能会有病毒重新沾到手上。我在这之后又挠痒将皮肤挠破是不是也没有感染风险了?
1.他的血乜有进入的血液,就不担心;HIV是可以检测的;
2.这个感觉有点偏离HIV的传播方式,如果放不下,医院是可以检测是否感染了HIV
3.HIV常见传播方式输血、共用针头、母婴传播。