A promising vaccine approach to induce longer-lasting protective immunity against COVID-19
新加坡国立大学杨潞龄医学院(NUS Medicine)和莫纳什大学的一个团队设计了一种COVID-19疫苗,该疫苗在临床前模型中通过单次免疫诱导了针对SARS-CoV-2病毒的非常持久的保护性免疫。
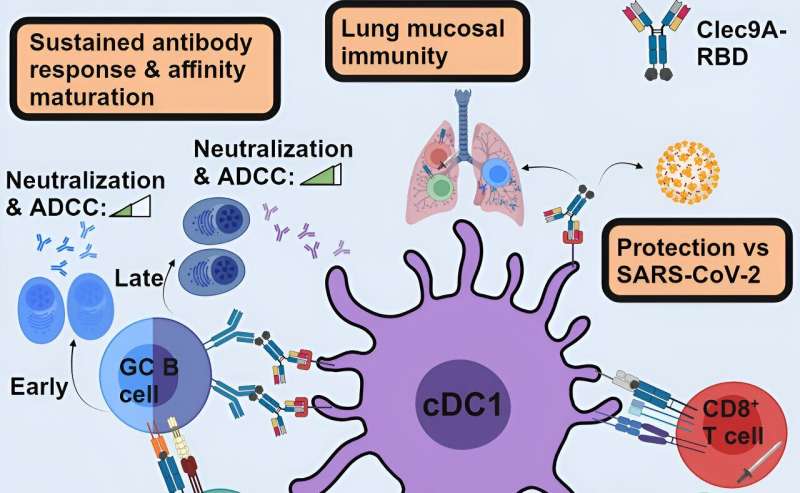
在一项持续四年的合作中,该团队利用一种新型疫苗平台将 SARS-CoV-2 病毒刺突蛋白的受体结合域 (RBD) 融合到 Clec9A 抗体。Clec9A 抗体靶向树突状细胞的特定亚群,树突状细胞是一种在皮肤等组织中发现的特殊类型的免疫细胞,负责启动我们体内的免疫反应。
在对Clec9A-RBD抗体构建体进行单次免疫后,研究小组监测了临床前模型中超过21个月的免疫反应,没有发现免疫力下降的迹象。相比之下,它观察到免疫反应的质量(特别是中和抗体反应)与随着时间的推移增加的保护有关。
该研究题为“靶向SARS-CoV-2候选疫苗的单次树突状细胞诱导小鼠广泛、持久和保护性的全身和粘膜免疫”,发表在《分子疗法》上。
这种新的 Clec9A 靶向技术可能会解决 COVID-19 疫苗免疫力减弱的问题,并消除重复加强针的需要,特别是对于 60 岁及以上的人、医疗脆弱的个人及其护理人员。
“我们在这项研究中看到的结果非常有希望,我们相信在临床前模型中进行的工作可以高度转化为人类,”这项研究的首席研究员Sylvie Alonso副教授说。“事实上,这种免疫细胞亚群的人类等价物存在,我们的合作者,莫纳什大学的Mireille Lahoud副教授正在开发这种方法,用于未来的人类应用。
Lahoud副教授说:“这项研究证明了我们针对特定免疫细胞的平台在疫苗改进方面的优势,并体现了从基础发现到转化研究的国际研究合作的力量。
“在许多疾病中,有效的疫苗已被证明难以产生。该平台的验证为应对此类挑战提供了强有力的概念验证,“她说。
据报道,当前的信使 RNA (mRNA) COVID-19 疫苗在接种后三周后显示出 62% 的峰值有效性,然后在 9 个月后降至 9%。据报道,加强剂量的保护作用减弱,从加强剂量后一个月的 60% 下降到 9 个月时的 13%。
“我们在新加坡国立大学医学院和莫纳什大学的团队预计,当用作加强疫苗策略时,Clec9A靶向技术诱导的免疫反应具有非凡的持久性,可以解决当前mRNA疫苗的缺点,其中最主要的是免疫反应的迅速减弱,”副教授Alonso说,他也是新加坡国立大学医学院传染病转化研究项目的联合主任。
更多信息:Nicholas You Zhi Cheang 等人,靶向 SARS-CoV-2 候选疫苗的单次树突状细胞诱导小鼠广泛、持久和保护性的全身和粘膜免疫,分子疗法 (2024)。DOI: 10.1016/j.ymthe.2024.05.003
Hits: 22
