Contents
Yellow Fever
CDC Yellow Book 2024
Travel-Associated Infections & Diseases
作者: Mark Gershman, J. Erin Staples
传染性病原体:黄热病病毒
流行
撒哈拉以南非洲
热带南美洲
暴露和感染风险最大的旅行者类别
未接种疫苗的人访问流行地区的森林或稀树草原地区,或访问黄热病持续暴发的目的地
预防方法
避免昆虫叮咬
黄热病是一种疫苗可预防的疾病
诊断支持
国家卫生部门;或联系CDC虫媒病毒病处(970-221-6400;dvbid@cdc.gov)
传染性病原体
黄热病(YF)病毒是一种单链RNA病毒,属于黄病毒属。
传播
黄热病病毒的媒介传播是通过受感染的蚊子叮咬发生的,主要是伊蚊或血蚊属。非人灵长类动物和人类是该病毒的主要宿主,并且发生了人为传播(人与媒介到人)。黄热病病毒有 3 个传播周期:森林(丛林)、中间(热带草原)和城市。
森林(丛林)循环涉及病毒在非人灵长类动物和森林树冠中发现的蚊子物种之间的传播。当职业或娱乐活动侵入丛林时,病毒通过蚊子从猴子传播给人类。在非洲,中间(稀树草原)周期涉及黄热病病毒从树洞繁殖的伊蚊属传播给丛林边境地区的人类。黄热病病毒可以通过这些蚊子从猴子传播给人类或从人传播到人类。城市循环涉及病毒在人与家禽周围蚊子(主要是埃及蚊)之间的传播。
感染黄热病病毒的人在发烧前不久和发病的前 3-5 天内经历最高水平的病毒血症,在此期间他们可以将病毒传播给蚊子。由于病毒血症水平很高,理论上可以通过输血或针刺发生血源性传播。已记录到一例野生型黄热病病毒围产期传播病例,该病例来自一名在分娩前 3 天出现黄热病症状的妇女;该名婴儿随后检测出黄热病病毒RNA呈阳性,并在出生后第12天死于暴发性黄热病。
流行病学
黄热病发生在撒哈拉以南非洲和热带南美洲,在那里流行且间歇性流行(黄热病病毒传播风险国家名单见表5-22和表5-23)。人类中的大多数黄热病是由森林或中间传播周期引起的。城市黄热病在非洲周期性发生,在美洲零星发生。在非洲黄热病病毒持续传播的地区,自然免疫力随着年龄的增长而积累;因此,婴儿和儿童患病的风险最大。在南美洲,黄热病最常见于未接种疫苗的年轻人,他们因在森林地区工作而接触蚊媒。
表5-22 黄热病病毒传播风险国家1
| 非洲 | ||
| 安哥拉 贝宁 布基纳法索 布隆迪 喀麦隆 中非共和国 乍得2 刚果、科特迪瓦共和国 | 刚果 民主共和国 赤道几内亚 埃塞俄比亚2 加蓬 冈比亚 加纳 几内亚 几内亚比绍 肯尼亚2 利比里亚 | 马里2 毛里塔尼亚2 尼日尔2 尼日利亚 塞内加尔 塞拉利昂 南苏丹 苏丹2 多哥 乌干达 |
| 美洲 | ||
| 阿根廷2 玻利维亚2 巴西2 哥伦比亚2 厄瓜多尔2 | 法属圭亚那 圭亚那 巴拿马2 巴拉圭 | 秘鲁2 苏里南 特立尼达和多巴哥2 委内瑞拉2 |
脚注显示/隐藏
1截至 2022 年 11 月。世界卫生组织 (WHO) 将其定义为“目前或过去已报告过黄热病,并且目前存在病媒和动物宿主”的国家或地区。见www.who.int/publications/m/item/countries-with-risk-of-yellow-fever-transmission-and-countries-requiring-yellow-fever-vaccination-(november-2022)。
2这些国家不是全地方病(该国只有部分地区有黄热病病毒+传播的风险)。有关详细信息,请参阅地图5-10,地图5-11和黄热病疫苗建议(第2节,第5章,黄热病疫苗和疟疾预防信息,按国家/地区划分)。
表5-23 黄热病病毒暴露可能性低的国家1
| 非洲 | ||
| 厄立特里亚2 卢旺达 | 索马里圣多美和普林西比2 | 坦桑尼亚 赞比亚2 |
脚注显示/隐藏
1该名单上的国家接触黄热病病毒的可能性较低,未被列入世界卫生组织黄热病病毒传播风险国家名单(表5-22)。除非一个国家要求所有入境旅客提供黄热病疫苗接种证明(表5-25),或另有规定,否则从本名单上国家抵达的旅客不应要求提供黄热病疫苗接种证明。
2仅在某些地区被归类为“接触黄热病病毒的可能性低”;其余地区被归类为没有接触黄热病病毒的风险。
旅行者面临的风险
旅行者感染黄热病的风险取决于其免疫接种状况以及目的地特定因素(例如,当地病毒传播率)和旅行相关因素(例如,暴露持续时间、职业和娱乐活动、季节)。报告的人类疾病病例是疾病风险的主要但粗略的指标。由于传播水平低、人群免疫水平高(例如,由于疫苗接种)或当地监测系统无法发现病例,目的地可能没有病例报告。由于“流行病学沉默”并不意味着没有风险,旅行者不应在没有采取保护措施的情况下进入流行地区。
黄热病病毒在西非农村地区的传播是季节性的;在雨季结束和旱季开始时,通常是7月至10月,风险升高的时期。在东非,黄热病病毒的传播通常难以预测,因为该地区的病毒活动之间往往间隔很长(几年);当黄热病病毒在东非传播时,季节性与西非相似。
在南美洲,雨季(1-5月,2月和3月为发病高峰)的森林病媒感染风险最大。然而,埃及埃吉普蒂菌可以在农村和人口稠密的城市地区偶发性传播黄热病病毒,即使在旱季也是如此。
在1970-2015年期间,美国和欧洲的黄热病患者报告了11例黄热病病例,这些患者曾前往西非(6例)或南美洲(5例);8例(73%)死亡。只有 1 名旅行者有黄热病疫苗接种史;那个旅行者活了下来。从2016年开始,与旅行相关的黄热病病例数量大幅增加,主要是因为安哥拉和巴西的疫情暴发。在2016年至2021年年中期间,在非流行地区或国家居民的未接种疫苗的旅行者中报告了>37例旅行相关病例,其中包括≥15名欧洲旅行者和1名前往秘鲁的美国旅行者。
由于病毒传播的生态决定因素各不相同,因此难以预测在旅行期间感染黄热病的风险。对于停留 2 周的未接种疫苗的旅行者访问流行地区,因 YF 引起的疾病和死亡的估计风险如下:在西非,患病风险为每 100,000 人中有 50 人,死亡风险为每 100,000 人中有 10 人;在南美洲,患病风险为每10万人中有5人患病,死亡风险为每10万人中有1人死亡。这些估计基于常住人口的风险,通常是在传播高峰期,可能无法准确反映具有不同免疫力、遵循蚊虫叮咬预防措施、户外暴露较少或在非高峰期旅行的旅行者的风险。当目的地发生疫情时,旅行者被感染的风险可能更大。
临床表现
大多数黄热病病毒感染者症状轻微或没有症状,不太可能就医。对于出现症状性疾病的患者,潜伏期通常为 3-6 天。最初的疾病是非特异性的:背痛、寒战、发热、头痛、肌痛、恶心和呕吐以及虚脱。大多数在初次就诊后有所改善。在短暂缓解 ≤48 小时后,≈12% 的感染患者进展为更严重的疾病形式,其特征是出血症状、黄疸,最终出现休克和多系统器官衰竭。重症病例的病死率为30%-60%。
诊断
黄热病是一种全国性的法定报告疾病。初步诊断基于临床表现和暴露细节。实验室诊断最好通过病毒分离或核酸扩增检测(例如逆转录 PCR [RT-PCR])或血清学检测进行。在病程早期进行 YF 病毒或 YF 病毒 RNA 的病毒分离或核酸扩增试验。当识别出更明显的症状时,病毒或病毒RNA可能不再可检测到;因此,不应使用病毒分离和核酸扩增检测来排除黄热病的诊断。
血清学检测可用于检测病毒特异性 IgM 和 IgG 抗体。然而,由于针对其他黄病毒的抗体之间可能存在交叉反应性,因此应进行更具特异性的抗体检测(例如,斑块减少中和试验)以确认感染。请联系您所在州或地方卫生部门,或致电 970-221-6400 联系美国疾病控制与预防中心 (CDC) 虫媒病毒病处,以协助进行 YF 病毒感染的诊断检测。
治疗
目前尚无治疗黄热病病毒感染的特效药物;治疗旨在缓解症状或挽救生命的干预措施。补液、休息以及使用镇痛药和解热药可能会缓解疼痛和发热的症状。避免开具可能增加出血风险的药物(例如阿司匹林或其他非甾体抗炎药)。在发病的最初几天,将感染者关在室内或蚊帐下,防止他们进一步接触蚊子,以免他们参与传播循环。
预防
个人防护措施
预防蚊媒疾病(包括黄热病)的最佳方法是避免蚊虫叮咬(见第4章,第6章,蚊子,蜱虫和其他节肢动物)。
疫苗
黄热病可以通过相对安全、有效的疫苗来预防。目前生产的所有黄热病疫苗都是减毒活病毒疫苗。只有一种黄热病疫苗(YF-VAX,赛诺菲巴斯德)获准在美国使用(表5-24)。在美国,由于生产问题,YF-VAX定期出现短缺,包括从2015年底持续到2021年初的短缺。为了解决最近的短缺问题,赛诺菲巴斯德与疾病预防控制中心和美国食品和药物管理局(FDA)合作,根据扩大准入的研究性新药方案进口和分销Stamaril(一种与YF-VAX相当的YF疫苗,在该公司位于法国的工厂生产)。
不同的黄热病疫苗产品,包括在美国以外生产的产品,在反应原性或免疫原性方面没有实质性差异。考虑接种其他国家/地区许可但未经 FDA 批准的 YF 疫苗的人可以预防 YF。有关黄热病疫苗供应的最新信息,请查看CDC旅行者健康网站。
表5-24 黄热病预防疫苗
| 疫苗
| 商品名称 (MANU- FACTURER) | 年龄
| 剂量
| 路线
| 附表
| 加强剂
|
| 17D型
| YF-VAX(赛诺菲巴斯德)
| ≥9个月1
| 0.5毫升2
| 皮下注射
| 1剂
| 不建议大多数人使用3 |
脚注显示/隐藏
1 6-8 个月和 60 ≥是预防措施,<6 个月是接种黄热病疫苗的禁忌症。
2 YF-VAX有单剂量和多剂量(5剂)小瓶。
3 有关重新接种的更多详细信息,请参阅本章中的预防:疫苗:加强剂量。
适应症
建议在非洲或南美洲有黄热病病毒传播风险的地区居住或旅行的 ≥9 个月大的人接种黄热病疫苗。此外,一些国家/地区要求提供黄热症疫苗接种证明才能入境。有关特定国家/地区的黄热病疫苗接种建议和要求,请参阅第 2 节,第 5 章,黄热病疫苗和疟疾预防信息,按国家/地区划分。
由于接种黄热病疫苗后存在发生严重不良事件的风险,临床医生应仅为有黄热病病毒暴露风险或需要疫苗接种证明才能进入一个国家的人接种疫苗。为进一步减低严重不良事件的风险,在接种黄热病疫苗前,应仔细观察禁忌症,并考虑疫苗接种预防措施(插文5-09)。有关更多信息,请参阅免疫实践咨询委员会 (ACIP) 的黄热病疫苗建议。
专栏5-09 黄热病疫苗禁忌症和注意事项
禁忌
- 年龄 <6 个月
- 对疫苗成分过敏1
- HIV 感染(有症状)或 CD4 T 淋巴细胞计数 <200/mL(或 <6 岁儿童淋巴细胞总数的 <15%)2,3
- 原发性免疫缺陷
- 免疫抑制和免疫调节疗法
- 恶性肿瘤
- 与免疫细胞功能异常相关的胸腺疾病
- 移植
预防 措施
- 年龄 6-8 个月
- 年龄 ≥60 岁
- 母乳喂养
- HIV 感染(无症状)和 CD4 T 淋巴细胞计数为 200-499/mL(或占 <6 岁儿童淋巴细胞总数的 15%-24%)2,3
- 怀孕
脚注显示/隐藏
1如果考虑接种疫苗,可以在过敏反应管理经验丰富的医生的直接监督下进行脱敏。
2HIV的症状在疾病控制和预防中心进行分类。1993年 修订了艾滋病毒感染分类系统,扩大了青少年和成人艾滋病监测病例的定义。MMWR Recomm Rep 1992;41(RR-17)。可查阅:www.cdc.gov/mmwr/preview/mmwrhtml/00018871.htm(见表1 成人和青少年);以及艾滋病毒感染儿童抗逆转录病毒治疗和医疗管理小组。2010年儿童HIV感染使用抗逆转录病毒药物指南。第20-2页。可从:www.hopkinsmedicine.org/som/faculty/appointments/_documents/_ppc_documents/portfolios/Hutton/Hutton-Portfolio-Samples/guidelines-for-the-use-of-antiretroviral-agents-in-pediatric-hiv-infection.pdf[PDF]。
32010年,免疫实践咨询委员会(ACIP)使用这种HIV感染者免疫抑制水平的临床分类来为黄热病疫苗建议提供信息(见Staples等人,黄热病疫苗:免疫实践咨询委员会的建议)。2014年公布了修订后的HIV感染监测病例定义。迄今为止,ACIP尚未更新针对HIV感染者的黄热病疫苗建议。
接种
对于所有符合条件的人群,皮下注射单次 0.5 mL 重组疫苗,这是标准剂量。
与其他疫苗共同给药
灭活疫苗
没有证据表明灭活疫苗会干扰对黄热病疫苗的免疫反应。因此,灭活疫苗可以同时接种,也可以在接种黄热病疫苗之前或之后的任何时间接种。
减毒活病毒疫苗
ACIP建议黄热病疫苗与其他活病毒疫苗同时接种。如果无法同时接种,请在两次疫苗接种之间等待 30 天,因为如果在接种另一种活病毒疫苗后 30 天内接种,对活病毒疫苗的免疫反应可能会受损。一项研究表明,黄热病疫苗和麻疹-腮腺炎-风疹 (MMR) 疫苗的联合接种降低了除麻疹外所有抗原的血清转化率。最近的两项研究也显示,在疫苗共同接种后血清转化的人中,抗体浓度较低。这些研究表明,只要有可能,最好间隔 30 天接种 YF 和 MMR 疫苗。然而,更重要的是确保旅行者在旅行前适当接种疫苗;因此,黄热病和MMR疫苗的联合接种是可以接受的。
没有关于鼻用减毒活流感疫苗与黄热病疫苗同时接种的免疫反应的数据。
活细菌疫苗
数据表明,口服Ty21a伤寒疫苗(Vivotif)是一种活细菌疫苗,可以同时接种,也可以在接种黄热病疫苗之前或之后的任何时间间隔接种。没有关于与黄热病疫苗同时接种的口服霍乱减毒活疫苗(Vaxchora)的免疫反应的数据。
分次接种
近年来,一些国家在黄热病大规模暴发期间通过接种部分疫苗剂量(通常为0.1毫升)来扩大疫苗供应,这种做法称为分次给药。有限的研究数据表明,在皮下给药后 1 个月和 ≤1 年,分次给药的免疫原性与全剂量 YF 疫苗接种相当;然而,关于分次给药的知识差距仍然存在。
在美国,FDA尚未批准黄热病疫苗的分次给药。此外,世卫组织指出,分次给药不符合《国际卫生条例》规定的黄热病疫苗接种要求;国际旅行的疫苗接种证明不能发给只接种过部分剂量的人。
加强剂量
2014年,世卫组织免疫战略咨询专家组得出结论,单剂初次接种黄热病疫苗可提供持续的免疫力和终生预防黄热病的保护,不需要重新接种(加强剂)。2016年,《国际卫生条例》正式修订,规定完整的国际疫苗接种或预防证书(ICVP或“黄卡”)在疫苗接种者的一生中有效,各国不得要求将再次接种黄热病疫苗的证明作为入境条件,即使最后一次接种疫苗是在10年前>。
ACIP还表示,单剂黄热病疫苗可提供持久的保护,对大多数旅行者来说已经足够了。然而,ACIP指南确实与世卫组织的指南略有不同,它明确建议以下旅行者群体接种额外剂量的黄热病疫苗:接种初始剂量疫苗时怀孕的人(在下一次面临黄热病风险之前再接种1剂);在接种一剂黄热病疫苗后接受造血干细胞移植的人(只要他们有足够的免疫功能,在下一次有黄热病风险之前重新接种疫苗);接种最后一剂黄热病疫苗时感染艾滋病毒的人(如果他们继续有患黄热病的风险,则每 10 年接种一剂)。
如果旅行者根据活动、旅行时间、地点和季节前往高风险环境,考虑对 ≥10 年前接种最后一剂 YF 疫苗的旅行者进行加强剂量。这一考虑适用于计划在流行地区长期逗留的旅行者、在传播高峰季节前往流行地区(例如西非农村)的旅行者,或访问持续暴发地区的旅行者。
尽管不建议大多数旅行者接种黄热病疫苗加强剂量,尽管2016年《国际卫生条例》进行了修改,但临床医生和旅行者仍应审查目的地国家的入境要求。有关特定国家的建议和要求的更多信息,请参阅第2节,第5章,黄热病疫苗和疟疾预防信息,按国家/地区划分。
不良事件
常见不良反应
对黄热病疫苗的反应通常较轻;10%-30% 的疫苗接种者报告有轻微的全身症状,包括头痛、低烧和肌痛,这些症状在接种疫苗后几天内开始,持续 5-10 天。
严重不良反应
超敏反应
以支气管痉挛、皮疹或荨麻疹为特征的即刻超敏反应并不常见。据报道,黄热病疫苗后的过敏反应发生率为每 100,000 剂 1.3 例。
黄热病疫苗相关神经系统疾病
黄热病疫苗相关神经系统疾病 (YEL-AND) 是一系列临床综合征,包括急性播散性脑脊髓炎、格林-巴雷综合征、脑膜脑炎,以及罕见的颅神经麻痹。从历史上看,YEL-AND主要在婴儿中被诊断为脑炎,尽管最近的病例报告描述了大多数年龄组人群中的各种神经系统综合征。YEL-AND很少致命。
全球报告的几乎所有YEL-AND病例都发生在首次接种疫苗的人身上。在美国,有记录的病例的发病时间为接种疫苗后 2-56 天。在美国,YEL-AND 的发病率为每 100,000 剂 0.8 例,但在 ≥60 岁人群中更高(每 100,000 剂 2.2 例)。
黄热病疫苗相关嗜脏疾病
黄热病疫苗相关内脏嗜病毒病(YEL-AVD)是一种类似于野生型黄热病的严重疾病,其中疫苗病毒在多个器官中增殖,常导致多器官功能障碍或衰竭,偶导致死亡。自2001年以来,全世界报告了100>确诊和疑似耶尔-AVD病例。
据报道,YEL-AVD仅在接种第一剂黄热病疫苗后发生;在加强剂量后,没有实验室确认的 YEL-AVD 报告。对于美国报告的 YEL-AVD 病例,从接种 YF 疫苗到出现症状的中位时间为 4 天(范围为 1-18 天)。病死率为≈48%,发病率为每10万剂疫苗0.3例。≥60 岁人群的 YEL-AVD 发病率更高(每 100,000 剂 1.2 例),≥70 岁人群的发病率更高。
禁忌
接种黄热病疫苗的禁忌症包括 <6 个月大;各种形式的免疫力改变,包括有症状的HIV感染或HIV感染伴有严重的免疫抑制;以及对疫苗成分的超敏反应。
有绝对黄热病疫苗禁忌症的人不应接种疫苗,因为他们的疾病会增加接种疫苗后发生严重不良事件的风险。鼓励这些人考虑其他旅行计划。如果他们无法避免前往黄热病流行地区,请向他们提供医疗豁免(详见下文),强调严格遵守蚊虫叮咬保护措施的重要性,并讨论与未接种疫苗相关的风险。
年龄小于 6 个月
黄热病疫苗禁用于 <6 个月大的婴儿,因为 YEL-AND 的发生率很高,每 100,000 名接种疫苗的婴儿中有 50-400 例。婴儿神经毒力增加的机制尚不清楚,但可能是由于血脑屏障不成熟、病毒血症增加或延长或免疫系统不成熟所致。应推迟或避免 <6 个月大的儿童前往黄热病流行国家。
免疫状态改变
HIV感染
YF疫苗禁用于艾滋病或其他HIV感染临床表现的患者,包括CD4 T淋巴细胞计数<200/mL,或<6岁儿童淋巴细胞总数的<15%)。该禁忌证基于该人群患脑炎的潜在风险增加。有关不符合上述标准的HIV感染者的指导,请参阅本章后面的“预防措施”部分。
胸腺疾病
黄热病疫苗禁用于与免疫细胞功能异常相关的胸腺疾病(例如重症肌无力、胸腺瘤)患者。没有证据表明,在偶然接受过胸腺切除术或远期接受过间接放射治疗的患者中,免疫功能障碍或黄热病疫苗相关严重不良事件的风险增加;这些人可以接种疫苗。
其他免疫缺陷
黄热病疫苗禁用于免疫缺陷或免疫抑制人群,无论是由于基础(原发性)疾病还是药物治疗。器官移植受者和恶性肿瘤患者是黄热病疫苗的禁忌症患者(见第 3 节,第 1 章,免疫功能低下的旅行者)。
免疫抑制和免疫调节疗法
黄热病疫苗禁用于免疫反应受到当前或近期放射治疗或药物抑制或调节的人群。具有已知免疫抑制或免疫调节特性的药物(表3-04)包括但不限于烷化剂、抗代谢物、大剂量全身性皮质类固醇、白细胞介素阻断剂(例如阿那白滞素、托珠单抗)、靶向免疫细胞的单克隆抗体(例如阿仑珠单抗、利妥昔单抗)或肿瘤坏死因子α抑制剂(例如依那西普)。
据推测,接受上述治疗的人发生黄热病疫苗相关严重不良事件的风险增加;大多数这些药物的包装说明书中禁止接种减毒活疫苗(见第 3 节,第 1 章,免疫功能低下的旅行者)。即使在已停止免疫抑制或免疫调节治疗的患者中,也应推迟接种活病毒疫苗,直到其免疫功能得到改善。免疫状态改变者的家人,如果本身没有禁忌症,可以接种黄热病疫苗。
过敏症
黄热病疫苗禁用于对先前剂量的疫苗或任何疫苗成分(包括鸡肉蛋白、鸡蛋、蛋制品或明胶)有急性超敏反应史的人群。如果对疫苗成分有可疑超敏反应史的人必须接种疫苗,则应由有经验的临床医生根据制造商的疫苗处方信息 [PDF] 中提供的说明进行皮肤试验和脱敏(如有指征)。
预防 措施
对黄热病疫苗采取预防措施(相对禁忌症)的人患有一种疾病,可能会增加他们在接种疫苗后发生严重不良事件的风险,或者可能干扰疫苗产生免疫力的能力。黄热病疫苗接种预防措施包括 6-8 个月、≥60 岁、无症状 HIV 感染伴中度免疫抑制、怀孕和母乳喂养。
与所有患者讨论黄热病疫苗接种的益处和风险,尤其是那些有潜在预防措施的患者,是旅行前咨询的重要组成部分。如果采取疫苗接种预防措施的人不可避免地前往黄热病风险地区,则关于疫苗接种的讨论应平衡黄热病病毒暴露风险与发生严重疫苗接种后不良事件的风险。
向旅行者征求有关其风险承受能力的信息,并将其纳入是否接种黄热病疫苗的共同决策中。如果决定不为旅行者接种疫苗,请提供医疗豁免,强调遵守昆虫叮咬预防措施的至关重要性,并讨论与未接种疫苗相关的风险。如果行程中不存在黄热病风险,但旅行者的目的地有国际旅行要求,则疫苗风险大于疾病;避免接种疫苗并签发医疗豁免以履行卫生法规是合理的,但这一决定应与患者一起商议。
年龄 6-8 个月
在 6-8 个月的婴儿中报告了两例 YEL-AND 病例。到 9 个月大时,YEL-AND 的风险被认为大大降低。ACIP建议,应尽可能推迟或避免6-8月龄儿童前往黄热病流行国家。
年龄 ≥60 岁
≥在60岁人群中,黄热病疫苗接种后报告的严重不良事件发生率为每10万剂7.7例,而所有黄热病疫苗接种者为每10万剂3.8例。该年龄组的 YEL-AND 和 YEL-AVD 风险增加。由于 YEL-AVD 仅在主要疫苗接种者中报告,并且几乎完全在 YEL-AND 中报告,因此请仔细考虑首次为老年旅行者接种 YF 疫苗的风险和益处。
HIV感染
对 >500 名无症状 HIV 感染者的联合研究被归类为中度免疫抑制,定义为 ≥6 岁人群的 CD4 T 淋巴细胞计数为 200-499/mL(或 <6 岁儿童淋巴细胞总数的 15%-24%),在接受 YF 疫苗后未发现严重不良事件。然而,HIV感染与对YF疫苗的免疫反应降低有关,这种免疫反应的减少与HIV RNA水平和CD4 T细胞计数相关。
如果无症状的HIV感染者没有基于CD4计数的免疫抑制证据(6岁人群CD4 T淋巴细胞计数≥500≥mL,<6岁儿童淋巴细胞总数的≥25%),则可以接种黄热病疫苗。由于黄热病疫苗接种在引发无症状HIV感染者的免疫反应方面可能效果较差,因此考虑在旅行前测量他们对疫苗接种的中和抗体反应。请联系您所在州的卫生部门或 CDC 虫媒病毒疾病处 (970-221-6400) 讨论血清学检测。
怀孕
妊娠期间接种黄热病疫苗的安全性尚未在任何大型前瞻性试验中得到研究。在两项针对妊娠期接种黄热病疫苗的人的观察性研究中,一项研究检测到轻微先天性异常(主要是色素痣)的风险略有增加,另一项研究报告的自然流产率更高。这两项发现均未得到后续研究的证实。
如果可能,孕妇应避免前往黄热病风险地区。如果旅行是不可避免的,并且认为黄热病病毒暴露的风险大于疫苗接种风险,建议接种疫苗是合适的。相反,如果认为疫苗风险大于黄热病病毒暴露风险,则建议或向旅行者提供医疗豁免,以履行卫生法规。
妊娠期接种疫苗的人出现黄热病病毒特异性 IgG 抗体反应的比例因研究而异(39% 或 98%),并且可能与接种疫苗的妊娠期相关。由于妊娠会降低免疫反应性,因此考虑进行血清学检测,以记录对疫苗的保护性免疫反应。虽然没有具体数据,但ACIP建议一个人在接种黄热病疫苗后等待4周再怀孕。
母乳喂养
在母亲接种了黄热病疫苗的纯母乳喂养婴儿中,至少有3例YEL-AND病例。3名婴儿在暴露时均为<1个月大,3名婴儿均被诊断为脑炎。在获得具体研究数据之前,避免为母乳喂养者接种黄热病疫苗。但是,当哺乳者无法避免或推迟前往黄热病流行地区时,建议接种疫苗。虽然没有数据支持这种做法,但一些专家建议,母乳喂养者应在接种黄热病疫苗后≥2周内吸出并丢弃母乳,然后再恢复母乳喂养。
其他注意事项
对于患有其他可能影响免疫反应的慢性疾病(例如糖尿病、肝病[包括丙型肝炎病毒感染]或肾脏疾病)的患者,接种 YF 疫苗后不良事件发生率可能增加或疫苗效力降低,尚无数据可用。有限的数据表明,自身免疫性疾病,无论是单独使用还是与其他危险因素(包括免疫抑制药物)联合使用,都可能增加 YEL-AVD 的风险。因此,如果考虑为此类患者接种疫苗,请谨慎行事。评估患者的一般免疫能力水平时要考虑的因素包括临床稳定性、合并症、并发症、疾病严重程度和持续时间,以及他们正在服用的药物。
国际疫苗接种或预防证书
《国际卫生条例》允许各国要求从某些国家抵达的旅行者(即使只是在过境)上记录黄热病疫苗接种证明(图5-02),以防止黄热病病毒在目的地国输入和传播。一些国家/地区要求所有入境旅客(包括直接从美国入境的旅客)提供疫苗接种证明(表5-25)。
患有黄热病疫苗禁忌症的人必须前往需要疫苗接种证明的目的地,应在出发前获得黄热病疫苗提供者的医疗豁免;请参阅下面的医疗豁免(豁免)。没有疫苗接种证明或医疗豁免的旅客到达需要此文件才能入境的目的地可能会被拒绝入境或面临强制隔离(最多 6 天)或现场接种疫苗。
图5-02国际疫苗接种或预防证书 (ICVP):填写说明1,2
脚注显示/隐藏
1提供黄热病疫苗的诊所可以从美国政府出版局网站或电话(866-512-1800)购买ICVP(CDC 731表格;以前称为PHS 731)。
2ICVP填写
说明 (1) 打印旅客姓名,与护照上的姓名完全相同。
(2、5、7) 按所示格式输入所有日期:日(数字)、月(字母拼写)、年。在上面的例子中,病人的出生日期被正确地输入为1960年3月22日。
(3)为患者签名预留的空间。
(4) 接种黄热病疫苗时,须在两个空格处注明“黄热病”。如果 ICVP 用于记录其他必需的疫苗接种或预防证明(根据《国际卫生条例》修正案或世界卫生组织的建议),请在此空白处写下疾病或病症名称。其他疫苗接种可能列在ICVP小册子的另一面。
(5) 输入疫苗接种日期,如图所示。
(6) 医务人员应输入他们的手写签名,如图所示。不接受签名印章。对于黄热病疫苗,签署ICVP的卫生保健提供者可能是印章持有人,或由邮票持有人授权管理或监督疫苗管理的其他卫生保健提供者。
(7) ICVP自初次黄热病疫苗接种日期起10天后起生效。如图所示,将该日期与建议的措辞“接种疫苗的人的生活”一起添加到此框中。
(8) 在此盒子中印上疫苗接种中心的统一印章。
表5-25 要求所有入境旅客提供黄热病疫苗接种证明的国家1
| 非洲 | ||
| 安哥拉 贝宁 布基纳法索 布隆迪 喀麦隆 中非共和国 刚果共和国 | 科特迪瓦、刚果 民主共和国、 加蓬 、加纳、 几内亚 、几内亚比绍、 马里 | 尼日尔 塞拉利昂 南苏丹 多哥 乌干达 |
| 美洲 |
| 法属圭亚那 |
脚注显示/隐藏
1截至 2023 年 1 月。国家/地区对黄热病疫苗接种的要求可能随时发生变化;出发前请咨询目的地国家的大使馆或领事馆。
ICVP 验证
任何在2007年12月15日之后接种黄热病疫苗的人,都必须提供新ICVP的疫苗接种证明。如果该人在2007年12月15日之前接种了疫苗,其原始的国际黄热病疫苗接种证书(ICV)卡仍可作为疫苗接种证明。接种疫苗者应收到一份完整的 ICVP,由疫苗提供者签署并加盖接种疫苗中心的印章。未能获得验证可能会导致旅行者在入境时被拒绝入境、隔离或可能重新接种疫苗。
正确填写的 ICVP 在初次疫苗接种日期后 10 天开始有效。截至2016年7月,《国际卫生条例》取消了黄热病疫苗加强针的要求,完整的ICVP被认为在接种疫苗者的一生中有效。提供黄热病疫苗的诊所可以从美国政府出版办公室网站或通过电话(866-512-1800)购买ICVP(CDC 731表格;以前称为PHS 731)。
指定的黄热病疫苗接种中心和提供者
ICVP 必须带有 YF 疫苗提供者的原始签名,该提供者可以是监督疫苗管理的医生或其他授权的有执照的医疗保健专业人员。不接受签名印章。黄热病疫苗接种必须在拥有官方“制服印章”的指定中心进行,该印章必须用于验证 ICVP。在美国,州和地区卫生部门负责指定非联邦黄热病疫苗接种中心,并向黄热病疫苗提供者发放统一印章。有关黄热病疫苗接种中心的位置和时间的信息,请访问CDC旅行者健康网站。
医疗豁免(豁免)
签发黄热病疫苗医疗豁免的黄热病疫苗提供者应填写并签署 ICVP 的疫苗接种医学禁忌症部分(图 5-03)。除医学禁忌症外,其他原因不能免于接种疫苗。黄热病疫苗提供者还应向旅行者提供一封签名并注明日期的信笺豁免信,明确说明疫苗接种的禁忌症,并盖上黄热病疫苗接种中心用于验证 ICVP 的统一印章的印记。应讨论与未接种疫苗相关的风险,并强调严格遵守蚊虫叮咬预防措施的重要性。
目的地国家可能不接受医疗豁免。为了提高边境官员批准豁免持有人进入其预定目的地的可能性,建议旅行者在旅行前尽早联系该国或国家的当地大使馆或领事馆,以获得有关豁免文件要求的具体和权威建议。所提供的所有信息应与填妥的疫苗接种医学禁忌症和弃权书一起保存。
图5-03国际疫苗接种或预防证书 (ICVP):疫苗接种的医学禁忌症部分
疫苗要求与建议
《国际卫生条例》规定的黄热病疫苗接种证明的国家入境要求与CDC的建议不同。允许各国制定黄热病疫苗入境要求,以防止黄热病病毒在其境内输入和传播。除非黄热病疫苗提供者签发医疗豁免,否则旅行者必须遵守这些要求才能进入该国。
某些国家/地区要求来自所有国家的旅客接种疫苗(表 5-25);其他人只要求来自有黄热病病毒传播风险的国家的一定年龄以上的旅行者接种疫苗(见第2节,第5章,黄热病疫苗和疟疾预防信息,按国家/地区划分)。世界卫生组织将黄热病病毒传播风险地区定义为目前或过去报告过黄热病病毒活动的地方,以及存在病媒和动物宿主的地方。包含黄热病病毒暴露可能性较低的地区(表5-23)的国家不包括在世卫组织黄热病病毒传播风险国家的官方名单中(表5-22)。除非一个国家要求所有抵达的旅客提供黄热病疫苗接种证明,否则不应要求来自被确定为黄热病病毒暴露可能性较低的国家的旅行者提供黄热病疫苗接种证明。由于国家/地区的入境要求可能随时发生变化,CDC鼓励旅客及其医疗保健提供者在出发前与相关大使馆或领事馆联系。
为了提出预防旅行相关黄热病病毒感染的建议,CDC对黄热病病毒传播使用了目的地特定风险分类:地方性、过渡性、低暴露可能性和无风险。CDC建议前往流行地区或过渡地区时接种黄热病疫苗(地图5-10和地图5-11)。由于黄热病病毒传播的变化,建议可能随时进行修订;出发前,请查看CDC旅行者健康网站目的地页面,了解最新的疫苗信息和相关的旅行健康通知。
CDC网站:www.cdc.gov/yellowfever
地图5-10非洲黄热病疫苗建议1,2
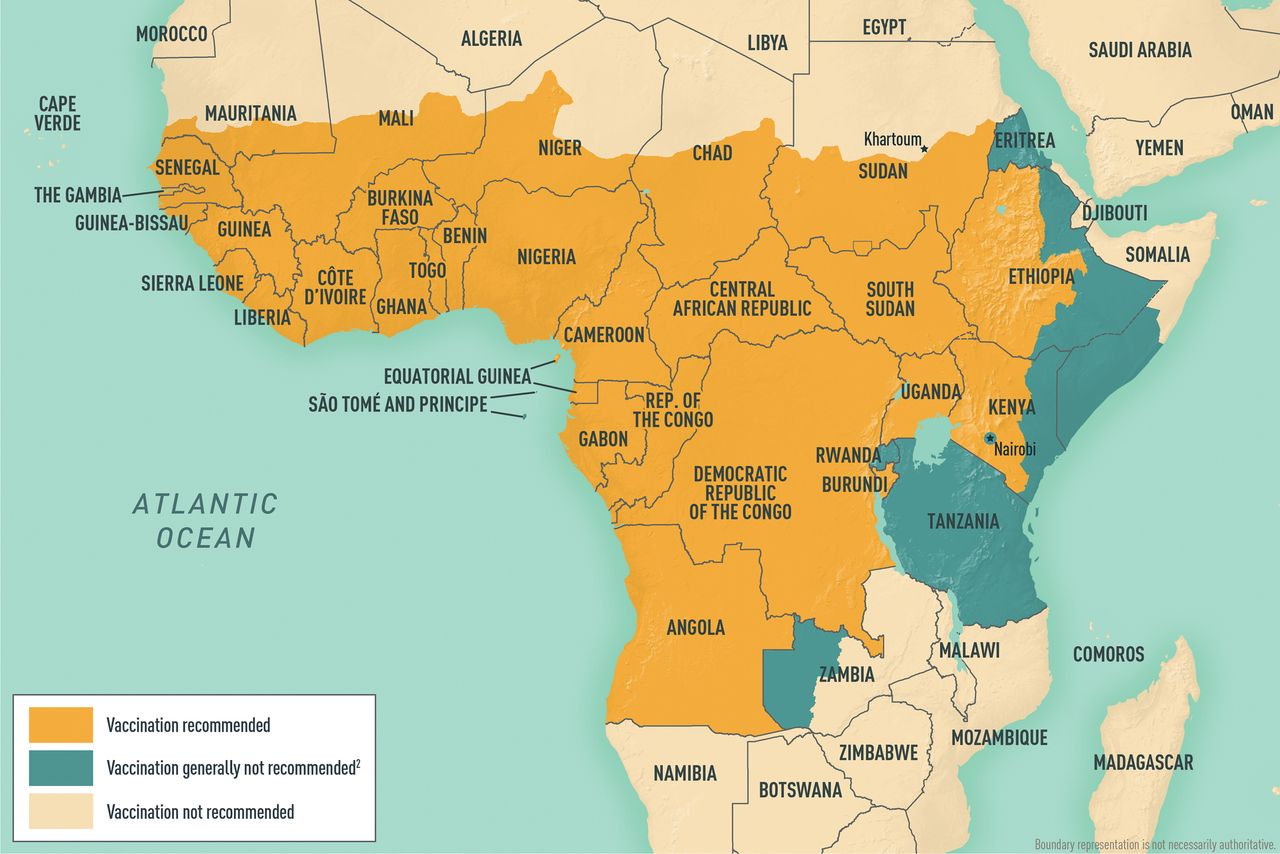
脚注显示/隐藏
1截至 2022 年 11 月。该地图是世卫组织黄热病地理风险非正式工作组2010年地图的更新版本。
2一般不建议前往黄热病病毒暴露可能性较低的地区接种黄热病疫苗。然而,对于前往这些地区的一小部分旅行者,由于长时间旅行、大量接触蚊子或无法避免蚊虫叮咬,接触黄热病病毒的风险增加,可以考虑接种疫苗。在决定是否为旅行者接种疫苗时要考虑的因素包括目的地特定和旅行相关的黄热病病毒感染风险;发生严重黄热病疫苗相关不良事件的个体潜在危险因素;和国家/地区入境要求。
地图5-11美洲黄热病疫苗建议1,2,3
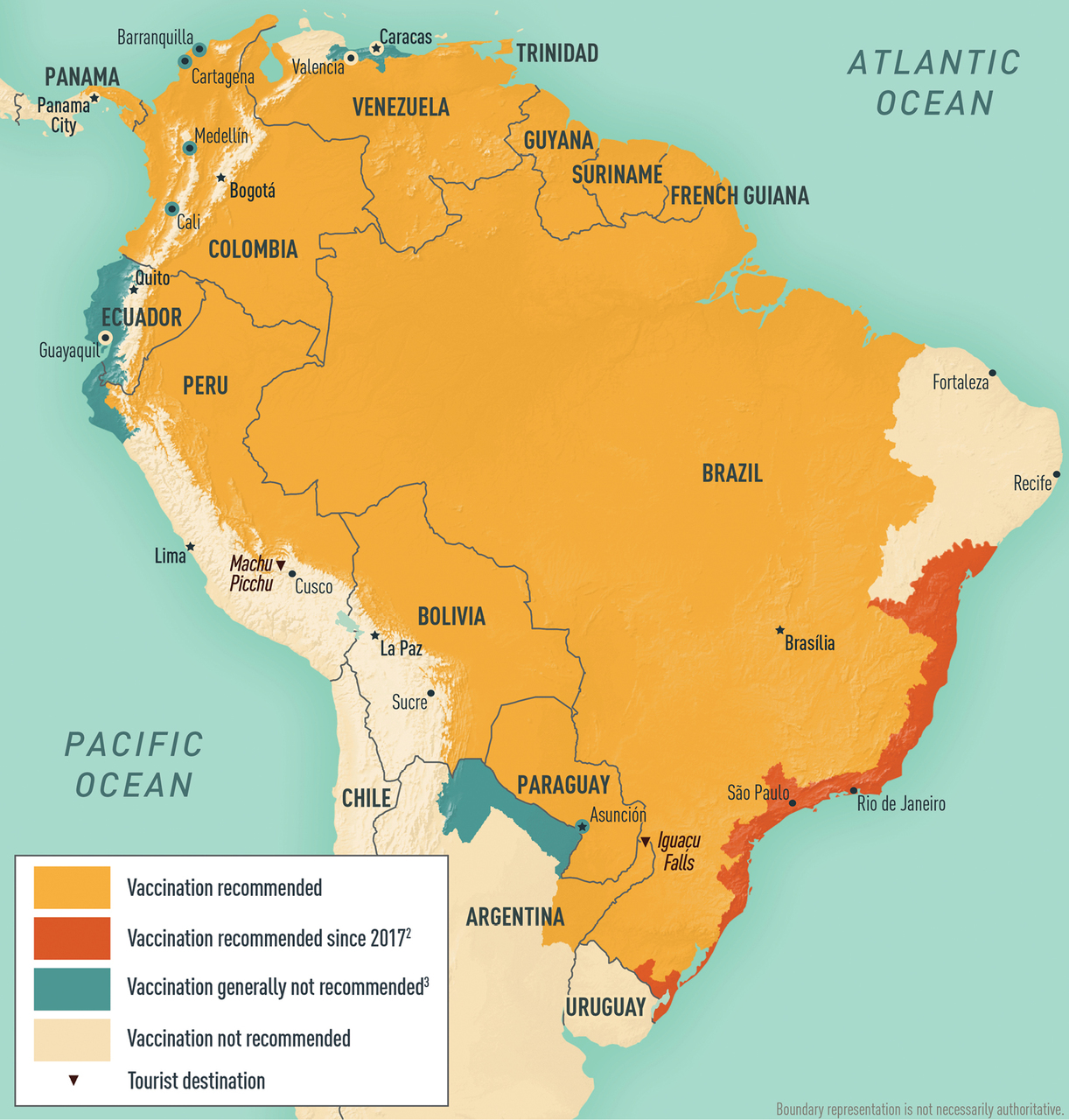
脚注显示/隐藏
以下作者为本章的先前版本做出了贡献:Mark D. Gershman、J. Erin Staples
书目
显示/隐藏
Gershman MD、Staples JE、Bentsi-Enchill AD、Breugelmans JG、Brito GS、Camacho LA 等。嗜内脏疾病:病例定义以及免疫安全数据收集、分析和呈现指南。疫苗。2012;30(33):5038–58.
Jentes ES、Poumerol G、Gershman MD、Hill DR、Lemarchand J、Lewis RF 等。2010年修订的全球黄热病风险地图和疫苗接种建议:世卫组织黄热病地理风险非正式工作组的共识。柳叶刀感染 Dis. 2011;11(8):622–32.
林赛 NP、拉贝 IB、米勒 ER、菲舍尔 M、斯台普斯 JE。2007-13年黄热病疫苗接种后的不良事件报告。J Travel Med. 2016 年;23(5):taw045.
Monath TP, Cetron MS. 预防热带地区旅行者的黄热病。2002 年临床感染病;34(10):1369–78.
Staples JE, Barrett ADT, Wilder-Smith A, Hombach J. 关于黄热病疫苗诱导的免疫力和保护持续时间的数据和知识差距的回顾。NPJ疫苗。2020;5(1):54.
Staples JE, Bocchini JA Jr, Rubin L, Fischer M. 黄热病疫苗加强剂量:免疫实践咨询委员会的建议,2015 年。MMWR Morb Mortal Wkly Rep. 20159;64(23):647–50.
Staples JE, Gershman M, Fischer M. 黄热病疫苗:免疫实践咨询委员会 (ACIP) 的建议。MMWR Recomm Rep. 2010;59(RR-7):1-27。
斯台普斯 JE、莫纳特 TP、格什曼医学博士、巴雷特 ADT。黄热病疫苗。在:Plotkin SA,Orenstein WA,Offit PA,编辑。疫苗,第 7 版。费城:爱思唯尔;2018 年,第 1181–265 页。
世界卫生组织。2005年国际卫生条例。日内瓦:本组织;2016. 可从:www.who.int/ihr/publications/9789241580496/en.
世界卫生组织。黄热病疫苗和疫苗接种。世卫组织立场文件——2013年6月。2013 年 Wkly 流行病学建议;88(27):269–83.
页面上次审核日期:2023 年 5 月 01 日
内容来源:国家新兴和人畜共患传染病中心(NCEZID)
全球移民健康司(DGMH)
Hits: 555
- 甲型肝炎 CDC黄皮书2024
- 基孔肯亚 CDC黄皮书2024
- 疫苗接种和免疫预防-一般原则 CDC黄皮书2024
- 乙型肝炎 CDC黄皮书2024
- 脑膜炎球菌病, CDC黄皮书,2024
- 沙特阿拉伯:朝觐和朝圣 CDC黄皮书2024
- 登革热 CDC 黄皮书 2024
- 蚊子、扁虱和其他节肢动物 CDC黄皮书2024
- 乙型脑炎 CDC黄皮书2024
- 动物传染病暴露:咬伤、螫伤、抓伤和其他危险 CDC黄皮书2024
- 狂犬病 CDC黄皮书2024
- 观点:狂犬病免疫 CDC黄皮书2024
- 蜱传脑炎 CDC黄皮书2024
- 伤寒和副伤寒 CDC黄皮书2024
- 黄热病 CDC黄皮书2024
- 按国家或地区分列的黄热病疫苗和疟疾预防信息 CDC黄皮书2024
- 婴儿和儿童疫苗建议 CDC黄皮书2024
- 游轮旅行 CDC黄皮书2024
- 病毒性出血热 CDC黄皮书2024
- 疟疾 2024 年 CDC 黄皮书
- 黄热病和疟疾信息,按国家划分(埃塞俄比亚)
- 旅行者的疾病模式 2024 年 CDC 黄皮书
- 天花和其他正痘病毒相关感染 2024 年 CDC 黄皮书
- 黄皮书 -脊髓灰质炎


