The groundbreaking history of the world’s first malaria vaccine
疟疾在人类历史上占有独特的地位。我们新石器时代的祖先深受其害;罗马的衰落甚至部分归因于它。仅在20世纪,疟疾估计占所有人类死亡的5%。在这个语境下,三十年是一个隐喻性的眨眼。但是对于那些将超过一半的职业生涯投入到研发世界上第一种抗疟疾疫苗的研究人员来说,这感觉像是永恒。
- 2021年12月3日
- 经过琳达·格迪斯
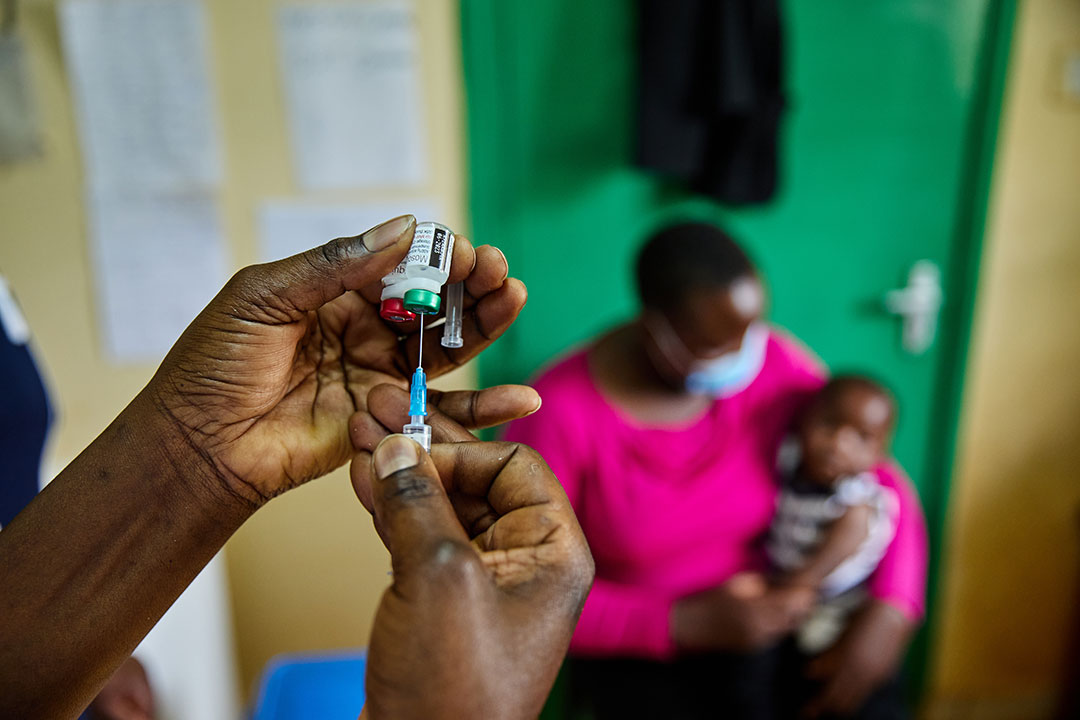
如今,这种疟疾疫苗已经推广到第一代儿童身上,将为人类长达几个世纪的抗击恶性疟原虫(这种寄生虫最致命的菌株)的斗争开启新的篇章。那么,这种疫苗是如何产生的,有没有一些经验可以在未来应用于其他疫苗?
“当我想起这件事时,我几乎又激动起来。这是针对人类寄生虫的疫苗首次达到这种保护水平,因此非常令人兴奋。”
疟疾是由疟原虫寄生虫,通过被感染女性的叮咬传播给人类疟蚊蚊子。第一症状通常在15天内出现,如果疟疾得到及时治疗,大多数人会完全康复。然而,由于这些早期症状——头痛、发烧和发冷——可能是轻微的或与其他疾病混淆,人们通常不会被诊断为疟疾,直到为时已晚。如果不治疗,恶性疟疟疾会在24小时内发展成严重疾病并导致死亡。
根据世卫组织2019年,全球约有2.29亿疟疾病例,409,000人死亡,其中5岁以下儿童占死亡人数的三分之二。大多数死亡发生在撒哈拉以南非洲。恶性疟是优势物种,负责超过90%的疟疾死亡病例,但是还有另外四个物种,其中疟原虫(指引起疟疾的单细胞动物)构成了最大的威胁。它是非洲以外大多数国家的主要物种。
疫苗vs寄生虫
尽管两者之间的联系疟原虫寄生虫和疟疾是在1880年制成的,开发一种有效的疫苗来对抗它们被证明是极其棘手的。疫苗的工作原理是训练免疫系统识别与传染性病原体相关的抗原——通常是在其表面发现的蛋白质。疟原虫也拥有这种蛋白质,但由于疟原虫的多阶段,靶向它们变得复杂生命周期以及它避免被免疫系统发现的积极努力。
“一般来说,寄生虫是非常复杂的有机体,疟原虫也不例外,”葛兰素史克疫苗R&D中心的发现和临床前R&D负责人Yannick Vanloubbeeck说。“最大的挑战是,寄生虫实际上改变了它的结构和它表面暴露的蛋白质,以逃避免疫系统。”
当一个疟蚊蚊子以感染者的血液为食,血液阶段形式的寄生虫,称为“配子母细胞”,进入蚊子的肠道并开始繁殖。经过10-18天的生长,它们的“子孢子”后代迁移到蚊子的唾液腺,当蚊子下一次叮咬人类时,这些子孢子被注射到那个人的血液中。
从这里,子孢子迁移到肝脏,在肝脏细胞内繁殖并成熟为“裂殖子”。它们离开肝脏并感染红细胞,在那里继续生长和繁殖,破坏红细胞,然后在循环过程中感染其他细胞。正是这些血液期裂殖子导致了疟疾的症状。其中一些最终发育成配子体,当另一只蚊子叮咬那个个体时,整个循环又开始了。
研发的早期
在20世纪80年代,美国沃尔特·里德陆军研究所(WRAIR)的科学家与来自史密斯克莱恩公司和葛兰素史克公司(GSK的前身)的科学家合作,试图开发一种新的药物蛋白质亚单位疫苗对抗寄生虫的子孢子。
“如果你能阻止子孢子到达肝脏,那么其余的循环就不会发生,”Vanloubbeeck解释说。
这个想法是试图训练免疫系统对抗一种叫做环子孢子蛋白(CSP)的子孢子表面蛋白。其他人以前曾试图这样做,但失败了。一个关键的问题是,子孢子在入侵肝细胞之前只在血液中存在约30分钟,因此免疫系统只有一个短暂的时间窗来发挥作用。然而,葛兰素史克的研究人员乔·科恩(Joe Cohen)提出了一个想法,即通过让免疫细胞认为它是病毒的一部分,通过使用乙型肝炎病毒表面蛋白(HBsAg)作为支架,将CSP展示为病毒样颗粒,来增强对CSP的免疫反应。
这种分子戏法有所帮助,但仍不够:“他们能够诱导一些免疫反应,但不能表明(疫苗)正在提供保护,”GSK全球疫苗医疗事务主管洛德·舒尔曼(Lode Schuerman)表示。因此,研究小组回到绘图板,用不同的组合进行实验辅助者–以各种方式增强对抗原的免疫反应的成分。
突破
一项重大突破是开发了一种人类挑战模型WRAIR——一种用感兴趣的病原体安全感染人类的方法恶性疟原虫,以快速鉴定众多候选疫苗中的哪一种诱导了针对它的最大程度的保护。这包括饲养一群疟蚊蚊子,并喂养他们的血液感染恶性疟已知寄生虫对常用的抗疟疾药物敏感。志愿者被分成不同的组,每组注射不同的候选疫苗。
一旦疫苗有时间发挥作用,这些志愿者就会被受感染的蚊子叮咬。一旦发现感染——这表明疫苗无效——志愿者就被给予抗疟药物以防止他们变得严重不适。
1997年,研究小组发现了一种佐剂配方,当它与CSP-HBsAg结合使用时高度预防疟疾。下一步是更大规模的人体试验:首先是成人,然后是受疟疾影响最严重的撒哈拉以南非洲国家的青少年、儿童和婴儿。
疫苗开发的新模式
然而,还有另一个障碍需要克服。与已经成功研制出疫苗的其他主要传染性杀手不同,疟疾主要是全球南方的一种疾病。这意味着,一旦疫苗最终获得批准,通过向富裕国家收取更多费用来分散风险和回收R&D疫苗成本的典型模式将行不通。必须开发一种全新的疫苗开发模式——从一开始就让外部合作伙伴参与进来,如比尔和梅林达·盖茨基金会、世卫组织和非营利的全球卫生组织PATH。
葛兰素史克疫苗公司(GSK Vaccines)负责疫苗全球健康接入的副总裁An Vermeersch表示:“这是一个联合、集成的端到端计划,从一开始就与主要合作伙伴保持一致,以便我们能够共同寻找最佳解决方案。“我认为我们在这方面的合作水平是独一无二的。”
她补充说,未来类似的模式可能会应用于其他疾病疫苗的开发。“有很多经验表明,不仅在(疫苗试验的)临床计划方面,而且在注册和生产阶段,以及寻找融资解决方案等所有这些方面,都需要尽早与关键合作伙伴保持一致。很明显,这需要一起完成,”弗米尔施说。
疫苗试验
另一个里程碑出现在2004年结果的一项在莫桑比克幼儿中进行的双盲、随机对照试验首次表明RTS,S疫苗是安全的、耐受性良好的,并有助于预防该年龄组的疟疾。
更多的试验接踵而至,直到2015年结果在超过七个非洲国家进行的一项大型3期试验表明,间隔一个月给予三剂RTS,S/AS01e,并在18个月后加强剂量,有助于在首次接种后至少三年内保护儿童和婴儿免受临床疟疾。在第一次接种疫苗的5-17个月大的儿童中,到研究结束时,临床疟疾病例数减少了39%(平均随访时间为4年),而对于第一次接种疫苗的6-12周的儿童,临床疟疾病例数减少了27%。在疟疾传播率较高的地区,避免了更多的病例。
“每当我想起这件事,我几乎又会激动起来,”舒尔曼说。“这是针对人类寄生虫的疫苗首次达到这种保护水平,因此非常令人兴奋。”
潜在的影响
比方说,与目前新冠肺炎疫苗的效力相比,39%听起来可能不算多,但与全球疟疾的巨大负担相比,这是病例的大幅减少。
舒尔曼说:“人们有时会认为,如果你没有达到80%或90%的疗效,它就不是一种好疫苗。但首先,没有其他疫苗——这是第一种对抗疟疾的疫苗。疟疾病例如此之多,所以如果你能预防(接近)其中的一半,那将是巨大的。”
举个例子,一项建模研究他认为,如果高发病率国家的所有儿童都接受完整系列的剂量,该疫苗每年可以防止23,000名儿童死亡。
“最终,我们想要的是80%或90%的疗效和持续多年的效果,但这是一个非常困难的目标,我认为我们过于关注百分比疗效,”PATH疟疾疫苗开发负责人Ashley J. Birkett说。“对于疟疾来说,这是一种非常普遍的疾病,儿童可能一年中多次反复患病。所以实际上,30%的减少意味着大量的案例得以避免。在参与3期试验的一个临床中心,我们看到每1000名接种疫苗的儿童就有6000多例疟疾得到预防。”
此外,这种疫苗不是为了单独使用而设计的,而是为了与其他疟疾预防工具一起使用,如驱虫蚊帐、杀虫剂喷洒或季节性疟疾化学预防(SMC)——在疟疾季节间歇施用抗疟药物以预防疾病。“我们已经证明,如果你有效地使用部分有效的工具来对抗疟疾,你可以将它转化为非常高的效果,”Birkett说。例如,一个最近的审判布基纳法索和马里的研究表明,与单独使用SMC相比,将RTS,S/AS01e疫苗与SMC结合使用可降低约70%的疟疾临床发作率、住院率和死亡率。
“我们的工作表明,季节性使用疟疾疫苗的组合方法——类似于各国使用流感疫苗的方法——有可能拯救非洲萨赫勒地区数百万年轻的生命,”伦敦卫生和热带医学院的研究负责人丹尼尔·钱德拉莫汉说。“现在需要进一步的研究来检查如何才能最有效地大规模提供季节性疟疾疫苗接种。”
方向
在这些试验结果于2015年公布后,世卫组织要求在三到五个非洲国家进行疫苗推广试点,以评估在现有疫苗方案的基础上向儿童提供四剂疫苗的可行性,并收集更多真实世界的安全性和有效性数据。这些试点方案于2019年在加纳、肯尼亚和马拉维启动,迄今已有超过83万名儿童接种疫苗。首批结果显示,因严重疟疾住院的人数减少了约30%。这种疫苗还增加了预防疟疾的机会,覆盖了三分之二以上没有驱虫蚊帐的儿童。在已经使用蚊帐的地区,接种疫苗并没有减少蚊帐的使用。
结合临床试验结果,正是这些数据让世卫组织有信心做出最近的建议。
它不是一种银弹,但其他疟疾疫苗可能会在未来几年出现。伯基特说:“很多人问我‘这种疫苗能用来消灭疟疾吗?’为了消灭疟疾,我们可能需要一种适用于所有年龄组的疫苗,可能还需要高水平的效力。所以,这确实是一个针对更小的孩子的工具。”
然而,RTS,S/AS01e与其他疟疾预防方法相结合,仍然可以大大减少疟疾的年度死亡人数——特别是在生命的头五年,这是儿童面临最大死亡风险的时期。仅此一点就足以让它在历史书上占有一席之地。
Hits: 57
