MenACWY: You’re Not Done If You Give Just One: Give 2 Doses to Strengthen Protection
MenACWY:如果你只给一剂,你没接种完:给第2剂加强保护
它很严重:脑膜炎球菌病虽然罕见,但往往可以在没有警告的情况下致残或死亡。
- 不可预测-大多数病例是随机发生的,而不是在疾病暴发中;在拥挤的环境中传播
- 突发-不同诊断;模仿常见疾病的症状
- 快速进展-会在24小时内导致休克、昏迷和死亡
- 即使对感染者进行适当治疗,约15%的人死亡1
- 10%- 20%的幸存者遭受终身残疾(脑损伤、手臂或腿部截肢,或听力丧失)1
它影响到所有年龄段,尤其是青少年和年轻人
- 16到20岁的人群在1岁以上的人群中风险最高1
可预防的方法:脑膜炎球菌疫苗(MenACWY*)是安全的、有效的,并且推荐使用。
- 不是1针,而是2针:在11岁或12岁时第一次注射MenACWY(自2005年以来推荐)和
- 16岁时第二次接种(自2010年起推荐)
尽管自2019年,第一剂MenACWY覆盖率很高,但第2剂覆盖率远远落后。
美国青少年中剂量1和剂量2的疫苗接种覆盖率*,2015-2019年2
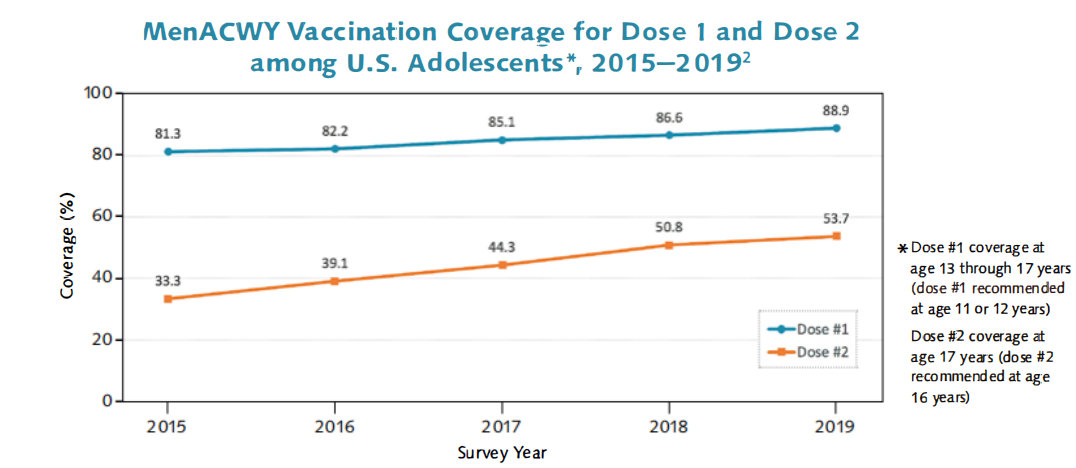
- 及时接种疫苗仍然是预防脑膜炎球菌病的一个挑战。几乎一半16岁时符合接种第二剂的条件的患者,但在17岁时没有接种。
你能做什么?
- 认识到青少年患者患脑膜炎球菌病的风险增加。
- 确保你的青少年患者(包括那些没有上大学的人)接种了抗脑膜炎球菌病的疫苗。
- 11岁或12岁时给予第一剂MenACWY,16岁时给予第二剂。
推荐!
- 将脑膜炎球菌病的预防作为您对青少年和年轻成人患者的预期指导的一部分。
论据
- 脑膜炎球菌病是罕见的,但对你这个年龄的年轻人可能是致命的。
- 从十几岁左右到二十几岁出头,你面临的风险越来越大。
- 疾病会毫无预兆地突然出现,而且很快就会危及生命。
- 脑膜炎球菌疫苗是安全有效的。
- 2剂量的MenACWY被推荐给你这个年龄的青少年。
- 你对MenACWY的强烈推荐将会有所不同。
接种疫苗!
| ACIP对MenACWY的建议1 11岁或12岁时接种第1剂,16岁时接种第2剂 | 如果第1剂延迟,建议:
a MenACWY剂量的最小间隔为8周。所以,在15岁时给予第一次剂量,在16岁时给予第二次剂量,只要观察到剂量之间的至少8周间隔。 |
评审
- 建立办公室协议(如筛查工具)以识别需要接种疫苗的青少年
- 利用有用的管理工具(提醒-召回系统、定期订单、免疫登记、电子健康记录提示)来跟踪和提高您的疫苗接种覆盖率。
- 不要错过机会!培训你的工作人员,以帮助确定那些需要接种疫苗的青少年。
| 考虑到每一个病人都有接种疫苗的机会 |
|
www.give2menacwy.org
REMEMBER: You’re not done if you give just one!
References
- Centers for Disease Control and Prevention. Meningococcal Vaccination: Recommendations of the Advisory Committee on Immunization Practices, United States, 2020. MMWR 2020;69(No. RR-9); 1–41. DOI: http://dx.doi. org/10.15585/mmwr.rr6909a1.
- Centers for Disease Control and Prevention. National, Regional, State, and Selected Local Area Vaccination Coverage Among Adoles cents Aged 13–17 years – United States, 2019. MMWR 2020;69(33)1109-1116. DOI: http:// dx.doi.org/10.15585/mmwr.mm6933a1.
- Centers for Disease Control and Prevention. Interim Clinical Considerations for Use of COVID-19 Vaccines Currently Authorized in the United States; Coadministration with other vaccines. www.cdc.gov/vaccines/covid-19/ clinical-considerations/covid-19-vaccines-us. html#Coadministration
www.give2menacwy.org/menacwy-factsheet Ĺ Item #P8011 (7/21)
Hits: 17
