Contents
- 1 丁型肝炎
- 1.1 摘要
- 1.2 介绍
- 1.3 方法
- 1.4 讨论
- 1.5 结论
- 1.5.1 参考
- 1.5.2 1.评估丁型肝炎病毒感染的全球患病率、疾病进展和临床结局。感染疾病。2020;221(10):1677-1687.doi:10.1093/infdis/jiz633PubMed谷歌学术交叉引用
- 1.5.3 2.陈海燕,沈大东,冀大洲,等。全球人群丁型肝炎病毒感染的患病率和疾病负担:一项系统综述和荟萃分析。勇气。2019;68(3):512-521.doi:10.1136/gutjnl-2018-316601PubMed谷歌学术交叉引用
- 1.5.4 3.斯托克代尔AJ,克雷尔斯B,亨利恩MYR,等。丁型肝炎病毒感染的全球流行:系统综述和荟萃分析。j肝醇。2020;73(3):523-532.doi:10.1016/j.jhep.2020.04.008PubMed谷歌学术交叉引用
- 1.5.5 4.丁型肝炎病毒感染综述。病毒。2022;14(8):1749.doi:10.3390/v14081749PubMed谷歌学术交叉引用
- 1.5.6 5.Fattovich G,Giustina G,Christensen E,等.丁型肝炎病毒感染对代偿性乙型肝硬化发病率和死亡率的影响:欧洲病毒性肝炎协调行动(Eurohep).勇气。2000;46(3):420-426.doi:10.1136/肠子PubMed谷歌学术交叉引用
- 1.5.7 6.丁型肝炎病毒的家庭内传播:分子证据。j肝醇。1999;30(4):564-569.doi:10.1016/S0168-8278PubMed谷歌学术交叉引用
- 1.5.8 7.蒙古的丁型肝炎病毒感染:地理分布、危险因素和疾病严重程度的分析。我想喝点什么。2006;75(2):365-369.doi:10.4269/ajtmhPubMed谷歌学术交叉引用
- 1.5.9 8.Stroffolini T,Ferrigno L,Cialdea L,等;SEIEVA合作小组。意大利急性丁型肝炎的发病率和危险因素:国家监测系统的结果。j肝醇。1994;21(6):1123-1126.doi:10.1016/S0168-8278PubMed谷歌学术交叉引用
- 1.5.10 9.2021年的丁型肝炎病毒:一种难治疾病的病毒学、免疫学和新的治疗方法。勇气。2021;70(9):1782-1794.doi:10.1136/gutjnl-2020-323888PubMed谷歌学术交叉引用
- 1.5.11 10.Rizzetto M,Canese MG,Aricò S,等. HBsAg携带者肝脏和血清中与乙型肝炎病毒相关的新抗原-抗体系统(δ/抗δ)的免疫荧光检测.勇气。1977;18(12):997-1003.doi:10.1136PubMed谷歌学术交叉引用
- 1.5.12 11.奈特HJ,巴里奥斯MH,小约翰M,袁LKW。丁型肝炎病毒(HDV)和丁型病毒样因子:对其起源的认识。前端微生物群。2021;12:652962.doi:10.3389/fmic b . 36386PubMed谷歌学术交叉引用
- 1.5.13 12.Pérez-Vargas J,Pereira de Oliveira R,Jacquet S,Pontier D,Cosset FL,Freitas N . HDV样病毒。病毒。2021;13(7):1207.doi:10.3390/v13071207PubMed谷歌学术交叉引用
- 1.5.14 13.当前ICTV分类法版本:分类法浏览器。国际分类学委员会。访问时间是2023年5月18日。https://ictv.global/taxonomy
- 1.5.15 14.丁型肝炎病毒:复制和发病机制。j肝醇。2016;64(1)(补编):S102-S116。doi:10.1016/j.jhepPubMed谷歌学术交叉引用
- 1.5.16 15.格伦JS,沃森JA,哈维尔CM,白JM。delta病毒大抗原中异戊二烯化位点的鉴定。科学。1992;256(5061):1331-1333.doi:10.1126科学PubMed谷歌学术交叉引用
- 1.5.17 16.Besombes C,Njouom R,Paireau J,等。喀麦隆丁型肝炎病毒感染的流行病学。勇气。2020;69(7):1294-1300.doi:10.1136/gutjnl-2019-320027PubMed谷歌学术交叉引用
- 1.5.18 17.库什纳T,塞珀M,卡普兰德。美国退伍军人医疗系统中的丁型肝炎:患病率、危险因素和预后。j肝醇。2015;63(3):586-592.doi:10.1016/j.jhepPubMed谷歌学术交叉引用
- 1.5.19 18.Patel EU,Thio CL,Boon D,Thomas DL,Tobian AAR。2011-2016年美国乙型肝炎和丁型肝炎病毒感染的患病率。临床感染疾病。2019;69(4):709-712.doi:10.1093/cid/ciz001PubMed谷歌学术交叉引用
- 1.5.20 19.丁型肝炎病毒感染筛查和患者评估的差距。j病毒性肝炎。2023;30(3):195-200.doi:10.1111/13779PubMed谷歌学术交叉引用
- 1.5.21 20.Béguelin C、Atkinson A、Boyd A等;欧洲开发署和SHCS。欧洲HIV感染者中的丁型肝炎感染。肝脏Int。2023;43(4):819-828.doi:10.1111/liv.15519PubMed谷歌学术交叉引用
- 1.5.22 21.意大利的移民流和丁型肝炎感染:第三个千年开始时的新挑战。j病毒性肝炎。2020;27(9):941-947.doi:10.1111/13310PubMed谷歌学术交叉引用
- 1.5.23 22.Burm R,Maravelia P,Ahlen G,等.抑制乙型和丁型肝炎病毒感染的新型初免-加强免疫疗法勇气。2023;72(6):1186-1195.doi:10.1136/gutjnl-2022-327216PubMed谷歌学术交叉引用
- 1.5.24 23.三角洲病毒感染对乙型肝炎严重程度的影响。柳叶刀。1982;2(8305):945-947.doi:10.1016/S0140-6736(82)90156-8PubMed谷歌学术交叉引用
- 1.5.25 24.Chin KP,Govindarajan S,Redeker AG。急性delta重叠感染后慢性乙型肝炎病毒感染的永久性HBsAg清除。消化疾病。1988;33(7):851-856.doi:10.1007/BF01550975PubMed谷歌学术交叉引用
- 1.5.26 25.丁型肝炎病毒通过干扰素依赖性和非依赖性机制干扰乙型肝炎病毒RNA的产生。j肝醇。2023;78(5):958-970.doi:10.1016/j.jhep.2023.01.005PubMed谷歌学术交叉引用
- 1.5.27 26.乙型肝炎表面抗原慢性携带者中HDV和HBV感染的相互作用。影响。1991;19(3):155-158.doi:10.1007/BF01643238PubMed谷歌学术交叉引用
- 1.5.28 27.乙型肝炎表面抗原携带者的慢性肝炎,肝内表达δ抗原:一种对免疫抑制治疗无反应的活动性和进行性疾病。安实习医生。1983;98(4):437-441.doi:10.7326/0003-4819-98-4-437PubMed谷歌学术交叉引用
- 1.5.29 28.yurdaydn C、Idilman R、Bozkaya H、Bozdayi AM。慢性丁型肝炎的自然史和治疗。j病毒性肝炎。2010;17(11):749-756.doi:10.1111/j.1365PubMed谷歌学术交叉引用
- 1.5.30 29.Niro GA,Smedile A,Ippolito AM,等:意大利慢性丁型肝炎的预后:一项长期队列研究。j肝醇。2010;53(5):834-840.doi:10.1016/j.jhep.2010.06.008PubMed谷歌学术交叉引用
- 1.5.31 30.Wranke A,Pinheiro Borzacov LM,Parana R,等;丁型肝炎国际网络。全球不同地区丁型肝炎的临床和病毒学异质性:丁型肝炎国际网络(HDIN)肝脏Int。2018;38(5):842-850.doi:10.1111/liv.13604PubMed谷歌学术交叉引用
- 1.5.32 31.埃勒曼·卡迈勒;D-SOLVE财团。未经治疗的HDV患者的自然病史:总是一种进行性疾病?肝脏Int。2023;43(补编1):5-21。doi:10.1111/liv.15467PubMed谷歌学术交叉引用
- 1.5.33 32.Palom A,Rodríguez-Tajes S,navascéS CA,等.慢性丁型肝炎患者的长期临床结果:持续性病毒血症的作用营养药物疗法。2020;51(1):158-166.doi:10.1111/15521单元PubMed谷歌学术交叉引用
- 1.5.34 33.高血清HDV RNA水平是慢性丁型肝炎患者肝硬化和肝癌的预测因子公共科学图书馆一号。2014;9(3):e92062。doi:10.1371PubMed谷歌学术交叉引用
- 1.5.35 34.二级医疗中心丁型肝炎病毒感染的长期研究:病毒血症对肝脏相关预后的影响。肝脏病学。2020;72(4):1177-1190.doi:10.1002/31214PubMed谷歌学术交叉引用
- 1.5.36 35.Roulot D,Brichler S,Layese R,等;德尔塔维尔研究小组。起源、HDV基因型和持续病毒血症决定慢性丁型肝炎患者的预后和治疗反应。j肝醇。2020;73(5):1046-1062.doi:10.1016/j.jhepPubMed谷歌学术交叉引用
- 1.5.37 36.阿尔法亚特D,克莱门特S,戈麦斯D,古森斯N,内格罗F。慢性丁型肝炎和肝细胞癌:一项观察性研究的系统综述和荟萃分析j肝醇。2020;73(3):533-539.doi:10.1016/j.jhep.2020.02.030PubMed谷歌学术交叉引用
- 1.5.38 37.乙型肝炎病毒和丁型肝炎病毒混合感染患者的肝细胞癌风险:一项纵向研究的系统综述和荟萃分析。j病毒性肝炎。2021;28(10):1431-1442.doi:10.1111/13577PubMed谷歌学术交叉引用
- 1.5.39 38.张特,苏志伟,黄,黄,侯明忠,吴建昌。与乙型肝炎病毒单一感染相比,丁型肝炎病毒双重感染增加肝细胞癌的风险:一项荟萃分析。中国医学协会。2022;85(1):30-41.doi:10.1097/JCMAPubMed谷歌学术交叉引用
- 1.5.40 39.欧洲肝脏研究协会。电子地址:easloffice @ easloffice.eu;欧洲肝脏研究协会。EASL丁型肝炎病毒临床实践指南。j肝醇。2023;79(2):433-460.doi:10.1016/j.jhepPubMed谷歌学术交叉引用
- 1.5.41 40.塔珀EB,帕里克ND。肝硬化及其并发症的诊断和治疗。睡衣裤。2023;329(18):1589-1602.doi:10.1001/jama 文章PubMed谷歌学术交叉引用
- 1.5.42 41.魏德迈,勒乌斯,巴特斯比,等;HBV论坛上的HDV RNA检测写作组。HDV RNA检测:性能特征、临床应用和挑战。肝脏病学。2023年8月28日在线发布。doi:10.1097/甲肝。59600.00000000001PubMed谷歌学术交叉引用
- 1.5.43 42.Le Gal F,Brichler S,Sahli R,Chevret S,Gordien E .血浆中丁型肝炎病毒RNA定量的首次国际外部质量评估。肝脏病学。2016;64(5):1483-1494.doi:10.1002/28772PubMed谷歌学术交叉引用
- 1.5.44 43.血浆HDV RNA的可靠定量对治疗监测至关重要:一项欧洲多中心研究。临床病毒学杂志。2021;142:104932.doi:10.1016/j . jcv . 2021.153636363627PubMed谷歌学术交叉引用
- 1.5.45 44.泰劳·纳、洛克·阿斯夫、麦克马洪·BJ等。慢性乙型肝炎预防、诊断和治疗的最新进展:AASLD 2018年乙型肝炎指南。肝脏病学。2018;67(4):1560-1599.doi:10.1002/29800PubMed谷歌学术交叉引用
- 1.5.46 45.萨林·斯克、库马尔·M、刘·GK等,《亚太地区乙型肝炎管理临床实践指南:2015年更新》。肝醇Int。2016;10(1):1-98.doi:10.1007/s12072-015-9675-4PubMed谷歌学术交叉引用
- 1.5.47 46.在HBsAg阳性个体中实施抗-HDV反射检测增加了对丁型肝炎的检测。JHEP代表。2022;4(10):100547.doi:10.1016/j . j . EPR . 19922PubMed谷歌学术交叉引用
- 1.5.48 47.拉扎维哈、布提米、特罗特纳等;北极星天文台。在低HBV和高HDV丁型肝炎病毒流行国家对所有乙型肝炎携带者进行丁型肝炎双重反射试验。j肝醇。2023;79(2):576-580.doi:10.1016/j.jhepPubMed谷歌学术交叉引用
- 1.5.49 48.丙型肝炎的抗病毒治疗和肝脏相关并发症。肝脏病学。2017;65(2):414-425.doi:10.1002/28876PubMed谷歌学术交叉引用
- 1.5.50 49.Heidrich B、yurdaydn C、Kabaç am G等;HIDIT-1研究小组。聚乙二醇干扰素α治疗慢性丁型肝炎后晚期HDV RNA复发。肝脏病学。2014;60(1):87-97.doi:10.1002/27102PubMed谷歌学术交叉引用
- 1.5.51 50.Abdrakhman A,Ashimkhanova A,Almawi WY。聚乙二醇干扰素单药治疗慢性丁型肝炎病毒感染的有效性:一项荟萃分析抗病毒研究。2021;185:104995.doi:10.1016/j .抗病毒药物。58666.68668686616PubMed谷歌学术交叉引用
- 1.5.52 51.干扰素α治疗慢性丁型肝炎的长期益处:晚期肝纤维化的消退。肠胃病学。2004;126(7):1740-1749.doi:10.1053/2004年3月17日PubMed谷歌学术交叉引用
- 1.5.53 52.慢性丁型肝炎病毒感染:开发行业治疗药物指南。美国美国食品药品监督管理局。2019年11月。2023年7月2日访问。https://www . FDA . gov/regulatory-information/search-FDA-guidance-documents/chronic-hepatitis-d-virus-infection-developing-drugs-treatment-guidance-industry
- 1.5.54 53.拉米夫定治疗慢性丁型肝炎:一项多中心随机对照初步研究。营养药物疗法。2005;22(3):227-232.doi:10.1111/j . 1365-2036.2005.02542 . xPubMed谷歌学术交叉引用
- 1.5.55 54.Wedemeyer H、yurdaydn C、Dalekos GN等;HIDIT学习小组。聚乙二醇干扰素联合阿德福韦酯与任一药物单独治疗丁型肝炎的比较。英国医学杂志。2011;364(4):322-331.doi:10.1056/NEJMoa0912696PubMed谷歌学术交叉引用
- 1.5.56 55.魏德迈、尤尔达丁、哈特克等;HIDIT-II研究小组。聚乙二醇干扰素α-2a联合富马酸替诺福韦酯治疗丁型肝炎(HIDIT-II):一项随机、安慰剂对照、2期试验。柳叶刀传染病。2019;19(3):275-286.doi:(18)30663-7PubMed谷歌学术交叉引用
- 1.5.57 56.Wedemeyer H,Schö neweis K,Bogomolov P,等.布来韦肽联合替诺福韦酯富马酸盐治疗乙型肝炎病毒和丁型肝炎病毒混合感染患者的安全性和有效性(MYR202):一项多中心、随机、平行分组、开放标签、2期试验。柳叶刀传染病。2023;23(1):117-129.doi:(22)00318-8PubMed谷歌学术交叉引用
- 1.5.58 57.干扰素α-2a治疗慢性丁型肝炎。英国医学杂志。1994;330(2):88-94.doi:10.1056/nejm 1994 . 1333036366315PubMed谷歌学术交叉引用
- 1.5.59 58.聚乙二醇干扰素治疗慢性丁型肝炎-2期LIMT-1临床试验。肝脏病学。2023;77(6):2093-2103.doi:10.1097/hep . 100000000000001PubMed谷歌学术交叉引用
- 1.5.60 59.Asselah T,Arama SS,Bogomolov P,等,《布来韦肽单药治疗和联合聚乙二醇干扰素α-2a治疗慢性丙型肝炎患者的安全性和有效性:MYR204期研究的24周中期数据》。j肝醇。2021;75(补编2):S291。2021年7月2日。2023年10月17日进入。https://easl . eu/WP-content/uploads/2021/06/EASL _ 2021 _ Version-3-new . pdf
- 1.5.61 60.魏德迈、埃勒曼、布鲁内托等人;MYR 301学习小组。一项3期随机试验:布来韦肽治疗慢性丁型肝炎。英国医学杂志。2023;389(1):22-32.doi:10.1056/NEJMoa2213429PubMed谷歌学术交叉引用
- 1.5.62 61.魏德迈尔H,埃勒曼S,布鲁内托M,等。96周的布来韦肽2 mg或10 mg单药治疗慢性丁型肝炎的疗效和安全性:一项3期随机研究的中期分析结果。j肝醇。2023;78(补编1):S57。doi:(23)00522-6谷歌学术交叉引用
- 1.5.63 62.Etzion O,Hamid SS,Asselah T,et al .第48周3 D-LIVR研究的结果,这是一项随机双盲、安慰剂对照试验,用于评估利托那韦加或不加聚乙二醇干扰素α对慢性丙型肝炎患者的安全性和疗效。j肝醇。2023;78(补1):S10。doi:(23)00451-8谷歌学术交叉引用
- 1.5.64 63.在慢性乙型肝炎病毒/丁型肝炎病毒混合感染中,REP 2139-Ca和聚乙二醇化干扰素治疗后对乙型肝炎病毒和丁型肝炎病毒感染的持续控制。肝细胞群落。2020;5(2):189-202.doi:10.1002/hep4.1633PubMed谷歌学术交叉引用
- 1.5.65 64.慢性丁型肝炎随机对照临床试验的十年随访。j病毒性肝炎。2020;27(12):1359-1368.doi:10.1111/13366PubMed谷歌学术交叉引用
- 1.5.66 65.刘DT,凯鹏华盈,公园Y,在比斯开利上午,霍夫纳格JH。干扰素α治疗12年后慢性丁型肝炎消退。肠胃病学。1999;117(5):1229-1233.doi:10.1016/S0016-5085PubMed谷歌学术交叉引用
- 1.5.67 66.慢性丁型肝炎患者的干扰素治疗持续时间及其对疾病自然病程的影响感染疾病。2018;217(8):1184-1192.doi:10.1093/infdis/jix656PubMed谷歌学术交叉引用
- 1.5.68 67.Sommereyns C,Paul S,Staeheli P,Michiels T . IFN-λ(IFN-λ)以组织依赖性方式表达,主要作用于体内上皮细胞。公共科学图书馆。2008;4(3):e1000017。doi:第1000017页PubMed谷歌学术交叉引用
- 1.5.69 68.Muir AJ,Arora S,Everson G,等;涌现学习小组。聚乙二醇干扰素λ-1a治疗慢性丙型肝炎病毒感染的随机2b期研究。j肝醇。2014;61(6):1238-1246.doi:10.1016/j.jhepPubMed谷歌学术交叉引用
- 1.5.70 69.陈莉莉,安盛,常,等;里拉-B研究小组。聚乙二醇干扰素λ治疗HBeAg阳性慢性乙型肝炎:一项随机2b期研究(LIRA-B)j肝醇。2016;64(5):1011-1019.doi:10.1016/j.jhep.2015.12.018PubMed谷歌学术交叉引用
- 1.5.71 70.Wedemeyer H,schneweis K,Bogomolov PO,等:慢性HBV病毒/丁型肝炎病毒混合感染患者接受48周高剂量(10 Mg)布来韦肽单药治疗或与聚乙二醇干扰素α-2a联合治疗。j肝醇。2020;73(补编1):S52至S53。doi:(20)30651-6谷歌学术交叉引用
- 1.5.72 71.Lampertico P,Roulot D,Wedemeyer H . Bulevirtide加或不加pegIFNα治疗代偿性慢性丁型肝炎患者:从临床试验到现实研究j肝醇。2022;77(5):1422-1430.doi:10.1016/j.jhepPubMed谷歌学术交叉引用
- 1.5.73 72.Hepcludex。欧洲药品管理局。2023年10月6日访问。https://www.ema.europa.eu/en/medicines/human/EPAR/hepcludex
- 1.5.74 73.丁型肝炎病毒相关性肝硬化患者使用布来韦肽单药治疗长达3年的安全性和有效性。j肝醇。2022;76(2):464-469.doi:10.1016/j.jhepPubMed谷歌学术交叉引用
- 1.5.75 74.Jachs M,Schwarz C,Panzer M,等.用布来韦肽对慢性丁型肝炎患者进行反应导向的长期治疗——一项“真实世界”研究的结果。营养药物疗法。2022;56(1):144-154.doi:10.1111/16945公寓PubMed谷歌学术交叉引用
- 1.5.76 75.Dietz-Fricke C,Tacke F,llner C,等,《用布来韦肽治疗丁型肝炎——114例患者的真实经验》。JHEP代表。2023;5(4):100686.doi:10.1016/j . j . EPR . 19926PubMed谷歌学术交叉引用
- 1.5.77 76.丁型肝炎病毒相关性代偿性肝硬化和具有临床意义的门静脉高压患者接受48周的布来韦肽单药治疗。j肝醇。2022;77(6):1525-1531.doi:10.1016/j.jhep.2022.07.016PubMed谷歌学术交叉引用
- 1.5.78 77.Yurdaydin C,Keskin O,Yurdcu E,等:一项关于使用或不使用干扰素α治疗慢性丁型肝炎的lonafarnib和利托那韦的2期剂量发现研究。肝脏病学。2022;75(6):1551-1565.doi:10.1002/32259PubMed谷歌学术交叉引用
- 1.5.79 78.Boulon R,Blanchet M,Lemasson M,Vaillant A,labontéP . REP 2139在体外对HBV生命周期的抗病毒作用的特征。抗病毒研究。2020;183:104853.doi:10.1016/j .抗病毒药物。58666.68668686616PubMed谷歌学术交叉引用
丁型肝炎
摘要
重要 丁型肝炎病毒(HDV)感染与乙型肝炎病毒(HBV)感染相关,并且影响全世界大约1200万至7200万人。与单独的HBV病毒或丙型肝炎病毒相比,丁型肝炎病毒导致更快的肝硬化进展和更高的肝细胞癌发生率。
观察 HDV需要HBV进入肝细胞,并组装和分泌新的病毒体。急性HDV-HBV共感染后,约95%的人体内两种病毒均被清除,而HBV感染者体内的HDV重叠感染导致超过90%的感染者出现慢性HDV-HBV感染。慢性丁型肝炎比HBV单独引起的肝病进展更快。大约30%至70%的慢性丁型肝炎患者在诊断时患有肝硬化,超过50%的患者在诊断后10年内死于肝病。然而,最近的研究表明,进展是可变的,超过50%的人可能有一个惰性的过程。只有大约20%到50%的感染丁型肝炎的人被诊断出来,这是由于缺乏对丁型肝炎病毒抗体和丁型肝炎病毒核糖核酸的认识和获得可靠诊断试验的途径有限。HBV疫苗通过预防HBV病毒感染来预防丁型肝炎病毒感染,但是没有疫苗可以保护那些已经确诊感染HBV病毒的人免受丁型肝炎病毒感染。干扰素α抑制HDV复制,并将肝脏相关事件(如肝脏失代偿、肝细胞癌、肝移植)的发生率或死亡率从每年8.5%降至每年3.3%。干扰素α的副作用,如疲劳、抑郁和骨髓抑制是常见的。HBV核苷类似物,如恩替卡韦或替诺福韦,对HDV无效。阻断HDV进入肝细胞的布来韦肽和干扰HDV组装的lonafarnib的3期随机临床试验表明,与安慰剂或观察相比,这些治疗在96周的布来韦肽单一治疗后达到了高达56%的患者的病毒学和生物化学应答,在48周的lonafarnib、利托那韦和聚乙二醇化干扰素α治疗后达到了19%。
结论和相关性 HDV感染影响了全世界大约1200万到7200万人,并且与单独感染HBV相比,HDV感染与更快进展为肝硬化和肝衰竭以及更高的肝细胞癌发生率相关。布来韦肽最近在欧洲被批准用于治疗HDV,而聚乙二醇干扰素α是大多数国家唯一可用的治疗方法。
介绍
丁型肝炎是由丁型肝炎病毒(HDV)引起的,这是一种小RNA病毒,依赖于乙型肝炎病毒(HBV)进入肝细胞并组装和分泌新形成的病毒体。因此,HDV只感染同时被HBV病毒感染的人。全球约有1200万至7200万人感染了HDV1–3。当两种病毒一起获得时,HDV感染可能作为与HBV的急性混合感染发生,或者当HDV感染患有慢性HBV感染的人时,作为重叠感染发生4。在大约95%的患者中,急性HDV-HBV共感染后两种病毒都被清除,而超过90%的HDV重叠感染导致慢性HDV-HBV感染。与单独的慢性乙型肝炎相比,慢性丁型肝炎与肝硬化的更快进展和一旦肝硬化形成后肝脏相关死亡率的更高发生率相关1,5。
HDV感染通过注射毒品等肠胃外接触、针刺伤等经皮接触或性接触传播6–8。HBV疫苗可以预防HBV病毒和丁型肝炎病毒感染,但是没有疫苗可以预防已经感染HBV病毒的人感染丁型肝炎病毒。目前,对于丁型肝炎没有批准的疗法。干扰素α及其长效制剂聚乙二醇化干扰素α抑制HDV复制,减少肝脏炎症和纤维化,并提高存活率;然而,这些效果仅在大约30%的治疗患者中是持久的9。
这篇综述总结了目前关于HDV诊断和治疗的证据(盒子)。
盒子。
常见问题
哪些患者应该进行丁肝检测?
只有乙型肝炎患者和乙型肝炎表面抗原(HBsAg)阳性者才应进行丁型肝炎检测。所有HBsAg阳性者都应进行丁型肝炎检测,特别是那些不明原因肝炎发作、活动性肝炎或尽管HBV-DNA水平低但迅速发展为肝硬化的患者。居住在丁型肝炎常见国家或从这些国家移民的人,以及暴露风险增加的人(例如,注射毒品使用者、男男性行为者、HDV感染者的家庭成员)也应进行丁型肝炎检测。
丁型肝炎是如何诊断的?
丁型肝炎是通过验血诊断的。丁型肝炎病毒抗体(抗-HDV)的存在表明正在或过去感染,而丁型肝炎病毒RNA的存在表明正在感染。
如何预防丁型肝炎?
通过HBV疫苗预防乙型肝炎是预防丁型肝炎的最有效方法。丁型肝炎患者应采取标准预防措施,如避免在家中共用剃须刀和牙刷。丁型肝炎患者的性接触者和家庭成员应接受乙型肝炎筛查,如果易感,应接受HBV疫苗接种。
方法
PubMed搜索2013年1月1日至2023年5月31日期间发表的英文文章,使用术语丁型肝炎, 丁型肝炎,以及丁型肝炎病毒。对检索到的出版物的参考文献进行相关文章的审查。在1812篇确定的文章中,386篇包括荟萃分析、随机临床试验、前瞻性队列研究和其他大型观察性研究。本文报道了具有类似发现的高质量文章研究。本文对数据进行了总结。
讨论
病毒学
HDV是由Rizzetto和他的同事在1977年发现的10同时检查人肝组织中的乙型肝炎核心抗原。HDV可能有很长的进化史,因为在包括白蚁等无脊椎动物在内的其他动物中已经发现了几种类似HDV的病毒,这表明第一种HDV可能起源于数百万年前11,12。
HDV目前被归类为德尔塔病毒的属科尔米奥病毒科家庭,8种基因型已被确定13。其基因组为约1700个核苷酸的环状单链RNA。它是已知影响人类的最小致病病毒14。循环病毒体包含基因组的单个分子,与唯一的HDV编码蛋白(丁型肝炎抗原[HDAg])复合,并被HBV表面抗原(HBsAg图1)。HDV需要与HBV共感染来装配和分泌,并且通过HBV表面蛋白与牛磺胆酸钠共转运多肽(肝细胞膜上的受体(图1)9。
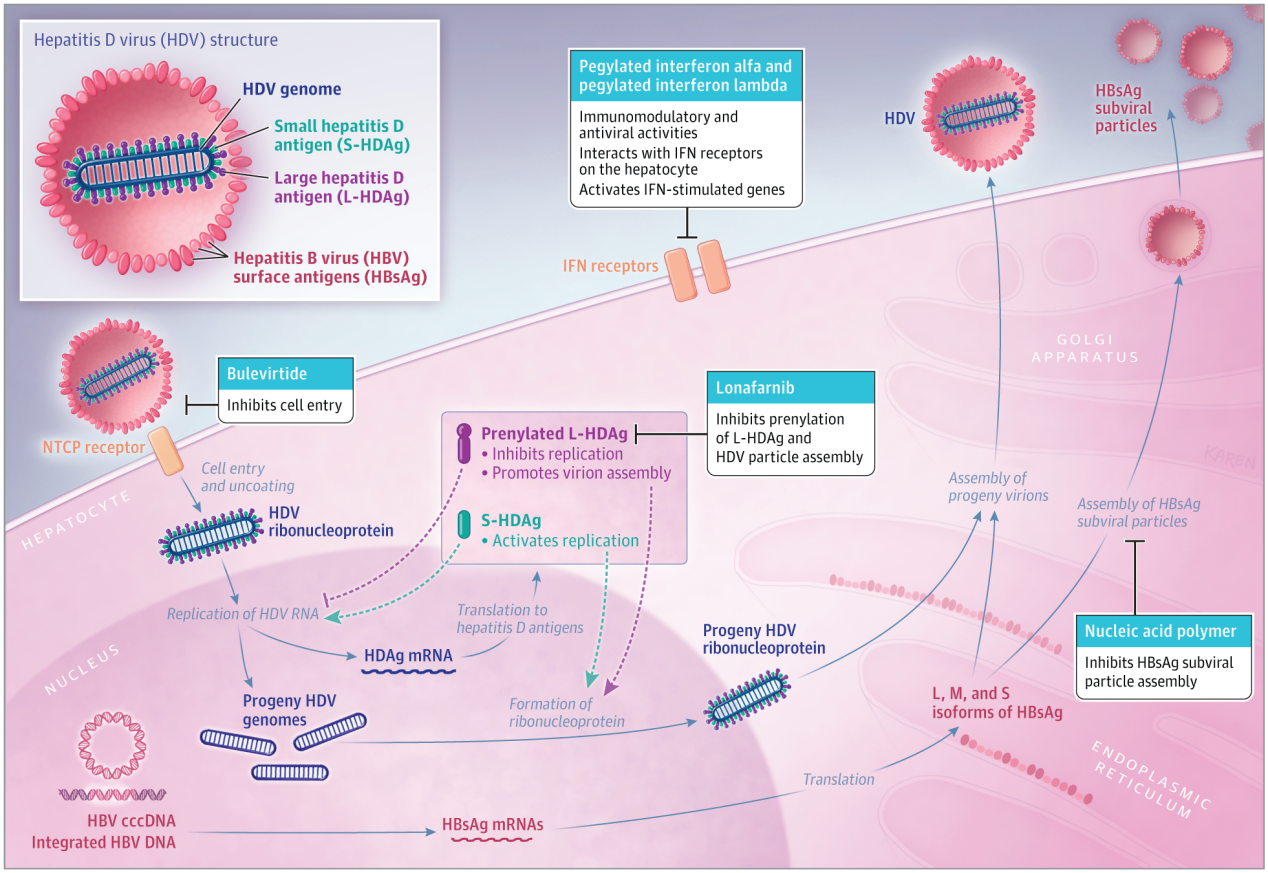
图1.丁型肝炎病毒(HDV)的结构、生命周期和抗病毒靶点
循环中的HDV病毒体包含一个由大(L)、中(M)和小(S) HBV表面抗原(HBsAg)和一个核糖核蛋白组成的包膜,该核蛋白具有与丁型肝炎抗原的2种亚型(S-HDAg和L-HDAg)复合的基因组HDVRNA。
HDV通过与牛磺胆酸钠共转运多肽(NTCP)结合进入肝细胞。进入后,HDV核糖核蛋白被转运到肝细胞核,在那里HDV RNA利用宿主酶复制。HDV信使RNA (mRNA)被翻译成S-HDAg和L-HDAg丁型肝炎抗原,它们与HDV-RNA结合形成核糖核蛋白。S-HDAg激活复制,而L-HDAg包含法尼基化信号,抑制复制,并促进病毒粒子组装。核糖核蛋白被HBV表面蛋白包裹,HDV病毒体被分泌出来。
布来韦肽是一种进入抑制剂,阻断HDV与其进入受体NTCP的相互作用。Lonafarnib是一种法尼基转移酶抑制剂,它参与L-HDAg的异戊二烯化,这是HDV颗粒组装的一个重要步骤。聚乙二醇干扰素α和聚乙二醇干扰素λ与肝细胞上的干扰素(IFN)受体相互作用。两者都激活IFN刺激的基因,并具有抗病毒和免疫调节活性。核酸聚合物阻断了HBsAg亚病毒颗粒的组装和分泌,导致循环中HBsAg水平的降低,这反过来可能通过恢复宿主免疫控制来抑制HDV的复制。
HDV-RNA复制使用宿主RNA聚合酶。HDAg(翻译自HDV RNA)以2种亚型存在:激活复制的小HDAg和抑制复制并促进病毒粒子包装的大HDAg。大的HDAg具有包含法尼基化信号的C-末端延伸,允许添加法尼基基团以促进病毒体装配9,15。
HDV不是直接的细胞病变,感染肝细胞的T细胞杀伤可能是HDV诱导的肝损伤的主要驱动因素9。
流行病学
在低收入或中低收入国家,最常见的感染途径是接触受污染的针头、医疗过程中未消毒的设备以及共用受污染的家庭用品,如牙刷。在发达国家,大约70%的新HDV传播与注射毒品和高风险性行为有关6–8,16。
世界各地都有HDV感染的报道。在北美和北欧的普通人群中,HDV感染的患病率低于1%,而在撒哈拉以南非洲、中亚和东欧的一些国家中,HDV感染的患病率超过2%(图补充)1–3。在大多数国家,HDV感染的实际流行率是未知的,因为很少进行基于人群的研究。丁型肝炎病毒高度流行的国家包括贝宁、加蓬、毛里塔尼亚、瑙鲁和蒙古1–3。HDV在HBsAg携带者中的流行率从一些西方国家的不到2%到蒙古的大约40%不等1–3。在美国,成人HBsAg携带者中HDV抗体(抗HDV)的流行率从3.4%和6%到43%不等17–19。估计值的大范围反映了小规模研究或在选定患者群体中进行的研究的不确定性。
在晚期肝病患者和高危感染人群中,如注射毒品者和性工作者、男男性行为者、接受血液透析的患者和合并感染HIV的患者中,HDV感染的患病率较高3,20。在意大利等一些国家,由于新生儿普遍接种HBV疫苗,1987年至2019年间,HDV感染率下降了50%以上,但这一下降被来自HDV感染流行国家的移民所抵消21。
预防
HBV疫苗通过预防HBV感染来预防HDV感染。在出生时将HBV疫苗和乙型肝炎免疫球蛋白结合,可防止感染了HDV-HBV病毒的母亲将HBV病毒和HDV病毒传播给其子女。HBV疫苗还被推荐用于对HBV易感的HDV感染者的性接触和家庭接触。然而,没有疫苗可以保护HBV感染者免受HDV双重感染。因此,对于慢性HBV病毒感染患者,唯一的预防措施是避免与HDV感染者进行非肠道接触或性接触。
最近在小动物中进行的一项研究表明,使用来自HBV和HDV、HBsAg前S1结构域和大HDAg的抗原进行疫苗接种,可在HBV感染的小鼠中诱导出对HDV-HBV共感染和HDV重叠感染有保护作用的抗体22。这一发现可能有助于开发用于人类的HDV疫苗。
丁型肝炎病毒感染的表现和结局
急性HDV-HBV混合感染可能表现为急性肝炎,通常随后两种病毒都被清除,尽管急性HDV-HBV混合感染患者的急性肝功能衰竭风险高于急性HBV单一感染患者4,23。
HDV重叠感染可能在先前未诊断的慢性HBV感染患者中表现为急性肝炎,或者在已知的慢性乙型肝炎患者中表现为慢性肝病的恶化。HDV重叠感染通常导致慢性HDV-HBV感染,定义为持续6个月以上的HDV病毒血症;然而,大约20%至30%的患者报告了慢性HDV感染的自发消退,并伴有间歇性或持续检测不到HDV RNA,通常是在感染多年后4。HBsAg丢失很少被报道24。
HDV干扰HBV复制25。因此,大多数慢性丁型肝炎患者的血清HBV-DNA水平较低26。然而,与单纯慢性乙型肝炎感染相比,慢性丁型肝炎病程加速,进展为肝硬化的速度更快,肝脏相关死亡率和肝细胞癌的发生率更高。大约30%至70%的慢性丁型肝炎患者在诊断时有肝硬化,50%的慢性丁型肝炎患者在诊断时没有肝硬化,但在诊断后5年内有15%发展为肝硬化。超过50%的慢性丁型肝炎患者在10年内有肝脏相关的死亡率5,27–29。慢性丁型肝炎患者的疾病进展率各不相同30–32。这种异质性部分与选择偏倚有关,即晚期肝病患者被选择性地纳入研究。结果的异质性也与一些研究中基于抗HDV阳性结果而非HDV RNA阳性结果纳入的患者有关,也与地理区域有关,这可能反映了HDV基因型、宿主和环境因素的差异。在一项对来自15个国家的1576名慢性丁型肝炎患者的研究中,7.5%至30.4%的患者发展为肝功能失代偿或肝细胞癌或需要肝移植。结果的可变性与患者居住的地理区域相关30。
持续的HDV RNA一直被认为是与肝硬化进展和死亡率相关的最重要因素32–35。与肝病进展风险增加相关的其他因素包括HDV基因型(例如,基因型1与其他基因型相比预后较差)35,高血清HBV-DNA水平、饮酒(男性每天超过2杯,女性每天超过1杯)、肥胖和糖尿病。
一项回顾性队列研究显示,在因HDV-HBV感染导致的肝硬化患者中,校正后的5年肝细胞癌风险为13%,而在仅有HBV感染的患者中为2 %- 4%5。三项系统综述和荟萃分析表明,与HBV单一感染相比,慢性丁型肝炎与肝细胞癌风险增加1.3-2.8倍相关36–38。
诊断
通过同时存在HBsAg和IgM乙型肝炎核心抗体(IgM抗-HBc)和HDV RNA(图2一个和图3)。血清HDAg可能只存在几天。因此,如果HDV-RNA检测不可用,抗HDV(总、IgG和IgM)可能是急性HDV-HBV混合感染的唯一标志,即使其出现可能延迟几个月。HDV感染的诊断通过检测血清中的HDV RNA来确定。诊断检查应包括评估急性肝炎的其他原因,如甲型肝炎和丙型肝炎,以及药物性肝损伤。HBsAg的消失和乙型肝炎表面抗体的出现表明HBV感染的消退,HDV RNA的消失表明HDV感染的消退。急性乙型肝炎患者应进行HDV检测,尤其是那些急性肝功能衰竭或有HDV感染危险因素的患者。
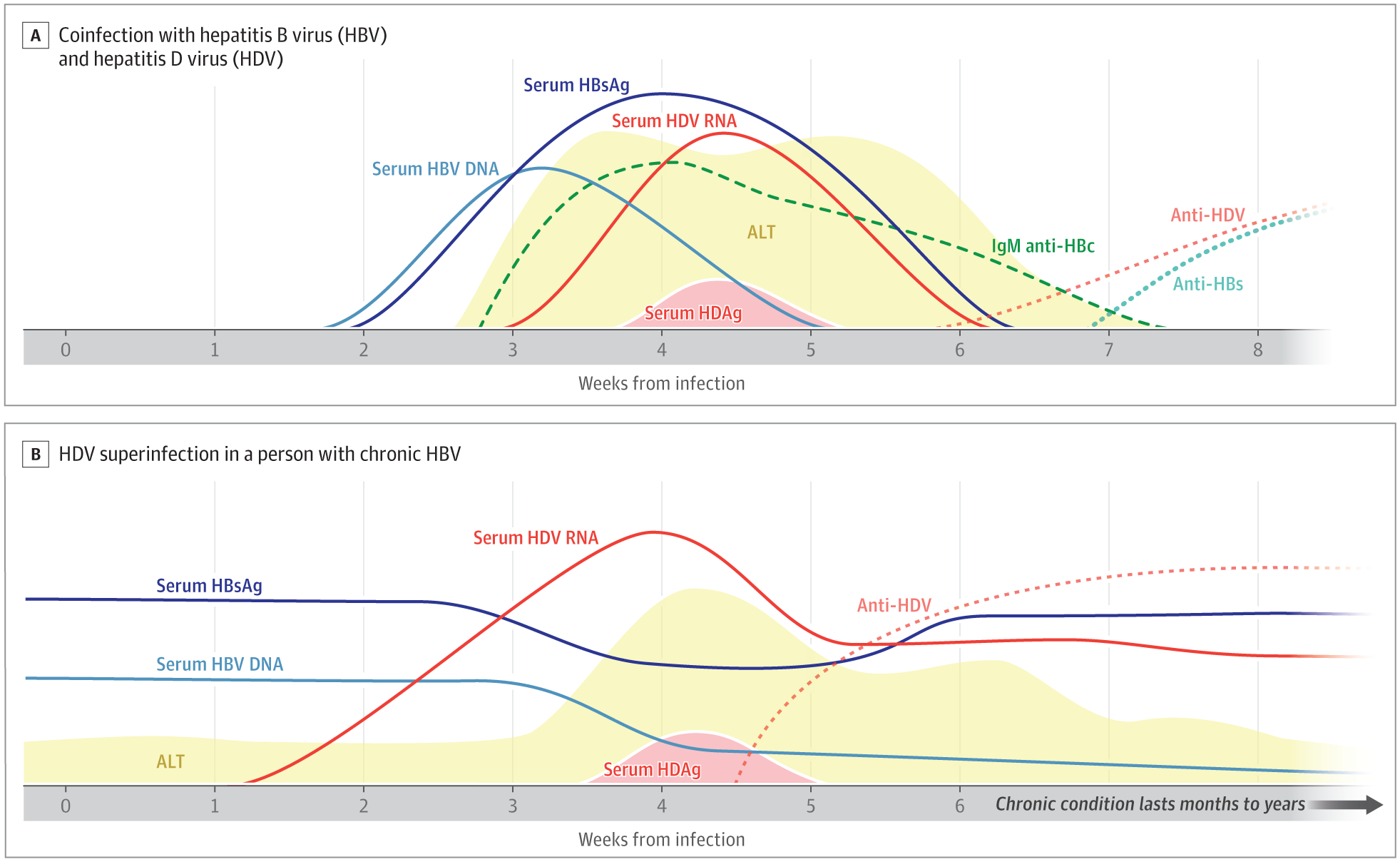
图2.乙型肝炎表面抗原检测阳性者中急性HDV-HBV混合感染和重叠感染的特征
丁型肝炎病毒和HBV病毒的混合感染通常表现为急性肝炎。通过检测HBsAg、HBV DNA和IgM抗-HBc,然后检测HDV RNA和抗-HDV进行诊断。血清HDAg可能出现的早,但时间短,难以检测。抗HDV出现较晚。如果HDV RNA检测不可用,抗HDV可能是近期HDV感染的唯一标志,因此可能需要后续检测以记录血清转换。共感染通常随后恢复,血清中检测不到HBsAg、HBV DNA和HDV RNA抗-HBs的发展;和持续检测抗-HDV。
乙,丁型肝炎病毒重叠感染可能表现为急性肝炎或慢性乙型肝炎的恶化。诊断是通过检测一个人的丁型肝炎病毒RNA和抗丁型肝炎病毒是阳性的HBsAg,但阴性的IgM抗HBc。HDV重叠感染通常伴随着HBsAg水平和HBV DNA水平的降低,但HBV和HDV感染都持续存在,并且患者的HBsAg、HBV DNA、抗-HDV和HDV RNA保持阳性。
ALT表示丙氨酸氨基转移酶;IgM抗HBc,抗HB核心抗原IgM抗体;抗HBs、HB表面抗体;抗HDV、抗HDV抗体、HBsAg、HB表面抗原;和HDAg,HD抗原。
HDV重叠感染的特征是存在HBsAg但不存在IgM抗-HBc,并且检测到抗-HDV和HDV RNA(图2b和图3)。如果没有进行HDV检测,在先前未诊断的慢性HBV感染患者中检测到HBsAg并表现出急性肝炎症状可能会导致急性乙型肝炎的错误诊断。由于HBV复制和宿主免疫控制之间的平衡发生变化、饮酒增加、甲型和丙型肝炎或药物性肝损伤,慢性HBV感染患者可能会出现肝炎发作。那些经历不明原因的肝炎暴发或不明原因的快速进展为肝硬化的人应该进行HDV重叠感染检测。患有慢性HDV感染的患者应进行丙型肝炎和HIV感染、甲型肝炎免疫和HBV复制(乙型肝炎e抗原和HBV DNA)测试,并评估肝病活动和纤维化阶段(图3)。血清标记物组(例如天冬氨酸转氨酶与血小板比率指数和纤维化4标记物[fi b-4];年龄、天冬氨酸氨基转移酶、丙氨酸氨基转移酶和血小板)和弹性成像广泛用于评估肝病中的纤维化;然而,晚期纤维化或肝硬化的阈值尚未在丁型肝炎中得到验证,肝活检仍然是纤维化分期最可靠的方法39。所有慢性丁型肝炎患者应每6至12个月进行一次监测,检测血细胞计数、肝组织、HDV RNA和HBV DNA,每2至3年进行一次无创性检测,评估纤维化分期。识别晚期纤维化或肝硬化患者非常重要,因为这些患者需要密切监测和筛查肝细胞癌和食管静脉曲张40。
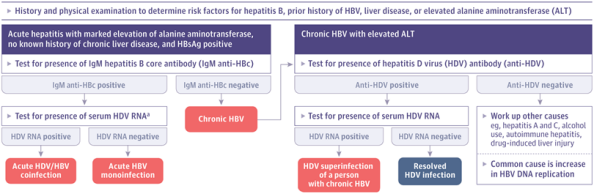
图3.丁型肝炎感染的诊断算法
所有乙型肝炎表面抗原(HBsAg)检测呈阳性的人,包括ALT水平正常的人,都应该通过抗-HDV检测进行一次HDV筛查。如果患者抗HDV检测呈阳性,他们应该接受进一步的HDV RNA检测,以确认正在发生的感染。1次HDV筛查对那些有HDV感染或快速进展性肝病风险因素的人尤其重要。有持续暴露于HDV风险的人应该每年重新筛查。
a如果无法进行HDV RNA检测,请检测恢复期是否存在抗HDV抗体。
HDV诊断测试的性能变化很大。由于HDV基因组的高度序列异质性,一些HDV-RNA检测可能在高达5%的样本中产生假阴性结果41或者低估某些基因型的病毒载量,并达到2-log10据报道,在不同的实验室测试同一样品时,定量结果会有(100倍)的差异42,43。
排查
HDV筛查的国际指南从检测所有HBsAg阳性的人39仅对HDV感染的高危人群或尽管HBV-DNA水平低或检测不到但患有活动性肝病的人群有效44,45。美国肝病研究协会HBV指南44建议对HBsAg检测呈阳性的人和HDV高危人群进行检测,包括艾滋病毒感染者、注射毒品者、男男性行为者和来自HDV高发区的移民。在HBsAg检测呈阳性的人群中,HDV筛查率在美国较低(9%-13%),在美国建议进行基于风险的筛查,44而在欧洲(8%-35%),建议普遍筛查39。这可能是由于对丁型肝炎的认识不足,认为丁型肝炎病毒感染罕见,或认为患者感染丁型肝炎病毒的风险较低。筛查率低也可能是由于缺乏批准的疗法,以及获得可靠和/或负担得起的HDV检测的机会有限。随着越来越多的人认识到,尽管丁型肝炎病毒感染比HBV单一感染引起更严重的肝病,但诊断不足,而且新的治疗方案可能很快得到批准,许多专家建议对反射性抗丁型肝炎病毒试验HBsAg阳性的人进行普遍筛查,如果阳性,随后进行丁型肝炎病毒RNA检测。来自西班牙的一项研究表明,在HBsAg患者中实施抗-HDV反射试验将筛查率从7.6%提高到93%。尽管抗-HDV阳性率保持稳定,但反射试验导致诊断为HDV感染的患者数量增加46。值得注意的是,60%检测呈阳性的人没有已知的感染HDV的危险因素。如果采用普遍检测,建议每年对HDV感染风险增加的HBsAg携带者进行重新检测39。一项建模研究表明,普遍筛查对于HBV低流行率或丁型肝炎高流行率的国家具有成本效益,但对于HBV高流行率和丁型肝炎低流行率的国家不具有成本效益47。另一种方法是美国肝病研究协会推荐的靶向筛查44。可能影响普及筛查的其他考虑因素包括可靠和负担得起的检测的可用性,以及有效、安全和负担得起的治疗。
治疗
HDV治疗的主要目标是通过抑制HDV复制和减少肝脏炎症和纤维化来预防肝硬化、肝脏失代偿、肝细胞癌和肝脏相关死亡率,从而改善临床结果。理想情况下,HDV治疗的终点是HBsAg血清清除,因为这与临床结果的改善相关,并且HBsAg是完成HDV生命周期所必需的48。在用聚乙二醇化干扰素α停止治疗24周后,用检测不到的HDV RNA抑制HDV复制与无事件生存率的提高相关,即使在长期随访期间偶尔有病毒学复发的患者中也是如此48,49。然而,只有大约30%接受聚乙二醇干扰素α治疗的患者达到这些终点50。基于一项小规模干扰素α研究的数据51 ,病毒学反应定义为HDV-RNA下降2 log10或更多(≥100倍)或检测不到的HDV RNA,以及生化反应(正常丙氨酸氨基转移酶)被认为是一种组合响应。这些终点的定义已经被监管机构采用来评估新的疗法52。
目前,美国美国食品药品监督管理局没有批准对丁型肝炎的治疗。干扰素α和聚乙二醇化干扰素α在临床试验中显示了一些功效。它们被批准用于乙型肝炎和丙型肝炎,但不用于丁型肝炎。HBV核苷(酸)类似物通过抑制HBV聚合酶来抑制HBV复制,但它们不抑制使用宿主酶的HDV RNA复制53–56。然而,HBV核苷(酸)类似物应该用于有HBV治疗指征的慢性丁型肝炎患者,即肝硬化患者和那些HBV DNA水平高(> 2000 IU/mL)和丙氨酸转氨酶水平升高或肝纤维化的患者,除非患者正在接受聚乙二醇化干扰素α,它可以抑制HBV病毒和丁型肝炎病毒的复制39,44,45。
因此,丁型肝炎的治疗旨在剥夺病毒完成其生命周期所必需的由HBV或宿主提供的功能。
HDV治疗的适应症
所有慢性丁型肝炎患者(HDV-RNA阳性,丙氨酸氨基转移酶水平升高或有肝纤维化迹象)在安全有效的治疗可用时,应考虑进行抗病毒治疗(表1)39。目前,聚乙二醇干扰素α是大多数国家唯一可以在标签外使用的HDV治疗方法。没有失代偿和禁忌症的HDV病毒血症和肝纤维化证据的患者应该用聚乙二醇干扰素α-2a治疗。在一些欧洲国家,可以获得布来韦肽,但是获得途径和保险范围不同,最佳剂量和持续时间仍不清楚。布来韦肽和洛那法尼的3期随机临床试验结果可能会扩大慢性丁型肝炎的治疗选择。聚乙二醇干扰素α和布来韦肽均不推荐用于失代偿期肝硬化患者,这些患者应进行肝移植评估。
干扰素α
干扰素抑制HDV复制并激活对HDV的免疫反应(图1)。在一项随机临床试验中,41名慢性丁型肝炎患者随机接受每周3次皮下注射干扰素α9百万单位(MU)或3百万单位(MU)或不治疗48周,结果显示较高剂量的干扰素α增加了治疗结束时检测不到HDV RNA的患者比例(71%比36%比0%)57 (表2)54,55,57–63。在12年的随访中,9 MU剂量治疗的14例患者中有2例发生肝脏相关死亡或肝移植,相比之下,3 MU剂量干扰素α治疗的14例患者中有7例发生肝脏相关死亡或肝移植,未治疗的13例对照组中有7例发生肝脏相关死亡或肝移植51。尽管在患者血清中持续检测到HDV RNA浓度,尽管HDV-RNA水平平均至少为2 log10,但在9-MU剂量组中观察到肝脏炎症和纤维化的组织学减少以及临床改善低于基线51。
干扰素α和聚乙二醇化干扰素α的功效已经在其他随机临床试验中得到证实(表2)50。Hep-Net–国际丁型肝炎干预试验I (HIDIT-I)试验54将61名患者随机分为聚乙二醇化干扰素α组和阿德福韦组,疗程48周。治疗结束时,接受联合治疗和阿德福韦的患者中有23%和0%检测不到HDV RNA。HIDIT-II试验将120名患者随机分为聚乙二醇干扰素α-2a组和替诺福韦组,为期96周55。无法检测或双对数2 log10在治疗结束时,接受两种药物治疗的患者中有48%和仅接受聚乙二醇化干扰素α-2a治疗的患者中有33%实现了HDV-RNA减少,在治疗后24周分别为31%和23%。这些试验表明,添加HBV核苷酸或将治疗时间从48周延长至96周并不能增加HDV-RNA反应或防止治疗后复发。在HIDIT-II试验中,大多数在第96周进行肝活检的患者具有稳定或改善的肝组织学。总的来说,随机临床试验和病例系列表明,干扰素α和聚乙二醇化干扰素α可以抑制HDV复制,约30%的患者在治疗后24周检测不到HDV RNA50,尽管10年后高达50%的患者会复发49,64。一些病例系列发现,干扰素α的重复疗程或超过2年的延长治疗可能会增加达到检测不到HBsAg的比率,但这尚未在随机临床试验中得到证实65,66。
聚乙二醇干扰素α-2a每周皮下注射,剂量为180 μg,持续48周。它与包括疲劳、流感样症状、抑郁、中性粒细胞减少症和血小板减少症在内的副作用有关,并具有诱发严重肝炎发作和基础自身免疫性疾病恶化的风险;由于肝炎发作和严重感染导致肝功能衰竭恶化的风险,它在失代偿性肝病中是禁忌的。
聚乙二醇化干扰素λ
干扰素λ可以诱导类似于干扰素α的抗病毒活性(图1),但与在大多数细胞类型上表达的干扰素α受体不同,干扰素λ受体主要限于上皮来源的细胞67。在乙肝和丙肝患者中,聚乙二醇化干扰素λ比聚乙二醇化干扰素α耐受性更好,尽管它尚未被批准用于这两种疾病68,69。开放标签,2期LIMT-158临床试验对33名患者进行了48周的聚乙二醇化干扰素λ的评估。在24周的随访中,分别有36%和16%接受180 μg和120 μg周剂量的患者检测不到HDV RNA(表2)。血细胞计数没有显著变化,只有1名患者有轻度抑郁,但8名患者(24%)因高胆红素血症而停止治疗,这在随访期间得到解决。
布勒韦肽
布来韦肽是一种对应于HBsAg前S1结构域的47个氨基酸的脂肽。它阻断了HDV(和HBV)病毒体与其肝细胞受体牛磺胆酸钠共转运多肽(图1)。布来韦肽每天皮下注射给药,耐受性良好,尽管它与胆汁酸水平的小幅增加有关。2期临床试验显示,在24周的每日2、5或10mg剂量的布来韦肽单药治疗后,高达77%的患者HDV-RNA水平达到了2-log10下降更多或检测不到,并且当布来韦肽与聚乙二醇化干扰素α(表2)59,70,71。
3期MYR301试验60将150名患者随机分为两组,一组接受每日2 mg的布来韦肽单药治疗,持续144周;一组接受每日10 mg的布来韦肽单药治疗,持续144周;另一组作为对照组,在第一个48周内未接受治疗,随后接受每日10 mg的布来韦肽治疗,持续96周。在第48周,在接受2 mg或10 mg布来韦肽或未接受治疗的组中,病毒学应答分别为71%、76%和4%,生物化学应答分别为51%、56%和12%,联合应答分别为45%、48%和2%(表2)。在第96周,病毒学应答(≥2-log10在试验开始时,在接受2 mg和10 mg布来韦肽治疗的2组患者中,分别有76%和82%的患者出现HDV RNA减少,20%和36%的患者未检测到HDV RNA,63%和64%的患者出现生化反应,55%和56%的患者出现联合反应61。严重不良事件发生率分别为4%和8%。严重不良事件包括新冠肺炎、乏力、胆结石、足部骨折和肺炎,这些事件均与研究治疗无关。HBsAg水平变化很小。
在2020年,欧洲药品管理局提供了每日2 mg布来韦肽的有条件批准,并在2023年7月提供了标准批准,用于慢性丁型肝炎和代偿性肝病患者的维持治疗,该药物单独使用或与HBV核苷(酸)类似物联合使用72。
在欧洲的几项观察性研究中证实了2mg剂量的布来韦肽单一疗法的抗病毒效果,这些研究显示,在24周的治疗后,超过50%的患者的HDV-RNA水平下降了 2-log或更多,一些患者在延长治疗期间检测不到HDV RNA73–75。对于代偿性肝硬化和有临床意义的门静脉高压患者,2mg剂量的布莱韦肽似乎是安全的76。然而,关于布来韦肽的确切作用方式、最佳剂量、长期安全性和HBV核苷(酸)类似物治疗的作用,仍有许多未解的问题。添加聚乙二醇干扰素α持续增加HDV病毒学应答率,约5%的患者清除HBsAg70,71。这些潜在的好处需要与聚乙二醇干扰素α的副作用相平衡。来自欧洲的观察性研究数据表明,布来韦肽可以改善肝硬化患者的临床结果74,76,但是这些数据需要确认。理论上担心在停用布来韦肽后可能会出现肝炎复发,但尽管出现了HDV病毒血症,但仅报告了一例。
Lonafarnib
Lonafarnib是一种抑制宿主法尼基转移酶(图1)。法尼基转移酶参与大HDAg的异戊二烯化,这是HDV颗粒组装的一个重要步骤15。Lonafarnib在美国和欧盟被批准用于治疗早衰症。Lonafarnib单一疗法具有剂量依赖性抗病毒作用,但高剂量与严重的胃肠道副作用(恶心、腹泻、体重减轻)相关。这导致了较低剂量的洛那法尼与利托那韦(一种细胞色素P450-3A4抑制剂)的组合。该组合旨在减少与洛那法尼相关的副作用,同时仍然获得足够高的洛那法尼吸收后水平以有效对抗HDV。在2期临床试验中77在55名参与者中,50毫克的lonafarnib加上100毫克的ritonavir,每天两次,提供了最高的病毒学应答率。3期Delta肝脏改善和病毒学应答(D-LIVR)试验62将407名参与者随机分为4组:洛那法尼加利托那韦加或不加聚乙二醇干扰素α、聚乙二醇干扰素α单药治疗和安慰剂,为期48周。初步结果显示,在治疗结束时,4个治疗组的综合反应分别为19%、10%、10%和2%,在治疗24周后分别为26%、16%、15%和0%表2)。
核酸聚合物
REP-2139,核酸聚合物,是一种硫代磷酸寡脱氧核糖核苷酸的甲基化衍生物,可以阻止HBsAg颗粒从肝脏释放到血流中78。在2期临床试验中63,12名患者接受REP-2139单药治疗,然后接受REP-2139联合聚乙二醇化干扰素α治疗,然后接受聚乙二醇化干扰素α单药治疗,共63周。在治疗结束时,9名患者检测不到HDV RNA,1名患者出现联合反应。完成治疗一年后,7名患者继续检测不到HDV RNA,6名患者出现联合反应。在治疗期间,4名患者(33%)出现显著的丙氨酸氨基转移酶升高(> 300 U/L)。
开发中的其他药物
鉴于HDV依赖于HBV,特别是表面蛋白,并且布来韦肽和lonafarnib对HBsAg水平的影响最小,临床开发中的其他药物,如阻断HBsAg产生的短干扰RNA或阻断HBsAg与牛磺胆酸钠共转运多肽结合的抗体和其他分子,正在作为单一疗法和联合疗法的一部分进行评估,以提高获得持续应答的比率。
限制
这篇综述有几个局限性。第一,可能漏掉了一些相关的文章。第二,没有进行正式评估文献质量的系统审查。第三,许多关于丁型肝炎自然史的研究包括了少量不同入选标准和不同随访时间的患者。结果可能无法广泛推广。第四,随着时间的推移,HDV-RNA检测的敏感性和特异性有所提高,这影响了对HDV感染流行率数据的解释以及HDV病毒血症对临床结果的作用。
结论
HDV感染影响了全世界大约1200万至7200万人,并且与单独感染HBV相比,HDV感染与肝硬化和肝衰竭的更快速进展以及肝细胞癌的更高风险相关。布来韦肽最近在欧洲获得批准,而聚乙二醇干扰素α是大多数国家唯一可用的治疗方法。
接受出版:2023年10月23日。
在线发布:2023年11月9日。doi:10.1001/jama
通讯作者:安娜·s·洛克(Anna S. Lok),医学博士,密歇根大学胃肠病学和肝病学部,1500 E医疗中心Dr,3912 Taubman Center,5362号信箱,密歇根州安阿伯,邮编:48109(aslok@med.umich.edu).
利益冲突披露:Negro博士报告在提交的工作之外收到了来自Gilead Sciences、Roche Diagnostics和AbbVie的演讲费或咨询费。Lok博士报告从雅培、杨梅、Chroma、Clear B、Enanta、Enochian、GNI、葛兰素史克、Grifol、让桑、诺和诺德、辉瑞、罗氏和Virion收取咨询费;以及提交作品之外的目标HBV研究的资助。
参考
1.评估丁型肝炎病毒感染的全球患病率、疾病进展和临床结局。感染疾病。2020;221(10):1677-1687.doi:10.1093/infdis/jiz633PubMed谷歌学术交叉引用
2.陈海燕,沈大东,冀大洲,等。全球人群丁型肝炎病毒感染的患病率和疾病负担:一项系统综述和荟萃分析。勇气。2019;68(3):512-521.doi:10.1136/gutjnl-2018-316601PubMed谷歌学术交叉引用
3.斯托克代尔AJ,克雷尔斯B,亨利恩MYR,等。丁型肝炎病毒感染的全球流行:系统综述和荟萃分析。j肝醇。2020;73(3):523-532.doi:10.1016/j.jhep.2020.04.008PubMed谷歌学术交叉引用
4.丁型肝炎病毒感染综述。病毒。2022;14(8):1749.doi:10.3390/v14081749PubMed谷歌学术交叉引用
5.Fattovich G,Giustina G,Christensen E,等.丁型肝炎病毒感染对代偿性乙型肝硬化发病率和死亡率的影响:欧洲病毒性肝炎协调行动(Eurohep).勇气。2000;46(3):420-426.doi:10.1136/肠子PubMed谷歌学术交叉引用
6.丁型肝炎病毒的家庭内传播:分子证据。j肝醇。1999;30(4):564-569.doi:10.1016/S0168-8278PubMed谷歌学术交叉引用
7.蒙古的丁型肝炎病毒感染:地理分布、危险因素和疾病严重程度的分析。我想喝点什么。2006;75(2):365-369.doi:10.4269/ajtmhPubMed谷歌学术交叉引用
8.Stroffolini T,Ferrigno L,Cialdea L,等;SEIEVA合作小组。意大利急性丁型肝炎的发病率和危险因素:国家监测系统的结果。j肝醇。1994;21(6):1123-1126.doi:10.1016/S0168-8278PubMed谷歌学术交叉引用
9.2021年的丁型肝炎病毒:一种难治疾病的病毒学、免疫学和新的治疗方法。勇气。2021;70(9):1782-1794.doi:10.1136/gutjnl-2020-323888PubMed谷歌学术交叉引用
10.Rizzetto M,Canese MG,Aricò S,等. HBsAg携带者肝脏和血清中与乙型肝炎病毒相关的新抗原-抗体系统(δ/抗δ)的免疫荧光检测.勇气。1977;18(12):997-1003.doi:10.1136PubMed谷歌学术交叉引用
11.奈特HJ,巴里奥斯MH,小约翰M,袁LKW。丁型肝炎病毒(HDV)和丁型病毒样因子:对其起源的认识。前端微生物群。2021;12:652962.doi:10.3389/fmic b . 36386PubMed谷歌学术交叉引用
12.Pérez-Vargas J,Pereira de Oliveira R,Jacquet S,Pontier D,Cosset FL,Freitas N . HDV样病毒。病毒。2021;13(7):1207.doi:10.3390/v13071207PubMed谷歌学术交叉引用
13.当前ICTV分类法版本:分类法浏览器。国际分类学委员会。访问时间是2023年5月18日。https://ictv.global/taxonomy
14.丁型肝炎病毒:复制和发病机制。j肝醇。2016;64(1)(补编):S102-S116。doi:10.1016/j.jhepPubMed谷歌学术交叉引用
15.格伦JS,沃森JA,哈维尔CM,白JM。delta病毒大抗原中异戊二烯化位点的鉴定。科学。1992;256(5061):1331-1333.doi:10.1126科学PubMed谷歌学术交叉引用
16.Besombes C,Njouom R,Paireau J,等。喀麦隆丁型肝炎病毒感染的流行病学。勇气。2020;69(7):1294-1300.doi:10.1136/gutjnl-2019-320027PubMed谷歌学术交叉引用
17.库什纳T,塞珀M,卡普兰德。美国退伍军人医疗系统中的丁型肝炎:患病率、危险因素和预后。j肝醇。2015;63(3):586-592.doi:10.1016/j.jhepPubMed谷歌学术交叉引用
18.Patel EU,Thio CL,Boon D,Thomas DL,Tobian AAR。2011-2016年美国乙型肝炎和丁型肝炎病毒感染的患病率。临床感染疾病。2019;69(4):709-712.doi:10.1093/cid/ciz001PubMed谷歌学术交叉引用
19.丁型肝炎病毒感染筛查和患者评估的差距。j病毒性肝炎。2023;30(3):195-200.doi:10.1111/13779PubMed谷歌学术交叉引用
20.Béguelin C、Atkinson A、Boyd A等;欧洲开发署和SHCS。欧洲HIV感染者中的丁型肝炎感染。肝脏Int。2023;43(4):819-828.doi:10.1111/liv.15519PubMed谷歌学术交叉引用
21.意大利的移民流和丁型肝炎感染:第三个千年开始时的新挑战。j病毒性肝炎。2020;27(9):941-947.doi:10.1111/13310PubMed谷歌学术交叉引用
22.Burm R,Maravelia P,Ahlen G,等.抑制乙型和丁型肝炎病毒感染的新型初免-加强免疫疗法勇气。2023;72(6):1186-1195.doi:10.1136/gutjnl-2022-327216PubMed谷歌学术交叉引用
23.三角洲病毒感染对乙型肝炎严重程度的影响。柳叶刀。1982;2(8305):945-947.doi:10.1016/S0140-6736(82)90156-8PubMed谷歌学术交叉引用
24.Chin KP,Govindarajan S,Redeker AG。急性delta重叠感染后慢性乙型肝炎病毒感染的永久性HBsAg清除。消化疾病。1988;33(7):851-856.doi:10.1007/BF01550975PubMed谷歌学术交叉引用
25.丁型肝炎病毒通过干扰素依赖性和非依赖性机制干扰乙型肝炎病毒RNA的产生。j肝醇。2023;78(5):958-970.doi:10.1016/j.jhep.2023.01.005PubMed谷歌学术交叉引用
26.乙型肝炎表面抗原慢性携带者中HDV和HBV感染的相互作用。影响。1991;19(3):155-158.doi:10.1007/BF01643238PubMed谷歌学术交叉引用
27.乙型肝炎表面抗原携带者的慢性肝炎,肝内表达δ抗原:一种对免疫抑制治疗无反应的活动性和进行性疾病。安实习医生。1983;98(4):437-441.doi:10.7326/0003-4819-98-4-437PubMed谷歌学术交叉引用
28.yurdaydn C、Idilman R、Bozkaya H、Bozdayi AM。慢性丁型肝炎的自然史和治疗。j病毒性肝炎。2010;17(11):749-756.doi:10.1111/j.1365PubMed谷歌学术交叉引用
29.Niro GA,Smedile A,Ippolito AM,等:意大利慢性丁型肝炎的预后:一项长期队列研究。j肝醇。2010;53(5):834-840.doi:10.1016/j.jhep.2010.06.008PubMed谷歌学术交叉引用
30.Wranke A,Pinheiro Borzacov LM,Parana R,等;丁型肝炎国际网络。全球不同地区丁型肝炎的临床和病毒学异质性:丁型肝炎国际网络(HDIN)肝脏Int。2018;38(5):842-850.doi:10.1111/liv.13604PubMed谷歌学术交叉引用
31.埃勒曼·卡迈勒;D-SOLVE财团。未经治疗的HDV患者的自然病史:总是一种进行性疾病?肝脏Int。2023;43(补编1):5-21。doi:10.1111/liv.15467PubMed谷歌学术交叉引用
33.高血清HDV RNA水平是慢性丁型肝炎患者肝硬化和肝癌的预测因子公共科学图书馆一号。2014;9(3):e92062。doi:10.1371PubMed谷歌学术交叉引用
34.二级医疗中心丁型肝炎病毒感染的长期研究:病毒血症对肝脏相关预后的影响。肝脏病学。2020;72(4):1177-1190.doi:10.1002/31214PubMed谷歌学术交叉引用
35.Roulot D,Brichler S,Layese R,等;德尔塔维尔研究小组。起源、HDV基因型和持续病毒血症决定慢性丁型肝炎患者的预后和治疗反应。j肝醇。2020;73(5):1046-1062.doi:10.1016/j.jhepPubMed谷歌学术交叉引用
36.阿尔法亚特D,克莱门特S,戈麦斯D,古森斯N,内格罗F。慢性丁型肝炎和肝细胞癌:一项观察性研究的系统综述和荟萃分析j肝醇。2020;73(3):533-539.doi:10.1016/j.jhep.2020.02.030PubMed谷歌学术交叉引用
37.乙型肝炎病毒和丁型肝炎病毒混合感染患者的肝细胞癌风险:一项纵向研究的系统综述和荟萃分析。j病毒性肝炎。2021;28(10):1431-1442.doi:10.1111/13577PubMed谷歌学术交叉引用
38.张特,苏志伟,黄,黄,侯明忠,吴建昌。与乙型肝炎病毒单一感染相比,丁型肝炎病毒双重感染增加肝细胞癌的风险:一项荟萃分析。中国医学协会。2022;85(1):30-41.doi:10.1097/JCMAPubMed谷歌学术交叉引用
39.欧洲肝脏研究协会。电子地址:easloffice @ easloffice.eu;欧洲肝脏研究协会。EASL丁型肝炎病毒临床实践指南。j肝醇。2023;79(2):433-460.doi:10.1016/j.jhepPubMed谷歌学术交叉引用
40.塔珀EB,帕里克ND。肝硬化及其并发症的诊断和治疗。睡衣裤。2023;329(18):1589-1602.doi:10.1001/jama
文章PubMed谷歌学术交叉引用
41.魏德迈,勒乌斯,巴特斯比,等;HBV论坛上的HDV RNA检测写作组。HDV RNA检测:性能特征、临床应用和挑战。肝脏病学。2023年8月28日在线发布。doi:10.1097/甲肝。59600.00000000001PubMed谷歌学术交叉引用
42.Le Gal F,Brichler S,Sahli R,Chevret S,Gordien E .血浆中丁型肝炎病毒RNA定量的首次国际外部质量评估。肝脏病学。2016;64(5):1483-1494.doi:10.1002/28772PubMed谷歌学术交叉引用
43.血浆HDV RNA的可靠定量对治疗监测至关重要:一项欧洲多中心研究。临床病毒学杂志。2021;142:104932.doi:10.1016/j . jcv . 2021.153636363627PubMed谷歌学术交叉引用
44.泰劳·纳、洛克·阿斯夫、麦克马洪·BJ等。慢性乙型肝炎预防、诊断和治疗的最新进展:AASLD 2018年乙型肝炎指南。肝脏病学。2018;67(4):1560-1599.doi:10.1002/29800PubMed谷歌学术交叉引用
45.萨林·斯克、库马尔·M、刘·GK等,《亚太地区乙型肝炎管理临床实践指南:2015年更新》。肝醇Int。2016;10(1):1-98.doi:10.1007/s12072-015-9675-4PubMed谷歌学术交叉引用
46.在HBsAg阳性个体中实施抗-HDV反射检测增加了对丁型肝炎的检测。JHEP代表。2022;4(10):100547.doi:10.1016/j . j . EPR . 19922PubMed谷歌学术交叉引用
47.拉扎维哈、布提米、特罗特纳等;北极星天文台。在低HBV和高HDV丁型肝炎病毒流行国家对所有乙型肝炎携带者进行丁型肝炎双重反射试验。j肝醇。2023;79(2):576-580.doi:10.1016/j.jhepPubMed谷歌学术交叉引用
48.丙型肝炎的抗病毒治疗和肝脏相关并发症。肝脏病学。2017;65(2):414-425.doi:10.1002/28876PubMed谷歌学术交叉引用
49.Heidrich B、yurdaydn C、Kabaç am G等;HIDIT-1研究小组。聚乙二醇干扰素α治疗慢性丁型肝炎后晚期HDV RNA复发。肝脏病学。2014;60(1):87-97.doi:10.1002/27102PubMed谷歌学术交叉引用
50.Abdrakhman A,Ashimkhanova A,Almawi WY。聚乙二醇干扰素单药治疗慢性丁型肝炎病毒感染的有效性:一项荟萃分析抗病毒研究。2021;185:104995.doi:10.1016/j .抗病毒药物。58666.68668686616PubMed谷歌学术交叉引用
51.干扰素α治疗慢性丁型肝炎的长期益处:晚期肝纤维化的消退。肠胃病学。2004;126(7):1740-1749.doi:10.1053/2004年3月17日PubMed谷歌学术交叉引用
52.慢性丁型肝炎病毒感染:开发行业治疗药物指南。美国美国食品药品监督管理局。2019年11月。2023年7月2日访问。https://www . FDA . gov/regulatory-information/search-FDA-guidance-documents/chronic-hepatitis-d-virus-infection-developing-drugs-treatment-guidance-industry
53.拉米夫定治疗慢性丁型肝炎:一项多中心随机对照初步研究。营养药物疗法。2005;22(3):227-232.doi:10.1111/j . 1365-2036.2005.02542 . xPubMed谷歌学术交叉引用
54.Wedemeyer H、yurdaydn C、Dalekos GN等;HIDIT学习小组。聚乙二醇干扰素联合阿德福韦酯与任一药物单独治疗丁型肝炎的比较。英国医学杂志。2011;364(4):322-331.doi:10.1056/NEJMoa0912696PubMed谷歌学术交叉引用
55.魏德迈、尤尔达丁、哈特克等;HIDIT-II研究小组。聚乙二醇干扰素α-2a联合富马酸替诺福韦酯治疗丁型肝炎(HIDIT-II):一项随机、安慰剂对照、2期试验。柳叶刀传染病。2019;19(3):275-286.doi:(18)30663-7PubMed谷歌学术交叉引用
56.Wedemeyer H,Schö neweis K,Bogomolov P,等.布来韦肽联合替诺福韦酯富马酸盐治疗乙型肝炎病毒和丁型肝炎病毒混合感染患者的安全性和有效性(MYR202):一项多中心、随机、平行分组、开放标签、2期试验。柳叶刀传染病。2023;23(1):117-129.doi:(22)00318-8PubMed谷歌学术交叉引用
57.干扰素α-2a治疗慢性丁型肝炎。英国医学杂志。1994;330(2):88-94.doi:10.1056/nejm 1994 . 1333036366315PubMed谷歌学术交叉引用
58.聚乙二醇干扰素治疗慢性丁型肝炎-2期LIMT-1临床试验。肝脏病学。2023;77(6):2093-2103.doi:10.1097/hep . 100000000000001PubMed谷歌学术交叉引用
59.Asselah T,Arama SS,Bogomolov P,等,《布来韦肽单药治疗和联合聚乙二醇干扰素α-2a治疗慢性丙型肝炎患者的安全性和有效性:MYR204期研究的24周中期数据》。j肝醇。2021;75(补编2):S291。2021年7月2日。2023年10月17日进入。https://easl . eu/WP-content/uploads/2021/06/EASL _ 2021 _ Version-3-new . pdf
60.魏德迈、埃勒曼、布鲁内托等人;MYR 301学习小组。一项3期随机试验:布来韦肽治疗慢性丁型肝炎。英国医学杂志。2023;389(1):22-32.doi:10.1056/NEJMoa2213429PubMed谷歌学术交叉引用
61.魏德迈尔H,埃勒曼S,布鲁内托M,等。96周的布来韦肽2 mg或10 mg单药治疗慢性丁型肝炎的疗效和安全性:一项3期随机研究的中期分析结果。j肝醇。2023;78(补编1):S57。doi:(23)00522-6谷歌学术交叉引用
62.Etzion O,Hamid SS,Asselah T,et al .第48周3 D-LIVR研究的结果,这是一项随机双盲、安慰剂对照试验,用于评估利托那韦加或不加聚乙二醇干扰素α对慢性丙型肝炎患者的安全性和疗效。j肝醇。2023;78(补1):S10。doi:(23)00451-8谷歌学术交叉引用
63.在慢性乙型肝炎病毒/丁型肝炎病毒混合感染中,REP 2139-Ca和聚乙二醇化干扰素治疗后对乙型肝炎病毒和丁型肝炎病毒感染的持续控制。肝细胞群落。2020;5(2):189-202.doi:10.1002/hep4.1633PubMed谷歌学术交叉引用
64.慢性丁型肝炎随机对照临床试验的十年随访。j病毒性肝炎。2020;27(12):1359-1368.doi:10.1111/13366PubMed谷歌学术交叉引用
65.刘DT,凯鹏华盈,公园Y,在比斯开利上午,霍夫纳格JH。干扰素α治疗12年后慢性丁型肝炎消退。肠胃病学。1999;117(5):1229-1233.doi:10.1016/S0016-5085PubMed谷歌学术交叉引用
66.慢性丁型肝炎患者的干扰素治疗持续时间及其对疾病自然病程的影响感染疾病。2018;217(8):1184-1192.doi:10.1093/infdis/jix656PubMed谷歌学术交叉引用
67.Sommereyns C,Paul S,Staeheli P,Michiels T . IFN-λ(IFN-λ)以组织依赖性方式表达,主要作用于体内上皮细胞。公共科学图书馆。2008;4(3):e1000017。doi:第1000017页PubMed谷歌学术交叉引用
68.Muir AJ,Arora S,Everson G,等;涌现学习小组。聚乙二醇干扰素λ-1a治疗慢性丙型肝炎病毒感染的随机2b期研究。j肝醇。2014;61(6):1238-1246.doi:10.1016/j.jhepPubMed谷歌学术交叉引用
69.陈莉莉,安盛,常,等;里拉-B研究小组。聚乙二醇干扰素λ治疗HBeAg阳性慢性乙型肝炎:一项随机2b期研究(LIRA-B)j肝醇。2016;64(5):1011-1019.doi:10.1016/j.jhep.2015.12.018PubMed谷歌学术交叉引用
70.Wedemeyer H,schneweis K,Bogomolov PO,等:慢性HBV病毒/丁型肝炎病毒混合感染患者接受48周高剂量(10 Mg)布来韦肽单药治疗或与聚乙二醇干扰素α-2a联合治疗。j肝醇。2020;73(补编1):S52至S53。doi:(20)30651-6谷歌学术交叉引用
71.Lampertico P,Roulot D,Wedemeyer H . Bulevirtide加或不加pegIFNα治疗代偿性慢性丁型肝炎患者:从临床试验到现实研究j肝醇。2022;77(5):1422-1430.doi:10.1016/j.jhepPubMed谷歌学术交叉引用
72.Hepcludex。欧洲药品管理局。2023年10月6日访问。https://www.ema.europa.eu/en/medicines/human/EPAR/hepcludex
73.丁型肝炎病毒相关性肝硬化患者使用布来韦肽单药治疗长达3年的安全性和有效性。j肝醇。2022;76(2):464-469.doi:10.1016/j.jhepPubMed谷歌学术交叉引用
74.Jachs M,Schwarz C,Panzer M,等.用布来韦肽对慢性丁型肝炎患者进行反应导向的长期治疗——一项“真实世界”研究的结果。营养药物疗法。2022;56(1):144-154.doi:10.1111/16945公寓PubMed谷歌学术交叉引用
75.Dietz-Fricke C,Tacke F,llner C,等,《用布来韦肽治疗丁型肝炎——114例患者的真实经验》。JHEP代表。2023;5(4):100686.doi:10.1016/j . j . EPR . 19926PubMed谷歌学术交叉引用
76.丁型肝炎病毒相关性代偿性肝硬化和具有临床意义的门静脉高压患者接受48周的布来韦肽单药治疗。j肝醇。2022;77(6):1525-1531.doi:10.1016/j.jhep.2022.07.016PubMed谷歌学术交叉引用
77.Yurdaydin C,Keskin O,Yurdcu E,等:一项关于使用或不使用干扰素α治疗慢性丁型肝炎的lonafarnib和利托那韦的2期剂量发现研究。肝脏病学。2022;75(6):1551-1565.doi:10.1002/32259PubMed谷歌学术交叉引用
78.Boulon R,Blanchet M,Lemasson M,Vaillant A,labontéP . REP 2139在体外对HBV生命周期的抗病毒作用的特征。抗病毒研究。2020;183:104853.doi:10.1016/j .抗病毒药物。58666.68668686616PubMed谷歌学术交叉引用
Negro F, Lok AS. Hepatitis D: A Review. JAMA. Published online November 09, 2023. doi:10.1001/jama.2023.23242
Hits: 165

孟博士,那抗HDA阴性后,还需要进行RNA检测吗?还是需要持续检测抗HDA
不需要