Why I volunteered to be infected with dengue fever
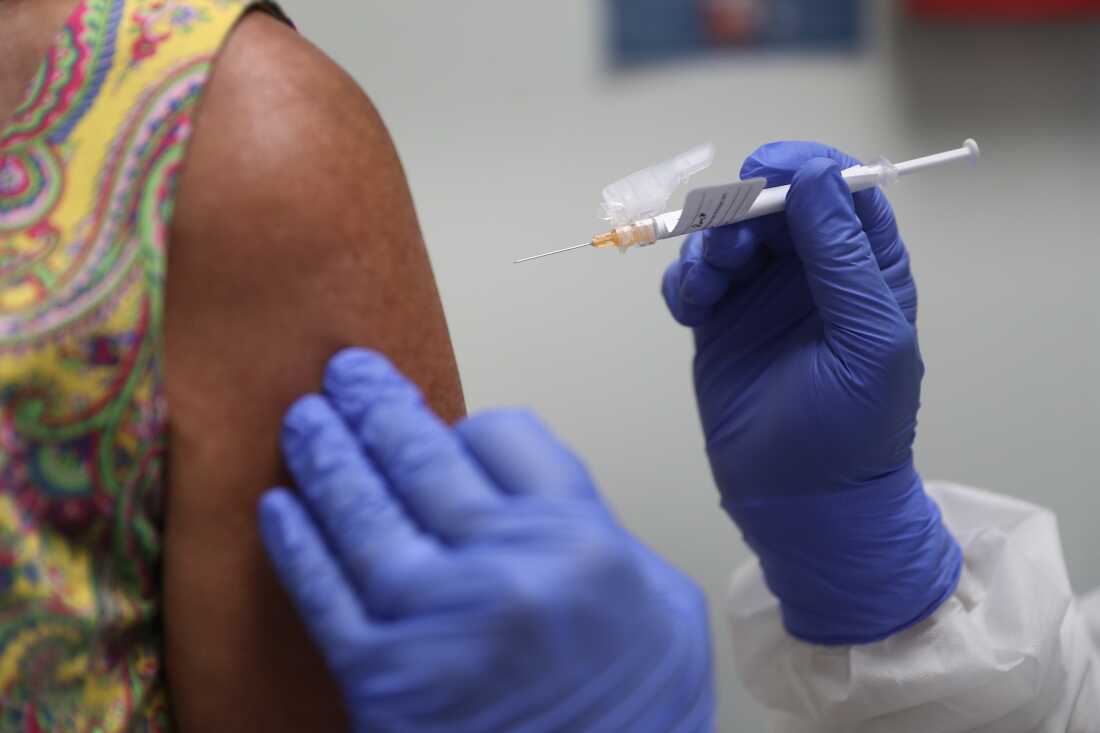
疫情初期,一名志愿者参与了一项旨在研发新冠病毒疫苗的临床试验。自2000年以来,美国政府已注册了超过50万项临床试验。但绝大多数试验最终并未促成新药获批。
乔·雷德尔/盖蒂图片社
就像蚊子叮咬的那一刻一样,我手臂上注射的登革热病毒疫苗来得如此迅速且无痛,以至于事后我甚至不确定它是否真的发生过。
几年前,我写过一篇关于一位年轻女子为了测试一种潜在疫苗而感染疟疾的故事。当时,我感到困惑不解,竟然有人会为了区区一笔钱就甘愿冒如此大的风险,忍受如此多的痛苦。
然而,每年都有许多人选择参与新药的临床试验。事实上,在美国医疗体系以及世界各地,药物在获准上市前,都必须经过三期临床试验,在人体受试者身上进行测试,以评估其安全性和有效性。
自 2000 年 2 月美国政府的临床试验追踪网站 ClinicalTrials.gov 上线以来,已有超过 50 万项临床试验在该网站注册。 每年用于开展临床试验的费用接近 1000 亿美元 。然而,绝大多数试验及其投入的资金最终都未能促成新药的获批。
所以,当我在 Instagram 信息流中看到一则广告,说我可以参加约翰·霍普金斯大学免疫研究中心 (CIR) 为期 5 个月的登革热研究,并获得高达 3,425 美元的报酬时,我被吸引住了。
我想更多地了解人体医学实验的商业运作和伦理问题。为了找到答案,我愿意承受一些痛苦。结果发现,业内人士一直在争论风险、种族、家长式作风、经济因素和剥削在临床试验中的作用。但即便如此,临床试验的开展仍然依赖于健康参与者的某种利他主义精神。
知情同意与非知情同意
登革热是全球最常见的蚊媒病毒性疾病。世界卫生组织估计, 每年约有 4 亿人感染登革热, 而最新研究表明, 气候变化正在加剧全球登革热的负担 ( 《美国国家科学院院刊》 2025,DOI:10.1073/pnas.2512350122)。然而,登革热仍被视为一种被忽视的热带病,部分原因是目前尚无美国食品药品监督管理局(FDA)批准的针对重症登革热的特效疗法 。当登革热与其他疾病(例如营养不良或艾滋病毒感染)同时发生时(不幸的是,这些疾病在一些登革热流行地区较为常见),登革热可能致命。
我申请的临床试验在巴尔的摩进行,而巴尔的摩并非登革热高发区。事实上,美国的登革热病例极其罕见,但即便疾病负担主要集中在其他地区,一期和二期药物试验在美国进行也相对常见。美国通常拥有开展此类试验所需的学术专长和资金,而低收入国家则缺乏这些资源。
我自愿参加一项二期临床试验,接受登革热病毒注射,以测试一种实验性药物预防重症登革热感染的疗效。该研究分为两个组。一组在注射登革热病毒前一天接受静脉注射药物或安慰剂,另一组在注射登革热病毒几天后接受药物或安慰剂。
在我能够自愿参与任何项目之前,CIR 需要我的同意——而且是大量的同意。我曾两次被要求仔细阅读厚厚的资料包,其中详细说明了我同意承担的风险、我作为研究参与者的权利以及行为准则。之后,我还要参加一个开卷考试,考试内容必须达到 70% 或以上才能继续。
“我们常说,知情同意是一个不断发展的过程,而且也必须如此,”CIR 主任安娜·P·德宾说道。德宾是我参与的登革热试验的首席研究员,尽管在我去试验中心期间从未见过她本人。她还负责监督 CIR 开展的其他几项试验。
不幸的是,历史上不乏未经同意就对他人进行研究的例子。二战期间,纳粹对犹太人和其他被关押在集中营的人进行了骇人听闻的医学实验。美国也有不道德医学研究的历史。从20世纪30年代到70年代进行的塔斯基吉梅毒实验,隐瞒了对非裔美国人的梅毒诊断和治疗,并在之后的数年里持续监测他们的健康状况。始于1956年、持续14年的威洛布鲁克实验,故意让患有智力障碍的儿童感染肝炎。
但随后,在 1978 年,美国国家生物医学和行为研究人类受试者保护委员会发表了《 贝尔蒙报告》 。这份里程碑式的文件概述了人类研究的三项核心伦理原则:尊重人格,即要求研究参与者知情同意并享有自主权;行善,这是“不伤害”理念的另一种说法;以及公正,即确保人类研究的益处和风险得到公平分配。
这反过来又促使美国出台法规,要求对人体受试者进行的医学研究必须由机构审查委员会 (IRB) 评估其伦理道德。
约翰·霍普金斯大学公共卫生学院伦理审查委员会成员杜宾表示,评估临床试验的伦理问题需要进行详细的讨论。
“我们真正关心的是如何让志愿者了解情况。所有程序是否符合伦理?存在哪些风险?如何降低这些风险?诸如此类的问题,”她说道。如果一项拟议的研究不能充分回答这些问题,那就得重新设计方案,修改研究方法。
伦理审查委员会讨论的大部分信息都必须传达给参与者。
“我们必须确保你清楚参与研究期间会发生什么,”德宾说。“你会得到报酬吗?这些都是重要的信息。你的样本会如何处理?你能退出吗?谁会看到你的信息?”
这对参与者来说理解起来很困难。如果他们不理解,就无法做出合乎伦理的同意。这就是为什么我必须先通过两项测试才能成为志愿者的原因。
“我仍然认为我们的同意书太长了,但我觉得也很难确切地知道应该删减哪些内容才能确保人们充分了解情况,”德宾说。
承担经过深思熟虑的风险
多亏了知情同意书,我觉得自己对这项研究有了比较清晰的了解。但我仍然很紧张。
我原本打算接受实验性单克隆抗体( 一种实验室合成的蛋白质,可以模拟人体免疫系统产生的天然抗体,用于抵抗感染)或安慰剂。但接受抗体治疗并不能保证长期免受登革热的侵害。
给药当天,我经历了长达五个小时的痛苦过程:输液、反复抽血,手臂都磨出了淤青。最终,除了不适之外,我当天没有其他痛苦。一期临床试验几乎已经证实,这种正在研发的药物是安全的。
第二天,一名护士给我的手臂注射了一种经过基因改造的登革病毒 DENV-3 血清型,这种病毒旨在只引起轻微的疾病,而不是像俗称的“断骨热”那样引发严重的疾病。
有人告诉我,登革热的症状和流感很像,但登革热还会出现全身皮疹、骨痛和眼后疼痛。注射疫苗一周后(不幸的是,在此之前我还感染了新冠病毒,持续了一周),我出现了所有这些症状。
比起病情轻微,更令我担忧的是,知情同意书中还警告说登革热病毒有一种叫做抗体依赖性增强的特性。具有抗体依赖性增强的病毒在第二次感染时会更加危险,因为病毒可以利用人体先前感染产生的不完善的抗体来更好地感染细胞。所以,如果我再次感染登革热,患重症的风险会大大增加。这种风险将伴随我一生。究竟是什么让这种风险变得可以接受?
罗格斯大学公共卫生学院的生物伦理学家尼尔·埃亚尔表示,针对患有某种疾病的人群开展的研究在确定何种治疗方案合适时,会考虑“风险收益平衡”。他指出,在研究环境之外,“有时,如果某种药物对你非常有益,那么服用这种风险很高的药物也是值得的;如果你的癌症病情严重且别无选择,那么有时危险的化疗也是值得的。”
对于健康人群的临床试验,计算方法有所不同。埃亚尔表示,计算合适的风险水平分为三个阶段。第一阶段是“尽可能降低风险,尽可能提高或促进益处”。例如,我接受的基因改造登革病毒血清型旨在尽可能减轻临床相关的疾病症状。
然而,并非所有风险都能通过设计消除,因此,第二阶段,也是埃亚尔认为最重要的阶段,是要问:个人所面临的风险与社会所获得的潜在利益是否成比例?
他说:“我不是在问,考虑到个人所获得的利益,个人所承担的风险是否可以接受?”
只要是为了更大的利益,参与试验的人可以承担一定的风险,而不获得任何医疗利益作为回报。
确定临床试验可接受风险的第三阶段是问:无论试验对社会有多大价值,对个人的绝对风险是否太高?
但埃亚尔表示,他认为没有必要为临床试验中个人的风险设定上限。他认为,只要个人被充分告知相关信息,并且能为社会带来足够的益处,那么个人就应该能够承担他们愿意承担的风险。
他说:“美国一些疟疾挑战试验的首批参与者是想要研发疫苗的研究人员,他们都是自愿参加的。”
埃亚尔关于临床试验风险上限的观点并非普遍被伦理学家和研究人员所认同,而他们才是决定是否批准临床试验的决策者。目前,伦理审查委员会在界定受试者可接受的风险时往往倾向于保守——考虑到该领域过往的医疗滥用历史,这种做法或许情有可原。
这种谨慎态度引发了人们对临床试验设计和实施中家长式作风作用的质疑。这已成为临床试验伦理讨论中的热门话题。
薪酬与家长式作风
为了补偿我被各种检查、难受得像垃圾一样难受了几天,以及在五个月内往返 CIR 设施 17 次(每次往返 2.5 小时)的辛苦,我获得了大约 3500 美元的报酬。这笔钱以后还得缴税。不过现在,一切即将结束,我觉得我的付出是值得的。这笔钱足够我度假,还能用来升级一下家里的东西。
但3500美元对不同的人来说意义不同。对于那些有幸积攒了不少钱的人来说,这可能并不诱人。而对于那些为支付账单而苦苦挣扎的人来说,这可能意味着能够保住住所或解决温饱问题。
历史上,负责监督临床试验开发的审查委员会一直不愿通过高额现金奖励来激励受试者参与。据杜宾称,这是因为他们担心过高的报酬会不当影响那些需要钱的人参与他们原本不愿意参与的项目。不过,杜宾本人并不认同这种观点,她一直倡导提高报酬。
倡导临床试验参与者权益的组织 1Day Sooner 的总裁兼联合创始人 Josh Morrison 表示,限制补偿背后的逻辑是“错误的、居高临下的,对那些因为需要钱而参加研究的人来说是不公平的”。
1Day Sooner 诞生于新冠疫情期间,是由一群希望通过参与新冠病毒挑战性研究来贡献力量的人们组成的联盟。在后疫情时代,1Day Sooner 现在代表参与者发声,与临床试验开发指导者进行对话。
莫里森表示,家长式作风和精英主义的态度是伦理审查委员会(IRB)担忧高额报酬的根源。但如果从一开始就尽一切努力确保研究符合伦理,“支付更多报酬并不会影响这一点”。莫里森说,只有当研究本身就不道德时,高额报酬才可能诱使人们参与。而这种情况绝不应该发生。莫里森认为,报酬应该基于参与试验所花费的时间和精力,而不是研究本身的风险,因为这些研究本身就不应该存在过高的风险。
北卡罗来纳大学教堂山分校的生物伦理学家吉尔·费舍尔认为,关于病人赔偿的争论有时会忽略更大的问题。
费舍尔说:“人们担心,如果你给人们钱,他们会感到被迫去做一些他们原本不想做的事情,但另一方面,我更担心如果我们不给他们足够的报酬,我们会剥削他们。”
费舍尔研究美国临床试验参与的伦理和人口统计学问题已有20多年。她说,虽然没有足够的数据来确定每年有多少人参与临床试验,但我们确实知道哪些人最有可能参与。
“参与这些研究的大多是黑人或非裔美国人,尤其是在东北部和中西部地区,而西南部和东南部地区则有很多西班牙裔或拉丁裔参与者,”她说道,并补充说,选择参与这些研究的人往往没有其他可靠的收入来源或获得负担得起的医疗保健的可靠途径。
在我接受静脉输液的那天,还有另外两名试验参与者和我一起在试验中心。其中一位是约翰·霍普金斯大学的研究生,他说他想为科学做更多贡献。另一位参与者则是“来这里挣点钱的”。杜宾要求我不要采访或透露任何其他试验参与者的身份信息,我同意了。
“我与数百名参与这些研究的人交谈过。一方面,他们中的大多数人都非常感激能有机会以这种方式赚钱,”费舍尔说。“但与此同时,你可能会对这个机会心存感激,但同时也会感到自己被剥削了。我认为他们中的很多人都有这种感觉。”
据我采访的几位消息人士透露,许多参与过一项临床试验的人最终还会参与另一项。有些人将临床试验作为主要收入来源之一,但这并不常见。更多时候,参与者觉得除了报酬之外,他们参与临床试验还有其他更充分的理由。
“这不是非此即彼的问题。人们既可以出于利他主义动机,也可以在意金钱,”莫里森说。
第一手证词
对雅各布·霍普金斯来说,利他主义是他选择参与试验的关键因素。早在 2020 年,霍普金斯就成为英国一项为期数周的住院临床试验中,首位接受新冠病毒挑战的人。
“自从我迈出这重要的一步,进入临床试验领域,并参与到相关的倡导工作中来,这已经成为我全新的热情所在,”他说。
与此同时,已经参与过两项新冠病毒挑战试验的鲁佩什·查夫达(Roopesh Chavda )并不认为参与临床试验是一种爱好,但他确实认为这有助于造福世界。他说:“这不一定是为了钱。但如果没有报酬,我绝不会做这样的事,因为这其中存在风险。”
霍普金斯参加临床试验时处于失业状态,查夫达在住院期间可以远程工作,而我则得到了雇主的许可,可以抽出时间参加试验。
对于那些觉得自己不得不出于需要而参加临床试验的人来说,像 Durbin、Eyal、Fisher、Morrison 以及我有幸共事的员工们,正在努力一点一点地改善试验参与者的体验。
在参与试验期间,我感到自己受到了欢迎、重视和尊重。我希望分享这段经历能够鼓励其他人也考虑参与志愿服务。
本文经《化学与工程新闻》(Chemical & Engineering News) 授权转载。版权所有 ©2025 美国化学学会。“药物试验究竟是如何进行的?我得了登革热来一探究竟”一文最初发表于 2022 年 5 月 22 日,刊登于第 103 卷第 21 期。https ://cen.acs.org/pharmaceuticals/drug-development/drug-trials-really-work-dengue/103/web/2025/10
马克斯·巴恩哈特是《化学与工程新闻》的助理编辑。此前,他曾是美国科学促进会(AAAS)在国家公共广播电台(NPR)的大众传媒研究员。
Hits: 2
