Contents
Rabies and other lyssaviruses
澳大利亚免疫手册提供有关狂犬病、疫苗和接种建议的信息。
某些人群的疫苗接种费用由各州和地区承担。
本页内容:概述建议疫苗、剂量和给药禁忌症和注意事项不良事件疾病的性质临床特征流行病学疫苗和免疫球蛋白信息疫苗的运输、储存和处理公共卫生管理与产品信息的差异参考页面历史记录
本页
概述
什么
狂犬病是一种人畜共患病,由接触感染狂犬病毒或其他狂犬病毒的动物的唾液或神经组织引起。人类可通过动物抓伤或咬伤导致皮肤破损而感染,也可通过病毒与人体黏膜表面(如鼻子、眼睛或嘴巴)直接接触而感染。
谁
建议以下人群接种狂犬病暴露前疫苗:
- 与蝙蝠有接触的人
- 根据风险评估,前往狂犬病地方性流行地区的人员
- 与活狂犬病毒打交道的实验室工作人员
对于可能接触过狂犬病毒或其他狂犬病毒的人,建议接种暴露后狂犬疫苗,在某些情况下,还建议注射人狂犬病免疫球蛋白 。
如何
暴露前预防有四种给药方案,区别在于给药周期、剂量和给药途径。选择给药方案和途径并无优先推荐。应考虑个人的具体情况和个人偏好。
暴露后预防措施包括及时处理伤口,接种狂犬病疫苗,在某些情况下还需注射人狂犬病免疫球蛋白 。这些干预措施的适当组合以及疫苗接种剂量取决于风险评估,该评估需考虑以下因素:
- 暴露程度
- 暴露的动物来源
- 人的免疫状态
- 该人既往疫苗接种史
为什么
狂犬病几乎总是致命的。澳大利亚并非狂犬病地方性流行区。在狂犬病地方性流行区,人们可能通过接触陆生动物和其他哺乳动物而感染经典狂犬病毒 。世界各地的蝙蝠都可能是狂犬病毒的潜在来源,并构成感染狂犬病的潜在风险,具体取决于人们的接触途径。在澳大利亚所有四种果蝠(飞狐)以及几种澳大利亚食虫蝙蝠中均已发现澳大利亚蝙蝠狂犬病毒感染的证据。
建议
接触狂犬病毒和其他丽沙病毒前接种疫苗(暴露前预防)
- 与蝙蝠接触的人员、在实验室接触活狂犬病毒的工作人员以及一些前往狂犬病流行地区的人员,建议接种狂犬病疫苗作为暴露前预防措施。建议以下人群进行狂犬病疫苗暴露前预防:
- 可能被蝙蝠咬伤或抓伤的人员包括:蝙蝠饲养员;兽医和兽医护士;野生动物官员、野生动物护理员和动物园管理员;野生动物研究人员;以及在任何国家(包括澳大利亚)与蝙蝠直接接触的其他人。
- 接触任何活的狂犬病毒的研究实验室工作人员
- 前往或居住在狂犬病流行地区的人员,应在进行风险评估后接受暴露前预防,风险评估应考虑该人员与动物接触的可能性及其获得紧急医疗救助的途径。
狂犬疫苗可通过肌内注射或皮内注射途径接种。所有疫苗皮内注射每次用量均为 0.1 毫升。肌内注射时,Verorab 疫苗每次用量为 0.5 毫升,Rabipur 疫苗每次用量为 1.0 毫升。皮内注射是一种未经许可的(“超适应症”)给药途径。如果考虑采用皮内注射进行狂犬病暴露前预防,则必须注意以下事项:
- 这种疫苗必须由具备皮内注射技术专业知识并经常进行实践的免疫接种人员接种,因为不正确的接种方式可能导致受种者无法获得充分的保护。
- 免疫功能低下者不宜使用此药,因为他们的免疫反应可能不足 1,2,3。
- 接种狂犬疫苗时或接种后 1 个月内,如果正在服用氯喹或其他与氯喹结构相关的抗疟疾药物(例如甲氟喹或羟氯喹),则不应接种狂犬疫苗,因为这些药物会降低皮内注射狂犬疫苗的免疫反应 。
- 免疫接种服务提供者遵循多剂量疫苗瓶的使用程序,并在接种后 8 小时或接种结束后(以先到者为准)丢弃剩余疫苗。
暴露前预防有四种给药方案,区别在于给药周期、剂量和给药途径。 选择给药方案和途径并无优先推荐 。应考虑个人的具体情况和个人偏好。2-visit schedulesSerological testing for people who are immunocompromised查看推荐详情
- 对免疫功能低下者进行血清学检测
- 每毫升,请向州或地区卫生部门或专科免疫诊所寻求建议。
- Rationale for pre-exposure prophylaxis
- 暴露前预防的理由
- 暴露后阶段,该人需要接种的狂犬病疫苗剂量较少。
- 除非免疫功能严重受损,否则患者不需要注射狂犬病免疫球蛋白 ( RIG )。
这一点尤为重要,因为狂犬病免疫球蛋白 ( RIG )——无论是人源 RIG、马源 RIG 还是单克隆 RIG—— 都难以获得且价格昂贵,而且在许多狂犬病地方性流行发展中国家,其安全性也无法得到保证。另见: 可能接触狂犬病毒或其他丽沙病毒后的疫苗接种(暴露后预防) 。
- 暴露前预防简化了对后续可能接触狂犬病毒或澳洲蝙蝠狂犬病毒的管理,原因如下:
- 两次访问安排
- 第0天注射1次(梅里埃和拉比普尔为1.0毫升,维罗拉布为0.5毫升)。
- 第7天注射1次(梅里埃和拉比普尔为1.0毫升,维罗拉布为0.5毫升)。
推荐的两次就诊暴露前预防方案采用皮内注射途径,包括 4 剂疫苗,具体接种方法如下:
- 第0天在不同部位注射2次,每次0.1毫升。
- 第7天在不同部位各注射2次,每次0.1毫升。
对于免疫功能低下者,请勿采用两次就诊的方案,因为他们的免疫反应可能不足 。5这种两剂接种方案可提供短期保护,尤其适用于前往狂犬病流行地区的旅行者 。 如果一年后需要进一步保护,抗体水平可能已不足。8-10 无论首次暴露前预防的给药途径如何,均应在首次暴露前预防一年后进行单次肌注加强针。即使在首次暴露前预防一年后进行肌注加强针,仍能提供足够的保护 。9,11,12,13
- 请勿对 30 至 50 岁及以上的成年人使用此两疗程皮内注射方案,因为研究表明,该年龄组的血清转化率低于年轻人。 6,7
- 建议的暴露前预防方案为两次就诊,采用肌肉注射途径,包括接种两剂疫苗,具体接种方法如下:
- Serological testing for people who received pre-exposure prophylaxis by the intradermal route
- 对接受皮内途径暴露前预防的人员进行血清学检测如果出行前没有足够的时间进行血清学检测 ,则应优先选择肌肉注射途径进行疫苗接种。
- 如果采用皮内注射途径进行暴露前预防 ,理想情况下应在完成暴露前预防疗程后 2-4 周检查狂犬病抗体水平,以确保狂犬病毒中和抗体 (VNAb) 水平 ≥0.5 IU /mL。如果抗体滴度低于 0.5 IU /mL,请咨询州或地区卫生部门或专科免疫诊所的专家意见。
- Booster doses
- 加强剂量
- 对于在澳大利亚或海外持续存在职业性狂犬病毒暴露风险的已接种狂犬疫苗的人员,建议接种狂犬疫苗加强针。参见 “建议持续存在职业性狂犬病毒暴露风险的人员接种狂犬疫苗加强针” 。
- 3-visit schedules
- 3次就诊安排
- 建议的 3 次就诊暴露前预防方案包括 3 剂疫苗,分别在第 0 天、第 7 天和第 21-28 天接种。这些疫苗可以通过肌肉注射或皮内注射途径接种。
- 皮内注射途径仅限具备相应资质和经验的医疗机构(例如旅行医学诊所)使用。参见 “疫苗接种”部分 。此途径仅适用于免疫功能正常的人群的暴露前疫苗接种。
- 建议前往狂犬病流行地区的旅行者进行风险评估,以指导疫苗接种决策;所有旅行者都应避免接触狂犬病毒和其他丽沙病毒。前往或居住在狂犬病流行地区的人员应由医疗专业人员进行风险评估,评估内容包括他们与动物接触的可能性以及在当地获得紧急医疗服务的便利程度。此评估结果对于决定是否接种狂犬病疫苗进行暴露前预防至关重要。为降低前往狂犬病流行地区的旅行者感染狂犬病毒和其他丽沙病毒的风险,应建议他们采取以下措施:
- 避免与野生和家养动物密切接触——这一点对儿童尤其重要。12-16 岁
- 避免接触流浪猫狗。步行、跑步或骑自行车时要保持警惕。
- 不要让幼儿喂食、抚摸或与动物玩耍。幼儿身高较矮,更容易被咬伤面部和头部。这些部位的咬伤会增加患狂犬病的风险,并缩短发病时间。带孩子前往狂犬病流行地区的家长应考虑为年幼的孩子进行暴露前预防。
- 请勿携带食物,也不要喂食或抚摸猴子,即使是在寺庙或市场等热门区域,即使那里可能会鼓励游客与猴子互动。尤其不要靠近带着幼崽的猴子,因为它们可能会感到威胁并突然咬人。
- 在世界任何地方,包括澳大利亚,都应避免接触蝙蝠。只有经过适当疫苗接种和培训的人员才能处理蝙蝠。如果必须处理蝙蝠,请遵循安全预防措施,例如佩戴防护手套和穿戴防护服。
- 了解被动物咬伤或抓伤后该怎么做 14-18 — 旅行者应该接受有关狂犬病暴露急救治疗的教育,无论他们是否接种过疫苗。
需要注意的是,即使旅行者并未主动与动物接触,也可能发生被咬伤的情况,包括那些正在给动物拍照的人 。19查看推荐详情
- 有关暴露前预防方案, 建议与蝙蝠接触的人员、与活狂犬病毒接触的实验室工作人员以及前往狂犬病地方性流行地区的部分人员接种狂犬病疫苗进行暴露前预防 。
- 在狂犬病流行地区,可能接触到患有狂犬病的陆生动物的人应该接受暴露前预防。
- 建议长期职业暴露于狂犬病毒的人员接种狂犬病疫苗加强针。对于在澳大利亚或海外持续存在职业暴露于狂犬病毒风险的已接种狂犬疫苗的人员,建议接种加强针 。9,11,21-23 参见图。持续存在暴露于狂犬病毒或其他狂犬病毒风险的人员的加强针接种流程图 。这些人员包括:
- 在研究实验室中接触活狂犬病毒的人员应每 6 个月检测一次狂犬病毒中和抗体(VNAb)滴度。如果滴度为 0.5 IU/mL,则应接受单次肌注加强针。免疫功能低下者应在加强针注射后 2-4 周检测 VNAb 滴度。如果滴度为 0.5 IU/mL,则应再次注射加强针。此次加强针注射后无需进行血清学检测。持续面临感染风险的实验室工作人员应继续每 6 个月检测一次 VNAb 滴度。
- 在澳大利亚或海外接触过蝙蝠的人,或可能在海外接触到潜在狂犬病陆生哺乳动物的人, 应在首次接种狂犬病疫苗暴露前预防剂(或首次接种暴露后预防剂(如在接种暴露前预防剂前曾发生 II 类或 III 类暴露; 参见表:狂犬病毒暴露类别 )后 1 年接受单次肌注加强针。此后,这些人应每 3 年检测一次病毒中和抗体(VNAb)滴度。如果 VNAb 滴度为 0.5 IU/mL,则应再次接种单次肌注加强针。或者,在首次加强针接种后,无需检测 VNAb 滴度,即可每 3 年再次接种单次肌注加强针。即使在首次接种暴露前预防剂一年后接种,肌注加强针仍应提供足够的保护。 9,11
狂犬疫苗加强针一定要采用肌肉注射途径。切勿采用皮内注射途径进行加强针注射。
- 他们预期的暴露风险——也就是说,他们是否经常接触患病动物或狂犬病流行地区的狂犬病宿主物种。
- 他们的健康状况,例如免疫功能低下程度(见表 :疾病类型、免疫抑制疗法及相关免疫功能低下程度 )或既往疫苗反应不良史。
- 如果他们暴露于病毒,应及时接种疫苗进行暴露后预防。

图. 针对持续面临狂犬病毒或其他狂犬病毒暴露风险人群的加强免疫算法显示图片描述
- IU = 国际单位;PEP = 暴露后预防;PrEP = 暴露前预防对于有风险的实验室工作人员,每 6 个月进行一次血清学检测。血清学检测后,对于病毒中和抗体滴度至少为 0.5 IU/mL 的人,无需采取进一步措施,直到再次暴露(然后按照狂犬病或蝙蝠狂犬病毒暴露后算法给予暴露后预防,除非暴露发生在接受完整的暴露后预防后的 3 个月内,在这种情况下无需立即接种疫苗)或下一个血清学检测期结束(然后进行血清学检测)。查看推荐详情
- 对于病毒中和抗体滴度为 0.5 IU/mL 的免疫功能正常者,给予单次肌注加强针。对于免疫功能低下者,给予单次肌注加强针,并在 2-4 周后复查血清学。如果抗体滴度仍为 0.5 IU/mL,则再次给予加强针。如果再次接触病毒,则按照陆生动物暴露后预防流程或蝙蝠暴露后预防流程进行预防。
- 对于兽医工作人员、接触蝙蝠或可能需要接触蝙蝠的人员,以及在狂犬病流行国家持续接触可能携带狂犬病毒的陆生哺乳动物的人员,应在暴露前预防接种一年后进行单次肌注加强针。之后,自首次加强针接种之日起,每三年进行一次血清学检测或再次接种加强针。
- 该流程图有助于确定持续存在职业风险的人员是否需要接种狂犬病疫苗加强剂。
- 要确定某人是否应该接种狂犬疫苗加强针(因为其病毒中和抗体滴度低于 0.5 IU/mL),应考虑以下因素:
可能接触狂犬病毒或其他狂犬病毒后接种疫苗(暴露后预防)
- 建议所有可能接触过狂犬病毒或其他丽沙病毒的人都应接受暴露后预防,包括接种狂犬疫苗,在某些情况下还应注射狂犬免疫球蛋白。狂犬病毒和其他丽沙病毒暴露后的预防措施包括:
- 及时伤口处理
- 狂犬病疫苗
- 人狂犬病免疫球蛋白(HRIG)
这些要素的适当组合取决于详细的风险评估,包括确定:
- 暴露类型( 见表:狂犬病毒暴露类别 )
- 暴露的动物来源
- 人的免疫状态
- 该人既往疫苗接种史
Post-exposure prophylaxis must include wound managementPotential exposure to terrestrial animals in rabies-enzootic countries查看推荐详情
- 在狂犬病流行国家可能接触陆生动物
- 大多数可能导致狂犬病感染的暴露途径来自亚洲、非洲以及中南美洲的狗和猴子。
- Potential exposure to Australian bats
- 可能接触到澳大利亚蝙蝠
- 患有发育障碍的人
- 醉酒的人
- 一个孩子
- 一个人在有蝙蝠存在的狭小空间里睡觉。
如果可能,且不会使其他人面临感染风险,请保留这只蝙蝠,并安排对其进行 ABLV (澳大利亚蝙蝠狂犬病毒)检测。按照图中所示的蝙蝠暴露算法进行狂犬病暴露后预防:蝙蝠暴露 。
- 如果蝙蝠的 ABLV 检测结果为阴性,则停止暴露后预防 。
- 伤口处理后(参见 “暴露后预防必须包括伤口处理 ”),如果蝙蝠的 ABLV 检测结果可在暴露后 48 小时内获得,则暂缓注射人狂犬病免疫球蛋白 (HRIG) 和狂犬疫苗。如果蝙蝠的 ABLV 检测结果无法在 48 小时内获得,则应尽快开始相应的暴露后预防 。对于头部和颈部的咬伤,即使动物已被送去检测,也应尽快进行暴露后预防 ,最好在暴露后 48 小时内进行。
- 接触澳大利亚蝙蝠的潜在途径可能难以归类。这可能是因为人们没有意识到自己可能接触过蝙蝠,或者无法沟通自己是否接触过蝙蝠——例如:
- 暴露后预防措施必须包括伤口管理。
- 立即用肥皂和水彻底清洗所有咬伤和抓伤。
- 使用杀病毒制剂,例如聚维酮碘溶液
避免缝合疑似狂犬病动物的咬伤。正确的做法是:清洁伤口,清除坏死组织,并用狂犬病免疫球蛋白充分浸润伤口。参见以下任一说明:
还要考虑伤口是否可能感染破伤风梭菌等病原体,并采取适当措施(参见破伤风 )。
- 接触狂犬病毒或其他狂犬病毒后,伤口处理至关重要。为了帮助预防狂犬病传播:
- 表格. 狂犬病毒暴露类别
暴露类别 描述 暴露后预防管理 第一类:无暴露 - 触摸或喂食动物
- 动物舔舐完好无损的皮肤
- 接触动物血液、尿液或粪便
如果接触史可靠,则无需预防。 第二类:暴露 - 轻咬裸露的皮肤
- 轻微划痕或擦伤,无出血
根据具体情况,请参见以下内容:
第三类:严重暴露 - 单次或多次经皮咬伤或抓伤
- 动物舔舐造成的唾液污染粘膜或破损皮肤
- 因直接接触蝙蝠而导致的暴露
根据具体情况,请参见以下内容:
- Assess all potential exposures from a terrestrial animal in a rabies-enzootic area, or from a bat anywhere in the world
- 评估在狂犬病地方性流行区,通过陆生动物或世界任何地方的蝙蝠可能接触到的所有潜在途径。根据狂犬病毒暴露情况的不同,有两种不同的暴露后预防管理方案:
- 来自狂犬病地方性流行国家的陆生动物—— 见图。狂犬病暴露后预防:陆生动物暴露 ,或
- 来自蝙蝠(澳大利亚或海外)—— 见图。狂犬病暴露后预防:蝙蝠暴露
这两个算法的不同之处在于: 24
- 蝙蝠造成的伤口风险往往难以确定——蝙蝠咬伤和抓伤造成的伤口通常比其他动物咬伤造成的伤口要小。
- 蝙蝠造成的浅表伤口比陆生动物造成的浅表伤口更容易导致人类感染 。
在可能发生人身暴露后,应尽一切努力对动物进行狂犬病毒检测,以避免不必要的暴露后预防 。对于头部和颈部咬伤,即使动物已被送去检测,也应尽快(最好在暴露后 48 小时内)进行暴露后预防 。评估接触活体和死亡动物后感染狂犬病的风险。一项小鼠研究表明,狂犬病毒在腐烂动物的脑组织中可存活 25 小时。
- 在 25°C 至 35°C 的温度下保存的尸体中,最多可存活 3 天。
- 在较低温度下保存的尸体最多可保存 18 天
即使事件报告存在相当长的延迟,也应根据暴露类别和暴露来源给予适当的暴露后预防措施 。参见表格:狂犬病毒暴露类别 。如有任何潜在暴露风险,请联系您所在州或地区的卫生部门。他们可以协助进行详细的风险评估并就管理措施提供建议。另请参阅公共卫生管理 。
- 但是,如果一个人在狂犬病流行国家被家养宠物咬伤或抓伤后 ≥15 天出现症状 ,并且已知该动物在暴露后 ≥15 天仍然健康,则该人不需要暴露后预防 。
- 评估所有接触陆生哺乳动物(在狂犬病地方性流行国家)和蝙蝠(在任何国家)的情况,以确定是否存在经典狂犬病毒传播的可能性。
- 建议可能接触过 II 类或 III 类狂犬病毒的人员接种狂犬疫苗作为暴露后预防措施。处理伤口后,根据狂犬病疫苗的种类和暴露来源,接种狂犬病疫苗,并根据情况是否同时注射人狂犬病免疫球蛋白(HRIG)。参见:
如果一个人的疫苗接种情况不确定,因为没有文件证明其已完成狂犬病疫苗的接种疗程,则应给予完整的暴露后预防方案。表格. 已接种疫苗人群:根据免疫状态和暴露类别进行暴露后狂犬病预防Use of human rabies immunoglobulin查看推荐详情
- 使用人狂犬病免疫球蛋白
- 表格. 狂犬病毒暴露类别
- 表格. 已接种疫苗人群:根据免疫状态和暴露类别进行暴露后狂犬病预防
- 表格. 未接种疫苗人群:根据免疫状态和暴露类别进行暴露后狂犬病预防
- 图. 狂犬病暴露后预防:陆生动物暴露
- 图.狂犬病暴露后预防:蝙蝠暴露
如有指征,应在接种第一剂疫苗后尽快(最好在 7 天(168 小时)内)注射一剂人免疫球蛋白 G(HRIG )。如果距离接种第一剂疫苗已超过 7 天(168 小时),则不得注射 HRIG 。以下人群不建议进行人乳头瘤病毒检测 :
- 在接受人免疫球蛋白 G 检测前超过 7 天(168 小时)接种了第一剂疫苗——也就是说,自他们接种第一剂疫苗以来已经超过 7 天(168 小时)。
- 在潜在暴露发生 12 个月后仍未接受医疗护理
- 有至少两剂狂犬病疫苗接种史(暴露前或暴露后预防) 者,因为接种疫苗可能会抑制免疫记忆和循环中和抗体(VNAb);这不包括严重免疫功能低下者,他们始终需要注射狂犬病免疫球蛋白( HRIG) (参见表 :已接种疫苗者:基于免疫状态和暴露类别的暴露后狂犬病预防 ,以及表:未接种疫苗者:基于免疫状态和暴露类别的暴露后狂犬病预防 )。
- 有记录显示,在暴露前 12 个月内曾接受过 1 剂肌肉注射狂犬疫苗。
- 既往任何时间均有记录显示 VNAb 滴度为 3E0.5 IU /mL。
这些人应该只接种狂犬病疫苗。
- 关于狂犬疫苗和人狂犬免疫球蛋白(HRIG) 作为暴露后预防手段, 预防除经典狂犬病毒以外的其他丽沙病毒感染的有效性数据有限。然而,现有的动物实验数据和临床经验支持其应用 。32-37
- 狂犬病免疫球蛋白(HRIG) 可在受者对狂犬病疫苗产生免疫反应期间提供局部抗狂犬病抗体保护。有关 HRIG 的注射方法,请参阅 “疫苗、剂量和注射”部分 。
- 建议一些可能接触过狂犬病毒或其他丽沙病毒的人群,在接种狂犬疫苗的同时,也接受人狂犬病免疫球蛋白 (HRIG) 作为暴露后预防措施 。参见:
- 已接种疫苗者需提供既往任何时间完成推荐的暴露前或暴露后预防方案的证据,或既往任何时间有记录的狂犬病毒中和抗体 (VNAb) 滴度达到 3E0.5 IU /mL。对于有部分免疫史者,请参阅 “未完成的暴露前预防方案” 。
免疫状态 暴露类别 HRIG 第 1 剂(第 0 天) 第二剂(第3天) 第3剂(第7天) 第 4 剂(第 14 天) 第5剂(第28天) 免疫功能正常 任何第二类或第三类 不需要 是的 是的 不需要 不需要 不需要 轻度或中度免疫功能低下 任何第二类或第三类 不需要 是的 是的 不需要 不需要 不需要 严重免疫功能低下 任何第二类或第三类 不需要 是的 是的 是的 是的 是的 HRIG = 人狂犬病免疫球蛋白
几天的偏差可能无关紧要 。27
有关免疫功能低下程度的定义,请参阅 “免疫功能低下人群疫苗接种中的疾病类型、免疫抑制疗法及相关免疫功能低下程度”部分中的定义和表格。
- Repeat rabies exposure
- 重复暴露于狂犬病
- 在完成先前暴露后预防治疗后 3 个月内再次暴露的人不需要再接种任何疫苗、 人免疫球蛋白 ,只需要伤口处理(无论免疫状态如何)。
- People who are immunocompromised
- 免疫功能低下的人群在末次接种疫苗后 2-4 周检测 VNAb 滴度。如果滴度为 0.5 IU /mL,则需再次接种疫苗。在再次接种疫苗后 2-4 周重复血清学检测 。如果滴度仍为 0.5 IU /mL,请咨询州或地区卫生部门。有关免疫功能低下程度的定义,请参阅定义和表格。 免疫功能低下人群疫苗接种中的医疗状况和免疫抑制疗法类型以及相关的免疫功能低下程度 。
- 免疫功能严重受损的人,即使以前接种过狂犬疫苗,也应该在接种狂犬疫苗的基础上再注射一剂狂犬病免疫球蛋白作为暴露后预防措施 。
- 如有可能,在进行暴露后预防性治疗期间,应停止任何免疫抑制治疗 (包括皮质类固醇)。此类治疗可能会干扰疫苗产生的保护性免疫反应。请咨询患者的主治医生,讨论此方案的可行性。
- Incomplete pre-exposure prophylaxis schedule
- 暴露前预防方案不完整
- 如果在暴露前 12 个月内进行单剂量肌肉注射,则无需进行 HRIG 注射 。
- 如果单次剂量是在暴露前 12 个月以上接种的,则需要进行 HRIG 检测 。
- 如果单剂量皮内注射,则无论何时注射,都需要进行人免疫球蛋白注射 (HRIG) 。
免疫功能低下且未完成暴露前预防程序的任何人,都应像未接种疫苗的人一样接受暴露后预防 ,包括人免疫球蛋白 (HRIG) 。
- 之前只接种过 1 剂疫苗进行暴露前预防的人,需要接种 4 剂疫苗进行暴露后预防 (与未接种疫苗的人类似):
- 不建议采用皮内注射方式接种狂犬病疫苗进行暴露后预防 。
- 目前尚无临床试验评估狂犬病疫苗的有效性 ,但支持对免疫功能正常者采用 4 剂接种方案的理论依据是多项研究。 27-29 在澳大利亚和国际上,均未报告过在可能接触过狂犬病病毒并已完成暴露后预防疗程的人群中出现疫苗接种失败的病例。 30
- 表格. 未接种疫苗人群:根据免疫状态和暴露类别进行暴露后狂犬病预防
免疫状态 暴露类别 HRIG 第 1 剂(第 0 天) 第二剂(第3天) 第3剂(第7天) 第 4 剂(第 14 天) 第5剂(第28天) 免疫功能正常 第二类陆生动物 不需要 是的 是的 是的 是的 不需要 第二类球棒和任何第三类球棒 是的 是的 是的 是的 是的 不需要 轻度或中度免疫功能低下 任何第二类或第三类 是的 是的 是的 是的 是的 是的 严重免疫功能低下 任何第二类或第三类 是的 是的 是的 是的 是的 是的 HRIG = 人狂犬病免疫球蛋白
几天的偏差可能无关紧要 。27
有关免疫功能低下程度的定义,请参阅“定义和表格”。 “免疫功能低下人群疫苗接种中涉及的疾病类型、 免疫抑制疗法及其相关的免疫功能低下程度”.
- 皮内注射疫苗用于暴露前或暴露后预防可视为既往接种疫苗。
- 建议在海外开始接受暴露后预防治疗且可能接触过狂犬病病毒的人员,在澳大利亚完成狂犬病疫苗接种疗程。前往海外旅行的澳大利亚人如果接触到可能患有狂犬病的动物(包括来自任何国家的蝙蝠),可能会接受暴露后预防,使用细胞培养衍生的疫苗和澳大利亚不使用的接种方案。如果某人在国外接种了鸡胚疫苗或细胞培养疫苗,建议其在澳大利亚继续接受标准的暴露后预防方案,使用人二倍体细胞疫苗或纯化鸡胚细胞疫苗。参见狂犬病疫苗的互换性 。表格:全球可用的狂犬病疫苗及其与澳大利亚注册疫苗的兼容性查看推荐详情
狂犬疫苗 疫苗信息 兼容的 人二倍体细胞疫苗(HDCV) 伊莫瓦克斯,赛诺菲巴斯德公司
康华狂犬病,成都康华生物制品中国
是的 纯化鸡胚细胞疫苗( PCECV ) RabAvert,葛兰素史克
Vaxirab-N,卡迪拉医疗保健印度
是的 纯化 Vero 细胞狂犬病疫苗(PVRV) RABIVAX-S,印度血清研究所
SPEEDA,成达生物中国
Abhayrab(除非在印度境内给药*),印度人类生物制品研究所
印度巴拉特生物技术公司
是的 纯化鸭胚疫苗(PDEV) Lyssavac,印度卡迪拉医疗保健公司
Vaxirab,卡迪拉医疗保健印度
是的 叙利亚仓鼠肾细胞疫苗(PHKCV) 中国本土生产商 是的 幼仓鼠肾细胞疫苗(BHKV) 俄罗斯科卡夫 是的 基于重组纳米颗粒的狂犬病 G 蛋白病毒样颗粒( VLP )疫苗 Thrabis,卡迪拉制药印度 不 乳鼠脑疫苗(SMBV) 在南美洲使用 不 神经组织疫苗(绵羊、山羊) 在亚洲、埃塞俄比亚和阿根廷使用 不 - * 印度已发现假冒的 Abhayrab® 狂犬疫苗(批号 KA24014)。请参阅 ATAGI 声明:《印度报告假冒狂犬疫苗 (Abhayrab®):旅行者和医疗保健提供者指南》(2026 年 1 月 11 日)。
- 世界卫生组织批准的用于未接种过狂犬病疫苗的人群的暴露后狂犬病疫苗肌注给药方案包括:
- 萨格勒布方案——第 0 天注射 2 剂,第 7 天和第 21 天注射(标注为 2-0-1-0-1)
- 埃森方案——在第 0、3、7、14 和 28 或 30 天给药(标注为 1-1-1-1-1)
- 改良埃森方案——在第 0、3、7 和 14-28 天给药(标注为 1-1-1-1-0)
世界卫生组织批准的用于暴露后狂犬病疫苗接种的皮内给药方案包括:
- 柬埔寨巴斯德研究所 ( IPC ) 方案——第 0、3 和 7 天各注射 2 剂(标注为 2 2 2 0 0)
- 更新后的泰国红十字会( TRC )方案——第 0、3、7 和 28 天各接种 2 剂(标注为 2 2 2 0 2)
在澳大利亚,如果符合以下情况,建议接受人狂犬病免疫球蛋白 ( HRIG )注射:
- 根据暴露类型和个人的免疫状态进行指示(参见图:狂犬病暴露后预防 :陆生动物暴露或图:狂犬病暴露后预防 :蝙蝠暴露)
- 潜在的暴露发生在过去12个月内,
- 他们在海外开始了暴露后预防, 但没有注射人狂犬病免疫球蛋白 (HRIG )或马狂犬病免疫球蛋白 (ERIG)。
- 他们在过去 7 天(168 小时)内接种了第一剂暴露后预防疫苗。人免疫球蛋白(HRIG) 应注射在与疫苗不同的肢体上。
如果澳大利亚的感染者在 7 天前已接种了第一剂暴露后预防疫苗,则不应再接种狂犬病免疫球蛋白 (HRIG) 。但是,他们仍应完成剩余狂犬病疫苗的相应剂次接种。建议旅客,如果在海外开始进行暴露后预防 ,必须向疫苗接种中心索取暴露后预防证明,并获取或记录以下信息(最好用英文):
- 就诊诊所的联系方式(电话和电子邮件地址)
- 所用狂犬病免疫球蛋白 ( RIG )的批次和来源(一些国家可能使用 ERIG 或单克隆 RIG 而不是 HRIG )。
- 注射的 RIG 量
- 所用细胞培养疫苗的类型
- 疫苗批号
- 所用小瓶数量
- 疫苗接种途径
- 注射 RIG 和/或疫苗的日期和时间
这些细节有助于为旅行者返回家乡后如何完成暴露后预防提供决策依据。
- 对于这些及其他情况, 表“在澳大利亚完成在海外开始的狂犬病暴露后预防” 概述了最常见的可能在海外开始的暴露后预防方案以及在澳大利亚完成暴露后预防的推荐时间表。
- 一般来说,如果细胞培养疫苗每剂至少含有 2.5 IU 的狂犬病毒,且有科学文献证明其能产生可接受的暴露后抗体反应(狂犬病毒中和抗体 ≥0.5 IU/mL),则该疫苗是可接受的。参见表格:全球可用的狂犬疫苗及其与澳大利亚注册疫苗的兼容性 。
- 如果该人接种过较早的神经组织来源狂犬疫苗,则这些剂量无效。这种情况非常罕见。参见表格:在澳大利亚完成在海外开始的暴露后预防 。
- 建议孕妇或哺乳期妇女在可能接触狂犬病后接种狂犬病疫苗。建议孕妇或哺乳期妇女在可能接触狂犬病毒、澳大利亚蝙蝠狂犬病毒或其他蝙蝠狂犬病毒后,根据需要接种狂犬疫苗和人狂犬病免疫球蛋白。 37,38 参见表格。不建议在妊娠期间常规接种的疫苗: 计划怀孕、怀孕或哺乳期妇女的疫苗接种指南中的灭活病毒疫苗 。查看推荐详情
表格和图表
另见表。狂犬病毒暴露类别 。
表格:在澳大利亚完成从海外开始的狂犬病暴露后预防治疗的情况
这些情景假设该人在暴露前未接受过暴露前预防 。更多详情请参见图:狂犬病暴露后预防:陆生动物暴露或图:狂犬病暴露后预防:蝙蝠暴露 。
| 海外情景 | 澳大利亚狂犬病疫苗接种计划(含或不含狂犬病免疫球蛋白) |
|---|---|
| 该人接种了神经组织衍生疫苗 |
|
| 疫苗或 RIG 的使用情况不确定或未知,或者记录不完整。 |
|
| 该患者免疫功能低下,疫苗采用皮内注射方式接种。 |
|
| 该情景已有详细记录。受试者于第 0 天接受了 2 剂皮内注射疫苗( IPC / TRC 方案) 。RIG (马源或人源)可能与第一剂疫苗同时注射,也可能未同时注射。 |
|
| 该情景已有详细记录。受试者在第 0 天和第 3 天分别皮内注射了两剂疫苗( IPC / TRC 方案)。RIG ( 马源或人源)可能与第一剂疫苗同时注射,也可能没有同时注射。 |
|
| 该情况已有详细记录。受试者在第 0 天、第 3 天和第 7 天分别皮内注射了两剂疫苗( IPC / TRC 方案)。RIG(马源或人源)可能与第一剂疫苗同时注射,也可能没有同时注射 。 |
|
| 该情景已有详细记录。受试者在第 0 天和第 3 天分别肌注了一剂疫苗(埃森方案/改良埃森方案)。 狂犬病免疫球蛋白 (马源或人源)可能与第一剂疫苗同时注射,也可能没有同时注射。 |
|
| 该患者于第 0 天接受了 2 剂肌肉注射疫苗(萨格勒布方案)。 免疫球蛋白 (马源或人源)可能与第一剂疫苗同时注射,也可能未同时注射。 |
|
| 脚注:HRIG = 人狂犬病免疫球蛋白 ; IPC / TRC = 柬埔寨巴斯德研究所/泰国红十字会(更新版); PEP = 暴露后预防 ; RIG = 狂犬病免疫球蛋白 | |
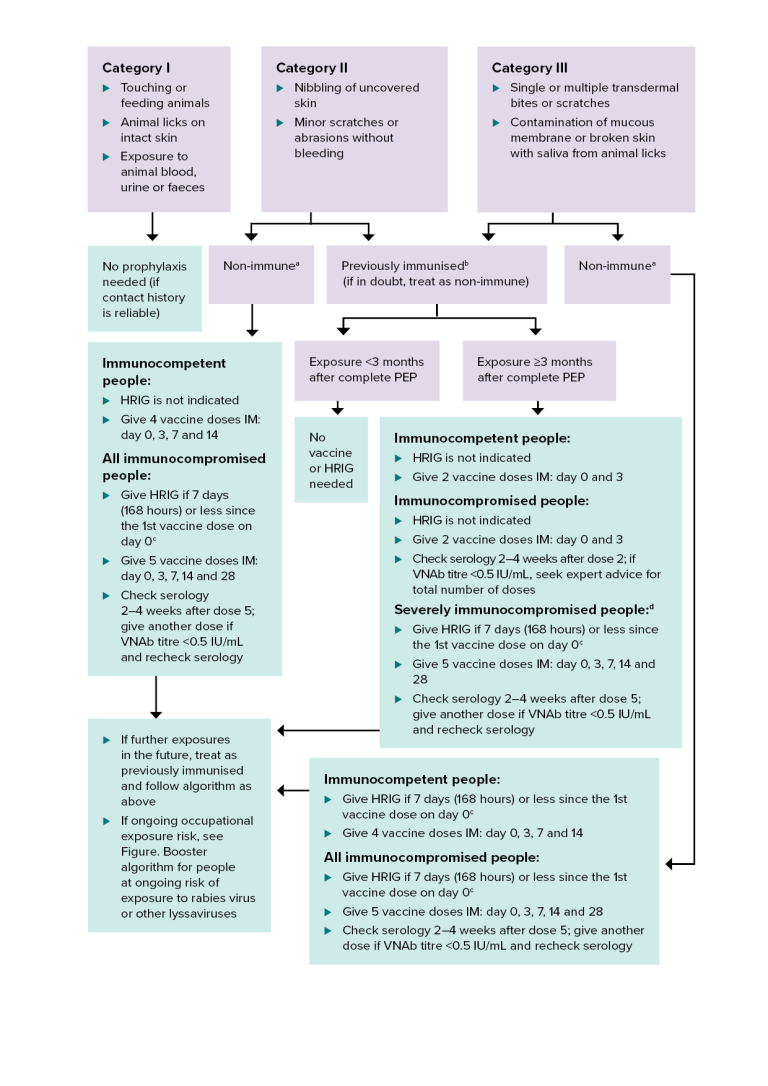
图. 狂犬病暴露后预防:陆生动物暴露
HRIG = 人狂犬病免疫球蛋白;IM = 肌内注射;IU = 国际单位;PEP = 暴露后预防;VNAb = 病毒中和抗体
非免疫者——从未接受过狂犬病疫苗暴露前或暴露后预防 ,或未完成(3C2 剂)基础疫苗接种疗程的人。
- 既往已接种疫苗——无论距上次接种时间多久,均需提供至少两剂狂犬病疫苗暴露前或暴露后预防接种的证明文件。可以是已完成的暴露前基础免疫程序,也可以是暴露后免疫程序。这包括已接种后续加强针或狂犬病病毒中和抗体(VNAb)滴度≥0.5IU/mL 的人员。更多详情,请参阅 “未完成的暴露前预防方案” 。
c 在与疫苗不同的肢体上注射人免疫球蛋白。
d 关于免疫功能低下程度的定义,请参见“定义和表格”。 免疫功能低下人群疫苗接种中涉及的疾病类型、免疫抑制疗法及其相关的免疫功能低下程度。.
该算法为在狂犬病流行地区接触陆生动物狂犬病毒后进行暴露后预防提供了指导。
狂犬病暴露分为 3 类 :
- 第1类:接触或喂食动物,动物舔舐完整皮肤,或接触动物血液、尿液或粪便。
- 第2类:动物啃咬裸露的皮肤,或轻微的划伤或擦伤,但不出血。
- 第 3 类。单次或多次经皮咬伤或抓伤;粘膜或破损皮肤被动物舔舐的唾液污染。
如果接触史可靠, 则 1 类暴露不需要任何预防措施。
对于非免疫人群的 2 类暴露(见注释 a),免疫功能正常者无需接种人免疫球蛋白(HRIG);应在第 0、3、7 和 14 天肌注 4 剂疫苗。对于所有免疫功能低下且有 2 类暴露史的人群,如果自第 0 天接种第一剂疫苗后 7 天(168 小时)或更短时间内接种 HRIG(见注释 c);应在第 0、3、7、14 和 28 天肌注 5 剂疫苗;在第 5 剂接种后 2-4 周进行血清学检查;如果疫苗中和抗体(VNAb)滴度低于 0.5 IU/mL,则需再接种一剂疫苗并复查血清学。
对于既往已接种过疫苗的人员,若发生 2 类或 3 类暴露(参见注释 b;如有疑问,按未免疫者处理),则无需接种疫苗或人免疫球蛋白(HRIG)。若暴露发生在完成暴露后预防 3 个月或更长时间后,则需要接种疫苗。对于免疫功能正常者,不建议使用 HRIG;在第 0 天和第 3 天肌注 2 剂疫苗。对于免疫功能低下者,不建议使用 HRIG;在第 0 天和第 3 天肌注 2 剂疫苗;在第 2 剂接种后 2-4 周检查血清学;如果疫苗中和抗体(VNAb)滴度为 0.5 IU/mL,请咨询专家以确定总接种剂量。对于严重免疫功能低下者(参见注释 d),如果自第 0 天接种第一剂疫苗后 7 天(168 小时)或更短时间内接种 HRIG(参见注释 c)。在第 0、3、7、14 和 28 天肌肉注射 5 剂疫苗;在第 5 剂后 2-4 周检查血清学;如果 VNAb 滴度为 <0.5 IU/mL,则再注射一剂并重新检查血清学。
对于非免疫人群,若暴露于第 3 类病毒(见注释 a),则应给予人免疫球蛋白 G(HRIG)。若距首次接种疫苗(第 0 天)不足 7 天(168 小时),则应给予 HRIG(见注释 c);在第 0、3、7 和 14 天肌注 4 剂疫苗。对于所有免疫功能低下者,若距首次接种疫苗(第 0 天)不足 7 天(168 小时),则应给予 HRIG(见注释 c);在第 0、3、7、14 和 28 天肌注 5 剂疫苗;在第 5 剂接种后 2-4 周进行血清学检查;若疫苗中和抗体(VNAb)滴度低于 0.5 IU/mL,则需再次接种疫苗并复查血清学。
对于所有暴露人群 ,如果未来再次暴露,应视为已接种疫苗,并遵循上述算法。如果存在持续的职业暴露风险,请参见图。图:持续存在狂犬病毒或其他丽沙病毒暴露风险人群的加强免疫算法 。
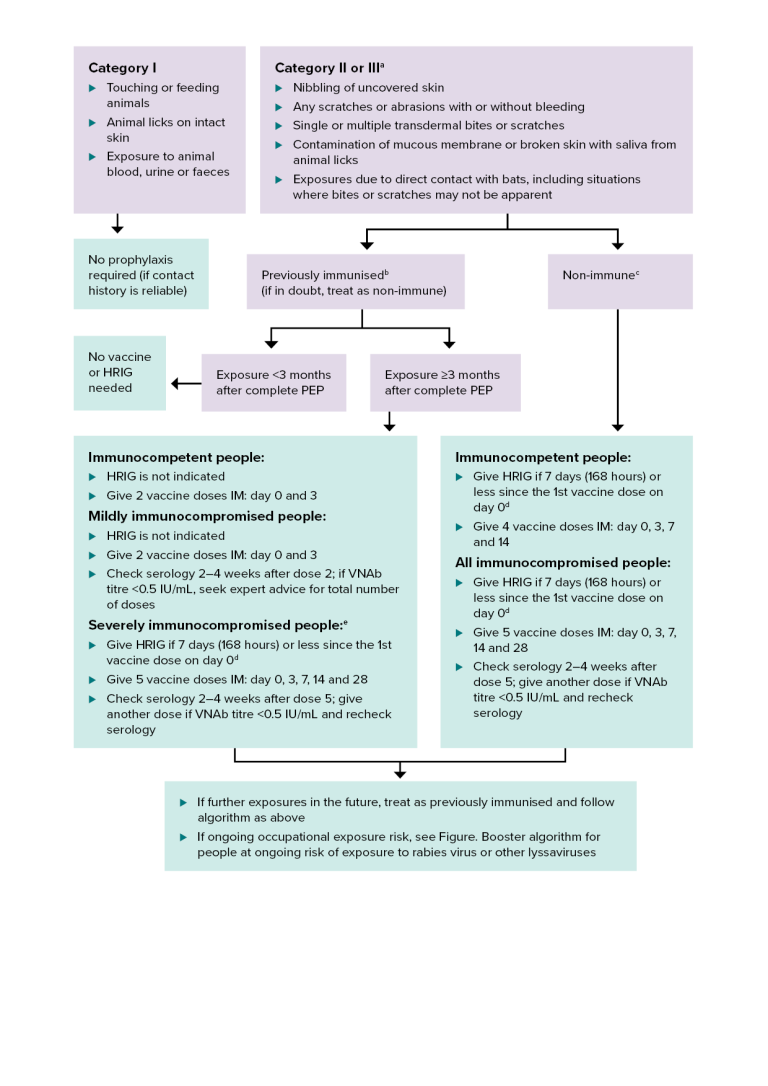
图.狂犬病暴露后预防(PEP):蝙蝠暴露
HRIG = 人狂犬病免疫球蛋白;IM = 肌内注射;PEP = 暴露后预防;VNAb = 病毒中和抗体
a 包括在难以界定接触蝙蝠情况时与蝙蝠的直接接触,因为当事人可能不知道或无法说明是否以及如何接触过蝙蝠。有些蝙蝠的牙齿和爪子很小,因此咬伤或抓伤可能并不明显。
- 既往已接种疫苗——无论距上次接种时间长短,均需提供至少两剂狂犬病疫苗暴露前或暴露后预防接种的证明文件。可以是已完成的暴露前基础免疫程序,也可以是暴露后免疫程序。这包括已接种后续加强针或狂犬病中和抗体滴度≥0.5 IU/mL 的人员。更多详情,请参阅“未完成的暴露前预防方案”。
c 非免疫者——从未接种过暴露前或暴露后狂犬病疫苗的人,或未完成(<2 剂)基础疫苗接种疗程的人。
d 在与疫苗不同的肢体上注射人免疫球蛋白。
e 关于免疫功能低下程度的定义,请参见“定义和表格”。 免疫功能低下人群疫苗接种中涉及的疾病类型、免疫抑制疗法及其相关的免疫功能低下程度。.
该算法为在澳大利亚或海外可能接触到蝙蝠狂犬病毒后进行暴露后预防提供指导。
接触蝙蝠狂犬病毒的途径分为三类:
- 第1类 :接触或喂食动物,动物舔舐完好的皮肤,或接触动物的血液、尿液或粪便。
- 第 2 类或第 3 类 。(见注释 a)动物啃咬裸露的皮肤;任何有或无出血的抓伤或擦伤;单次或多次经皮咬伤或抓伤;粘膜或破损的皮肤被动物舔舐的唾液污染;或因与蝙蝠直接接触而暴露,包括咬伤或抓伤可能不明显的情况。
如果接触史可靠,则第 1 类病例不需要任何预防措施。
对于既往已接种过疫苗的人群,若发生 2 类或 3 类暴露(参见注释 b;如有疑问,按非免疫人群处理),则无需接种疫苗或人免疫球蛋白(HRIG)。若暴露发生在完成暴露后预防 3 个月或更长时间后,则需要接种疫苗。对于免疫功能正常者,不建议使用 HRIG;于第 0 天和第 3 天肌注 2 剂疫苗。对于轻度免疫功能低下者,不建议使用 HRIG;于第 0 天和第 3 天肌注 2 剂疫苗;于第 2 剂接种后 2-4 周检查血清学;若疫苗中和抗体(VNAb)滴度低于 0.5 IU/mL,请咨询专家以确定总接种剂量。对于重度免疫功能低下者(参见注释 e),若距第 0 天首次接种疫苗不超过 7 天(168 小时)(参见注释 d),则需使用 HRIG。在第 0、3、7、14 和 28 天肌肉注射 5 剂疫苗;在第 5 剂后 2-4 周检查血清学;如果 VNAb 滴度为 <0.5 IU/mL,则再注射一剂并重新检查血清学。
对于非免疫人群,若暴露于第 2 类或第 3 类病毒 (参见注释 c),则应给予人免疫球蛋白 G (HRIG),若距首次接种疫苗(第 0 天)不足 7 天(168 小时)(参见注释 d);在第 0、3、7 和 14 天肌注 4 剂疫苗。对于所有免疫功能低下者,若距首次接种疫苗(第 0 天)不足 7 天(168 小时)(参见注释 d),则应给予 HRIG;在第 0、3、7、14 和 28 天肌注 5 剂疫苗;在第 5 剂疫苗接种后 2-4 周进行血清学检查;若疫苗中和抗体 (VNAb) 滴度低于 0.5 IU/mL,则需再次接种疫苗并复查血清学。
对于所有暴露人群,如果未来再次暴露,应视为已免疫,并遵循上述算法。如果存在持续的职业暴露风险,请参见图。图:持续存在狂犬病毒或其他丽沙病毒暴露风险人群的加强免疫算法 。
疫苗、剂量和给药
澳大利亚有售狂犬病疫苗
美国药品管理局网站提供每种疫苗的产品信息。
狂犬病疫苗
- 拉比普尔灭活狂犬病毒疫苗赞助:注册后可供任何年龄段的人群使用。冻干粉末装于单剂量小瓶中,以 1.0 mL 蒸馏水作为稀释剂。
- ≥2.5 IU 灭活狂犬病毒
还含有少量:
- 新霉素
- 氯四环素
- 氨丁三醇
- β-丙内酯
- 谷氨酸单钾
- 两性霉素 B
可能含有微量:
- 牛明胶
- 鸡蛋蛋白
有关 Rabipur 灭活狂犬病毒疫苗的产品信息和消费者用药信息,请访问澳大利亚药品管理局网站 。查看疫苗详情
- 每1.0毫升复溶剂量含有:
- PCECV——纯化鸡胚细胞疫苗
- 塞奇鲁斯
- 管理路线:
- 肌内注射
- Verorab 灭活狂犬病毒疫苗赞助:注册后可供任何年龄段的人群使用。冻干粉末,装于单剂量小瓶中,配有单独的稀释剂。
- 3.25 IU 灭活狂犬病毒
- 麦芽糖
- 20%白蛋白溶液
- Eagle 基础培养基,含 4.1 微克苯丙氨酸
- 氯化钠
还含有少量:
- 盐酸和/或氢氧化钠
可能含有微量:
- 新霉素
- 链霉素
- 多粘菌素
有关 Verorab 灭活狂犬病毒疫苗的产品信息和消费者用药信息,请访问澳大利亚药品管理局网站 。查看疫苗详情
- 每0.5毫升复溶剂量含有:
- PVRV——纯化 Vero 细胞狂犬病疫苗
- 赛诺菲-安万特澳大利亚
- 管理路线:
- 皮内注射、肌肉注射
剂量和途径
用于暴露前和暴露后预防的狂犬病疫苗剂量为: 肌肉注射时,Rabipur 灭活狂犬病毒疫苗剂量为 1.0 mL,Verorab 灭活狂犬病毒疫苗剂量为 0.5 mL。该剂量适用于婴幼儿、儿童和成人。
所有狂犬病疫苗用于暴露前预防的剂量均为 0.1 毫升,采用皮内注射 。婴儿、儿童和成人的剂量相同。皮内注射途径只能由具备相应资质和经验的医护人员进行。如果采用皮内注射途径接种狂犬病疫苗,一次接种过程中,总剂量可用于多人。接种结束后,剩余的疫苗应丢弃。参见 “疫苗接种”部分 。
狂犬疫苗应接种于三角肌区域,因为接种于其他部位可能导致狂犬病毒中和抗体(VNAb)滴度降低。建议 12 个月及以下婴儿在大腿前外侧接种狂犬疫苗。臀中肌也是婴儿可接受的接种部位。参见 “疫苗接种” 部分。
不要在臀部注射狂犬疫苗,因为在该部位注射疫苗可能导致暴露后预防失败 。24
与其他疫苗联合接种
狂犬病疫苗可以与其他疫苗同时接种,但需使用不同的注射部位。
人狂犬病免疫球蛋白
KamRAB 狂犬病免疫球蛋白
赞助:
Link Medical Products Pty Ltd
接种路线:
肌内注射
人狂犬病免疫球蛋白 (HRIG) 以单次使用小瓶包装,每瓶 2 毫升或 10 毫升。
每 1.0 毫升含有:
- 150 IU 狂犬病免疫球蛋白(来自人血浆)
- 甘氨酸
- 注射用水
- 氢氧化钠(用于调节 pH 值)
人狂犬病免疫球蛋白 ( HRIG )的剂量为每公斤体重 20 国际单位 。婴儿、儿童和成人的剂量相同。
需要注射狂犬病免疫球蛋白(HRIG) 的人应在接种第一剂狂犬病疫苗(第 0 天)的同时注射。HRIG 应注射在与疫苗不同的肢体上。
如果距离首次接种狂犬疫苗已超过 7 天(168 小时),请勿注射人狂犬病免疫球蛋白(HRIG )。这是因为 HRIG 可能会干扰疫苗的免疫反应。更多详情,请参阅 “建议”部分 。
在特殊情况下,例如产品短缺时,澳大利亚可能会使用其他 HRIG 产品。
各州和领地公共卫生部门可就人源化免疫球蛋白(HRIG) 产品的使用提供建议。另请参阅公共卫生管理 。
用 HRIG 浸润伤口
必须使用尽可能多计算出的剂量,将 HRIG 浸润到所有伤口及其周围。
任何剩余的、无法安全渗入伤口及其周围的狂犬病免疫球蛋白(HRIG) 都应在远离狂犬疫苗注射部位的肌肉注射。根据注射剂量,可以选择注射到三角肌、大腿外侧或臀肌。
如果没有明显的伤口或浸润部位,例如粘膜暴露,则应全部肌注 HRIG 剂量。
如果伤口严重,计算出的 HRIG 体积不足以完全浸润所有伤口(例如幼儿被狗严重咬伤),则将 HRIG 用生理盐水稀释,以达到足够的体积,从而小心地浸润所有伤口。
手指和手部的伤口可能很小,尤其是蝙蝠造成的伤口。在这些伤口中注射人免疫球蛋白(HRIG) 可能既有技术难度,也会给受者带来疼痛。 39 然而,由于手指和手部神经分布丰富, 40-42 因此,使用 25 号或 26 号针头尽可能多地注射计算出的 HRIG 剂量至关重要。
为避免筋膜室综合征,应非常轻柔地进行指环神经阻滞麻醉。麻醉剂不应导致邻近手指组织苍白或发白。必要时,可能需要使用局部麻醉剂进行指环神经阻滞麻醉 。39
狂犬病疫苗的互换性
最好在整个疗程中使用同一品牌的疫苗。但是,如有必要,可以使用世界卫生组织认可的(也称为“预认证”)其他狂犬病细胞培养疫苗完成暴露前或暴露后预防疗程。如果某人在国外接种了鸡胚或细胞培养疫苗,建议其在澳大利亚继续使用注册的澳大利亚疫苗进行标准的暴露后预防方案。
多个国际疫苗咨询小组指出,狂犬病细胞培养疫苗可以互换使用。这可以从以下相似之处得到佐证:
- 组织培养疫苗生产方法
- 抗体反应
- 接种疫苗后的不良反应
一项研究专门评估了人二倍体细胞疫苗和纯化鸡胚细胞疫苗的互换性。165 名受试者被随机分配接受狂犬病暴露前预防 (第 0、7 和 21-28 天),分别使用人二倍体细胞疫苗或纯化鸡胚细胞疫苗。43 名受试者在暴露前预防接种 1 年后,每组均接受了 1 剂或 2 剂纯化鸡胚细胞疫苗的加强免疫。加强免疫后,所有受试者在第 7 天均产生了回忆性免疫应答(几何平均滴度达到几个数量级,即 3E0.5 IU /mL)。无论初次免疫接种使用的是哪种疫苗,均观察到了这种应答。预计其他狂犬病细胞培养衍生疫苗也会产生类似的应答。
禁忌症和注意事项
禁忌症
对于可能接触过狂犬病毒或其他丽沙病毒的人群,使用狂犬疫苗或人狂犬病免疫球蛋白进行暴露后预防并无绝对禁忌症。这是因为狂犬病几乎总是致命的。
防范措施
对鸡蛋过敏的人
有对鸡蛋或鸡蛋蛋白发生过敏性休克或严重过敏反应史的人不应接种纯化鸡胚细胞疫苗。他们应改用人二倍体细胞疫苗或纯化 Vero 细胞疫苗。
另见不良事件 。
不良事件
细胞培养疫苗通常耐受性良好。一项大型研究报告称,成人接种人二倍体细胞疫苗后出现以下不良事件: 44
- 手臂酸痛(15-25%的疫苗接种者出现这种情况)
- 头痛(5-8%)
- 不适或恶心,或两者兼有(发生率为 2%~5%)
- 过敏性水肿(0.1%)
纯化鸡胚细胞疫苗和纯化 Vero 细胞狂犬病疫苗均报告了类似的不良事件情况。 45,46
这些反应在儿童中发生率相同 。47-53
过敏性休克和过敏反应
虽然接种人二倍体细胞疫苗后发生过敏性休克的情况很少见(大约每 10,000 例接种中发生 1 例),但约有 6%的人在接种加强针后可能会出现过敏反应。这些反应通常发生在加强针接种后 2-21 天,可能包括: 44
- 全身性荨麻疹
- 关节痛
- 关节炎
- 浮肿
- 恶心
- 呕吐
- 发烧
- 不适
这些反应不会危及生命。它们被认为是由疫苗中经β-丙内酯修饰的人血清白蛋白引起的。
不良事件管理
一旦开始狂犬病暴露后预防治疗, 切勿因局部反应或轻微全身反应而延误或停止治疗。简单的镇痛药即可帮助控制这些反应。
由于狂犬病几乎总是致命的,即使接种狂犬疫苗后出现严重的过敏反应,也应继续执行推荐的疫苗接种方案,尤其是暴露后预防方案。抗组胺药可以减轻后续反应的症状。
在决定停止疫苗接种计划之前,应仔细考虑该人感染狂犬病毒或狂犬病的风险。
人狂犬病免疫球蛋白注射后的不良反应
人狂犬病免疫球蛋白具有极佳的安全性,通常不会引起即刻超敏反应。而某些在国外使用的马狂犬病免疫球蛋白则更容易引起超敏反应。
疾病的性质
狂犬病毒是弹状病毒科狂犬病毒属的一类单链 RNA 病毒。 狂犬病毒属目前已知有 12 个种,包括经典狂犬病毒和与其密切相关的狂犬病毒,例如澳大利亚蝙蝠狂犬病毒( ABLV )和欧洲蝙蝠狂犬病毒。 54
临床特征
狂犬病是一种人畜共患病,由接触感染狂犬病毒或其他狂犬病毒的动物的唾液或神经组织引起。
由经典狂犬病毒和其他丽沙病毒引起的临床疾病无法区分。“狂犬病”一词指的是由任何已知丽沙病毒种类引起的疾病。
狂犬病几乎总是致命的。
狂犬病和丽沙病毒的传播
人类可能通过以下途径接触到: 55
- 动物抓伤或咬伤导致皮肤破损
- 病毒与人体黏膜表面(例如鼻子、眼睛或嘴巴)直接接触会导致感染。
- 从死于未确诊狂犬病的捐献者身上进行组织或器官移植
以下情况人们很少会感染狂犬病:
- 动物抓伤了它们
- 动物舔舐开放性伤口
- 动物唾液接触完整的黏膜
自然环境中的气溶胶传播从未得到充分记录 。56
狂犬病毒可能通过未经巴氏消毒的牛奶传播给人类。然而,通过这种途径传播的罕见报告尚未得到证实 。57
潜伏期
狂犬病的潜伏期通常为 3-8 周,但最短可至 1 周,极少数情况下可长达数年。
狂犬病风险更高, 潜伏期更短:
- 中枢神经系统附近(例如头部和颈部)遭受严重且多处创伤后
- 在神经支配丰富的部位(例如手指)
狂犬病初期症状
狂犬病前驱期可持续长达 10 天。在此期间,患者可能会出现一些非特异性症状,例如: 40
- 厌食症
- 咳嗽
- 发烧
- 头痛
- 肌痛和疲劳
- 恶心和呕吐
- 咽喉痛
患者伤口处或附近可能出现异常感觉(感觉异常)或肌肉抽搐(肌束颤动)。他们也可能出现焦虑、烦躁和恐惧。
死于狂犬病
大多数狂犬病患者表现为狂躁型(也称脑炎型) 。41
脑炎期,神经系统受累的客观体征包括: 41
- 恐飞症
- 恐水症
- 怪异行为
- 迷失方向
- 多动症
- 流涎过多、体温过高和呼吸急促(自主神经功能紊乱的迹象)
患者的神经系统状况会在长达 12 天的时间内恶化。死亡可能是由于心脏或呼吸骤停而突然发生,也可能是在昏迷后死亡。
流行病学
狂犬病的流行病学因狂犬病毒种类和动物宿主而异。除南极洲外,所有大陆均已发现狂犬病毒。
澳大利亚各州或领地卫生部门可就潜在的狂犬病毒暴露及其处理措施提供建议。参见公共卫生管理 。
国际权威机构可以提供有关全球狂犬病发生情况的信息。
陆生动物中的经典狂犬病毒
由经典狂犬病毒引起的狂犬病主要流行于非洲、亚洲、美洲以及欧洲部分地区,感染对象为陆生哺乳动物。在这些地区,该病毒在某些哺乳动物物种中得以维持,尤其是犬类。 26
在北美和欧洲等家畜狂犬病疫苗接种较为普遍的国家,浣熊和狐狸等野生动物是重要的狂犬病病毒宿主。这些国家动物种群中狂犬病的持续存在被称为地方性狂犬病。
一个国家的狂犬病风险状况随时可能发生变化。例如,2008 年,印度尼西亚巴厘岛报告了犬类狂犬病病例,随后又报告了人类病例。 58 在此之前,巴厘岛一直被认为没有狂犬病,尽管已知印尼其他地区存在狂犬病。 59 英国公共卫生署维护着一份按国家/地区划分的陆生动物狂犬病风险清单。
澳大利亚蝙蝠狂犬病毒
在世界某些地区,蝙蝠是经典狂犬病毒以及其他狂犬病毒的重要宿主。在一些被认为没有陆生狂犬病的地区,例如澳大利亚,也发现了蝙蝠狂犬病毒。
1996 年首次在蝙蝠中发现了 ABLV (澳大利亚蝙蝠狂犬病毒)。此后,澳大利亚分别在 1996 年、1998 年和 2013 年报告了 3 例由 ABLV 引起的致命性脑炎病例 。60-62 这 3 名患者都曾被蝙蝠咬伤或抓伤。
已在所有 4 种澳大利亚果蝠(狐蝠)和几种澳大利亚食虫蝙蝠中发现了 ABLV 感染的证据。因此,应假定所有澳大利亚蝙蝠都可能感染 ABLV 。
澳大利亚陆生哺乳动物中首次确诊的 ABLV 病例发生在 2013 年昆士兰州的 2 匹马身上 。63
在狂犬病非地方性流行地区,例如澳大利亚,陆生动物感染蝙蝠狂犬病毒的情况极其罕见。目前尚无证据表明病毒会从受感染的陆生动物传播给人类。然而,理论上存在这种可能性。
全球蝙蝠体内的狂犬病毒
世界各地的蝙蝠都可能是狂犬病毒的潜在来源,并可能导致人们感染狂犬病,具体取决于人们接触蝙蝠的方式。
澳大利亚以外的蝙蝠中尚未分离出 ABLV 病毒 。
然而,其他国家的蝙蝠携带密切相关的狂犬病毒。例如,欧洲部分地区的蝙蝠可能携带欧洲蝙蝠狂犬病毒 1 型和欧洲蝙蝠狂犬病毒 2 型。至少有 4 人死于欧洲蝙蝠狂犬病毒变种。他们均无狂犬病预防性免疫接种记录。 64,65
有报道称,蝙蝠狂犬病毒感染了其他动物 66-68 (例如马匹感染了 ABLV )。
疫苗和免疫球蛋白信息
澳大利亚目前有 2 种灭活狂犬病细胞培养衍生疫苗。
狂犬疫苗用于狂犬病暴露前或暴露后预防均有效。 26,47,69 虽然关于狂犬疫苗预防其他狂犬病毒感染的有效性数据有限,但现有的动物实验数据和临床经验支持其应用。 32,34,70-74
就初始抗体反应强度而言,3 剂肌内注射( IM ) 暴露前预防方案优于 3 剂皮内注射 (ID ) 方案。 75-78 然而,研究表明,只要皮内注射剂量正确,标准皮内注射暴露前预防后的短期和长期记忆性抗体反应与肌内注射后的抗体反应相似。在加速暴露前预防方案(1、2 或 3 剂, 肌内或皮内注射)后 1 年内给予加强剂量,也可在 7-14 天内产生有效的记忆性抗体反应。 10
澳大利亚已注册并上市的两种狂犬病疫苗——Rabipur(纯化鸡胚细胞疫苗)和 Verorab(纯化 Vero 细胞狂犬病疫苗)——的免疫原性已在可能接触过狂犬病的人群和健康志愿者中进行了评估。 69,79,80 在大多数研究中,100%的受试者在第 14 天时几何平均滴度(GMT)均高于 0.5 IU /mL。在所有评估接种 4 剂狂犬病疫苗后第 30 天抗体反应的研究中,100%的受试者 GMT 均高于 0.5 IU /mL。 28,29,69,81,82
对于严重免疫功能低下的人群,狂犬病疫苗的免疫反应可能不理想。 1 轻度或中度免疫功能低下且先前已接种过狂犬病疫苗的人群,仅需接种两剂暴露后预防疫苗即可产生免疫反应。然而,免疫功能严重低下的人群可能产生较低的免疫反应。 83
大量针对肌注(IM) 和皮内注射( ID) 暴露前和暴露后预防方案的临床研究表明,在第 28 天和第 90 天, 病毒中和抗体(VNAb)滴度达到 3E0.5 IU /mL,且 VNAb 水平直至第 180 天才降至 0.5 IU /mL 以下。这些数据表明,接受狂犬病暴露前或暴露后预防方案的人员,如果在 3 个月内再次暴露于狂犬病病毒,则无需再次接种疫苗。 84
两次就诊的暴露前预防(PrEP)方案
HDCV 和 PCECV 狂犬病疫苗的研究表明,2 剂 PrEP 方案产生的免疫反应与 3 剂 PrEP 方案相当,尤其是在接种疫苗后的 7-28 天内。
三项临床试验表明,接种两剂 PrEP 方案后 7-28 天内,狂犬病 VNAb 血清转化率(96.7%-100%)与接种三剂 PrEP 方案(100%)相当,后者是衡量免疫系统对疫苗反应的指标。 69,85,86 同期观察性研究也得出了类似结果。 7,87,88
一项临床试验表明,接种两剂 PrEP 方案后 180 天,狂犬病 VNAb 血清转化率(46%)略低于接种三剂 PrEP 方案(55%)。 69
关于两剂 PrEP 与三剂 PrEP 的长期疗效,目前证据有限且尚不确定。三项临床试验表明,接种两剂 PrEP 方案后 365 天或更长时间,狂犬病 VNAb 血清转化率(7%–60%)低于三剂 PrEP 方案(35%–64%)。 69,85,86 观察性研究也显示了类似的结果。 7,88,89 两剂 PrEP 与三剂 PrEP 血清转化率差异的临床意义尚不明确。
对 PVRV 狂犬疫苗的研究表明,两剂 PrEP 方案产生的免疫反应与三剂 PrEP 方案相当,尤其是在接种后 14-28 天内。这些研究比较了 PrEP 方案中两剂或三剂 Verorab 与相同剂量 HDCV 或 PCECV 狂犬疫苗的效果,发现 Verorab 在免疫原性方面不劣于 HDCV 或 PCECV,且安全性相当。 45,46,69,87,89
疫苗的运输、储存和处理
狂犬疫苗
按照国家疫苗储存指南进行运输:力争达到 5.91 储存在 +2°C 至 +8°C。不要冷冻。
所有狂犬病疫苗都必须进行复溶 。将整瓶稀释液倒入疫苗瓶中,摇晃至粉末完全溶解。复溶后的疫苗应立即使用。
人狂犬病免疫球蛋白
按照国家疫苗储存指南进行运输:力争达到 5.91 储存于 +2°C 至 +8°C。切勿冷冻。避光保存。
打开小瓶后立即使用。
公共卫生管理
在澳大利亚,所有州和地区都将人类感染经典狂犬病毒和澳大利亚蝙蝠狂犬病毒( ABLV )列为法定报告疾病。
在澳大利亚,所有州和地区都必须上报其他不符合 ABLV 或狂犬病毒 感染病例定义的狂犬病毒病例。
澳大利亚传染病网络制定的狂犬病毒和其他丽沙病毒暴露和感染国家指南详细介绍了狂犬病和其他丽沙病毒感染(包括澳大利亚狂犬病毒) 的管理。
各州和领地公共卫生部门可就狂犬病和其他狂犬病毒感染的公共卫生管理提供进一步建议。
各州和地区公共卫生部门均提供人狂犬病免疫球蛋白和狂犬病疫苗,用于暴露后预防 。
与产品信息的差异
用于暴露前和暴露后预防
澳大利亚提供的两种疫苗的产品信息表明,它们可用于 ABLV (澳大利亚蝙蝠狂犬病毒)暴露前和暴露后预防 。
ATAGI (澳大利亚免疫技术咨询小组)建议,在有指征的情况下,任何可用的狂犬病疫苗都可以用作 ABLV 暴露前或暴露后预防 ,以及经典狂犬病毒和其他狂犬病毒暴露的预防——参见建议 。
用于暴露前预防的纯化鸡胚细胞疫苗
纯化鸡胚细胞疫苗的产品信息表明,该疫苗仅供肌肉注射 。
ATAGI 建议,皮内注射是暴露前预防中肌肉注射的可接受替代方案。
纯化鸡胚细胞疫苗的产品信息建议,对于被认为持续面临狂犬病暴露风险的人(例如兽医及其助手、野生动物工作者、猎人),通常应至少每 2 年进行一次血清学检测,如果根据感知到的风险程度适当,则应缩短检测间隔。
ATAGI 建议,对于持续存在职业风险的人群,应每 3 年接种一次加强针。参见 “建议”部分中关于“持续职业暴露于狂犬病毒的人群应接种狂犬疫苗加强针”的内容 。
用于暴露后预防的纯化鸡胚细胞疫苗
纯化鸡胚细胞疫苗的产品信息建议在暴露后 28 天常规接种第 5 剂。
ATAGI 建议免疫功能正常的人可以接受 4 剂细胞培养衍生疫苗进行暴露后预防 。
ATAGI 建议免疫功能低下的人可以在第 28 天接种第 5 剂疫苗。
ATAGI 建议,免疫功能低下且在接受第 5 剂暴露后预防治疗后狂犬病 VNAb 滴度为 0.5 IU /mL 的人群可以接受进一步的剂量。
参考
- Tantawichien T、Jaijaroensup W、Khawplod P、Sitprija V. CD4+ T 淋巴细胞计数低的人类免疫缺陷病毒患者多部位皮内暴露后狂犬病疫苗接种失败。临床传染病 2001;33:E122–4。
- Kopel E、Oren G、Sidi Y、David D.免疫功能低下患者对狂犬病疫苗的抗体反应不足。新发传染病 2012;18:1493-5。
- Gongal G, Sampath G. 皮内狂犬疫苗的引入——亚洲暴露后预防的范式转变。疫苗 2019;37 增刊 1:A94-a8。
- Endy TP、Keiser PB、Cibula D 等。抗疟疾药物对暴露后预防方案下肌肉注射狂犬疫苗免疫反应的影响。传染病杂志 2020;221:927-33。
- Garcia Garrido HM、van Put B、Terryn S 等。接受免疫抑制单药治疗的成年人中,三剂肌肉注射狂犬病暴露前预防方案的免疫原性和 1 年加强免疫力:一项前瞻性单中心临床试验。《旅行医学杂志》2023;30。
- Furuya-Kanamori L、Ramsey L、Manson M、Gilbert B、Lau CL。老年旅行者皮内狂犬病暴露前疫苗接种方案:初次接种和加强接种后免疫原性的比较。《旅行医学杂志》2020;27。
- Mills DJ、Lau CL、Fearnley EJ、Weinstein P. 改良皮内暴露前狂犬病疫苗接种方案的免疫原性 ——420 名旅行者的病例系列研究。《旅行医学杂志》2011;18:327-32。
- Xu C、Lau CL、Clark J 等。暴露前和暴露后狂犬病疫苗接种的免疫原性:系统评价和剂量反应荟萃分析。疫苗 2021;39:1044-50。
- Guo Y, Mills DJ, Lau CL, Mills C, Furuya-Kanamori L. 澳大利亚蝙蝠护理人员狂犬病暴露前预防和加强剂量后的免疫反应。人畜共患病公共卫生 2023。
- Langedijk AC、De Pijper CA、Spijker R 等。加强免疫后狂犬病抗体反应:系统评价和荟萃分析。临床传染病 2018;67:1932-47。
- De Pijper CA、Langedijk AC、Terryn S 等。初次免疫后 10-24 年单次肌肉注射狂犬病加强疫苗后的长期记忆反应。传染病杂志 2022;226:1052-6。
- Giovanetti F. 旅行儿童的免疫接种。旅行医学和传染病 2007;5:349-64。
- Gunther A、Burchard GD、Schoenfeld C.狂犬病疫苗接种与交通事故[信函]。旅行医学与传染病 2008;6:326-7。
- Neilson AA, Mayer CA.狂犬病:旅行者的预防。澳大利亚家庭医生 2010;39:641-5。
- Gautret P、Schwartz E、Shaw M 等。归国旅客中与动物相关的伤害和疾病:GeoSentinel 监测网络的回顾。疫苗 2007;25:2656-63。
- Meslin FX.狂犬病作为旅行者的风险,尤其是在高流行地区。旅行医学杂志 2005;12 增刊 1:S30-40。
- Mudur G. 外国游客对印度的狂犬病风险缺乏了解。BMJ 2005;331:255。
- Piyaphanee W、Shantavasinkul P、Phumratanaprapin W 等。东南亚外国背包客狂犬病暴露风险。美国热带医学与卫生杂志 2010;82:1168-71。
- Mills DJ、Lau CL、Weinstein P. 澳大利亚旅行者的动物咬伤和狂犬病暴露。澳大利亚医学杂志 2011;195:673-5。
- Gherardin AW、Scrimgeour DJ、Lau SC 、Phillips MA、Kass RB。使用人二倍体细胞狂犬病疫苗对先前皮内免疫的旅行者进行肌肉注射加强免疫的早期狂犬病抗体反应。《旅行医学杂志》2001;8:122-6。
- Mansfield KL、Andrews N、Goharriz H 等。狂犬病暴露前预防可在人类中产生持久免疫力。疫苗 2016;34:5959-67。
- Lim PL, Barkham TM. 新加坡潜在职业暴露人群狂犬病暴露前疫苗接种的血清学反应。国际传染病杂志 2010;14:e511-3。
- Morris J、Crowcroft NS、Fooks AR、Brookes SM、Andrews N.英国蝙蝠处理人员狂犬病抗体水平:纯化鸡胚细胞狂犬病加强免疫接种前后的免疫反应。Hum Vaccin 2007;3:165-70。
- 美国疾病控制与预防中心 (CDC)、Manning SE、Rupprecht CE 等。人类狂犬病预防——美国,2008 年:免疫实践咨询委员会的建议。MMWR。建议和报告 2008;57(RR-3):1-28。
- McElhinney LM、Marston DA、Brookes SM、Fooks AR。尸体腐烂对狂犬病毒感染性和检测的影响。病毒学方法杂志 2014;207:110-3。
- 世界卫生组织(世卫组织)。狂犬病疫苗:世卫组织立场文件——2018 年 4 月。《每周流行病学记录》2018;93:201-19。
- Jones RL、Froeschle JE 、Atmar RL 等。经色谱纯化的 Vero 细胞狂犬病疫苗在成人中的免疫原性、安全性和批次一致性:一项与人二倍体细胞狂犬病疫苗进行的随机、双盲试验。Vaccine 2001;19:4635-43。
- 王超,张晓,宋强,唐凯。中国生产的纯化 Vero 细胞狂犬疫苗有望成为发展中国家暴露后预防狂犬病的有效疫苗。临床与疫苗免疫学 2010;17:688-90。
- 王晓军,郎军,陶晓荣等。纯化 Vero 细胞狂犬疫苗在中国重度狂犬病暴露患者中的免疫原性和安全性。东南亚热带医学与公共卫生杂志 2000;31:287-94。
- Wilde H. 暴露后狂犬病预防失败。疫苗 2007;25:7605-9。
- Bose A、Munshi R、Tripathy RM 等。一项随机非劣效性临床研究,旨在评估通过肌肉注射和皮内注射途径给药的新型纯化 Vero 细胞狂犬病疫苗 (Rabivax-S) 的暴露后预防效果 。Vaccine 2016;34:4820-6。
- Brookes SM、Parsons G、Johnson N、McElhinney LM、Fooks AR。狂犬病人二倍体细胞疫苗可诱导针对欧洲和澳大利亚蝙蝠狂犬病毒的交叉中和和交叉保护性免疫反应。疫苗 2005;23:4101-9。
- Lang J、Simanjuntak GH、Soerjosembodo S、Koesharyono C. 人类或马狂犬病免疫球蛋白对 2 1 1 方案下暴露后狂犬病疫苗免疫原性的抑制作用:印度尼西亚的一项现场试验。世界卫生组织公报 1998;76:491-5。
- Nel LH. 狂犬病以外的狂犬病毒疫苗。疫苗专家评论 2005;4:533-40。
- Sampath G、Madhusudana SN、Sudarshan MK 等。Indirab 的免疫原性和安全性研究:一种基于 Vero 细胞的色谱纯化人狂犬病疫苗。疫苗 2010;28:4086-90。
- Vodopija I、Sureau P、Smerdel S 等。狂犬病疫苗与人狂犬病免疫球蛋白的相互作用以及 2 1 1 程序在暴露后治疗中的可靠性。疫苗 1988;6:283-6。
- Chutivongse S、Wilde H、Benjavongkulchai M、Chomchey P、Punthawong S. 妊娠期暴露后狂犬病疫苗接种:对 202 名妇女及其婴儿的影响。临床传染病 1995;20:818-20。
- Sudarshan MK、Giri MS、Mahendra BJ 等。评估妊娠期暴露后狂犬病免疫的安全性。人类疫苗 2007;3:87-9。
- Suwansrinon K、Jaijaroensup W、Wilde H、Sitprija V. 用狂犬病免疫球蛋白注射手指是否危险?美国热带医学与卫生杂志 2006;75:363-4。
- Nel LH,Markotter W. 狂犬病毒。微生物学评论 2007;33:301-24。
- Jackson AC. 狂犬病最新进展。热带医学研究与报告 2011;2:31-43。
- Rupprecht CE、Hanlon CA、Hemachudha T. 狂犬病重新检查。 《柳叶刀传染病》2002 年;2:327-43。
- Briggs DJ、Dreesen DW、Nicolay U 等。纯化鸡胚细胞培养狂犬病疫苗:与人二倍体细胞培养狂犬病疫苗的互换性以及对先前已免疫者进行一剂与两剂暴露后加强免疫方案的比较。Vaccine 2000;19:1055-60。
- Rupprecht CE、Nagarajan T、Ertl H. 狂犬病疫苗。见:Plotkin SA、Orenstein WA、Offit PA、Edwards KM,编辑。普洛特金的疫苗。第 7 版。宾夕法尼亚州费城:爱思唯尔; 2018.
- Shanbag P、Shah N、Kulkarni M 等。保护印度学龄儿童免受狂犬病侵害:使用纯化鸡胚细胞疫苗 ( PCECV ) 或纯化 Vero 细胞狂犬病疫苗 (PVRV) 进行暴露前免疫接种。Hum Vaccin 2008;4:365-9。
- Ajjan N, Pilet C. 人二倍体细胞培养的狂犬病疫苗 (HDCV) 与 Vero 细胞培养的新疫苗在暴露前使用的安全性和保护价值的比较研究。疫苗 1989;7:125-8。
- Dobardzic A、Izurieta H、Woo EJ 等。纯化鸡胚细胞狂犬病疫苗的安全性评价:来自疫苗不良事件报告系统 (VAERS) 1997-2005 年的数据。疫苗 2007;25:4244-51。
- Madhusudana SN、Sanjay TV、Mahendra BJ 等。采用泰国红十字会皮内注射方案,以 0.1 mL 的剂量比较纯化鸡胚细胞狂犬病疫苗 (PCEV) 和纯化 Vero 细胞狂犬病疫苗 (PVRV) 的安全性和免疫原性 。Human Vaccines 2006;2:200-4。
- Mattner F、Bitz F、Goedecke M 等。290 名接触狂犬病感染器官捐献者或移植受者的医护人员的狂犬病暴露前和暴露后预防的不良反应。感染 2007;35:219-24。
- Mattner F、Henke-Gendo C、Martens A 等。接触狂犬病毒感染的肺移植受者的医护人员和其他患者接触者感染狂犬病的风险以及暴露后预防的不良反应。感染控制与医院流行病学 2007;28:513-8。
- Pengsaa K、Limkittikul K、Sabchareon A 等。一项为期三年的临床研究,评估纯化鸡胚细胞狂犬病疫苗(肌内或皮内注射)与日本脑炎疫苗同时接种于 12 至 18 个月大的泰国儿童的免疫原性、安全性和加强免疫反应。儿科传染病杂志 2009;28:335-7。
- Ruef C. 狂犬病疫苗的安全性[社论].感染 2007;35:211.
- Sabella O. 狂犬病疫苗的副作用和风险[信函]。加拿大全科医生 2009;55:470。
- Calisher CH, Ellison JA. 其他狂犬病毒:蝙蝠和其他脊椎动物狂犬病毒的出现及其重要性。旅行医学与传染病 2012;10:69-79。
- Waggoner JJ、Soda EA、Deresinski S. 移植受者中罕见和新出现的病毒感染。临床传染病 2013;57:1182-8。
- Gibbons RV、Holman RC、Mosberg SR、Rupprecht CE。美国洞穴探险者对蝙蝠狂犬病和人类暴露的认知。新发传染病 2002;8:532-4。
- 美国疾病控制与预防中心(CDC)。1996-1998 年马萨诸塞州饮用未经巴氏消毒的狂犬病奶牛牛奶的人群的大规模治疗。[勘误见《发病率和死亡率周报》1999;48:274]。《发病率和死亡率周报》1999;48:228-9。
- Gautret P、Lim PL、Shaw M、Leder K. 2008 年 11 月至 2010 年 3 月期间从印度尼西亚巴厘岛返回的旅行者狂犬病暴露后预防。 临床微生物学和感染 2011;17:445-7。
- Windiyaningsih C、Wilde H、Meslin FX、Suroso T、Widarso HS。印度尼西亚弗洛雷斯岛的狂犬病疫情 (1998-2003 年)。泰国医学会杂志 2004;87:1389-93。
- Hanna JN、Carney IK、Smith GA 等。澳大利亚蝙蝠狂犬病毒感染 :第二例人类病例, 潜伏期较长。澳大利亚医学杂志 2000;172:597-9。
- Francis JR、Nourse C、Vaska VL 等。澳大利亚蝙蝠狂犬病毒感染儿童:首例报告病例。儿科学 2014;133:e1063-7。
- Allworth A、Murray K、Morgan J.最近在果蝠中发现的狂犬病毒引起的人类脑炎病例。传染病情报 1996;20:504。
- Annand EJ,Reid PA。澳大利亚蝙蝠狂犬病毒食虫蝙蝠株感染两例致命马病例的临床回顾。澳大利亚兽医杂志 2014;92:324-32。
- 沃雷尔 MJ,沃雷尔 DA。狂犬病和其他狂犬病病毒性疾病。 《柳叶刀》2004 年;363:959-69。
- Fooks AR、McElhinney LM、Pounder DJ 等。病例报告:从一例致命的人类狂犬病脑炎病例中分离出欧洲蝙蝠狂犬病毒 2a 型。医学病毒学杂志 2003;71:281-9。
- Müller T、Cox J、Peter W 等。欧洲蝙蝠狂犬病毒 1 型溢出到德国的一只石貂 (Martes foina) 中。兽医学杂志 B,传染病和兽医公共卫生 2004;51:49-54。
- Tjørnehøj K、Fooks AR、Agerholm JS、Rønsholt L. 丹麦蝙蝠来源的欧洲蝙蝠狂犬病毒 1 型对绵羊的自然和实验感染 。比较病理学杂志 2006;134:190-201。
- Dacheux L、Larrous F、Mailles A 等人。欧洲蝙蝠狂犬病病毒在欧洲猫之间传播。新发传染病 2009 年;15:280-4。
- Quiambao BP、Lim JG、Bosch Castells V 等。采用人二倍体细胞疫苗或 Vero 细胞狂犬病疫苗进行为期一周的肌内或皮内暴露前预防 ,随后在一年后进行模拟暴露后预防 :一项评估免疫原性和安全性的 III 期开放标签随机对照试验。Vaccine 2022;40:5347-55。
- Young MK,McCall BJ。昆士兰州东南部地区接触澳大利亚蝙蝠狂犬病毒的潜在风险:12 年来发生了哪些变化?传染病情报 2010;34:334-8。
- Brookes SM、Healy DM、Fooks AR。狂犬病疫苗株诱导交叉中和抗体的能力。生物制品进展 2006;125:185-93。
- Hanlon CA、Kuzmin IV 、Blanton JD 等。狂犬病生物制剂对来自欧亚大陆的新型狂犬病毒的疗效。病毒研究 2005;111:44-54。
- Harkess G, Fooks AR. 狂犬病毒:特别强调狂犬病毒和狂犬病毒属的其他成员。分子生物学方法 2011;665:279-307。
- Horton DL、McElhinney LM、Marston DA 等。狂犬病毒抗原关系的量化。病毒学杂志 2010;84:11841-8。
- Bernard KW、Fishbein DB、Miller KD 等。用人二倍体细胞疫苗进行暴露前狂犬病免疫:发展中国家免疫者的抗体反应降低。美国热带医学与卫生杂志 1985;34:633-47。
- Dreesen DW、Fishbein DB、Kemp DT 、Brown J. 纯化鸡胚细胞狂犬病疫苗用于暴露前免疫的免疫原性和不良反应的两年比较试验。疫苗 1989;7:397-400。
- Lemon S、Pang L、Miller R、Prier R、Bernard K. 皮内和肌肉注射人二倍体细胞狂犬病疫苗未能达到预期的抗体反应。柳叶刀 1984;323:1098–100。
- Nicholson KG、Farrow PR、Bijok U、Barth R. 纯化鸡胚细胞培养狂犬病疫苗和人二倍体细胞疫苗的暴露前研究:人体血清学和临床反应。疫苗 1987;5:208-10。
- Ambrozaitis A、Laiškonis A、Balčiuniene L、Banzhoff A、Malerczyk C. 采用纯化鸡胚细胞疫苗 ( PCECV ) 和纯化 Vero 细胞狂犬病疫苗 (PVRV) 进行狂犬病暴露后预防性四点皮内注射方案 (4-0-2-0-1-1):一种具有免疫原性、经济有效且实用的方案。Vaccine 2006;24:4116-21。
- Shantavasinkul P、Tantawichien T、Wilde H 等。暴露后狂犬病预防在 1 周内完成:初步研究。临床传染病 2010;50:56-60。
- Aoki FY、Rubin ME、Fast MV。 暴露后预防后,儿童与成人血清中狂犬病中和抗体的比较。Biologicals 1992;20:283-7。
- Hasbahceci M、Kiyan M、Eyol E、Ewalt LC、Lodmell DL。人二倍体细胞狂犬病疫苗:四剂的疗效 [信函]。柳叶刀 1996;347:976-7。
- Sibunruang S、Jaijaroensup W、Khawplod P 等。既往接受过狂犬病初次免疫的 HIV 感染患者加强免疫接种后的免疫反应。临床微生物学和感染会议:第 22 届欧洲临床微生物学和传染病大会;伦敦。2012 年。
- Sudarshan MK、Ravish HH、Narayana DH。既往接种过狂犬疫苗的受试者再次接触狂犬病后加强免疫接种的时间间隔。亚洲生物医学 2011;5:589-93。
- Endy TP、Keiser PB、Wang D 等。已获许可的狂犬病疫苗用于暴露前预防的 2 剂与 3 剂以及皮内注射与肌肉注射的血清学反应。传染病杂志 2020;221:1494-8。
- Kamoltham T、Thinyounyong W、Phongchamnaphai P 等。皮内注射纯化鸡胚细胞狂犬病疫苗进行暴露前狂犬病疫苗接种具有免疫原性和安全性。儿科学杂志 2007;151:173-7。
- Strady A、Lang J、Lienard M 等。细胞培养狂犬疫苗暴露前方案后抗体的持久性:10 年随访及新的加强免疫策略建议。传染病杂志 1998;177:1290-5。
- Lau CL,Hohl N. 使用纯化鸡胚细胞疫苗改良皮内暴露前狂犬病疫苗接种方案的免疫原性:一项观察性研究。旅行医学与传染病 2013;11:427-30。
- Kitala PM、Lindqvist KJ、Koimett E 等。采用两种不同的抗体滴定方法比较人类对纯化 Vero 细胞和人二倍体细胞狂犬病疫苗的免疫反应。临床微生物学杂志 1990;28:1847-50。
- 澳大利亚政府卫生与老年护理部。《国家疫苗储存指南:力争达到 5 级》。第 3 版。堪培拉:澳大利亚政府卫生与老年护理部;2019 年。https://www.health.gov.au/resources/publications/national-vaccine-stora…
页面历史记录
最后更新时间
18 December 2025
上次审核
18 December 2025
显示所有页面更新(7)
18 December 2025
由于发现了假冒的阿拜拉布狂犬病疫苗,因此更新了国际认可的有效疫苗表 ,删除了在印度接种的阿拜拉布狂犬病疫苗剂量。
2 May 2025
修改免疫功能低下程度的定义,使其与免疫功能低下人群疫苗接种章节中更新的定义保持一致。
9 October 2024
最新消息:
- 本章通篇提供有关狂犬病免疫球蛋白与狂犬病疫苗联合用药的相关信息。
- 移除已停产的梅里埃疫苗
- 移除 Verorab 的乳胶警告,以反映澳大利亚配方不含乳胶。
- 将 RABIVAX-S 纳入世界卫生组织预认证的狂犬病疫苗名单,供全球使用。
19 July 2024
对两次就诊给药方案的信息进行了编辑更新,以提高信息的清晰度。
13 December 2023
临床指南中关于暴露前预防方案进行了修改,新增了两剂接种方案。本章内容也进行了更新,以反映 Verorab 疫苗的上市情况。
27 September 2021
建议已更新,允许皮内接种疫苗和加快狂犬病暴露前预防的接种程序。
对于从事特定高风险职业且持续面临暴露风险的人员,建议更新为在完成第一个暴露前预防疗程 1 年后进行加强剂量,之后每 3 年进行一次加强剂量。
对于暴露后预防,建议已更新,明确规定了疫苗剂量数量以及轻度免疫功能低下者和重度免疫功能低下者是否需要人狂犬病免疫球蛋白。
6 June 2018
关于在可能接触狂犬病毒的高风险情况下延迟使用人狂犬病免疫球蛋白(HRIG)的建议已更新。对于头部和颈部的咬伤,应尽快进行暴露后预防,最迟不得晚于暴露后 48 小时,即使动物已被送去检测。
相关疫苗
Hits: 104
- 如何使用 澳大利亚免疫手册
- 白喉-澳大利亚免疫手册
- 免疫接种基础知识
- 准备接种疫苗
- 补种疫苗
- 免疫功能低下人群的疫苗接种
- 疫苗接种
- 接种疫苗后
- 早产儿疫苗接种
- 备孕、孕期或哺乳期女性的疫苗接种
- 麻醉或手术前后接种疫苗
- 为有职业风险的人群接种疫苗
- 国际旅行者的疫苗接种
- 近期接受过正常人免疫球蛋白和其他血液制品的人群接种疫苗
- 澳大利亚为移民、难民和寻求庇护者接种疫苗
- 为出血性疾病患者接种疫苗
- 霍乱-澳大利亚免疫手册
- 新冠肺炎
- b 型流感嗜血杆菌(Hib)
- 乙型肝炎
- 人乳头瘤病毒(HPV)
- 流感(流行性感冒)
- 日本脑炎
- 麻疹
- 脑膜炎球菌病
- 猴痘(以前称为monkeypox)
- 腮腺炎
- 百日咳
- 肺炎球菌病
- 脊髓灰质炎
- Q 热
- 狂犬病和其他狂犬病毒
- 呼吸道合胞病毒(RSV)
- 轮状病毒
- 风疹
- 破伤风
- 结核

 显示图片描述
显示图片描述
孟博好,鞋子踩到死亡动物尸体,如果是狂犬病动物,鞋子上的狂犬病毒多久失去传染性?伤口碰到鞋子上的尸体碎片需要打狂犬疫苗吗?
1.1天内大概率就无感染性
2.你也恐狂
咨询一下:
1.去年6月份、10月份各打过加强针2针,如果隔着三到多层裤子被狗咬、抓腿部会有感染的可能吗?
2.隔着裤子被狗的头侧部或者头前面嘴巴位置撞击到了人的腿部有感染的可能吗?
我当时走路一个不经意,猛的撞击到了一只栓绳小狗。是小腿,当时还挺疼的,就是没有看到伤口,摸着酒精擦拭也不刺痛。
3.出现头疼、喉咙疼、肩膀酸痛、腿酸胀感、肚子胀、吃东西就想排便、中性粒细胞高、白细胞高这些症状与狂症状有关吗?
4.我需要打加强针吗?
5.2月14号事情发生以后到3月19号才打加强针,算不算打晚了。
6.近期出现被撞位置刺痛感或者其他异常痒这些是不是真的与狂有关呢?
7.加强针可以保护非出血的咬伤抓伤对吗?
基于你说的情况,你现在安全
咨询一下:
1.去年6月份、10月份各打过加强针2针,如果隔着三到多层裤子被狗咬、抓腿部会有感染的可能吗?
2.隔着裤子被狗的头侧部或者头前面嘴巴位置撞击到了人的腿部有感染的可能吗?
我当时走路一个不经意,猛的撞击到了一只栓绳小狗。是小腿,当时还挺疼的,就是没有看到伤口,摸着酒精擦拭也不刺痛。
3.出现头疼、喉咙疼、肩膀酸痛、腿酸胀感、肚子胀、吃东西就想排便、中性粒细胞高、白细胞高这些症状与狂症状有关吗?
4.我需要打加强针吗?
5.2月14号事情发生以后到3月19号才打加强针,算不算打晚了。
6.近期出现被撞位置刺痛感或者其他异常痒这些是不是真的与狂有关呢?
现在安全
孟博士您好,首先祝您工作顺利,万事如意,我想咨询您一下,我2023年接种过全程狂犬疫苗,2024年打过两针加强针,2025年4月17打一针加强针,2025年9月2号打一针加强针。昨天晚上放狗子后洗澡发现小腿有道线状的伤口破皮了,不知道是不是狗抓的,回想没有被抓的感觉裤子也没破,狗子常年拴在家里晚上放出在院子活动,像我这种情况还要打加强针吗?平时比较焦虑恐狂咨询严教授他可能忙没得到回来了,希望孟博士百忙之中回来了一下,不胜感激
1.如果我是你,我不打
2.已经打了这么多,还有保护