Contents
- 1 Prevention of Varicella Recommendations of the Advisory Committee on Immunization Practices (ACIP)
- 1.1 摘要
- 1.2 介绍
- 1.3 方法
- 1.4 水痘流行病学
- 1.5 产前和围产期接触
- 1.6 带状疱疹监测
- 1.7 阿昔洛韦用于治疗和预防水痘的用途
- 1.8 预防水痘的疫苗
- 1.9 疫苗接种的免疫反应
- 1.10 疫苗功效和疫苗效力
- 1.11 突破性疾病
- 1.12 豁免权的证据
- 1.13 疫苗同时接种
- 1.14 疫苗接种的经济学分析
- 1.15 水痘疫苗的储存、处理和运输
- 1.16 接种疫苗后的不良事件
- 1.17 疫苗病毒的传播
- 1.18 水痘疫苗接种的基本原理概述
- 1.19 水痘疫苗的使用建议
- 1.20 疫苗接种的特殊注意事项
- 1.21 保健人员
- 1.22 为控制疫情接种疫苗
- 1.23 禁忌症
- 1.24 预防措施
- 1.25 暴露后预防
- 1.26 健康的人
- 1.27 附录
- 1.28 水痘疫苗接种建议摘要
- 1.29 爆发控制
- 1.30 进入儿童保育、学校、大学和其他中学后教育机构的要求
- 1.31 水痘免疫的证据
Prevention of Varicella Recommendations of the Advisory Committee on Immunization Practices (ACIP)
医学博士Mona Marin,医学博士Dalya Güris, 斯科特·施密德博士, 简·苏厄德,MBBS
美国疾病预防控制中心国家免疫和呼吸系统疾病中心病毒疾病部
本报告中的材料来源于国家免疫和呼吸系统疾病中心,Anne Schuchat,医学博士,主任;和病毒性疾病部主任Larry Anderson医学博士。
摘要
在美国有两种含水痘带状疱疹病毒的减毒活疫苗可用于预防水痘:1)单抗原水痘疫苗(VARIVAX®,Merck & Co .,Inc .,Whitehouse Station,New Jersey),其于1995年在美国获得许可,用于年龄为>12个月、青少年和成人;和2)麻疹、腮腺炎、风疹和水痘联合疫苗(ProQuad®,Merck & Co .,Inc .,Whitehouse Station,New Jersey),其于2005年在美国获得许可,用于12个月- 12岁的健康儿童。免疫实践咨询委员会(ACIP)于1995年发布的水痘预防建议(CDC。水痘的预防:免疫实践咨询委员会的建议[ACIP]。MMWR 1996年;45[编号RR-11])包括对12 – 18个月的儿童进行常规接种,对19个月- 12岁的易感儿童进行补充接种,对与严重并发症高危人群有密切接触的易感人群(如卫生保健人员和免疫功能低下者的家庭接触者)进行接种。建议12个月至12岁的儿童接种一剂疫苗,年龄在4 – 8周的人接种两剂疫苗>13年。1999年,ACIP更新了建议(疾病预防控制中心。水痘的预防:免疫实践咨询委员会的最新建议[ACIP]。MMWR 1999年;48[第RR-6号]),包括确定儿童保育和入学要求、接触后疫苗的使用和疫情控制、某些感染人类免疫缺陷病毒的儿童使用疫苗,以及接触或传播风险高的青少年和成人接种疫苗。
2005年6月和2006年6月,ACIP通过了关于使用减毒水痘活疫苗预防水痘的新建议。本报告修订、更新并取代了1996年和1999年预防水痘的ACIP声明。新的建议包括1)对儿童实施常规的2剂水痘疫苗接种计划,第一剂在12 – 15个月大时接种,第二剂在4 – 6岁时接种;2)为先前已接种1剂疫苗的儿童、青少年和成人接种第2剂水痘疫苗;3)对所有年龄>13岁无豁免证据健康的人进行常规疫苗接种;4)产前评估和产后接种疫苗;5)将水痘疫苗的使用范围扩大到年龄特异性CD4+T淋巴细胞百分比为15% – 24%的艾滋病毒感染儿童以及CD4+T淋巴细胞计数为10%的青少年和>200个细胞/µl的成人;以及6)建立初中、高中和大学入学疫苗接种要求。ACIP也批准了水痘免疫证据的标准。
介绍
水痘是由水痘带状疱疹病毒(VZV)引起的高度传染性疾病。对于易感的家庭接触者,这种病毒的二次发作率可能达到90%。VZV病毒会引起全身性感染,通常会导致终生免疫。在其他方面健康的人,再次暴露后的临床疾病是罕见的。
在1995年,预防水痘的疫苗(VARIVAX®,Merck & Co .,Inc .,Whitehouse Station,New Jersey)已在美国获得许可,可用于年龄在>12个月、青少年和成人;免疫实践咨询委员会(ACIP)关于水痘疫苗使用的建议以前已经发表过(1,2)本报告修订、更新并取代了早期的ACIP声明(表1)。
方法
为了应对在高度接种疫苗的人群中水痘爆发的增加的报告(3–6),ACIP的麻疹-腮腺炎-风疹和水痘(MMRV)工作组于2004年2月首次召开会议,回顾自1995年实施疫苗接种计划以来美国水痘疫苗使用的相关数据,并考虑改善水痘疾病控制的推荐方案。该工作组每月召开电话会议,一年见面三次。工作组审查了关于1剂水痘疫苗接种计划影响的数据,包括疫苗接种覆盖率、水痘流行病学变化、水痘疫苗接种者的传播、疫苗有效性、疫苗接种的免疫反应、免疫证据和疫苗失败的潜在风险因素。与保护性、安全性、免疫原性和有效性相关的已发表和未发表的数据†新的四价MMRV疫苗的免疫原性和第二剂水痘疫苗的效力也进行了审查。考虑了成本效益和成本效益分析,包括儿童1剂和2剂疫苗接种方案与无疫苗接种方案相比的修订成本效益分析,以及第二剂疫苗的增量效益。在2004年10月、2005年2月、2005年6月和2006年6月的ACIP全体会议上做了发言。MMRV工作组制定并讨论了建议选项。当缺乏明确的研究证据时,建议会纳入工作组成员的专家意见。工作组向合作组织(即美国儿科学会[AAP]、美国家庭医师学会[AAFP]、美国妇产科医师学会、州和地区流行病学家委员会以及免疫管理者协会)以及各州公共卫生专业人员和免疫计划主管寻求意见。2005年6月和2006年6月向整个ACIP提交了建议和声明草案。经过审议,ACIP会议的最终建议于2005年和2006年获得批准。在CDC和外部审查流程之后,对声明草案进行了修改,以更新和澄清文件中的措辞。
水痘流行病学
一般
VZV病毒通过直接接触、吸入急性水痘或带状疱疹皮肤损伤的水疱液中的气溶胶或也可能雾化的受感染呼吸道分泌物而在人与人之间传播。病毒通过上呼吸道或结膜进入宿主。
水痘的平均潜伏期为14 – 16天§接触后出现皮疹;然而,这一时期可以变化(范围:10 – 21天)。受感染者的传染性期估计开始于皮疹发作前1 – 2天,结束于所有损害结痂时,通常在皮疹发作后4 – 7天(7)。患有进行性水痘(即出现新病变超过7天)的人可能会传染更长时间,这可能是因为他们的免疫反应受到抑制,这使得病毒复制持续存在。VZV在感觉神经神经节中保持休眠状态,并可能在稍后的时间被重新激活,导致带状疱疹(HZ)(即带状疱疹),这是一种典型地出现在一个或两个感觉神经根的皮肤分布中的疼痛性水疱性皮疹。
自从1995年实施普遍的儿童水痘疫苗接种计划以来,美国水痘的流行病学和临床特征发生了变化,水痘的发病率和死亡率显著下降。没有关于HZ流行病学的一致变化的记录。
接种疫苗的人可能发展为具有非典型表现的改良水痘疾病。接种疫苗后> 42天出现的水痘疾病(即突破性水痘)通常是轻度的,具有< 50个皮肤损伤,低热或无热,并且病程较短(4 – 6天)。皮疹更可能主要是斑丘疹而不是水疱。然而,突破水痘是传染性的。
前疫苗时代
在1995年引入水痘疫苗之前,水痘在美国是一种普遍的儿童疾病,发病高峰在春季,平均年发病率为每1000人中15 – 16例。根据1980 – 1990年全国健康访问调查(NHIS)的数据,估计每年平均发生400万例(年发病率:每1,000人口15例) (8)。1995年引入疫苗时,水痘并不是全国性的法定传染病,监测数据也很有限。1994年,只有28个州、哥伦比亚特区和纽约市向CDC的国家法定疾病监测系统报告了病例;报告是被动的,估计的完整性从< 0.1%到20%(9)。
在多项研究中,年龄特异性发病率数据来自NHIS以及州和地方调查(8,10,11)。在1980 – 1990年期间,估计33%的病例发生在学龄前儿童(即12个月- 4岁的儿童)中,44%发生在学龄儿童(即5 – 9岁的儿童)中(年发病率分别为每1000名儿童82.8例和91.1例)。大约90% – 92%的病例发生在15岁以下的人群中,病例很少发生在15岁以下的人群中>50年了。然而,使用1990 – 1992年期间和1994 – 1995年期间进行的州和地方调查数据的研究表明,水痘的最高发病率发生在学龄前儿童中,而不是学龄儿童中,这表明该疾病在较早的年龄(10,11)。1988 – 1994年的全国血清阳性率数据表明,95.5%的20 – 29岁成年人、98.9%的30 – 39岁成年人和> 99.6%的20-29岁成年人>40年对VZV免疫(12)。然而,由于不太清楚的原因,在温带和热带气候的国家之间水痘的流行病学不同(13–18)。在大多数温带气候国家,超过90%的人在青春期感染,而在热带气候国家,更高比例的感染是在老年获得的,这导致成人中更高的易感性(19)。
水痘住院治疗负担的估计因研究年份、数据来源和水痘相关住院治疗的定义而异(20 – 23)。如果水痘被列为住院的主要原因或次要原因,估计值会更高,在这种情况下,可能会包括一些偶然的水痘住院。在1988 – 1995年期间,在美国估计每年有10,632例住院治疗可归因于水痘(范围:8,198 – 16,586)(20)。另一项研究表明,1993 – 1995年期间,年平均住院人数为15,073人,但这一时期可能包括了一个流行病年(22)。1988 – 1995年期间水痘住院总比率为每100,000人中2.3至6.0例。如果包含任何水痘相关的出院诊断代码,发病率在每100,000人中5.0至7.0例之间(20–23)。
在1988 – 1995年期间,没有严重免疫损害状况或治疗的人占每年水痘相关住院治疗的最大比例(89%)20)。接种疫苗前,儿童年龄<4岁以下的人占住院人数的43% – 44%>20年占32% – 33%(20,22)。年龄较大的人水痘并发症的发生率明显较高>20岁及婴儿(即小于1岁的儿童)。成年人年龄>20岁以下儿童患水痘住院的可能性是5 – 9岁儿童的13倍,1岁以下婴儿住院的可能性是5 – 9岁儿童的6倍(20)。导致住院的水痘最常见的并发症是皮肤和软组织感染(尤其是侵袭性A组链球菌感染)、肺炎、脱水和脑炎。1980年,确定了Reye综合征和在水痘或流感样疾病期间使用阿司匹林之间的关联;从那以后,曾经被认为是由水痘感染引起的常见并发症的Reye综合征变得罕见(24–26)。
在1970 – 1994年期间,以水痘为主要原因的年均死亡人数为105人;水痘的总体平均年死亡率为每100万人口0.4例死亡。在此期间,水痘死亡的年龄分布发生了变化。在1970 – 1974年期间,年龄< 20岁的人占水痘死亡的80%,而在1990 – 1994年期间为46%。在1970 – 1994年期间,所有年龄组水痘的平均病死率(CFR)在每100,000例中为2.0-3.6例,其中婴儿和>20岁的成人的病死率较高(27)。尽管CFR在此期间大幅下降,但1990 – 1994年期间成人水痘相关死亡风险仍比12个月- 4岁儿童高25倍(CFR:分别为每10万例21.3和0.8)。在同一时期,89%的儿童水痘死亡病例和75%的成人水痘死亡病例发生在没有严重潜在免疫缺陷疾病的人群中。死于水痘的人中最常见的并发症是肺炎、中枢神经系统并发症(包括脑炎)、继发感染和出血性疾病。最近对水痘死亡的重新分析也认为水痘是除了先前报告中研究的潜在原因之外的一个死亡原因(28)。在1990 – 1994年期间,水痘诊断被列入每年平均145份死亡证明(105份为潜在原因,40份为促成原因),每年水痘总死亡率为每100万人口0.6例死亡。
妊娠期水痘可能对胎儿和婴儿产生不良后果,包括先天性水痘综合征(见产前和围产期暴露)。没有关于先天性水痘综合征病例数量的可靠数据。然而,根据年龄特异性水痘发病率(来自NHIS)、每年出生人数和先天性水痘综合征的风险(妊娠前20周的总风险为1.1%),在疫苗接种前的时代,估计美国每年发生44例先天性水痘综合征(29)。
后疫苗时代
在1995年,水痘疫苗(VARIVAX®,Merck & Co .,Inc .,Whitehouse Station,New Jersey)已在美国获得许可,可用于年龄在>12个月,青少年和成人。当时,ACIP建议对12 – 18个月的儿童进行常规水痘疫苗接种,对19个月- 12岁的易感儿童进行补充疫苗接种,并对与严重并发症高危人群有密切接触的易感人群(如卫生保健工作者和免疫缺陷者的家庭接触者)进行疫苗接种(1; 表1)。1999年,ACIP更新了这些建议,纳入了儿童保育和入学要求、暴露后疫苗的使用和疫情控制、某些感染人类免疫缺陷病毒(HIV)的儿童使用疫苗,以及处于暴露或传播高风险的青少年和成人的疫苗接种(2; 表1)。
在1997 – 2005年期间,19 – 35个月儿童的全国水痘疫苗接种覆盖率从27%增加到88%,在种族或族裔覆盖率方面没有统计学显著差异(30)。2005年,各州水痘疫苗接种覆盖率从69%到96%不等(31)。国家监测数据仍然有限,但某些州的被动监测数据记录了水痘发病率的下降。
在四个州(伊利诺伊州、密歇根州、德克萨斯州和西弗吉尼亚州)有足够的(1990 – 1994年期间预期病例的>5%)向国家营养和社会服务部报告,与1990 – 1994年的平均发病率相比,2004年水痘发病率下降了53% – 88%,19 – 35个月儿童的疫苗接种覆盖率从82%到88%(32;疾病防治中心,未公布的数据,2006年)。在2003 – 2005年期间,伊利诺伊州和德克萨斯州的病例数有所增加;最大的增长(56%)发生在德克萨斯州(图1)。密歇根州的病例数保持稳定(图1)在西弗吉尼亚州下降幅度最小。
1995年,随着国家疫苗接种计划的实施,CDC在三个社区(加州羚羊谷;德克萨斯州特拉维斯县;和宾夕法尼亚州西费城)与州和地方卫生部门合作建立基线数据,并在引入水痘疫苗后监测水痘疾病的趋势。到2000年,这三个社区19 – 35个月儿童的疫苗接种覆盖率达到74% – 84%,报告的水痘病例总数下降了71% – 84%(33)。尽管12个月至4岁儿童的发病率下降幅度最大(83% – 90%),但所有年龄组的发病率均下降,包括婴儿和成人,这表明了疫苗接种计划的群体免疫效应。自2001年以来,只有两个地点获得了继续监测的资金(羚羊谷和西费城)。到2005年,这两个地点的疫苗接种覆盖率已提高到90%,发病率的下降分别达到90%和91%(34)。1996 – 2005年期间,随着疫苗接种覆盖面的不断扩大,接种过水痘疫苗的人的比例从2%增加到56%。在1995 – 2004年期间,积极监测点水痘病例的发病率高峰从3 – 6岁转移到9 – 11岁。
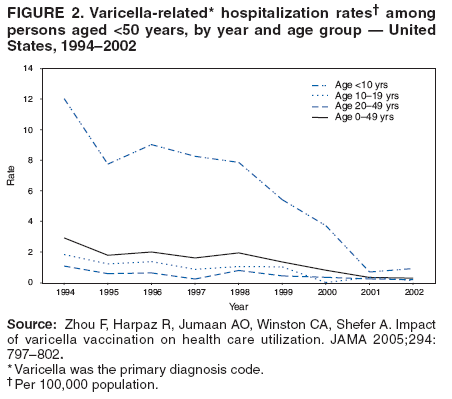
在1995年引入疫苗后,每年水痘相关的住院人数和比率下降。在1993 – 2001年进行的一项全国代表性样本研究中,水痘住院率下降了75%(22)。在另一项研究中,1994 – 2002年期间,水痘相关的年度住院率下降了88%23) (图2)。婴儿的住院率下降了100%,所有其他年龄组(50岁以下)的住院率也大幅下降;10岁以下儿童的住院率下降了91%,10 – 19岁儿童和青少年的住院率下降了92%,20 – 49岁成人的住院率下降了78%。儿童住院率的大幅下降导致成人水痘相关住院率的上升(2002年40%的住院率发生在老年人中>20年) (23)。在综合积极监测区,水痘相关住院率从1995 – 1998年期间的每10万人中2.4 – 4.2人下降到2000年的每10万人中1.5人(33)和2005年每10万人0.8人(34)。
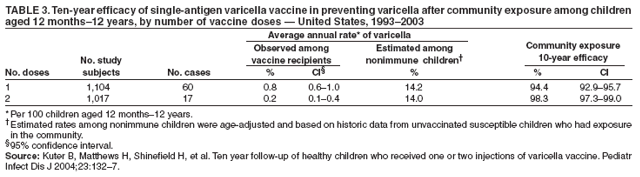
在1995 – 2001年期间,水痘被列为根本原因的死亡人数从115人下降到26人(28) (图3)。此后,死亡人数进一步下降;2003年报告了16例死亡。年龄调整死亡率下降了66%,从1990 – 1994年期间平均每百万人口0.41例死亡下降到1999 – 2001年期间的0.14例。在50岁以下的所有年龄组中都观察到了下降,其中12个月至4岁的儿童下降幅度最大(92%),其次是5岁至9岁的儿童,下降幅度为88%(每100万人口死亡0.10人)。>50岁人口的死亡没有下降到同样的程度;然而,该年龄组水痘死亡报告的有效性较低(35),并且这些死亡中的大多数不被认为是由水痘引起的。1999 – 2001年期间,所有种族和民族人口中水痘的平均死亡率低于每100万人0.15例死亡。没有高风险疾病(如恶性肿瘤、艾滋病毒/艾滋病和其他免疫缺陷)的人占水痘死亡人数的92%。与1990 – 1994年相比,1999 – 2001年期间水痘被列为死亡原因的平均死亡率也有所下降。
尽管1剂疫苗接种覆盖率高,且疫苗接种计划成功降低了水痘发病率和死亡率,但来自主动监测点和具有良好实施的疫苗接种计划和监测的州的报告显示,在某些州和一个主动监测点,报告的水痘病例数保持不变或最低程度下降,并且继续发生疫情。在2001 – 2005年期间,在水痘疫苗接种覆盖率高(范围96% – 100%)的学校中报告了疫情(3,4)。疫情在某些方面相似:1)都发生在小学,2)疫苗效力相似(范围:72% – 85%),3)年龄较小的学生发病率最高,4)每次疫情持续约2个月,5)指示病例发生在接种疫苗的学生中(尽管他们的疾病较轻)。接种疫苗儿童的总体发病率各不相同(范围:11% – 17%),某些教室的发病率高达40%。这些数据表明,即使在疫苗接种覆盖面接近普及且疫苗按预期发挥作用的情况下,1剂疫苗接种计划也不能完全预防水痘暴发。
产前和围产期接触
在前疫苗时代,产前感染并不常见,因为大多数育龄妇女对VZV具有免疫力(12,36)。孕妇患水痘与VZV病毒传播给胎儿或新生儿的风险有关。子宫内VZV感染可能导致先天性水痘综合征、新生儿水痘或婴儿期或幼儿期的水痘(37–46)。出生前暴露于VZV的婴儿,即使无症状,也可能在新生儿期具有可测量的水痘特异性IgM抗体,在1岁后具有持续的水痘特异性IgG免疫,且无出生后水痘病史,或表现出对VZV抗原应答的阳性淋巴细胞转化(37)。
先天性水痘综合征于1947年首次被发现(40)。先天性水痘综合征可发生在妊娠前半段感染的母亲所生的婴儿中,并可能表现为出生体重低、皮肤瘢痕、肢体发育不全、小头畸形、皮质萎缩、脉络膜视网膜炎、白内障和其他异常。在一项研究中,使用1986 – 2002年间进行的9项队列研究的汇总数据计算先天性水痘综合征的发病率(47)。妊娠2 – 12周的发病率为0.6%(725例中的4例),13 – 28周为1.4%(642例中的9例),28周后为0(385例中的0例)。
在1980 – 1993年期间在英国和西德进行的一项对1373名妊娠期水痘母亲的前瞻性研究中,观察到当母体感染发生在妊娠13 – 20周(43)。孕0 – 12周母体感染后的风险为0.4%。在366名妊娠期有水痘的母亲的婴儿中,没有发生先天性水痘综合征的病例。据报道,在妊娠20周以上的母亲患水痘后,出现了9例涉及先天水痘综合征的出生缺陷的孤立病例(最近一次发生在28周) (47,48)。在一项前瞻性研究中,在妊娠13 – 24周暴露于VZV的477名婴儿中,有4名(0.8%)在婴儿期或儿童早期出现HZ,在妊娠25 – 36周暴露于该病毒的345名婴儿中,有6名(1.7%)出现HZ43)。
孕妇在分娩前5天至分娩后2天内发生水痘,估计会导致17% – 30%的新生儿发生严重的水痘感染。这些婴儿暴露于VZV,但没有足够的母源抗体来减轻疾病的严重程度。据估计,母亲出现皮疹的婴儿中,分娩前4天新生儿死亡的风险为<31%(45)。这一估计是基于有限的婴儿死亡人数,可能高于实际风险,因为这项研究是在新生儿重症监护可用之前进行的。此外,某些病例不是前瞻性研究的一部分,而是回顾性报告,使结果受到选择偏倚的影响。当这些病例随后被另一位研究者重新评估时,某些婴儿被证明由于出生体重低而具有更高的死亡风险;在至少一个案例中,可能有另一种死因(46)。据报道,水痘-带状疱疹免疫球蛋白(VZIG)可降低严重新生儿水痘疾病的发病率(49)并因此在这种情况下被指明。然而,未接受VZIG暴露后预防的新生儿的死亡风险可能比先前估计的要低得多。
带状疱疹监测
原发感染后,VZV作为一种潜伏感染持续存在于感觉神经神经节中。病毒可以重新激活,导致带状疱疹。控制VZV潜伏期的机制还不清楚。带状疱疹的危险因素包括衰老、免疫抑制和在子宫内或幼儿期(即年龄< 18个月)初次感染水痘。据估计,15% – 30%的普通人群在其一生中会经历带状疱疹(50,51);随着预期寿命的增加,这一比例可能会增加。带状疱疹最常见的并发症,尤其是老年人,是带状疱疹后神经痛(PHN),带状疱疹消退后持续数周至数月的疼痛。带状疱疹也会出现危及生命的并发症;这些疾病包括可能导致失明的眼疱疹。另一个严重的表现是播散,可能涉及全身性皮疹、中枢神经系统、肺、肝和胰腺并发症。播散、肺炎和内脏受累通常仅限于免疫缺陷者。VZV病毒可以从患有带状疱疹患者的病灶传播给易感接触者。尽管可用于评估这种风险的数据很少,但一项家庭接触研究报告称,从带状疱疹传播VZV病毒的风险约为从水痘传播的风险的20%52)。
水痘疫苗接种可能在个体和群体水平上改变带状疱疹的风险(即群体免疫)。正如野生型VZV可导致野生型带状疱疹,减毒疫苗病毒有可能潜伏并在以后重新激活,导致疫苗病毒株(也称为Oka株)带状疱疹(53)。多项研究评估了免疫缺陷或健康儿童接种疫苗后Oka-菌株带状疱疹的风险(54–58)。在一项对白血病儿童的研究中,在平均4.1年的随访(范围:6个月- 10年)后,疫苗接受者的带状疱疹发生率为2%,而有水痘病史的对照组为15%(54)。根据化疗方案,这些疫苗接受者中的96个子集与96个经历过自然水痘的白血病儿童进行前瞻性匹配。分析表明,疫苗接种者的带状疱疹发生率(0.80/100人-年)比患有自然水痘的匹配白血病儿童(2.46/100人-年)低约三倍(p = 0.01)。健康儿童的数据更为有限,研究结果可能受到多种因素的影响(例如,不完整的确定、有限的随访时间或没有对年龄较大的受试者进行随访、在接种疫苗前后没有对野生型水痘感染进行全面筛查,或没有对所有病例进行测试以区分Oka-和野生型带状疱疹)。尽管如此,这些研究表明,单剂水痘疫苗后Oka株带状疱疹的风险低于野生型水痘感染后的风险(56–58)。随着时间的推移,Oka株带状疱疹的风险和表现应检查老年人谁是带状疱疹并发症的更大风险。在接种疫苗之前(即,由于子宫内或不明显的感染)或接种疫苗之后(即,由于突破性感染)经历水痘感染的人可能潜在地感染了两种VZV菌株。这些人患带状疱疹的风险未知。尚未进行长期研究来比较接受1剂水痘疫苗的人与接受2剂水痘疫苗的人的Oka-株带状疱疹风险。
水痘疫苗也可能在人群水平上改变带状疱疹的风险。随着群体免疫的发展和暴露可能性的降低,水痘疫苗接种计划预防了疫苗接受者和非疫苗接受者中的野生型VZV感染,消除了这些人中野生型带状疱疹的风险。野生型水痘感染可能性的降低也增加了患水痘的中位年龄(尽管年龄特异性发病率本身较低)。这降低了幼儿期(即年龄< 18个月)水痘感染的风险,从而降低了儿童期带状疱疹的风险因素。
潜伏野生型VZV病毒感染者与水痘患者的接触被认为可增强特异性免疫,这可能有助于控制VZV病毒的再激活和水痘(50)。有人担心,通过减少既往有野生型水痘感染史的人接触水痘的机会,减少接触水痘的可能性可能会增加患水痘的风险,这可能发生在接种水痘疫苗后短短5年内(59)并达到90%以上的疫苗接种覆盖率。
在美国,带状疱疹不是一种全国性的应报告疾病,已经使用多种方法、研究地点或数据来源进行了带状疱疹监测。对于某些研究,基线数据可在水痘疫苗接种计划开始前获得。一项包括基线数据的研究是对1992 – 2002年间一个健康维护组织(HMO)的电子医疗记录的回顾性分析(60)。这项HMO研究表明,在1992 – 2002年期间,随着水痘发病率的下降,经年龄调整的水痘发病率保持稳定(60)。经年龄调整和特异的带状疱疹年发病率随时间略有波动;1992年的年龄调整率最高,为每1 000人年4.1例,2002年为每1 000人年3.7例。对于后疫苗时代开始的其他研究,基线数据不可用(61–63)。对Medstat数据库中国家发病率数据的分析(可在http://www.medstat.com/Products/view/?id=71)证明了2000年和2001年每1000人-年3.2人(95%可信区间[CI] = 3.1 – 3.2)的带状疱疹总体发病率(61),代表在过去的20年里,与早期公布的数据相比,美国的年龄调整后的带状疱疹没有增加(64)。俄勒冈州和华盛顿州两个健康维护组织1997 – 2003年的数据表明,除了10 – 17岁的儿童外,带状疱疹发病率没有统计学显著增加(相对风险[RR] = 1.12,CI = 1.05-1.18);这些增加归因于口服类固醇(62)。另一项对马萨诸塞州1999 – 2003年间的全州电话调查收集的数据的研究表明63)。特别受影响的年龄组包括25 – 44岁的人和65岁以上的人。最后,在两个积极的水痘监测点(加利福尼亚州羚羊谷和宾夕法尼亚州西费城),自2000年以来一直在对年龄< 20岁的儿童进行积极的水痘监测。在2000 – 2004年期间,10岁以下儿童的麻疹发病率显著下降(p<0.05),从每1000名儿童0.75例降至0.23例(65;CDC未公布的数据,2006年)。总之,多项研究和监测数据表明,自1995年实施水痘疫苗接种计划以来,美国的水痘发病率没有一致的趋势。
阿昔洛韦用于治疗和预防水痘的用途
阿昔洛韦是一种合成核苷类似物,可抑制包括VZV在内的人类疱疹病毒的复制。自20世纪80年代初以来,静脉注射阿昔洛韦已可用于治疗患有水痘的免疫缺陷者。当在皮疹发作的24小时内接种时,阿昔洛韦已被证明可有效降低该人群中水痘相关的发病率和死亡率(66–68)。
1992年,食品药品监督管理局(FDA)批准使用口服阿昔洛韦治疗其他健康儿童的水痘。这一批准是基于安慰剂对照的双盲研究(69,70)证明了阿昔洛韦在皮疹发作24小时内接种时出现的有益临床效果(即,出现新病变的天数、发热持续时间以及皮肤和全身体征和症状的严重程度减少)。用药期间未发生严重不良事件。接种阿昔洛韦没有减少水痘的传播或减少缺课时间。因为很少出现并发症(1% – 2%),这些研究不能确定阿昔洛韦是否对健康儿童的疾病严重程度有统计学意义的影响。在这些研究中,接受阿昔洛韦的儿童感染后的抗体滴度与对照组儿童的滴度没有实质性差异(69,70)。在青少年和成人中进行的临床试验表明,如果阿昔洛韦在皮疹发作的24小时内接种(71–73)。
在1993年,AAP传染病委员会发表了关于使用阿昔洛韦(74)。AAP不认为对健康儿童施用阿昔洛韦具有足以证明其常规施用合理性临床益处;然而,AAP指出,在某些情况下可能有理由使用死刑。AAP建议,对于中度至重度水痘风险增加的其他健康人(例如,年龄> 12岁的人,患有慢性皮肤或肺部疾病的人,接受长期水杨酸盐治疗的人,以及接受短期、间歇或雾化皮质类固醇治疗的人),应考虑口服阿昔洛韦。某些专家还建议与受感染儿童生活在同一家庭的继发病例患者使用口服阿昔洛韦(74)。
阿昔洛韦在FDA妊娠用药评级中被归类为B类药物。虽然涉及动物的研究未显示致畸作用,但尚未对孕妇进行充分、良好控制的研究。然而,一项在妊娠期间使用阿昔洛韦的前瞻性登记收集了596名婴儿的结果数据,这些婴儿的母亲在妊娠的前三个月暴露于全身性阿昔洛韦,该登记表明出生缺陷的比率和类型接近于普通人群(75)。AAP不建议孕妇常规使用口服阿昔洛韦,因为对胎儿和母亲的风险和益处未知。然而,在严重的病毒介导的并发症(如肺炎)的情况下,AAP建议应考虑静脉注射阿昔洛韦(74)。
两种核苷类似物,阿昔洛韦和泛昔洛韦,已经被FDA批准用于治疗带状疱疹。如果在皮疹发作的72小时内接种,阿昔洛韦可以加快皮肤愈合的速度,并降低患有荨麻疹(76)。在同一时期口服泛昔洛韦具有相似的疗效(77)。
阿昔洛韦不适用于接触水痘后无免疫证据的健康儿童、青少年或成人的预防性使用。在这些情况下,接种疫苗是首选的方法。没有关于在免疫功能低下的人群中预防性使用阿昔洛韦的研究;因此,在这些情况下,建议使用VZIG。
预防水痘的疫苗
两种减毒水痘病毒活疫苗在美国获得许可用于预防水痘:单抗原水痘疫苗(VARIVAX®,Merck & co . Inc .,Whitehouse Station,New Jersey)和组合MMRV疫苗(ProQuad®,新泽西州怀特豪斯的默克公司)。这两种疫苗都来自减毒活VZV Oka株。Oka株是在日本(1978)在20世纪70年代早期,来自一名健康儿童的水泡液,该儿童患有天然水痘,并通过在人胚胎肺细胞、胚胎豚鼠细胞和人二倍体细胞(WI-38)的培养物中的连续繁殖而减毒。Oka/Merck疫苗中的病毒已经通过人类二倍体细胞培养物(MRC-5)进行了进一步传代,总共传代31次。
1995年,单一抗原水痘疫苗在美国获得许可,可用于年龄>12个月的健康人。这种疫苗是冻干的;当按照包装说明书中的说明重新配制并在室温下储存最多30分钟时,每0.5毫升剂量的Oka株/默克VZV至少含有1,350个蚀斑形成单位(79)。每剂还含有12.5毫克水解明胶、微量新霉素和胎牛血清、25毫克蔗糖、微量MRC-5细胞残留成分(包括DNA和蛋白质)。疫苗不含防腐剂。自1995年以来,在美国已经分发了超过5500万剂。严重不良事件的报告很少(见疫苗相关不良事件)。
2005年,MMRV复合疫苗在美国获得许可,用于12个月至12岁的健康儿童。ProQuad®中的减毒麻疹、腮腺炎和风疹疫苗病毒与麻疹、流行性腮腺炎和风疹(MMR)疫苗MMRII®中的相同且效价相等 (80)。Oka株/默克VZV的滴度在MMRV中比在单抗原水痘疫苗中高,最低为3.99 log10pfu与相比1,350 PFUs(约为3.13 log10)每0.5毫升剂量。其他成分类似于单抗原水痘疫苗中的成分。
疫苗接种的免疫反应
在许可前进行的单抗原水痘疫苗临床试验中,使用具有不同pfu量的大量疫苗和具有不同灵敏度和特异性水平的实验室分析来评估血清转化。使用一种专门开发的、敏感的gp-酶联免疫吸附测定(ELISA)试验,在1 – 12岁的6889名易感儿童中,在接种1剂水痘疫苗后约4 – 6周观察到约97%血清转化(定义为获得任何可检测的水痘抗体> 0.3 gpELISA单位)(79)。12 – 15个月儿童的血清转换率为98%,5 – 12岁儿童的血清转换率为95%(81)。13 – 17岁的青少年接种单剂疫苗后,血清转换率较低(79%)。在获得许可后进行的一项研究使用免疫接种后16周的膜抗原荧光抗体(FAMA)滴度来评估血清学反应,并证明在1剂单抗原水痘疫苗,80名健康儿童疫苗接受者中有61名(76%)血清转化(FAMA滴度>1:4)(82)。
疫苗接种后6周对疫苗的初级抗体反应与对疾病的保护相关(83,84)。在临床试验中,儿童中水痘抗体滴度为>5个gpELISA单位比那些滴度< 5个单位的突破性疾病的发生率较低(84);疫苗接种6周后,抗体滴度< 5 gpELISA单位的儿童比滴度为>5个gpELISA单位的儿童患突破性水痘的可能性高3.5倍。后来的免疫原性研究(85)报告了达到这一抗体水平而非血清转化的接种儿童的比例。接种1剂单抗原水痘疫苗后,86%的儿童的gpELISA水平为>5单位/毫升(85)。使用FAMA进行的研究表明,疫苗接种后16周的滴度> 1:4与对疾病的保护相关(82)。在接种疫苗后16周滴度> 1:4的健康人中,< 1%的人在家庭暴露后患过水痘(n = 130)。相比之下,在滴度< 1:4的人群中,发病率为55% (n = 60)。
短期和长期随访研究表明,儿童接种1剂单抗原水痘疫苗后抗体持续存在。在一项临床研究中,对277名儿童进行9年随访后,通过gpELISA检测到的抗体持续率接近100%(85)。另一项研究表明,尽管接种疫苗后12 – 24个月抗体滴度(由FAMA检测)可能下降,但1 – 4年后中值滴度没有变化,甚至在10年后上升(86)。在日本,38名7 – 10年前接种水痘疫苗的儿童中有37名(97%)出现了VZV抗体(其滴度与29名在过去10年内自然感染水痘的儿童相当) (87)并且在长达20年的随访中25名儿童中的100%(即,抗体水平高于10年前观察到的水平) (88)。至少有两个因素使长期研究的解释变得复杂。首先,暴露于野生型VZV很可能会无症状地增强疫苗诱导的免疫力。因为水痘疫苗在日本不是常规推荐的疫苗,所以在1991 – 1993年期间,儿童接种率估计很低(大约20%)。其次,由于接种疫苗后随着时间的推移,随访的儿童数量减少,样本量有限。
儿童接种第二剂水痘疫苗产生了与保护作用增强相关的免疫应答。对间隔3个月接种1或2剂单抗原水痘疫苗的健康儿童进行的一项比较研究表明,第二剂疫苗提供了更高的抗体水平,这是通过滴度为>5 gpELISA单位和几何平均滴度(GMTs)和更高的功效(85; 表2—4)。抗体滴度为的受试者比例>5 gpELISA单位在第二次给接种后6周高于第一次接种后(分别为99.6%和85.7%),并在9年随访期结束时保持高水平,尽管两种方案之间的差异缩小(分别为97%和95%)。第二剂后6周的GMT显著高于单剂后的GMT(分别为142和12)。在疫苗接种后血清转化的受试者中,两种方案之间的GMT差异在9年的随访中没有持续存在,尽管在研究结束时两种方案的GMT仍然很高。然而,接受第二剂疫苗显著降低了水痘突破率(3.3倍)并提高了疫苗效力(p<0.001)。另一项研究评估了第一剂疫苗4 – 6年后接受的第二剂疫苗的免疫原性,结果显示,大多数受试者在第一个7 – 10天内抗体水平显著增加,表明存在记忆反应。第二次接种当天,GMT为25.7,而第二次接种后7 – 10天GMT为143.6, 60%的接受者抗体滴度至少增加了四倍,另外17%的接受者抗体滴度至少增加了两倍(89)。第二次接种后三个月,GMT仍高于第二次接种当天(分别为119.0和25.7)。在儿童中,间隔4 – 6年接种2剂后的VZV抗体水平和GMT与间隔3个月接种2剂时获得的结果相当。
MMRV联合疫苗的许可是基于抗原成分的免疫原性与MMR和水痘疫苗相比不劣于在单独的检查点同时施用的疫苗,而不是基于临床疗效(80)。对12 – 23个月的健康儿童进行的临床研究表明,接受1剂MMRV疫苗的儿童的麻疹、腮腺炎、风疹和水痘抗体水平与在不同注射部位同时接受1剂MMR和1剂水痘疫苗的儿童的水平相似。对于MMRV中的水痘成分,接种疫苗6周后,91.2% (CI = 87.0% – 94.4%)的儿童获得的抗体滴度为>5 gpELISA单位/毫升(90)。一组儿童在第一剂疫苗接种后约3个月接种了第二剂MMRV疫苗。血清学反应(>5 gpELISA单位/mL)为99.2% (CI = 97.0% – 99.9%)(表2)。此外,接种第二剂MMRV疫苗后水痘的GMT增加了大约41倍(90)。对4 – 6岁的健康儿童施用MMRV联合疫苗,这些儿童以前接种过MMR和单抗原水痘疫苗,结果抗体水平相似,GMT水平增加了25倍(91)。
在>13岁的人群中,多项研究描述了接受单抗原水痘疫苗后的血清转换率(范围:第一剂后为72% – 94%,第二剂4 – 8周后为94% – 99%)(79,92,93)。在临床研究中,在间隔4 – 8周给予2剂疫苗的97%的青少年和成人中,可检测的抗体水平持续了至少5年(79)。然而,其他研究表明,25% – 31%血清转化的成人疫苗接受者在接种疫苗后的多个时间间隔(范围:1 – 11年)失去了可检测的抗体(通过FAMA检测)93,94)。对于接触水痘后出现突破性疾病的人,疾病的严重程度或发病率不会随着时间的推移而增加(95)。
先天(即非特异性)和适应性(即体液和细胞)免疫在控制原发性水痘感染中很重要。引发细胞介导的免疫的能力对于病毒清除是重要的,提供对疾病的长期保护并防止有症状的VZV再激活。对儿童和成人的研究表明,即使在没有血清转化的疫苗接受者或失去可检测抗体的疫苗接受者中,突破性水痘通常也是轻微的,这表明VZV特异性细胞介导的免疫在缺乏可检测抗体反应的情况下为疫苗接受者提供保护(94,95)。在儿童中对疫苗接种的细胞免疫反应的研究表明,1剂水痘疫苗的免疫接种诱导了VZV特异性T细胞增殖,这在疫苗接种后1年的29名儿童中的26名(90%)和疫苗接种后5年的60名儿童中的52名(87%)中得以维持(96)。在这项研究中,平均刺激指数(SI)是细胞介导免疫的标志,1年后为12.1,5年后为22.1。在一项许可前研究中,从一组儿童中获得的疫苗接种后1年的数据比较了间隔3个月接受1剂和2剂疫苗的儿童中的免疫反应,该数据表明,接受2剂疫苗的儿童的水痘特异性淋巴细胞增殖反应显著高于接受1剂疫苗的儿童(平均SI分别为34.7和23.1;p = 0.03)(97)。在间隔4 – 6年施用的2次剂量的研究中,结果还表明在第二次剂量后6周和3个月时的淋巴细胞增殖反应显著高于第一次剂量后的相同时间点(p<0.01)(89; 表2)。
在成人中,疫苗诱导的VZV特异性T细胞增殖在17名受试者中的16名(94%)在疫苗接种后1年和5年保持(96,98)。1年后平均SI为9.9,5年后为22.4。
保护的相关因素
对于儿童,接种疫苗后6周通过gpELISA测量的水痘抗体反应与中和抗体水平、VZV特异性T细胞增殖反应、疫苗效力和暴露于VZV后对水痘的长期保护作用相关(83,84,99,100)。效价为>5 gpELISA单位/mL与预防疾病相关,尽管它不应被视为绝对的保护保证。突破性的案例发生在患有>5 gpELISA单位/毫升。FAMA滴定度>1:4在疫苗接种后16周也与对疾病的保护相关(82)。然而,这两种抗体测试都不能在市场上买到。在疫苗接种后的其他时间间隔测量的抗体水平之间的关系,尤其是在暴露前不久测量的抗体水平和突破性疾病之间的关系尚未进行研究。没有对成年人的保护相关因素进行评估。
疫苗功效和疫苗效力
单剂量疗法
许可前效力
在对12个月至14岁儿童进行的许可前研究中,单抗原水痘疫苗的保护效力各不相同,这取决于每剂注射的活病毒量、暴露环境(社区或家庭)以及临床随访的质量和时间长度。大多数许可前研究报告,在接种疫苗后7 – 10年内,1剂水痘疫苗对任何临床疾病的效力在70% – 90%范围内,对严重疾病的效力在95%范围内(81,101,102)。在12个月至14岁的儿童中进行了一项随机安慰剂对照疗效试验,但配方不同于目前的疫苗(每剂17,000 pfu(103,104),对接种疫苗后7年的儿童进行随访(105)。据报道,接种疫苗后1年和2年的有效率分别为100%和98%,在家庭中暴露于VZV后分别为100%和92%。虽然没有对成人进行随机对照研究,但通过评估成人疫苗接受者在家庭中暴露于水痘时的保护作用,确定了单抗原水痘疫苗的效力。根据未接种疫苗儿童家庭暴露后自然水痘的历史发病率为87%的报道,成人的估计疗效约为80%(79)。没有研究家庭中暴露的未接种疫苗的成人的发病率。
许可后功效和有效性
预防所有水痘疾病
许可后研究已经评估了在儿童护理、学校、家庭和社区环境中使用多种方法进行单抗原水痘疫苗接种的有效性¶。经常对所有水痘以及中度和重度水痘(以不同方式定义)的有效性进行评估。疫情调查评估了对临床定义的水痘的有效性。这些研究中的大部分已证明疫苗在许可前试验中描述的相同范围内对预防水痘有效(70% – 90%)(3–6,106–113),有的更低(44%,56%)(114,115)和一些更高的(在调查的两所学校之一中为100%)估计(107)。一项在11个儿童保育中心进行的回顾性队列研究表明,疫苗对预防临床诊断的水痘有83%的有效性(116)。在一项1997 – 2003年间在儿科诊所进行的测量疫苗对实验室确认的水痘的有效性的病例对照研究中,疫苗有效性在前四年为85% (CI = 78% – 90%),在整个研究期间为87% (CI = 81% – 91%)117,118)。最后,在一项关于家庭二次发作率的研究中,由于暴露的强度而被认为是疫苗性能的最强有力的测试,水痘疫苗在预防年龄为12个月- 14岁且无水痘疾病或疫苗接种史的暴露家庭接触者中临床定义的水痘方面有79% (CI = 70% – 85%)有效(119)。针对所有疾病的疫苗有效性的上市后数据已经进行了总结(表5)。
许可后进行的一项随机临床试验中,比较了1剂水痘疫苗与2剂水痘疫苗的效力,在10年观察期内,1剂水痘疫苗的估计效力为94.4% (CI = 92.9% – 95.7%)(85; 表3)。在同一项研究中,1剂疫苗在家庭暴露10年后预防水痘的有效率为90.2% (CI = 83.7% – 96.7%)(表4)。这项研究没有使用安慰剂对照,而是使用未接种疫苗儿童发病率的历史数据来计算疫苗效力。
预防中度和重度水痘
评估疫苗在预防中度和重度水痘中的性能的上市后研究一直显示出高效性。疾病严重程度的定义在不同的研究中有所不同。某些研究使用了明确的疾病等级,包括皮肤损伤、发热、并发症的数量和研究者对疾病严重程度的评估,而其他研究仅使用了皮肤损伤、报告的并发症或住院的数量。中度水痘通常被定义为50 – 500或250 – 500个损害,重度水痘被定义为> 500个损害或任何住院或并发症。在随机的许可后临床试验中,严重水痘被定义为> 300个损害和发热>102℉(38.9℃),相当于口腔温度。不考虑不同的定义,多项研究表明,单抗原水痘疫苗>>95%有效预防中度和重度疾病(3–6,85,106,107,109–113,115–119);一项研究表明有效率为86%(114)。当单独测量时,对严重疾病的有效性为100%(6,85,109,111,117,119)。针对中度和重度水痘的疫苗有效性的上市后数据已总结如下(表5)。
两剂疗法
在一项单抗原水痘疫苗的随机临床试验中,比较了1剂疫苗与间隔3个月施用的2剂疫苗的效力,在10年观察期内,2剂疫苗的估计效力为98.3% (CI = 97.3% – 99.0%),显著高于1剂疫苗的效力(p<0.001)(85; 表5)。2剂量方案对严重水痘也100%有效。在同一项研究中,2剂单抗原水痘疫苗在家庭暴露10年后预防疾病的功效为96.4% (CI = 92.4% – 100%),与1剂(90.2%)无显著差异(p = 0.112)(表4)。然而,涉及家庭接触的病例数量有限。
尚未进行评估MMRV复合疫苗临床疗效的正式研究。之前在单抗原疫苗的临床研究中已经确定了单个组分的功效。
突破性疾病
突破性疾病被定义为接种疫苗后> 42天发生的野生型VZV感染病例。在临床试验中,在接种疫苗的人中水痘疾病的严重程度明显低于未接种疫苗的人,未接种疫苗的人通常有发热和数百个水疱性病变(120)。在突破性疾病的情况下,皮肤损伤的中值数目通常< 50(99,121–123)。此外,与未接种疫苗的人相比,疫苗接种者的水疱性病变较少(更常见的是非典型病变,丘疹不会发展为水疱),病程较短,发热发生率较低。
多项许可后调查也表明,大多数突破性水痘病例明显比未接种疫苗儿童的病例轻(p<0.05)(3,5,107–114,116–118,124)。然而,大约25% – 30%的突破性病例并不轻微,其临床特征更类似于未接种疫苗的儿童(124)。自1999年水痘死亡成为全国通报以来,已向CDC报告了两例突破性水痘疾病死亡;一个9岁女孩有哮喘史,在突破性感染时正在接受类固醇治疗,另一个7岁女孩有恶性室管膜瘤史,在死亡时也在接受类固醇治疗(CDC,未发表的数据,2006)。
单剂量疗法
在临床试验中,1,114名1 – 12岁的儿童接受了1剂单抗原水痘疫苗,每剂疫苗含有2,900 – 9,9,000 PFUs的减毒病毒,并在接种疫苗后接受了长达10年的积极随访(79)。在95名家庭暴露于水痘的疫苗接受者中,8名(8%)报告了轻度水痘(10 – 34处病变)。
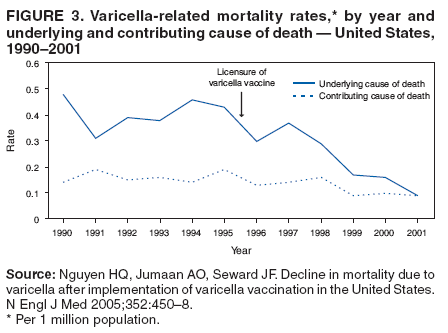
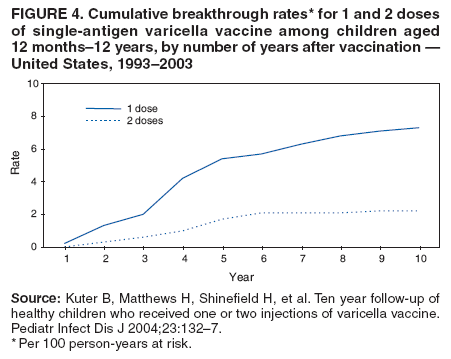
在一项为期10年的随机临床试验中,比较了1剂疫苗与2剂疫苗的疗效,在接受1剂疫苗的儿童中,水痘突破的累积发生率为7.3%(85)。每年在1剂疫苗的接受者中有0.2% – 2.3%发生突破性病例。在整个观察期内都有病例发生,但大多数是在接种疫苗后2 – 5年报告的(图4)。在57例有突破性病例的儿童中,13例(23%)有> 50个病灶。
在横断面研究中,爆发调查中突破性疾病的发病率在11%和17%之间(某些教室高达40%)3)和15%的家庭环境(119)。
两剂疗法
儿童数据
在一项比较1剂疫苗与2剂疫苗效力的随机临床试验中,在10年观察期内,接受2剂疫苗的儿童的突破性水痘累积发生率比接受1剂疫苗的儿童低3.3倍(分别为2.2%和7.3;p<0.001)(85)。在0.8%的2剂疫苗接受者中偶尔出现突破性病例。大多数突破性疾病病例发生在接种疫苗后2 – 5年;接种疫苗后7 – 10年没有病例报告(图4)。在16名有突破性病例的儿童中,3名(19%)有> 50个病灶。在1剂和2剂方案之间,具有> 50个病变的儿童的比例没有差异(p = 0.5)。
青少年和成人中的突破性感染
在对接受2剂疫苗的青少年和成人进行的许可后研究中,461名疫苗接受者在接种疫苗后随访8周- 11.8年(平均3.3年),出现40例(9%)突破性水痘病例(95),随访1个月- 20.6年(平均4.6年)的120名疫苗接种者中有12例(10%)发生(94)。一项对已接种2剂疫苗的人进行的许可前研究报告称,在接种疫苗后随访5 – 66个月(平均30个月)的152名疫苗接受者中,出现了12例(8%)突破性病例(93)。
传染性
许可前临床试验报告了水痘病例疫苗接种者向其疫苗接种同胞的疾病传播率。在1981 – 1989年期间进行的10项试验中,在积极监测的1 – 8年随访期内,2163名接种疫苗的儿童中有114名(5.3%)发生突破性感染,他们的90名接种疫苗的兄弟姐妹中有11名(12.2%)发生二次传播(121)。索引和二级病例患者的疾病都很轻微。据报道,已接种疫苗的患有突破性疾病的儿童向易感成人(其中一人死亡)的家庭传播(CDC,未发表的数据,2006)。一项研究调查了水痘疫苗接种者和未接种者对12个月至14岁疫苗接种者和未接种者家庭接触者的二次发作率(119)。这项研究表明,接种疫苗的水痘患者(病变少于50处)的传染性仅为未接种疫苗的水痘患者的三分之一。然而,接种水痘疫苗的人>50处病变的传染性与未接种水痘疫苗的人一样(119)。接种水痘疫苗的人往往病情较轻,尽管他们比未接种水痘疫苗的人传染性低,但他们可能不会得到诊断并被隔离。因此,他们可能有更多的机会在社区环境中感染他人,从而进一步加剧VZV病毒的传播。接种过水痘疫苗的人也是水痘暴发中的指数病例患者(3,4,115)。
疫苗失败的风险因素
在疫情调查期间的疫苗有效性研究和其他专门设计的研究中,已经确定了疫苗失效的潜在风险因素(5,108–110,113–115,118,125)。在疫情调查中,低病例数限制了研究人员进行多变量分析和检查疫苗失败的每个风险因素的独立影响的能力。随着接种疫苗年龄的降低,突破性疾病的风险增加,14个月以下接种疫苗的儿童突破性疾病的风险增加三倍(110),在一项研究中增加了两倍,在另一项研究中增加了近四倍108,115),年龄< 19个月接种疫苗的儿童增加9倍(113)。其他疫情调查表明,自接种疫苗以来的时间(可变定义为>3,> 5,或>5年)与突破性疾病风险增加相关(相对风险[RR] = 2.6,6.7和2.6分别) (5,114,115)。然而,接种疫苗时的年龄和接种疫苗后的时间高度相关,它们与突破性疾病风险的独立关联仅在一项疫情调查中得到评估(113)。一项针对其他潜在风险因素进行调整的回顾性队列研究表明,年龄< 15个月接种疫苗的儿童发生突破性疾病的风险增加(调整后的相对风险[aRR]= 1.4;CI = 1.1% – 1.9%)(125)。一项病例对照研究表明,接种疫苗后第一年的疫苗有效性在年龄小于15个月的儿童中显著低于年龄在15岁的儿童(73%)>15个月(99%) (p = 0.01)(118)。然而,在这些年龄接种疫苗的儿童之间的总体有效性差异在随后几年(8年随访)中没有统计学意义(分别为81%和88%;p = 0.17)。分析了1995 – 2004年期间从350,000人的哨点人群中收集的主动监测数据,以确定自接种疫苗以来突破性水痘病例的严重性和年发病率是否随时间而增加(126)。接种疫苗> 5年的儿童比接种疫苗< 5年的儿童患中度和重度突破性水痘的可能性高2.6倍(p = 0.016)。在校正感染年龄、接种疫苗年龄和感染年份的影响后,12个月- 12岁儿童接种疫苗后水痘突破的年发生率随时间显著增加(p<0.01)。
其他多项研究调查了疫苗效力较低的可能原因,但没有发现接种疫苗时的年龄(3–5,111,114)或接种疫苗后的时间(3,110,111)与疫苗失效有关。一项正在进行的研究正在检查这些因素和疫苗失败的风险(127)。在对7,449名在12 – 23个月大时接种疫苗的儿童进行了8年的积极随访后,结果并未表明在12 – 14个月大时接种疫苗的儿童比在15 – 23个月大时接种疫苗的儿童患突破性疾病的风险增加。此外,趋势检验显示,在接种疫苗时,每增加一个月,报告的突破性疾病发生率没有变化(127)。
两项疫情调查指出,患有哮喘和湿疹的儿童患突破性疾病的风险增加(109,113)。在这些研究中,没有研究使用类固醇治疗哮喘或湿疹。类固醇曾与未接种疫苗者的严重水痘有关(128–130)。只有一项回顾性队列研究同时控制了多种风险因素的影响,包括类固醇的使用,该研究表明突破性疾病的风险与哮喘或湿疹(125)。然而,这项研究记录了如果儿童在突破性疾病的3个月内接受了口服类固醇(当暴露于水痘时被认为是口服类固醇的替代物)的处方,突破性疾病的风险增加(调整后RR[aRR]= 2.4;CI = 1.3% – 4.4%)和在接种MMR疫苗的28天内接种水痘疫苗时(aRR = 3.1CI = 1.5% – 6.4%)。
豁免权的证据
ACIP已批准水痘免疫证据标准(盒子)。只有提供了接种日期书面文件的水痘疫苗剂量才被认为是有效的。无论是自我报告的剂量还是父母提供的疫苗接种史,其本身都不能被视为足够的免疫证据。缺乏足够疫苗接种证明或其他免疫证据的人应该接种疫苗。
从历史上看,成人或父母为其子女自我报告水痘疾病被认为是免疫的有效证据。在流行前疫苗时代,成人自我报告阳性疾病史的预测价值极高,尽管在关于其子女的父母报告中缺乏阳性预测值的数据(131–133)。随着发病率的降低和接种水痘疫苗的人的比例增加,水痘在临床上不容易被识别。最近的一项研究表明,报告水痘阳性病史的12个月- 4岁未接种疫苗的儿童中,只有75%实际上是免疫的(经血清学试验证实),而5 – 9岁和10 – 14岁的儿童中有89%是免疫的(134)。为了限制假阳性报告的数量并确保免疫力,ACIP建议免疫力的证据应该是由保健提供者对水痘的诊断或保健提供者对疾病史的核实,而不是父母或自我报告。上述引用的研究表明,99%的15 – 19岁的人和100%的20 – 29岁的人报告有水痘病史134)。因为VZV感染的血清学证据已在96% – 97%的20 – 29岁美国出生的成人和97% – 99%的20-29岁成人中得到证实>在1998 – 1999年期间测试了30年(12),1980年前在美国出生的婴儿被认为是免疫的证据,除了卫生保健人员(HCP)、孕妇和有免疫能力的人。对于这三类人群,免疫方面的确定性是可取的,因为有可能通过医院传播给高危患者;病毒传播给胎儿,可能导致先天性水痘综合征;以及严重疾病的可能性。通常不建议进行疫苗接种后血清学试验来验证对水痘疫苗的免疫反应,因为可用的商业试验在检测疫苗诱导的免疫方面缺乏敏感性,并可能给出假阴性结果。
疫苗同时接种
单抗原水痘疫苗与MMR疫苗在不同的注射点,用不同的注射器同时接种或间隔4周分别接种时,对年龄在>12个月的健康儿童具有良好的耐受性和有效性。同时接受VARIVAX和MMRII的儿童中发生的不良事件的数量和类型与在不同就诊时接种疫苗的儿童没有差异(79,135)。关于同时接种VARIVAX和含有MMR、白喉和破伤风类毒素以及百日咳(DTP)的各种组合的疫苗的效果的数据,以及b型流感嗜血杆菌(Hib)尚未出版(79)。一项对694名受试者进行的随机研究确定,与第四剂肺炎球菌结合疫苗(PCV7)同时接种的MMR、水痘和Hib疫苗的免疫应答不劣于未接种时的免疫应答;对于两组的所有抗原,血清转换的受试者百分比> 90%(136)。
还评估了MMRV疫苗与其他疫苗的联合接种。在涉及1913名12 – 15个月的健康儿童的临床试验中,比较了三组(137)。一组同时接受MMRV疫苗、白喉和破伤风类毒素和无细胞百日咳吸收疫苗(DTaP)、Hib结合物(脑膜炎球菌蛋白结合物)疫苗和乙型肝炎(重组)(乙型肝炎)疫苗(在不同的地点)的接种。第二组在初次就诊时接种MMRV疫苗,6周后同时接种DTaP、Hib和乙肝疫苗。第三组接种MMR和水痘疫苗,6周后同时接种DTaP、Hib和乙肝疫苗。前两组的麻疹、腮腺炎、风疹和水痘成分的血清转换率和抗体滴度相当。第三组未报告免疫学数据。接受这些疫苗的两组人群的Hib和Hep B血清转换率也是相当的。
MMRV疫苗与灭活脊髓灰质炎疫苗、肺炎球菌结合疫苗、流感疫苗和甲型肝炎疫苗同时使用的数据缺乏或有限。同时施用大多数广泛使用的活疫苗和灭活疫苗产生的血清转换率和不良反应率与分别施用疫苗时观察到的相似。因此,单一抗原和复合MMRV疫苗可以与推荐给12 – 15个月和4 – 6岁儿童的其他疫苗同时接种。当卫生保健提供者预计,由于某些因素(例如,以前错过的疫苗接种机会),儿童可能不会回来进行随后的疫苗接种时,同时接种尤为重要。
疫苗接种的经济学分析
在美国开始水痘疫苗接种计划之前进行了成本效益分析(138)。研究结果表明,考虑到直接和间接成本,学龄前儿童常规疫苗接种每花费1美元可节省5.4美元。仅考虑直接医疗成本时,效益成本比为0.9:1.0。当使用较低的疫苗短期和长期有效性估计值时,效益成本比仅略低。
最近进行的一项分析使用了发病率和死亡率的当前估计值(20,28,33)和当前的直接和间接成本(ACIP,未发表的介绍,2006年)。该模型认为,第一剂后,第二剂将减少水痘疾病残留79%。从社会的角度来看,1剂和2剂疫苗接种计划与无计划相比都节省成本。疫苗项目成本估计为1剂3.2亿美元,2剂5.38亿美元。1剂方案预防水痘疾病的节省估计约为13亿美元,2剂方案约为14亿美元。与1剂方案相比,第二剂方案的增量成本估计为每挽救一个质量调整生命年(QALY)96,000美元。如果将预防接种人群中A组链球菌感染和甲型H1N1流感的益处加在一起,则每QALY节省的增量成本分别为91,000美元和17,000美元。由于具有水痘病史的人群中带状疱疹增加的模型预测的不确定性,以及没有一致的趋势表明带状疱疹增加归因于美国的水痘疫苗接种计划的事实,具有水痘病史的人群中的带状疱疹不包括在模型中。
水痘疫苗的储存、处理和运输
单抗原水痘疫苗和组合MMRV疫苗具有相似但不相同的分布、处理和储存要求(79,80)。为了保持效力,冻干水痘疫苗必须在5℉(-15℃)或更低的平均温度下冷冻储存。自20世纪80年代中期以来制造的家用冰柜被设计用于保持从-4℉(-20℃)到5℉(-15℃)的温度。经过测试,VARIVAX在无霜冰箱中保持稳定。可靠地保持平均温度< 5℉(<-15℃)并有单独密封冷冻箱门的冷冻箱可用于储存VARIVAX和ProQuad。医疗服务提供者可以使用独立的冷冻箱或冰箱-冷冻箱组合的冷冻箱,前提是冷冻箱有自己单独的、密封的和隔热的外门。不接受带有内部冷冻室门的装置。应该在每天开始和结束时记录温度。供应商应在使用新购买的单元储存疫苗前至少记录1周的所需温度,并在此后定期记录。当水痘疫苗储存在组合冰箱的冷冻室中时,应仔细监控两个室的温度。将恒温器设置得足够低以储存含有水痘的疫苗可能会无意中将冷藏的疫苗暴露在冷冻温度下。不可接受带有冰室的冰箱(如小型宿舍式冰箱)用于储存水痘疫苗,冰室不是密封的或带有未密封、未隔热的门。
稀释剂应单独存放在室温或冰箱中。疫苗应根据包装说明书中的说明重新配制,并且仅使用疫苗随附的稀释剂,该稀释剂不含防腐剂或其他可能使疫苗病毒失活的抗病毒物质。一旦重组,疫苗应立即使用,以尽量减少效力损失。如果在复原后30分钟内没有使用,应丢弃疫苗。
在场外诊所内处理和运输水痘疫苗
当在远离储存疫苗的冷藏库的地点进行免疫接种时,免疫接种所需的疫苗瓶数量应包装在疫苗运输容器(从制造商处收到)或隔热冷却器中,并装有足够量的干冰(即每箱至少6磅)以保持效力。当放置在合适的容器中时,干冰将保持<5℉(<-15℃)。干冰到达诊所后应保留在容器中。如果在收货地点打开容器时没有剩余干冰,应联系制造商(默克公司)寻求指导(电话:1-800-982-7482)。如果接收地点有干冰,可以用来储存疫苗。温度计或温度指示器不能在装有干冰的容器中使用。稀释剂不应在干冰上运输。
如果没有干冰,只能运输单抗原水痘疫苗,用冷冻包装将温度保持在36℉-46℉(2℃-8℃)之间。应监控运输温度,温度指示器或温度计应放置在集装箱中,并在到达时进行检查。在免疫期间,容器应尽可能保持封闭;应该每小时检查并记录温度。如果温度保持在36℉-46℉(2℃-8℃)之间,单抗原水痘疫苗从冰箱中取出后可使用长达72小时。日期和时间应该标在疫苗瓶上。在冷藏温度下储存任何时间的单抗原水痘疫苗不得再次冷冻以备将来使用。
不允许在36℉-46℉(2℃-8℃)的温度下运输和储存MMRV复合疫苗。与单一抗原水痘疫苗相比,MMRV联合疫苗必须保持在<5℉(<-15℃ ),直至复溶和接种。在规划异地诊所时,必须考虑疫苗储存温度的差异。因此,不建议将MMRV疫苗运输到场外诊所。如果对单一抗原水痘疫苗或MMRV联合疫苗的储存有任何疑虑,应联系制造商寻求指导。
尽量减少疫苗的浪费
通过准确确定给定患者群体所需的剂量数量,可以最大限度地减少疫苗浪费。为确保最大的疫苗效力,应更频繁地订购小批量疫苗(最好至少每3个月一次)。单抗原水痘疫苗不应分发给没有能力在使用前将其妥善保存在冰箱中的供应商。水痘疫苗的运输应保持在最低限度,以防止效力损失。非现场诊所站点应仅接收其在短时间内(如果在冷藏温度下储存单抗原水痘疫苗,则为72小时)可以使用的疫苗量。
接种疫苗后的不良事件
由于疫苗接种后的不良事件可能继续由野生型VZV引起,即使水痘疾病有所减少,医疗保健提供者也应获取与事件相关的临床标本(例如脑炎的脑脊液、支气管灌洗或肺炎的肺活检)进行实验室评估,包括菌株鉴定。关于菌株鉴定的信息可从默克公司的VZV鉴定项目(电话:1-800-652-6372)或从CDC的国家水痘参考实验室(电话:404-639-0066;电子邮件:vzvlab@cdc.gov)或http://www.cdc.gov/nip/diseases/varicella/surv/default.htm。商业实验室不具备菌株鉴定能力。
1986年的国家疫苗伤害法案要求使用疫苗的医生和其他卫生保健提供者保持永久的免疫记录,并报告包括水痘疫苗在内的选定疫苗的不良事件的发生。应将怀疑由水痘疫苗引起的严重不良事件(即所有需要医疗关注的事件)报告给疫苗不良事件报告系统(VAERS)。表格和说明可从以下网址获得https://secure.vaers.org/vaersDataEntryintro.htm,在FDA药品公告中http://www.fda.gov/medwatch,或拨打1-800 822-7967的24小时VAERS信息记录。
预许可
单抗原水痘疫苗
在许可前临床试验期间,对超过11,000名健康儿童、青少年和成人施用单抗原水痘疫苗时,耐受性良好。在一项对914名12个月至14岁的易感健康儿童进行的双盲、安慰剂对照研究中,报告的唯一有统计学意义(p<0.05)的不良事件是注射部位的疼痛和发红,这些不良事件在疫苗接受者中比在安慰剂接受者中更常见(103)。这项研究还描述了2%的安慰剂和4%的疫苗接种者在接种后43天内出现非特异性皮疹。在28例报告的皮疹中,10例(36%)由医生检查;在接受检查的人中,疫苗接受者的七个非注射部位皮疹中有四个被判断为水痘样,而安慰剂接受者中没有皮疹。
在一项比较1剂单抗原水痘疫苗与间隔3个月接种的2剂疫苗的安全性的研究中,在约2,000名年龄为12个月至12岁的健康受试者中,未报告与疫苗接种相关的严重不良事件,这些受试者在每次注射后随访42天。2剂疫苗方案通常耐受性良好,其安全性与1剂方案相当。观察到的注射部位不适的发生率<接种后3天,第2剂(25.4%)比第1剂(21.7%)略高。剂量2后全身性临床症状的发生率较低;第1剂后第7 – 21天的发热发生率为7%,第2剂后为4%(p = 0.009),第1剂后水痘样皮疹发生率为3%,而第2剂后为1%(p = 0.008),高峰发生在疫苗接种后8 – 21天(139)。
在对>13岁以上的人进行的无对照试验,对接受1剂单抗原水痘疫苗的约1600名疫苗接受者和接受2剂疫苗的955名疫苗接受者进行了42天的不良事件监测(79)。在第一剂和第二剂疫苗接种后,分别有24.4%和32.5%的疫苗接种者抱怨注射部位。第一次注射后,3%的疫苗接种者在注射部位出现水痘样皮疹,第二次注射后为1%。在第一次注射后,5.5%的疫苗接受者出现非局部皮疹,在第二次注射后,0.9%的疫苗接受者出现非局部皮疹,分别在接种后7 – 21天和0 – 23天达到高峰。
MMRV联合疫苗
在临床试验中,对4,497名12 – 23个月的儿童接种MMRV联合疫苗,而不与其他疫苗同时接种(80)。将第一剂的安全性与MMRII疫苗和VARIVAX在不同注射部位同时接种的安全性进行了比较。随访期为疫苗接种后42天。在接受MMRV疫苗的人群中,系统性疫苗相关不良事件的报告率在统计学上显著高于在单独注射部位同时接受两种疫苗的人群:发热(>102 F [>38.9 C]口服等效),(分别为21.5%和14.9%),麻疹样皮疹(分别为3.0%和2.1%)。发烧和麻疹样皮疹通常在接种疫苗后5 – 12天内出现,持续时间短,并在没有长期后遗症的情况下消退。据报告,注射部位的疼痛、压痛和酸痛在接受MMRV联合疫苗的人群中的发生率(22.0%)显著低于接受MMRII和VARIVAX疫苗的人群(26.7%)。接受1剂MMRV疫苗的受试者(2.3%)比分别接受两种疫苗的受试者(1.5%)更容易在注射部位出现皮疹。一项研究还比较了MMRV与MMRII和VARIVAX作为第一剂接种的使用,证明了类似的结果(90)。在第5 – 12天,接受MMRV组的儿童比接受MMRII和VARIVAX组的儿童有更高的体温升高率(分别为27.7%和18.7%;p = 0.034)。
为了证明MMRV疫苗可以作为第二剂接种,进行了一项研究,涉及799名4 – 6岁的儿童,他们在>12个月时已经接受了MMRII和VARIVAX疫苗的第一剂,无论是否同时接受,研究登记前1个月(91)。这些儿童随机接种疫苗(MMRV和安慰剂,MMR和安慰剂,或MMRII和VARIVAX ),然后监测安全性。未报告与疫苗相关的严重不良事件。总体而言,接受MMRV、MMRII、MMRII和VARIVAX治疗的受试者中出现一种或多种不良事件的比例相当。接受MMRV疫苗的组在疫苗接种后1 – 5天在注射部位具有红斑(p = 0.01)和肿胀(p = 0.008)的受试者的比例在统计学上显著更高。另一项研究检查了480名12 – 23个月大的儿童间隔3个月接种2剂MMRV的安全性(90)。第二剂MMRV后的不良事件发生率通常低于第一剂。接种第二剂MMRV后水痘样皮疹的发生率低于同时接种MMRII和VARIVAX疫苗后的发生率(分别为0.0%和1.9%;p = 0.01)。
许可后
在1995年3月1日至2005年12月31日期间,在美国共分发了4770万剂水痘疫苗,VAERS报告了25306例水痘疫苗接种后发生的不良事件,其中1276例(5%)被归类为严重事件。总的不良事件报告率为每100,000剂分发52.7例。严重不良事件的报告率为每100,000剂分发2.6例。报告的所有不良事件中有一半发生在12 – 23个月的儿童中(VAERS,未公布的数据,2006)。
非所有疫苗接种后发生的不良事件都有报告,许多报告描述了可能由混杂或无关因素(如药物和其他疾病)引起的事件。由于水痘疾病持续发生,野生型病毒可能是某些报告事件的原因。对于背景发病率数据已知的严重不良事件,VAERS报告率低于自然水痘后的预期或低于社区中疾病的背景发生率。被动安全性监测的固有局限性阻碍了对VAERS报告的疫苗接种后的不良事件率与自然疾病后并发症的不良事件率进行比较。然而,这些差异的程度表明,接种疫苗后严重不良事件的发生率比自然发病后低得多。自从实施水痘疫苗接种计划以来,与水痘相关的严重并发症、住院和死亡的数量显著下降,证实了这一假设(22,23,28)。
与许可前的经验相似,使用单抗原水痘疫苗后的许可后安全性监测数据表明,皮疹、发热和注射部位反应是最常报告的不良事件(140,141)。在疫苗接种计划的前4年,当野生型VZV病毒仍在广泛传播时,使用这些来自不良事件被动监测的报告,聚合酶链反应(PCR)分析证实,接种后42天内发生的大多数皮疹事件主要是由野生型水痘带状疱疹病毒引起的。来自野生型病毒的皮疹平均在接种后8天出现(范围:1 – 24天),而来自疫苗株的皮疹平均在接种后21天出现(范围:5 – 42天) (140)。
作为VARIVAX短期安全性上市后评估的一部分,在1995年4月至1996年12月期间,从医院自动化临床数据库、急诊室就诊和诊所就诊中确定了89,753名接种疫苗的成人和儿童(56)。在确定的所有潜在不良事件中,暴露随访期间未发现任何事件的一致时间关联或聚集。在这组疫苗接受者中,在接受水痘疫苗后未发现共济失调或脑炎病例。在前疫苗时代,在< 15岁的儿童中,急性小脑共济失调的发生率估计为1/4000水痘病例,无共济失调的水痘脑炎的发生率估计为1/33000水痘病例(142)。
实验室确认由疫苗病毒株引起的严重并发症很少见,包括肺炎(140)、肝炎(143),严重的播散性水痘感染(140,141,144,145),以及来自五名疫苗接种者的二次传播(140,146–148)。除二次传播病例外,这些病例都发生在免疫功能低下的患者或在接种疫苗时患有其他未确诊的严重疾病的人。
尽管报告了其他严重的不良事件,但涉及的疫苗株未经实验室确认。血小板减少症(140,141,149)和急性小脑性共济失调(140,141,150)被描述为可能与单抗原水痘疫苗相关。两名儿童在接种水痘疫苗后被诊断为急性轻偏瘫(一名在第5天,另一名在第3周) (151)。在这两种情况下,单侧梗死的基底神经节和内囊被注意到;这种分布符合水痘血管病。水痘疫苗接种后的荨麻疹与明胶过敏有关(152)。据报道,复发性丘疹性荨麻疹可能与水痘疫苗接种有关(153)。然而,关于水痘疫苗接种后潜在不良事件的可用数据不足以确定因果关系。报告信息的质量差异很大,与其他疫苗(尤其是MMR)同时接种可能会混淆归因。
带状疱疹。与野生型VZV病毒相似,疫苗病毒可以建立潜伏感染并随后重新激活,在疫苗接受者中引起带状疱疹疾病。在获得疫苗许可之前,对白血病儿童的研究表明,与那些(年龄和方案匹配的)既往有水痘(54)。健康疫苗接受者中的带状疱疹病例已被证实由疫苗病毒和野生型病毒引起,这表明疫苗接受者中的某些带状疱疹病例可能是由患者可能未检测到的先前自然水痘感染引起的,或者是由接种疫苗后的感染引起的(140)。报告的一例病例中,一名儿童被诊断为神经母细胞瘤,并患有严重的慢性带状疱疹,原因是疫苗病毒株随着时间的推移产生了耐药性(145)。一项大型的上市后安全性研究通过每6个月进行一次的调查进行,并在15年随访研究的前9年通过医疗图表审查进行验证,该研究对超过7,000名在12 – 24个月时接种单抗原水痘疫苗的登记儿童进行了研究,据父母报告,估计带状疱疹疾病发病率为每100,000人-年22例(CI = 13-37)(Steven Black,MD,Northern California Kaiser Permanente Medical Care Program,未发表的陈述,2005)。在5 – 9岁的健康儿童中,带状疱疹的发病率为每100,000人年30人(154)和46/10万人年<14年(64)。然而,这些比率来自不同的人群,基于不同的方法。此外,这些年龄组中的一部分儿童没有经历过水痘疾病;这些比率可能低估了全部感染野生型VZV病毒的儿童队列中的比率,使得与接种疫苗的队列进行直接比较变得困难。
疫苗病毒的传播
单抗原水痘疫苗的许可前疫苗试验结果表明,水痘疫苗病毒从健康人传播到易感接触者是罕见的。这种风险在接受安慰剂的健康接种儿童的兄弟姐妹中进行评估(103)。439名安慰剂接受者中有6名(1%)血清转化,无皮疹;这六名儿童接种疫苗的兄弟姐妹也没有出现皮疹。血清学数据表明,这六个血清转换者中有三个错误地代替他们的同胞接种了疫苗。在一项较小的研究中,对接受水痘疫苗的免疫受损的健康儿童的兄弟姐妹进行了临床评估,并测试了体液或细胞介导的免疫反应(155)。没有证据表明疫苗病毒传播给接受水痘疫苗的37名健康儿童中的30名免疫受损同胞。
许可后监测活动积累的数据表明,水痘疫苗病毒从健康人传播给易感接触者的风险较低。自获得许可以来,已分发了超过5500万剂VARIVAX,通过PCR分析仅记录了5人接种疫苗后来自免疫活性人的传播,导致6人继发感染,均为轻度(140,146–148)。三起事件涉及从1岁健康儿童到健康家庭接触者的传播,包括一名4个月大的兄弟姐妹、一名父亲和一名怀孕母亲。在后一事件中,母亲选择终止妊娠,但随后通过PCR检测的胎儿组织对水痘疫苗病毒呈阴性(147)。这些事件中的儿童分别有2个、12个和30个损伤。第四起事件涉及一名免疫能力正常的青少年的传播,该青少年是一所慢性残疾儿童机构的居民。该青少年在接种疫苗后出现超过500处病变,疫苗病毒被传染给该机构的另一名具有免疫能力的住院医师和一名卫生保健工作者,这两人都有水痘病史(146)。第五个事件代表了来自白血病疫苗接种者的健康同胞接触者的三级传播(148)。两个健康同胞的皮疹都是轻微的(即,分别为40和11处损伤),并且从所有三个病例患者中分离出疫苗病毒。第三个兄弟姐妹在第二个病例-患者发病18天后出现皮疹,在接种疫苗的白血病儿童出现皮疹33天后出现皮疹。除了这五个事件之外,据报告,一名儿童在接种水痘疫苗后5个月传播了带状疱疹疫苗病毒;2周后,在该儿童接种疫苗的兄弟中出现轻度水痘样皮疹,从中分离出疫苗水痘病毒(156)。
虽然水痘疫苗不推荐用于细胞免疫缺陷的儿童,但来自白血病儿童的许可前疫苗试验的经验是有益的。一项关于白血病儿童水痘疫苗接种的研究数据表明,在88名白血病疫苗接受者的健康易感同胞中,有15名(17%)发生水痘病毒疫苗传播;在15名受感染的同胞中,有11名(73%)出现轻微皮疹(148)。传播风险与免疫缺陷疫苗接受者的皮肤损伤数量相关。
这些数据表明,健康的接种过疫苗的人将疫苗病毒传播给其接触者的风险最小,特别是在疫苗接受者没有出现疫苗皮疹的情况下。出现疫苗相关皮疹的疫苗接种者,特别是HCP和免疫功能低下者的家庭接触者,应避免接触无免疫证据但有严重并发症高风险的人(见卫生保健人员)
水痘疫苗接种的基本原理概述
在美国,水痘疫苗是一种有效的预防工具,用于减轻水痘疾病及其并发症的负担。在前疫苗时代,水痘是一种儿童期疾病,400万病例中的90%以上,大约11,000例住院治疗中的三分之二,以及每年100 – 150例死亡中的大约一半发生在< 20岁的人群中。单一抗原水痘疫苗已获准在>12个月以上的健康人群中使用,MMRV复合疫苗已获准用于12个月至12岁的健康儿童。许可前和许可后的研究表明,1剂单一抗原水痘疫苗在预防水痘方面大约有85%的有效性。疫苗接种后经常发生的突破性水痘疾病是温和的和可改变的。水痘疫苗在预防严重水痘疾病方面有> 95%的有效性。自1995年实施水痘疫苗接种计划以来,水痘发病率、住院率和死亡率大幅下降。MMRV的许可是基于其疫苗抗原成分的免疫非劣效性。最初的水痘疫苗政策建议是,12个月至12岁的儿童接种1剂水痘疫苗,年龄在4 – 8周的人接种2剂水痘疫苗>13年。2006年6月,ACIP批准了儿童常规2剂建议。第一剂应在12 – 15个月大时注射,第二剂应在4 – 6岁时注射。
在美国,儿童接种第二剂水痘疫苗的理由是为了进一步减少水痘疾病及其并发症。尽管儿童1剂疫苗接种计划取得了成功,但85%的疫苗有效性仍不足以预防水痘爆发,尽管水痘爆发少于前疫苗时代,但仍继续在高度接种疫苗的学校人群中发生。突破水痘是传染性的。对接种1剂和2剂水痘疫苗后的免疫应答的研究表明,在接种第二剂水痘疫苗后6周测量时,GMT增加了10倍以上。更高比例(> 99%)的儿童获得了>5个gpELISA单位,相比之下,76% – 85%的儿童在接种一剂水痘疫苗后出现这种情况。预计水痘疫苗的第二剂将为15% – 20%的儿童提供更好的保护,这些儿童对第一剂疫苗没有足够的反应。来自许可后进行的随机临床试验的数据表明,儿童接种2剂单抗原水痘疫苗后的疫苗效力(98.3%;CI = 97.3% – 99.0%)显著高于单剂后(94.4%;CI =92.9% – 95.7%)。接受2剂疫苗的儿童患突破性疾病的风险比接受1剂疫苗的儿童低3.3倍。疫苗效力的这种提高(通常高于在野外条件下观察到的)如何转化为在社区使用条件下的疫苗效力将是一个重要的研究领域。
水痘疫苗常规第一剂(12 – 15个月)和第二剂(4 – 6岁)的推荐年龄与MMR疫苗使用的推荐年龄一致,旨在限制儿童没有水痘抗体的时期。水痘的当前流行病学支持第二次剂量的推荐年龄,学龄前儿童发病率低且暴发少,小学年龄儿童发病率高且暴发多。然而,如果第一剂和第二剂之间的间隔为3个月,则第二剂可以在更早的年龄接种。根据在12个月至12岁的儿童中评估两次剂量的研究设计,提出了最小剂量间隔的建议。MMRV疫苗可用于同时为儿童接种麻疹、腮腺炎、风疹和水痘疫苗。由于在学校、大学和其他高等教育机构的学生中传播的风险可能很高,没有免疫证据的学生应接种2剂水痘疫苗。所有以前接种过1剂水痘疫苗的儿童和青少年应接种第2剂。
水痘疾病在青少年和成人中更严重,其并发症更频繁。建议所有无免疫证据的青少年和成人接种疫苗将为这些年龄组提供保护。因为水痘可能在无资格接种疫苗的免疫缺陷人群中更严重,并且因为VZV病毒在医疗机构传播的风险,HCP必须接种疫苗。妊娠前两个月的水痘疾病可能会感染胎儿并导致先天性水痘综合征。因此,现在建议对无免疫证据的孕妇进行常规产前免疫筛查和产后疫苗接种。
水痘疫苗的使用建议
建议>12个月儿童皮下注射两剂0.5毫升水痘疫苗、青少年和无免疫证据的成人。对于12个月- 12岁的儿童,建议两次剂量之间的最小间隔为3个月。然而,如果第一次注射后>28天施用了第二剂,第二次注射被认为是有效的,无需重复。对于>13岁的人,建议最小间隔4周。单抗原水痘疫苗被批准用于年龄>12个月的健康人群。MMRV复合疫苗被批准用于12个月至12岁的健康儿童。MMRV疫苗适用于同时接种麻疹、腮腺炎、风疹和水痘疫苗。当联合疫苗的任何成分被指明而其他成分没有被禁止时,使用许可的联合疫苗,如MMRV疫苗,比单独注射同等成分的疫苗(157)。
常规疫苗接种
12个月至12岁的人
学龄前儿童
所有健康儿童应在12 – 15个月大时常规接种第一剂水痘疫苗。
学龄儿童
建议所有4 – 6岁的儿童(即在进入幼儿园前、幼儿园或一年级之前)常规接种第二剂水痘疫苗。但是,如果第一剂和第二剂之间的间隔大于3个月,则可以在更早的年龄接种。
由于VZV病毒在学校传播的风险,所有入学儿童都应接种过2剂含水痘成分的疫苗或有其他水痘免疫证据(见免疫证据)。
>13岁的人
>13岁无水痘免疫证据的热应接受两次0.5毫升剂量的单抗原水痘疫苗皮下注射,间隔4 – 8周。如果第一次接种后超过8周,可在不重新开始接种的情况下进行第二次接种。只有单一抗原水痘疫苗可用于该年龄组人群的疫苗接种。MMRV不允许在>13岁以上的人群中使用。
学龄儿童、大学生和其他中学后教育机构的学生
所有学生都应接受水痘免疫评估,没有免疫证据的学生应间隔4 – 8周常规接种2剂单抗原水痘疫苗。由于接触率高,水痘在学龄儿童、大学生和其他大专教育机构的学生中传播的风险可能很高。
其他成年人
所有健康的成年人都应进行水痘免疫评估,那些没有免疫证据的人应间隔4 – 8周接种2剂单抗原水痘疫苗。暴露或传播风险可能增加且没有免疫证据的成年人应特别考虑接种疫苗,包括1) HCP,2)免疫缺陷者的家庭接触者,3)在VZV病毒可能传播的环境中生活或工作的人(如教师、日托员工、居民和机构中的工作人员),4)在已报告传播的环境中生活或工作的人(如大学生, 囚犯和惩教机构的工作人员以及军人)、5)非怀孕的育龄妇女、6)生活在有孩子的家庭中的青少年和成人,以及7)国际旅行者。
第二剂补种疫苗
为了提高水痘的个人防护能力并对学校爆发产生更快的影响,建议儿童、青少年和以前接种过1剂水痘疫苗的成人接种第2剂水痘疫苗。对于岁的儿童,建议第一剂和第二剂补种之间的最小间隔<12岁的人为3个月,>13岁的人间隔4周。然而,可以在比最小推荐间隔更长的任何间隔施用第二次补充剂量。补充疫苗接种可以在常规卫生保健提供者访问期间以及通过学校和大学入学要求来实施。
作为面向所有青少年的综合健康服务的一部分,ACIP、AAP和AAFP建议在11 – 12岁时进行健康维护检查。该访问还应作为免疫访问,以评估疫苗接种状态并实施必要的疫苗接种(158)。医生应该利用这种和其他常规访问来确保所有没有水痘免疫证据的儿童已经接种了2剂水痘疫苗。
进入儿童保育、学校、大学和其他中学后教育机构的要求
水痘免疫的儿童护理和入学要求以前已被推荐(2)。2005年,ACIP建议将要求扩大到所有年级的学生。官方卫生机构应采取必要措施,包括制定和执行学校免疫要求,以确保所有年级(包括大学)的学生和儿童保育中心的儿童免受水痘和其他疫苗可预防疾病(157)。
产前评估和产后疫苗接种
建议对妇女进行水痘免疫证据的产前评估。1980年以前的出生不被认为是孕妇免疫的证据,因为怀孕期间水痘感染的潜在严重后果,包括胎儿感染。妊娠结束或终止后,没有水痘免疫证据的妇女应在出院前接种第一剂疫苗。第二剂应在4 – 8周后接种,这与产后访视(分娩后6 – 8周)一致。对于分娩的妇女,应在产后访视时注射第二剂。应建议女性在每次接种水痘疫苗后1个月内避免怀孕。完成或终止妊娠的卫生保健机构应使用长期规定,确保对无免疫证据的妇女接种水痘疫苗。
疫苗接种的特殊注意事项
艾滋病毒感染者接种疫苗
CD4+ T淋巴细胞百分比> 15%的HIV感染儿童应考虑接种单抗原水痘疫苗。水痘疫苗以前被推荐用于CDC临床和免疫分类N1和A1的HIV感染儿童,具有年龄特异性CD4+ T淋巴细胞百分比>25% (2)。来自一项临床试验的有限数据显示,37名感染HIV的儿童(CDC临床类别N、A或B和免疫学类别2 [CD4+ T淋巴细胞百分比>15% – 24%])表明该疫苗具有良好的耐受性,并且在免疫接种后1年内> 80%的受试者具有可检测的VZV特异性免疫应答(抗体或细胞免疫应答或两者兼有(159)。这些儿童对水痘疫苗产生抗体反应的可能性不低于免疫功能受HIV感染影响较小的受试者。因为与健康儿童相比,感染HIV的儿童患水痘和带状疱疹(即带状疱疹)的风险更高,所以ACIP建议,在权衡潜在风险和益处后,应该考虑对CD4+ T淋巴细胞百分比为>15%,符合条件的儿童应间隔3个月接种2剂单抗原水痘疫苗。因为细胞免疫受损的人在接种活疫苗后出现并发症的潜在风险更大,所以如果这些疫苗接受者在接种后出现水痘样皮疹,应鼓励他们回来进行评估。目前尚无关于MMRV疫苗在HIV感染儿童中的安全性、免疫原性或有效性的数据,在对这些儿童进行疫苗接种时,MMRV疫苗不应作为单一抗原水痘疫苗的替代品。Oka株/默克VZV疫苗在MMRV联合疫苗中的效价高于单一抗原水痘疫苗。先前已经公布了对感染HIV的儿童接种麻疹、腮腺炎或风疹疫苗的建议(160)。
缺乏关于感染HIV的青少年和成人使用水痘疫苗的数据。然而,根据专家意见,水痘疫苗对年龄> 8岁且免疫功能水平相当的HIV感染者(CD4+T淋巴细胞计数>200个细胞/µl)可能与8岁以下儿童的情况相似。与1 – 8岁儿童相比,年龄较大的HIV感染儿童、青少年和成人的免疫原性可能较低。然而,在权衡野生VZV引发严重疾病的风险和疫苗接种的潜在益处后,可考虑对CD4+T淋巴细胞计数正常的HIV感染者进行疫苗接种(2剂,间隔3个月接种)>200个细胞/µl在这些年龄段中。如果艾滋病毒感染者接种疫苗导致临床疾病,使用阿昔洛韦可能会减轻疾病的严重程度。
可能存在某种程度免疫缺陷的情况
体液免疫受损的人可以接种疫苗。关于没有免疫证据的人仅接受吸入、鼻内或局部剂量的类固醇是否可以安全接种疫苗,还没有数据发表。然而,临床经验表明,这些人对疫苗的耐受性良好。无免疫证据的人因某些疾病(如哮喘)正在接受全身性类固醇治疗,并且没有其他免疫缺陷,如果他们正在接受< 2 mg/kg体重或总计< 20mg/天的泼尼松或其等效物,则可以接种疫苗。某些专家建议,如果安全的话,在接种疫苗后2 – 3周停用类固醇(1)。日本一项使用Oka/Biken水痘疫苗(在美国无法获得,但其免疫原性和效力与美国使用的水痘疫苗相似)的研究数据表明,当在接种前暂停使用类固醇1 – 2周时,因肾病而接种类固醇的儿童可以安全接种疫苗,尽管在类固醇治疗未暂停时接种疫苗的儿童中没有发生严重反应(161)。正在接受高剂量全身性类固醇(即,>2毫克/千克泼尼松)>2周的人,一旦类固醇治疗停止>1个月,可接种疫苗,根据使用活病毒疫苗的一般建议(157)。
处于缓解期且没有水痘免疫证据的白血病儿童的疫苗接种应仅在专家指导下进行,并在出现并发症时进行抗病毒治疗。患有白血病、淋巴瘤或其他恶性肿瘤的患者,其疾病处于缓解期且其化疗已终止至少3个月,可接受活病毒疫苗(157)。当对可能存在某种程度免疫缺陷的人进行免疫接种时,只能使用单抗原水痘疫苗。
免疫缺陷者的家庭接触者的疫苗接种
免疫功能低下的人是严重水痘感染的高危人群。约30%的原发感染者会出现严重疾病。因为水痘疫苗现在被推荐给所有没有免疫证据的健康儿童和成人,免疫缺陷者的家庭接触者应该常规接种。尽管现在免疫缺陷者暴露于野生VZV病毒的风险比以前低,但疫苗应该提供给没有免疫缺陷者免疫证据的儿童和成人家庭接触者。通过降低野生型VZV传入家庭的可能性,家庭接触者的疫苗接种为免疫缺陷者提供了保护。免疫缺陷者的家庭接触者接种疫苗理论上可能对免疫缺陷者造成最小的疫苗病毒传播风险,尽管在一项研究中,在对30名患有恶性肿瘤的儿童的37名健康兄弟姐妹接种疫苗后没有证明疫苗病毒传播的证据(155)。在美国,在发放了超过5500万剂疫苗后,还没有疫苗病毒传播给免疫缺陷者的病例记录。其他数据表明,在免疫缺陷者中由疫苗病毒引起的疾病比野生型疾病更轻微,并且可以用阿昔洛韦(148,159)。为免疫缺陷者的易感家庭接触者接种疫苗的益处超过了将疫苗病毒传播给免疫缺陷者接触者的极低潜在风险。发生疫苗相关皮疹的疫苗接种者,特别是HCP和免疫功能低下者的家庭接触者,应避免接触具有严重并发症高风险的易感人群。如果一个易感的、免疫功能低下的人无意中接触了一个患有疫苗相关皮疹的人,则不需要使用VZIG进行暴露后预防,因为与此类病毒相关的疾病预计是轻微的。
哺乳的母亲
没有免疫证据的妇女的产后疫苗接种不必因母乳喂养而推迟。产后已接种水痘疫苗的女性可继续母乳喂养。大多数活疫苗与母乳中的病毒分泌无关(157)。一项涉及12名在哺乳期间接受单一抗原水痘疫苗的妇女的研究表明,在收集的217份母乳样本中或在两种疫苗剂量后检测的婴儿中均未发现VZV DNA(162)。没有婴儿血清转化。另一项研究没有在接种疫苗后的母乳样本中检测出水痘基因序列(163)。因此,没有免疫证据的哺乳母亲应接种单抗原水痘疫苗。MMRV混合疫苗未被批准用于>13岁人群。
保健人员
VZV的医院传播是众所周知的(131,164–173),而预防医院内VZV感染和HCP感染控制指南已经发表(174,175)。医院内暴露的来源包括感染水痘或带状疱疹的患者、医院工作人员和访客(如医院员工的子女)。在医院中,当与指示病例患者没有直接接触的易感人群中发生水痘时,已证明VZV病毒通过空气传播(176–180)。
为防止VZV疾病和医院传播,卫生保健机构应确保所有HCP人都有对水痘免疫的证据。1980年以前的出生不被视为HCP免疫的证据,因为有可能通过医院传播给高危患者。在卫生保健机构中,对有水痘阴性或不确定病史的人员和未接种疫苗的人员在接种疫苗前进行血清学筛查可能具有成本效益。机构可以选择检测所有HCP,而不考虑疾病史,因为一小部分有阳性疾病史的人可能易感。
不建议在接种2剂疫苗后对水痘免疫进行常规检测,以管理已接种的HCP。在所有情况下,可用的商业测定法不够灵敏,不足以检测接种后的抗体。敏感试验表明,99%的成年人在第二次注射后会产生抗体。然而,血清转换并不总是导致对疾病的完全保护,并且没有关于成人保护相关性的数据。
应通过员工健康计划或由感染控制护士在暴露后的第10 – 21天每天监测已接种2剂疫苗并暴露于VZV的HCP,以确定临床状态(即每天筛查发烧、皮肤损伤和全身症状)。水痘患者在皮疹发作前2天可能具有传染性。此外,应指导HCP立即报告发热、头痛或其他全身症状以及任何不典型的皮肤损害。如果出现症状,HCP应该立即请病假。医疗保健机构应制定HCP筛查和疫苗接种以及工作场所暴露后HCP管理的方案和建议。
已接种1剂疫苗并暴露于VZV的HCP人应在暴露于皮疹后3 – 5天内接种第二剂单抗原水痘疫苗(前提是第一剂疫苗接种后已过去4周)。接种疫苗后,管理类似于2剂疫苗接受者。
暴露于VZV病毒的无其他免疫证据的未接种HCP人在暴露后10 – 21天具有潜在的传染性,在此期间应休假。他们应尽快接受暴露后疫苗接种。如果发生感染,在接触皮疹3 – 5天内接种疫苗可能会缓解疾病。暴露后接种疫苗> 5天仍然是必要的,因为它诱导对随后暴露的保护(如果当前暴露没有引起感染)。
疫苗接种后出现水痘样皮疹的疫苗接受者传播疫苗病毒的风险较低,并且已有记录表明在家庭和长期护理机构中暴露后(140,146–148)。接种HCP疫苗后没有病例记录。在没有免疫证据的情况下接种HCP疫苗的益处超过了这种极低的潜在风险。作为一项保障措施,机构应考虑对接种疫苗后出现皮疹的人员采取预防措施。出现疫苗相关皮疹的HCP应避免接触无免疫证据的人,这些人有患严重疾病和并发症的风险,直到所有病变消退(即结痂或消退)或24小时内没有新的病变出现。
水痘IgG抗体检测
在HCP自然水痘感染后,最广泛用于检测水痘IgG抗体的试验是乳胶凝集(LA)和ELISA。使用涂有VZV糖蛋白抗原的乳胶颗粒的市售LA测试可以在15分钟内完成,并且不需要特殊设备(181)。在检测自然水痘感染后的抗体反应方面,LA试验的敏感性和特异性与FAMA相当。LA测试通常比商业ELISAs更敏感。在接种水痘疫苗后长达11年的时间里,LA试验一直检测到抗体(182)。然而,为了筛查HCP对水痘的易感性,应考虑一种灵敏度较低且更具特异性的商业ELISA。最近的一份报告指出,LA试验会产生假阳性结果,特别是当只评估单一浓度的血清时(183);这导致了HCP有记录的假阳性结果病例,这些病例最终未接种疫苗,随后感染了水痘。
为控制疫情接种疫苗
建议接种水痘疫苗以控制疫情。没有足够免疫证据的人应酌情接种第一剂或第二剂疫苗。此外,在学龄前儿童中爆发时,建议接种2剂疫苗以获得最佳保护,接种1剂疫苗的儿童应接种第二剂疫苗,前提是自第一剂疫苗接种后已过3个月。州和地方卫生部门可能会建议没有免疫证据的暴露者联系他们的卫生保健提供者进行疫苗接种,或者他们可能会通过卫生部门或学校(或其他机构)疫苗接种诊所提供疫苗接种。尽管疫情控制工作最好应在发现疫情后立即实施,但即使疫情发现较晚,也应提供疫苗接种。水痘在某些环境(如儿童护理机构、学校或机构)中的爆发可持续长达4 – 5个月。因此,在疫情爆发期间提供疫苗可能会为尚未暴露的人提供保护,并缩短疫情爆发的持续时间(184)。作为疫情控制规划的一部分,接受第一剂或第二剂疫苗的人可以立即重新入学。作为疫情控制措施的一部分,接种第一剂疫苗的人应根据年龄安排第二剂疫苗。在最后一例水痘病例出现皮疹后21天之前,未接种疫苗且没有其他免疫证据的人应被排除在发生疫情的机构之外。此外,对于2剂学校疫苗接种要求所涵盖的学龄人群,建议在疫情爆发期间排除那些在疫情爆发前已接受第一剂疫苗但未接受作为oubtreak控制计划一部分的第二剂疫苗的疫苗接受者。对接种疫苗有禁忌症的严重水痘高危人群应在暴露后96小时内注射VZIG。
禁忌症
一般
如果发生过敏反应,应准备好足够的过敏反应治疗用品,包括肾上腺素注射液(1:1000 ),以便立即使用。在接种疫苗之前,医疗保健提供者应获得疫苗接种者的疫苗接种史,并确定该人之前是否对任何疫苗有任何反应,包括Varivax、ProQuad或任何含麻疹、腮腺炎或风疹的疫苗。
对疫苗成分过敏
接种含水痘的活疫苗很少导致超敏反应。注射疫苗前,应仔细阅读包装说明书中的信息。对疫苗的任何成分(包括明胶)有过敏反应史的人禁用疫苗接种。单抗原水痘疫苗不含防腐剂或卵蛋白;这些物质引起了对其他疫苗的过敏反应。对于MMRV联合疫苗,麻疹活疫苗和腮腺炎活疫苗是在鸡胚培养中生产的。然而,在对鸡蛋过敏的人群中,接种含麻疹或腮腺炎疫苗后发生严重过敏反应的风险较低。因为用疫苗进行皮肤试验不能预测对疫苗接种的过敏反应,所以在给对鸡蛋过敏的人注射MMRV联合疫苗之前,不需要进行皮肤试验(160)。对含麻疹和腮腺炎疫苗的过敏反应大多与对鸡蛋抗原的超敏反应无关,而是与其他疫苗成分有关。对新霉素有过敏反应史的人不应接种单一抗原水痘疫苗或MMRV联合疫苗。然而,新霉素过敏通常表现为接触性皮炎,这是一种迟发型免疫反应,而不是过敏反应。对于经历这种反应的人,不良反应(如果有的话)将在疫苗接种后48 – 96小时出现红斑、瘙痒性结节或丘疹。新霉素接触性皮炎史不是接种水痘疫苗的禁忌症。
免疫力改变
单一抗原水痘疫苗和MMRV联合疫苗未获准用于患有任何恶性疾病的人,包括血液恶液质、白血病、任何类型的淋巴瘤或影响骨髓或淋巴系统的其他恶性肿瘤。MMRV联合疫苗不应用于患有原发性或获得性免疫缺陷(包括与艾滋病相关的免疫抑制或HIV感染的其他临床表现、细胞免疫缺陷、低丙种球蛋白血症和异常丙种球蛋白血症)的人。在给感染HIV的儿童接种疫苗时,MMRV复合疫苗不应作为组分疫苗的替代品。
水痘疫苗不应用于一级亲属(如父母和兄弟姐妹)中有先天性或遗传性免疫缺陷家族史的人,除非潜在疫苗接受者的免疫能力已得到临床证实或实验室验证。
接受高剂量全身免疫抑制治疗的人,包括口服类固醇的人,>2毫克/千克体重或总共>20 mg> 每天等同于10 kg的人接种泼尼松或等效药物,使用>2两周,不应接种水痘疫苗。这些人比健康人更容易受到感染。在接受免疫抑制剂量皮质类固醇(185)。这一禁忌症不适用于正在接受吸入、鼻腔或局部皮质类固醇或低剂量皮质类固醇(通常用于哮喘预防或皮质类固醇替代疗法)的患者(见可能存在某种程度免疫缺陷的情况)。
怀孕
因为水痘疫苗对胎儿的影响未知,所以孕妇不应接种疫苗。接种疫苗的非孕妇应避免在每次注射后1个月内怀孕。对于没有免疫证据的人来说,有一个怀孕的家庭成员不是接种疫苗的禁忌症。
如果孕妇接种了疫苗或在接种后1个月内怀孕,应告知她对胎儿的潜在影响。野生型水痘对胎儿的风险较低(见产前和围产期暴露)。因为疫苗中使用的减毒病毒的毒性小于野生型病毒,所以对胎儿的风险(如果有的话)应该更低。在1995年,默克公司与疾病预防控制中心合作,建立了VARIVAX妊娠登记处,以监测在怀孕前3个月或怀孕期间任何时间无意中接种水痘疫苗的孕妇的母胎结局(报告电话:1-800-986-8999)(186)。在妊娠登记的前10年中,没有记录任何先天性水痘综合征或与先天性水痘综合征相符的出生缺陷(187,188)。在预期报告的血清反应阴性妇女的131名活产婴儿中(其中82名婴儿的母亲在最高风险期[即妊娠前三个月或后三个月]接种了疫苗),没有记录到符合先天性水痘综合征的出生缺陷(患病率= 0;CI = 0 – 6.7%),报告了3种主要出生缺陷(患病率= 2.3%;CI = 0.5% – 6.7%)。注册中心前瞻性报告中的重大出生缺陷发生率与美国普通人群中报告的发生率(3.2%)相似,且缺陷无特定模式或靶器官。虽然研究结果没有排除怀孕前或怀孕期间意外接种水痘疫苗的妇女的风险,但潜在风险(如果有的话)很低。
预防措施
疾病
患有急性重症疾病(包括未经治疗的活动性肺结核)的人的疫苗接种应推迟到康复后进行。推迟接种疫苗的决定取决于症状的严重程度和疾病的病因。没有关于单一抗原水痘疫苗或MMRV联合疫苗是否会加重结核病的数据。单独接种减毒麻疹、腮腺炎和风疹病毒活疫苗可能会导致结核菌素皮肤敏感性暂时降低。因此,如果要进行结核菌素试验,应在MMRV联合疫苗之前、同时或至少4 – 6周后进行。然而,结核菌素皮肤试验不是接种单一抗原水痘疫苗或MMRV联合疫苗的先决条件。
水痘疫苗可用于患有轻度疾病、伴有或不伴有低烧(如腹泻或上呼吸道感染)的无免疫证据的儿童(189)。医生应警惕疫苗相关的体温升高,这可能主要发生在接种疫苗后的第二周,尤其是使用MMRV复合疫苗时。研究表明,未能为患有轻微疾病的儿童接种疫苗会阻碍疫苗接种工作(190)。
血小板减少
血小板减少不是单一抗原水痘疫苗的禁忌症。没有关于接种MMRV复合疫苗的人发生或恶化血小板减少症的临床数据。在接种MMR疫苗和水痘疫苗后有血小板减少的病例报告。MMR活疫苗的上市后经验表明,血小板减少症患者在接种疫苗后可能会出现更严重的血小板减少症。对于血小板减少症儿童接种MMRV复合疫苗,卫生保健提供者应参考MMR疫苗接种的ACIP建议(160)。
最近使用的血液、血浆或免疫球蛋白
尽管已知被动获得的抗体会干扰对麻疹和风疹疫苗的反应(191),施用免疫球蛋白(IG)对水痘病毒疫苗应答的影响是未知的。对麻疹疫苗接种反应的干扰持续时间与剂量相关,范围为3 – 11个月。由于被动转移的抗体可能抑制对水痘疫苗接种的反应,因此水痘疫苗不应在施用血液(除了洗涤的红细胞)、血浆或IG后以与麻疹疫苗相同的间隔(3 – 11个月,取决于剂量)施用。针对不同适应症的含抗体产品与水痘疫苗之间的建议接种间隔之前已经公布(157)。此外,接种水痘疫苗的人不应在接种疫苗后2周内接种含抗体的产品,除非其益处超过接种疫苗的益处。在这种情况下,疫苗接种者应根据所接受的剂量,在适当的时间间隔内再次接种疫苗或进行免疫试验,如果血清反应阴性,则再次接种疫苗。
水杨酸盐的用途
尚无水痘疫苗接种后使用水杨酸盐相关的不良事件报道;然而,疫苗制造商建议疫苗接种者在接种水痘疫苗后的6周内避免使用水杨酸盐,因为阿司匹林的使用与水痘后的Reye综合征有关。对于患有类风湿性关节炎或其他需要阿司匹林治疗的疾病的儿童,应考虑接种疫苗并随后密切监测。与接种含减毒VZV疫苗的儿童相比,患有自然水痘的儿童发生阿司匹林相关严重并发症的风险可能更大。没有证据表明Reye综合征与不含水杨酸的止痛剂或退烧药有关。
暴露后预防
健康的人
来自美国和日本的关于家庭、医院和社区环境中儿童水痘暴露的许可前数据表明,如果在暴露于皮疹的3天内,可能长达5天内给未接种疫苗的儿童施用单抗原水痘疫苗,则可有效预防疾病或减轻水痘的严重程度(78,101,192)。暴露于皮疹3天内接种疫苗>90%有效预防水痘,而在暴露于皮疹5天内接种疫苗大约70%有效预防水痘,100%有效改善严重疾病(101,192)。有限的上市后研究也表明,如果在暴露后3天内接种水痘疫苗(193,194)。对于没有其他免疫证据的未接种者,建议在暴露后接种水痘疫苗。如果暴露于VZV病毒不会导致感染,那么暴露后接种疫苗应该可以预防随后的暴露。如果暴露导致感染,没有证据表明在疾病的症状前或前驱症状阶段使用单抗原水痘疫苗会增加疫苗相关不良事件的风险。没有关于暴露后给1剂疫苗接种者注射第2剂疫苗的潜在益处的数据。然而,对于之前已注射1剂的患者,应考虑注射第2剂,以使其达到最新水平。水痘疫苗暴露后使用的研究仅在儿童中进行。较高比例的成年人对第一剂水痘疫苗没有反应。然而,暴露后的疫苗接种应该提供给没有免疫证据的成年人。尽管暴露后使用水痘疫苗在医院环境中有潜在的应用,但对于没有免疫证据的所有HCP人,建议常规接种疫苗,这是在医疗保健环境中预防水痘的首选方法(195)。最好,HCP应该在他们开始工作时接种疫苗。尚无关于使用复方MMRV raccine进行暴露后预防的数据。
无免疫证据的人,有疫苗接种禁忌症的人,有患严重疾病和并发症风险的人
1969年进行的研究表明,通过在暴露于带状疱疹病毒72小时内给予带状疱疹免疫球蛋白(ZIG)(从从带状疱疹病毒中恢复的患者中制备)来预防非免疫健康儿童的临床水痘(196)。如果在暴露后96小时内接种,ZIG还降低了免疫缺陷者的发病率(196)。VZIG(从通过常规筛选确定具有高VZV抗体滴度的健康志愿者献血者获得的血浆中制备)于1978年上市。血清学和临床评估均表明,该产品在预防或改善暴露于水痘的非免疫、免疫受损人群的临床疾病方面等同于ZIG(197,198)。在一项对暴露96小时内注射VZIG的免疫缺陷儿童的研究中,大约五分之一的暴露导致临床水痘,20分之一的暴露导致亚临床疾病(198)。临床水痘的严重程度(通过大于100个病变或并发症的患者的百分比评估)低于基于历史对照的预期。
目前在美国使用的VZIG产品,VariZIG™(加拿大温尼伯的Cangene Corporation),可根据研究性新药申请扩大准入协议(可在http://www.fda.gov/cber/infosheets/mphvzig020806.htm)。美国的许可申请将来可能会提交给FDA。VariZIG是一种冻干制剂,当适当复溶时,它是大约5%的IgG溶液,可以肌肉注射(199)。VariZIG可通过美国唯一授权经销商(FFF企业公司,加州Temecula)1-800-843-7477或在线获得http://www.fffenterprises.com.
VZIG的注射
VZIG在暴露后尽快注射可提供最大益处,但如果在暴露后96小时才注射可能有效。尚未评估初次暴露后> 96小时注射VZIG的有效性。施用VZIG后提供的保护持续时间未知,但保护应至少持续IG的一个半衰期(即约3周)。水痘疫苗接种禁忌的高危易感人群和接受一剂VZIG后>3周再次暴露的人群,应接受另一剂全剂量的VZIG。每月接受大剂量免疫球蛋白静脉注射(IGIV)的患者(>400 mg/kg)可能受到保护,如果最后一剂IGIV在暴露前< 3周接种,可能不需要VZIG(200)。尚未证明VZIG可用于治疗临床水痘或带状疱疹或预防播散性带状疱疹,因此不推荐使用。VZIG可能会将病毒的潜伏期从10 – 21天延长到>28天。注射VZIG时,暴露后应考虑到这一点。
剂量
VariZIG以125-U小瓶提供。推荐剂量为125 U/10公斤体重,最多625U(五小瓶)。最低剂量为125 U。人IgG含量为每125单位剂量的VariZIG 60-200mg。
注射VZIG进行暴露后预防的适应症
给予VZIG的决定取决于三个因素:1)患者是否缺乏免疫力的证据,2)暴露是否可能导致感染,以及3)患者是否比普通人群有更大的并发症风险。
已证实水痘阳性病史的健康和免疫缺陷儿童和成人(骨髓移植受者除外)可被视为免疫(见免疫证据)。骨髓供体水痘阳性病史与移植后受者水痘易感性之间的关系尚未得到充分研究。因此,接受骨髓移植的人应该被认为是非免疫的,不管他们自己或他们的捐献者以前是否有水痘疾病或水痘疫苗接种史。移植后出现水痘或带状疱疹的骨髓受者应被认为是免疫的。
VZIG不适用于接种过2剂水痘疫苗并在以后的生活中因疾病或治疗而变得免疫低下的人。应对这些人进行密切监测;如果疾病发生,应在最早的体征或症状开始使用阿昔洛韦治疗。对于没有免疫证据和使用类固醇治疗剂量的患者>2 mg/kg体重或总计20mg/天的泼尼松或等效药物,适用于VariZIG。
暴露类型
某些类型的暴露会使没有免疫力证据的人面临水痘风险。直接暴露是指在室内与感染者面对面的接触。持续时间的面对面接触注射VZIG保证不确定。然而,这种暴露不应该是短暂的。某些专家建议,超过5分钟的接触构成重大暴露,而其他专家将密切接触定义为超过1小时(200)。医院接触者的大量暴露包括与传染病患者共用同一病房,或与传染病患者直接面对面接触(如HCP)。与感染者短暂接触(如接触x光技术人员或家政人员)比长期接触更不容易导致VZV病毒传播。
与患有水痘或传播性疱疹的家庭成员持续接触的人感染的风险最大。水痘发生在大约85%(范围:65% – 100%)的暴露于VZV的易感家庭接触者中。局部带状疱疹的传染性远低于水痘或播散性带状疱疹(52)。密切接触后,如在家庭环境中,更有可能从局部带状疱疹传播。在这种情况下,医生可以考虑推荐使用VZIG进行暴露后预防。在家庭暴露于水痘后,注射VZIG的免疫缺陷儿童的发病率高达60%(197)。没有关于未使用VZIG的无免疫证据的免疫缺陷儿童的比较数据。然而,严重疾病(定义为> 100处皮肤损伤)的发生率低于正常儿童从疾病自然史预测的发生率(分别为27%和87%),肺炎的发生率低于肿瘤儿童的发生率(分别为6%和25%)(201)。密切接触(如与玩伴接触)或医院暴露后患水痘的风险估计约为家庭暴露风险的20%。
出生后7天内在子宫内暴露于VZV并在出生后接受VZIG治疗的健康新生儿的发病率为62%,这与报道的类似,暴露但未接受VZIG治疗的新生儿的发病率没有显著差异(49)。然而,接受VZIG治疗的新生儿比未接受VZIG治疗的新生儿并发症和致命性结果的发生率显著降低。
在一项研究中,对VZV没有免疫力的孕妇暴露于水痘并注射VZIG,感染率为30%。这大大低于未接种过水痘疫苗的女性的预期发病率(70%以上)199,202)。
使用VZIG的建议
以下患者群体有患水痘严重疾病和并发症的风险,应接受VZIG治疗:免疫力低下的病人。VZIG主要用于直接接触水痘或播散性带状疱疹患者后无免疫证据的免疫缺陷者的被动免疫,包括1)患有原发性和获得性免疫缺陷疾病,2)患有肿瘤疾病,以及3)正在接受免疫抑制治疗的人。接受每月高剂量IGIV的患者(>400 mg/kg)可能受到保护,并且如果施用最后剂量的IGIV,可能不需要VZIG<暴露前3周(200)。
母亲在分娩时有水痘症状和体征的新生儿。VZIG适用于母亲在分娩前5天至分娩后2天出现水痘体征和症状的新生儿。对于母亲在分娩前5天以上有水痘体征和症状的新生儿来说,VZIG不是必需的,因为这些婴儿应通过经胎盘获得的母体抗体来防止严重水痘。没有证据表明,分娩后48小时以上发生水痘的母亲所生的婴儿患严重并发症(如肺炎或死亡)的风险增加。
早产儿出生后暴露。水痘在医院托儿所的传播是罕见的,因为大多数新生儿受到母体抗体的保护。出生后有大量暴露的早产儿应进行个体化评估。早产儿出生后获得性水痘并发症的风险未知。然而,由于早产儿的免疫系统尚未完全发育,因此对出生于>28周、在新生儿期暴露且其母亲没有免疫证据的妇女,注射VZIG。小于28周出生的早产儿或体重<1,000 g并在新生儿期暴露的婴儿应注射VZIG,而不考虑母体免疫,因为这些婴儿可能没有获得母体抗体。大多数早产儿出生于孕>28周至免疫母亲有足够的获得性母源抗体来保护她们免受严重疾病和并发症。虽然婴儿发生严重和致命并发症的风险高于较大的儿童,但出生后暴露于水痘的健康足月婴儿的风险大大低于母亲在分娩前5天至分娩后2天感染的婴儿。不建议出生后暴露的健康足月婴儿使用VZIG,即使他们的母亲没有水痘感染史。
孕妇。因为孕妇患严重水痘和并发症的风险更高(37,42,203),对于已经暴露的无免疫证据的孕妇,应强烈考虑使用VZIG。尚未发现对这些妇女施用VZIG可预防病毒血症、胎儿感染、先天性水痘综合征或新生儿水痘。因此,孕妇VZIG的主要适应症是预防母亲水痘并发症,而不是保护胎儿。分娩前5天至分娩后2天出现水痘症状和体征的母亲所生的新生儿应注射VZIG,无论母亲是否注射VZIG。
注射VZIG和水痘疫苗的间隔时间
任何接受VZIG预防水痘的患者应随后接受水痘疫苗,前提是该疫苗无禁忌。水痘疫苗接种应推迟至VZIG注射后5个月。如果患者在注射VZIG后出现水痘,则无需接种水痘疫苗。
抗病毒治疗
因为VZIG可能会延长潜伏期>1周,任何接受VZIG的患者应在暴露后28天内密切观察水痘的体征或症状。如果出现水痘疾病的体征或症状,应立即开始抗病毒治疗。抗病毒治疗的途径和持续时间应由具体的宿主因素、感染程度和对治疗的初始反应决定。有关如何获取VariZIG的信息,请访问http://www.cdc.gov/mmwr/preview/mmwrhtml/mm5508a5.htm (204)。
致谢
Gregory Wallace(医学博士)、Mary Mulholland(医学硕士)、MA(硕士)、MPH(公共卫生硕士),美国疾病控制和预防中心国家免疫和呼吸系统疾病中心免疫服务部,协助撰写了疫苗储存和处理部分。中国疾病预防控制中心免疫与呼吸系统疾病中心免疫服务部门的周博士进行了经济分析。美国疾病预防控制中心国家免疫和呼吸系统疾病中心病毒疾病部公共卫生硕士Jessica Leung帮助制作了图表、表格和参考资料。
参考
1.疾病控制中心。水痘的预防:免疫实践咨询委员会的建议(ACIP)。MMWR 1996年;45(编号RR-11)。
2.疾病控制中心。水痘的预防:免疫实践咨询委员会的最新建议(ACIP)。MMWR 1999年;48(编号RR-6)。
3.Lopez AS,Guris D,Zimmerman L,等。一剂水痘疫苗不能预防学校爆发:是时候打第二剂了吗?儿科2006;117:e1070 – 7。
4.疾病控制中心。2003年密歇根州接种疫苗儿童水痘爆发。MMWR 2004年;53:389 – 92.
5.Tugwell BD,Lee LE,Gillette H,Lorber EM,Hedberg K,Cieslak PR。在高度接种疫苗的学校人群中爆发水痘。儿科2004;113:455 – 9.
6.Parker AA,Reynolds M,Leung J,等.在没有常规两剂疫苗接种要求的情况下,在水痘爆发期间实施第二剂疫苗接种的挑战-缅因州,2006年。感染疾病(补充)。出版于2007年。
7.水痘的临床表现。在:李北A,格尔森A,编辑。水痘带状疱疹病毒。英国剑桥:剑桥大学出版社;2000:206 – 19.
8.水痘带状疱疹病毒感染的流行病学。传染病临床杂志1996;10:571 – 81.
9.疾病控制中心。对1972 – 1997年美国国家法定疾病监测系统水痘报告的评估。MMWR 1999年;48;55 – 8.
10.芬格R,休斯JP,米德BJ,等。水痘的年龄特异性发病率。酒吧健康代表1994;190:750 – 5.
11.儿童水痘感染的社区影响。《儿科杂志》1997年;130:759 – 65.
12.基尔戈·平、克鲁森-莫兰·D、苏厄德·JF等,《NHANES III美国人水痘:通过常规免疫控制的意义》。医学病毒学杂志2003;70附录1:S111 – 8。
13.朗菲尔德JN,温RE,吉布森RL,朱豪SV,霍夫曼PV。波多黎各新兵水痘爆发。热带人群水痘易感性。Arch Intern Med 1990150:970 – 3.
14.疾病控制中心。2000年墨西哥成年人水痘暴发-阿拉巴马州。MMWR 2000年;49;735 – 6.
15.Garnett GP,Cox MJ,Bundy DAP,Didier JM,St. Catherine J .西印度群岛圣卢西亚水痘带状疱疹病毒的感染年龄。流行病传染1993年;110:361 – 72.
16.热带国家气候因素和人口密度对水痘带状疱疹病毒流行病学的影响。Am J Trop Med Hyg 200164:131 – 6.
17.Mandal BK,Mukherjee PP,Murphy C,Mukherjee R,纳伊克t .热带地区成人对水痘的易感性是一个农村现象,因为以前缺乏接触。j传染疾病调查,1998年;178(补):S52 – 4。
18.Seward J,Galil K,Wharton M .水痘的流行病学。在:李北A,格尔森A,编辑。水痘带状疱疹病毒。英国剑桥:剑桥大学出版社;2000:187 – 205.
19.李BW。印度和东南亚水痘带状疱疹血清流行病学回顾。Trop Med国际卫生1998;3:886 – 90.
20.Galil K,Brown C,Lin F,Seward j . 1988-1999年美国水痘住院病例。儿科传染病杂志2002;21:931 – 5.
21.拉特纳AJ。疫苗时代水痘相关的住院治疗。儿科传染病杂志2002;21:927 – 30.
22.美国引入水痘疫苗后儿童和成人水痘相关住院和费用的下降。儿科2004;114:786 – 92.
23.水痘疫苗接种对卫生保健利用的影响。JAMA 2005294: 797 – 802.
24.雷氏综合征和药物的公共卫生服务研究。试验阶段的报告。新英格兰医学杂志1985;313:849 – 57.
25.雷明顿RL,罗利D,McGee H,等,《1979年至1984年密歇根瑞氏综合征和阿司匹林使用的下降趋势》。儿科学1986;77:93 – 8.
26.Belay ED,Bresee JS,Holman RC,等。1981年至1997年美国的雷氏综合征。新英格兰医学杂志1999;340:1377 – 82.
27.Meyer P,Seward JF,Jumaan AO,Wharton M .水痘死亡率:美国疫苗许可前的趋势,1970 – 1994。j传染疾病2000年;182:383 – 90.
29.阮总部,朱曼奥,苏厄德JF。美国实施水痘疫苗接种后水痘死亡率下降。英国医学杂志2005;352:450 – 8.
30.妊娠和新生儿水痘和带状疱疹。在:李北A,格尔森A,编辑。水痘带状疱疹病毒。英国剑桥:剑桥大学出版社;2000:317 – 47.
31.卢曼等人,程普利,朱曼奥,苏厄德JF。美国幼儿水痘疫苗接种率:消除种族和民族差异的成功故事。儿科2006;117: 999 – 1008.
32.疾病控制中心。2005年美国19-35个月儿童全国、州和城市地区疫苗接种覆盖率。MMWR 2006年;55: 988 – 93.
33.疾病控制中心。1990 – 2001年选定州水痘年发病率的下降。MMWR 2003年;52:884 – 5.
34.苏厄德·JF、沃森·BM、彼得森·CL等,《美国引进水痘疫苗后的水痘疾病,1995 – 2000》。JAMA 2002287:606 – 11.
35.Guris D,Jumaan AO,Mascola L,等,《积极监测点中水痘流行病学的变化》-美国,1995 – 2005年。感染疾病(补充)。出版于2007年。
36.Galil K,Pletcher MJ,Wallace BJ等,《追踪水痘死亡:死亡证明和出院记录的准确性和完整性》,纽约州,1989 – 1995年。Am J公共卫生2002;92:1248 – 50.
37.格申AA,拉克尔R,斯坦伯格S,托普夫-奥尔斯坦B,德鲁辛LM。临产妇女及其子代在生命第一年中的水痘带状疱疹病毒抗体。儿科学1976;58:692 – 6.
38.李北AM的Paryani SG。母亲水痘后宫内感染水痘-带状疱疹病毒。英国医学杂志1986;314:1542 – 6.
39.布鲁内尔PA,科奇马尔GS。婴儿期带状疱疹:宫内感染后未能维持病毒潜伏期。《儿科杂志》1981年;98:71 – 3.
40.宾夕法尼亚州布鲁内尔。妊娠、胎儿和新生儿水痘:管理中的问题。j传染疾病1992年;166(补1):S42 – 7。
41.母亲水痘后的多种先天性缺陷。英国医学杂志1947年;236:534 – 7.
42.妊娠期间水痘-带状疱疹病毒感染。1984年病毒学进展;29:166 – 96.
43.巴尔杜奇J,罗迪斯JF,罗森格伦S,Vintzileos AM,Spivey G,Vosseller C .妊娠早期水痘感染后的妊娠结局妇产科1992年;79:5 – 6.
44.Enders G,Miller E,Cradock-Watson J,Bolley I,里德哈尔夫m .妊娠期水痘和带状疱疹的后果:1739例前瞻性研究。柳叶刀1994;343:1548 – 51.
45.妊娠前20周母亲水痘感染后的结局。英国医学杂志1994;330:901 – 5.
46.迈耶斯法学博士。足月儿的先天性水痘:风险重新考虑。j传染Dis 1974129:215 – 7.
47.宾夕法尼亚州布鲁内尔。胎儿和新生儿水痘带状疱疹感染。塞明·佩里纳托尔1983;7:47 – 56.
48.妊娠期水痘:再探讨。Reprod Toxicol 200621:e410 – 20。
49.白PV,约翰TJ。妊娠晚期水痘后的先天性皮肤溃疡。儿科杂志1979年。94:65 – 7.
50.围产期母亲感染水痘-带状疱疹病毒后给予抗水痘-带状疱疹免疫球蛋白的新生儿的结局柳叶刀1989;2:371 – 3.
51.霍普-辛普森再保险。带状疱疹的本质:一项长期研究和一项新假设。1965年医学会议录;58:9 – 20.
52.布里森M,埃德蒙兹WJ,律师B,等。加拿大和英国水痘带状疱疹病毒感染的流行病学。流行病传染2001年;127:305 – 14.
53.西勒河。带状疱疹的研究,特别是它与水痘的关系。j . Hyg(Lond)1949年;47:253 – 62.
54.接种水痘疫苗的健康儿童中的带状疱疹。儿科传染病杂志2000;19: 169 – 70.
55.接种水痘减毒活疫苗后带状疱疹的发病率。一项针对白血病儿童的研究。英国医学杂志1991;325:1545 – 50.
56.Lawrence R,Gershon AA,Holzman R,Steinberg SP,NIAID水痘疫苗合作研究组。白血病儿童接种水痘疫苗后发生带状疱疹的风险。英国医学杂志1988;318: 543 – 8.
57.水痘疫苗的安全性和有效性的上市后评估。儿科传染病杂志1999;18:1041 – 6.
58.白色CJ。健康儿童水痘疫苗的临床试验。传染病临床杂志1996;10:595 – 608.
59.格申AA。水痘疫苗:罕见的严重问题-但好处仍然大于风险。j传染疾病2003年;188:945 – 7.
60.Brisson M,Edmunds WJ,Gay NJ,Law B,De Serres G .模拟免疫对水痘带状疱疹病毒流行病学的影响。流行病传染2000年;125:651 – 69.
61.朱曼奥,余,杰克逊拉,博克K,加利尔K,苏厄德JF。水痘疫苗接种前后带状疱疹的发病率:1992 – 2002年水痘发病率的降低。j传染疾病2005年;191:2002 – 7.
62.因辛加RP,伊茨勒RF,佩利西尔JM,萨迪耶P,尼卡斯AA。美国行政数据库中带状疱疹的发病率。2005年实习医师杂志;20:748 – 53.
63.Mullooly JP,Riedlinger K,Chun C,Weinmann S,Houston h . 1997-2002年带状疱疹发病率。流行性传染病2005年;133:245 – 53.
64.Yih WK,Brooks DR,列特SM,等. 1998 – 2003年水痘疫苗覆盖率增加期间,通过行为危险因素监测系统(BRFSS)测量的马萨诸塞州水痘和带状疱疹发病率。BMC公共卫生2005;5:68.
65.多纳休·JG,朱波,曼森·JE,普拉特r .带状疱疹的发病率。Arch Intern Med 1995155:1605 – 9.
66.Civen RH,Maupin TJ,Xiao H,Seward J,Jumaan AO,Mascola L .水痘疫苗许可后儿童和青少年带状疱疹的人群研究。在加利福尼亚州圣地亚哥举行的第41届美国传染病学会年会上发表;2003年10月9日至12日。
67.探测器CG,柯克乐,基尼RE。免疫抑制儿童水痘的阿昔洛韦治疗:一项合作研究。《儿科杂志》1982年;101:622 – 5.
68.免疫缺陷儿童静脉注射阿昔洛韦治疗水痘。《儿科杂志》1984年;104:134 – 6.
69.Nyerges G,Meszner Z,Gyarmati E,Kerpel-Fronius S .阿昔洛韦预防免疫缺陷儿童水痘传播。j传染Dis 1988157:309 – 13.
70.巴尔弗HH,凯利JM,苏亚雷斯CS,等。阿昔洛韦治疗水痘在其他健康儿童。《儿科杂志》1990年;116:633 – 9.
71.邓克尔LM,李北AM,惠特利RJ,等。阿昔洛韦治疗正常儿童水痘的对照试验。英国医学杂志1991;325:1539 – 44.
72.Balfour HH Jr,Rotbart HA,Feldman S,等。健康青少年水痘的阿昔洛韦治疗。《儿科杂志》1992年;120:627 – 33.
73.华莱士先生,鲍勒瓦,默里NB,布罗丁SK,奥德菲尔德欧共体三。口服阿昔洛韦治疗成人水痘。安实习医师医学1992;117:358 – 63.
74.口服阿昔洛韦治疗成人水痘。Arch Intern Med 1990150:2061 – 5.
75.美国儿科学会传染病委员会。口服阿昔洛韦在水痘患儿中的应用。儿科学1993;91:674 – 6.
76.Stone KM,Reiff-Eldridge R,White AD,等.产前全身性阿昔洛韦暴露后的妊娠结局:国际阿昔洛韦妊娠登记的结论,1984 – 1999。出生缺陷研究2004 (Pt A)70:201 – 7。
77.口服阿昔洛韦治疗带状疱疹。Am J Med 1988第85页(补编2A):第84 – 9页。
78.匿名泛昔洛韦治疗带状疱疹。1994年药物和治疗学医学通讯;36:97 – 8.
79.Takahashi M,Otsuka T,Okuno Y,浅野长晟Y,Yazaki T .用于预防住院儿童水痘传播的活疫苗。柳叶刀1974;2:1288 – 90.
80.默克公司vari VAX[包装插页]。新泽西州怀特豪斯站:默克公司;1995.
81.默克公司ProQuad(麻疹、腮腺炎、风疹和水痘[Oka/默克]病毒活疫苗)[包装插页]。新泽西州怀特豪斯站:默克公司;2005.
82.怀特·CJ,库特·BJ,希尔德布兰德·CS,等.健康儿童和青少年的水痘疫苗(VARIVAX ):临床试验结果,1987-1989。儿科学1991;87:604 – 10.
83.米查利克德,拉鲁萨PS,斯坦伯格SP,赖特P,爱德华兹K,格尔森AA。接种一剂水痘疫苗后的初次免疫失败可能是健康接种儿童突破性感染的原因。在:第44届美国传染病学会年会,加拿大安大略省多伦多;2006年10月11日至14日。
84.使用统计模型评估抗体反应与水痘保护的相关性。统计医学2002;21:3411 – 30.
85.疫苗接种后六周水痘抗体对疫苗的反应与长期突破性感染的可能性成反比。儿科传染病杂志2002;21:337 – 42.
86.Kuter B,Matthews H,Shinefield H,等。接受一次或两次水痘疫苗注射的健康儿童的十年随访。儿科传染病杂志2004;23:132 – 7.
87.约翰逊行政长官,斯坦辛T,法特拉尔D,罗马LP,库马尔ML。健康儿童水痘疫苗的长期前瞻性研究。儿科学1997;100:761 – 6.
88.浅野长晟Y,盖娜T,宫田T,等。水痘活疫苗OKA株受体的长期保护性免疫。儿科1985;75:667 – 71.
89.浅野长晟Y,菅S,吉川T,等。经验与原因:Oka株水痘活疫苗保护性免疫的20年随访。儿科学1994;94:524 – 6.
90.初次免疫后6年水痘疫苗加强剂量的安全性和细胞及体液免疫应答。j传染疾病调查1995年;172:217 – 9.
91.对健康儿童接种四价麻疹、腮腺炎、风疹和水痘疫苗的评估。儿科传染病杂志2005;24:665 – 9.
92.雷辛格KS,Hoffman Brown ML,Xu J,等。一种麻疹、腮腺炎、风疹和水痘联合疫苗(ProQuad ),接种于4-6岁健康儿童,之前接种过M-M-RII和Varivax。儿科2006;117:265 – 72.
93.库特·BJ、恩加伊·A、帕特森·CM等。Oka株/默克水痘疫苗两种方案的安全性、耐受性和免疫原性®)在健康的青少年和成人中。1995年疫苗;13: 967 – 72.
94.葛松AA,Steinberg SP,LaRussa P,等。水痘疫苗合作研究组。健康成人接种水痘减毒活疫苗。j传染Dis 1988158:132 – 7.
95.Saiman L,LaRussa P,Steinberg SP,等。卫生保健工作者对水痘带状疱疹病毒疫苗免疫的持久性。2001年医院流行病信息;22:279 – 83.
96.Ampofo K,Saiman L,LaRussa P,Steinberg S,Annunziato P,Gershon A .健康成人对水痘减毒活疫苗的免疫持久性。Clin Infect Dis 200234:774 – 9.
97.泽博尼L,纳德S,青木K,李北AM。水痘疫苗免疫儿童和成人后体液免疫和细胞免疫持久性分析。j传染疾病调查,1998年;177:1701 – 4.
98.健康儿童接种一剂或两剂水痘疫苗后的体液免疫和细胞免疫应答。Clin Infect Dis 199520:316 – 9.
99.纳德S,伯根R,夏普M,李北上午。接种水痘减毒活疫苗的儿童和成人对水痘-带状疱疹病毒的细胞免疫的年龄相关差异。j传染疾病调查1995年;171:13 – 7.
100.怀特·希杰,库特·BJ,恩加伊·阿,等。水痘疫苗接种后水痘的改良病例:保护作用与抗体反应的相关性。儿科传染病杂志1992;11:19 – 23.
101.克拉DL,赵我,施菲尔德T,埃利斯RW。对Oka/Merck水痘活疫苗(VARIVAX)的gpELISA和中和抗体反应的比较®)在儿童和成人中。1997年疫苗;15:61 – 4.
102.阿尔比特上午,斯塔尔东南,普罗特金萨。健康儿童和成人水痘疫苗研究。儿科学1986;78(补编):748 – 56。
103.克劳斯公关,克林曼营销。水痘减毒活疫苗的效力、免疫原性、安全性和使用。《儿科杂志》1995年;127:518 – 25.
104.韦贝尔·雷,内夫·BJ,库特·BJ等,《水痘减毒活疫苗:健康儿童疗效试验》。英国医学杂志1984;310:1409 – 15.
105.Gershon AA,Takahashi M,Seward J .水痘疫苗。载于:Plotkin SA,Orenstein WA编辑。疫苗。第四版。费城:WB桑德斯公司;2004.
106.库特·BJ、韦贝尔·雷、盖斯·哈等,《健康儿童Oka/默克水痘疫苗:2年疗效研究和7年随访研究的最终报告》。1991年疫苗;9:643 – 7.
107.苏厄德·JF,马林·M,瓦斯奎兹·M。美国疫苗接种计划中水痘疫苗的有效性:综述。感染疾病(补充)。出版于2007年。
108.疫苗许可后水痘爆发:他们应该让你吃鸡吗?儿科1999;104:561 – 3.
109.伊利诺伊州学龄前和小学儿童水痘暴发。Clin Infect Dis 200235:102 – 4.
110.伊苏列塔HS,斯特雷贝尔下午,布莱克PA。水痘疫苗在儿童保健中心爆发期间的许可后有效性。JAMA 1997278:1495 – 9.
111.Galil K,Fair E,Mountcastle N,Britz P,Seward J .接种疫苗时年龄较小可能增加水痘疫苗失败的风险。j传染疾病研究所2002年;186:102 – 5.
112.Marin M,Nguyen HQ,Keen J,等,《补充疫苗接种的重要性:2002 – 2003年缅因州水痘暴发的经验》。儿科2005;115:900 – 5.
113.疾病控制中心。2004年内布拉斯加州接种疫苗儿童水痘爆发。MMWR 2006年;55;749 – 52.
114.2002 – 2003年犹他州学龄儿童水痘暴发期间疫苗的有效性。儿科2005;115:1488 – 93.
115.Galil K,Lee B,Strine T,等:尽管接种了疫苗,但一家日托中心爆发水痘。英国医学杂志2002;347:1909 – 15.
116.李BR,费弗SL,米勒CA,赫德伯格CW,Ehresmann KR。归因于疫苗失败的水痘小学爆发:政策含义。j感染疾病信息系统2004年;190:477 – 83.
117.Clements DA,Moreira SP,Coplan PM,Bland CL,Walter EB日托机构水痘疫苗有效性的许可后研究。儿科传染病杂志1999;18:1047 – 50.
118.Vázquez医学博士,LaRussa PS,Gershon AA,Steinberg SP,Freudigman KF,Shapiro E .水痘疫苗在临床实践中的有效性。英国医学杂志2001;344:955 – 60.
119.Vázquez MD,LaRussa PS,Gershon AA,等.水痘疫苗随时间的有效性。JAMA 2004291:851 – 5.
120.苏厄德,张,毛平TJ,马斯科拉L,朱曼奥。接种疫苗病例中水痘的传染性:一项家庭接触研究。JAMA 2004292:704 – 8.
121.Bernstein HH,Rothstein EP,Pennridge Pediatric Associates,等。接种Oka/Merck水痘减毒活疫苗后自然水痘与突破性水痘的临床调查比较。儿科学1993;92:833 – 7.
122.沃森BM,皮尔西SA,普洛特金SA,斯塔尔SE。Oka/Merck水痘疫苗免疫儿童的改良水痘。儿科学1993;91:17 – 22.
123.健康儿童水痘疫苗试验:比较和随访研究摘要。Am J Dis Child 1984138:434 – 8.
124.维塞·SJR,陈茜,库特·BJ等。儿童水痘疫苗接种:抗体持久性,保护持续时间和疫苗效力。2001年儿科杂志;139:297 – 304
125.Chaves SS,Zhang J,Civen R,等。1997 – 2005年接种疫苗人群中水痘的临床和流行病学特征。感染疾病(补充)。出版于2007年。
126.疫苗安全数据链研究组。水痘疫苗失败与哮喘、类固醇使用、疫苗接种年龄和麻疹-腮腺炎-风疹疫苗接种之间关系的回顾性队列研究。儿科2003;112: e98 – 103。
127.Chaves SS,Gargiullo P,张,等。水痘疫苗诱导的免疫随时间的推移而丧失。英国医学杂志2007;356:1121 – 9.
128.Black S,Ray P,Shinefield H,Saddier P和Nikas A .北加州Kaiser Permanente水痘疫苗接种年龄与突破性疾病风险缺乏关联。感染疾病。出版于2007年。
129.Peterson CL,Vugia DJ,Meyers HB,等。水痘患儿侵袭性A组链球菌感染的危险因素:一项病例对照研究。儿科传染病杂志1996;15:151 – 6.
130.西尔克·HJ,瓜伊-伍德福德L,佩雷兹-阿泰德AR,Geha RS,布罗夫医学博士:类固醇依赖性哮喘中的致命水痘。变态反应临床免疫学杂志1988;81:47 – 51.
131.Dowell SF,Bresee JS。类固醇使用相关的严重水痘。儿科学1993;92:223 – 8.
132.奥尔特SJ,哈蒙德JA,麦克维CJ,迈尔斯MG。高暴露风险成人对水痘带状疱疹病毒的易感性。Am J感染控制1986;7:448 – 51.
133.斯特鲁因JP,海姆斯KC,图勒JE,格雷GC。年轻人患麻疹、腮腺炎和水痘的风险:美国海军和海军陆战队新兵的血清调查。1993年美国公共卫生杂志;83:1717 – 20.
134.麦金尼WP,霍洛维茨MM,巴蒂奥拉RJ。医院保健人员对水痘-带状疱疹病毒感染的易感性。Am J感染控制1989;17:26 – 30.
135.Perella D,Fiks A,Spain CV,等.报告的水痘病史作为水痘带状疱疹病毒免疫标记的有效性[海报]。2005年儿科学术协会年会,DC华盛顿州;2005年5月14日至17日。
136.英格兰贾,苏亚雷斯政务司司长,凯利J,泰特迪,鲍尔弗HH。水痘疫苗与麻疹-腮腺炎-风疹疫苗同时或之后接种的安慰剂对照试验。《儿科杂志》1989年;114:37 – 44.
137.Black SB,Cimino CO,Hansen,J,等.麻疹-腮腺炎-风疹、水痘和风疹的免疫原性和安全性流感嗜血杆菌与未接种七价肺炎球菌结合疫苗的疫苗相比,与第四剂七价肺炎球菌结合疫苗同时接种的b型疫苗。儿科传染病杂志2006;25:306 – 11.
138.麻疹、流行性腮腺炎、风疹和水痘联合疫苗的安全性和免疫原性流感嗜血杆菌B型结合物/乙型肝炎疫苗和三联疫苗-破伤风-无细胞疫苗。儿科传染病杂志2006;25:287 – 92.
139.美国儿童常规水痘疫苗接种计划的成本效益。JAMA 1994271:375 – 81.
140.恩加伊等人,斯塔勒博,库特BJ等。健康儿童注射Oka株/默克水痘疫苗一次与两次的安全性和免疫原性。儿科传染病杂志1996;15:49 – 54.
141.水痘疫苗上市后的安全性分析。2001年疫苗;19:916 – 23.
142.Wise RP,Salive ME,Braun MM,等。水痘疫苗上市后安全性监测。JAMA 2000284:1271 – 9.
143.猜哈,布劳顿DD,梅尔顿LJ,第三,库兰有限公司。水痘并发症的人口为基础的研究。儿科学1986;78 (4第2部分):723 – 7。
144.Ghaffar F,Carrick K,Rogers BB,Margraf LR,Krisher K,Ramilo O .表现为腺苷脱氨酶缺乏儿童肝炎的水痘-带状疱疹病毒疫苗株播散性感染。儿科传染病杂志2000;19:764 – 6.
145.Levy O,Orange JS,Hibberd P,等.水痘-带状疱疹病毒疫苗株引起的播散性水痘感染,患者的自然杀伤T细胞存在新的缺陷。j传染疾病2003年;188: 948 – 53.
146.莱文MJ,达尔公里,温伯格,吉勒R,帕特尔A,克劳斯公关。免疫抑制儿童水痘-带状疱疹病毒Oka疫苗株慢性感染期间对阿昔洛韦产生耐药性。j传染疾病2003年;188:954 – 9.
147.Grossberg R,Harpaz R,Rubtcova E,Loparev V,Seward JF,Schmid DS。儿童慢性护理机构中水痘疫苗病毒的二次传播。2006年儿科杂志;148:842 – 4.
148.Salzman MB,Sharrar RG,Steinberg S,LaRussa P .水痘疫苗病毒从一个12个月大的健康婴儿到其怀孕母亲的传播。《儿科杂志》1997年;131:151 – 4.
149.Tsolia M,Gershon AP,Steinberg SP,Gelb L .水痘减毒活疫苗:病毒减毒的证据以及皮肤病变在水痘-带状疱疹病毒传播中的重要性。《儿科杂志》1990年;116:184 – 9.
150.水痘带状疱疹疫苗接种后的血小板减少性紫癜。美国儿科血液肿瘤杂志1986;8:78 – 80.
151.水痘疫苗接种后出现MRI异常病变的急性小脑性共济失调。儿科神经病学1995;13:340 – 2.
152.水痘疫苗接种后的中风。2004年《儿科杂志》;145:845 – 7.
153.水痘疫苗接种后出现与明胶过敏相关的荨麻疹。1999年疫苗;17: 327 – 9.
154.布朗斯坦德,科塔利尔J,沃塔瓦-史密斯JK,等:1名15个月大女童水痘免疫接种后复发性丘疹性荨麻疹。儿科传染病杂志2005;24:269 – 70.
155.猜哈,布劳顿DD,梅尔顿LJ,Kurland LT。儿童和青少年带状疱疹的流行病学:一项基于人群的研究。儿科1985;76:512 – 7.
156.Diaz PS,Au D,Smith S .免疫缺陷儿童在对其同胞进行免疫接种后缺乏水痘减毒活疫苗病毒传播。儿科学1991;87:166 – 70.
157.宾夕法尼亚州布鲁内尔市,Argaw T .水痘可归因于从带状疱疹疫苗接种者处感染的疫苗病毒。儿科2000;106:e28。
158.疾病控制中心。关于免疫的一般性建议:免疫实践咨询委员会的建议(ACIP)。MMWR 2006年;55(编号RR-15)。
159.疾病控制中心。青少年的免疫接种:免疫接种实践咨询委员会、美国儿科学会、美国家庭医师学会和美国医学协会的建议。MMWR 1996年;45(编号RR-13)。
160.莱文MJ、格尔森AA、温伯格A、宋立、芬廷T、诺瓦克B;儿科艾滋病临床试验组265团队。对目前或过去CD4(+) T细胞显著抑制的HIV感染儿童施用水痘活疫苗。j传染疾病2006年;194: 247 – 55.
161.疾病控制中心。麻疹、流行性腮腺炎和风疹——疫苗使用和消除麻疹、风疹和先天性风疹综合征和控制流行性腮腺炎的策略:免疫实践咨询委员会的建议(ACIP)。MMWR 1998年;47(编号RR-8)。
162.高桥M,神谷H,巴巴K,小崎T,堀内K。日本Oka水痘活疫苗的临床经验。1985年获得医学博士学位;61(补编):61 – 7。
163.Bohlke K,Galil K,Jackson LA,等。产后水痘疫苗接种:疫苗病毒是否分泌到母乳中?妇产科2003年;102:970 – 7.
164.Dolbear GL,Moffat J,Falkner C,Wojtowycz M .一项初步研究:产后免疫后母乳中是否存在减毒水痘病毒?妇产科2003年;101(补):S47。
165.迈耶斯法学博士,麦格理MB,梅里根TC,詹尼森MH。医院水痘。第1部分:儿童医院肿瘤患者的爆发。西J医学1979;130:196 – 9.
166.Morens DM,Bregman DJ,West CM,等。癌症患者中水痘带状疱疹病毒感染的爆发。安实习生医学1980;93:414 – 9.
167.巴尔的摩遥感。儿科重症监护室的医院感染。耶鲁大学生物医学1984年;57:185 – 97.
168.古斯塔夫森TL,谢哈卜Z,布鲁内尔PA。新生儿重症监护病房水痘爆发。Am J Dis Child 1984138:548 – 50.
169.海姆斯·PJ、斯图维·麦克、海泽诉医院员工带状疱疹引起水痘:一种随意态度的代价。Am J感染控制1984;12:2 – 5.
170.谢哈卜ZM,布鲁内尔宾夕法尼亚州。医院人员对水痘带状疱疹病毒的易感性。j传染Dis 1984150:786.
171.魏特康先生,尚P,但RC。控制院内水痘-带状疱疹病毒感染的算法。Am J感染控制1985;13:193 – 8.
172.Krasinski K,Holzman RS,LaCouture R,Florman A .水痘带状疱疹病毒的医院经验。感染控制1986;7:312 – 6.
173.医院人员中的水痘:对感染控制从业者的挑战。Am J感染控制1987;15:207 – 11.
174.大学医院水痘预防的影响和成本。美国公共卫生杂志,1988年;78: 19 – 23.
175.加纳JS。医院隔离预防措施指南。传染病控制医院Epid 199617:54 – 80.
176.博利亚德EA,塔布兰,OC,威廉姆斯WW。以及其他人医护人员感染控制指南,1998年:医院感染控制实践咨询委员会。传染病控制医院Epid 199919:407 – 63.
177.浅野长晟Y,岩山S,宫田T,等。水痘在与带状疱疹无直接接触的住院儿童中的传播及其通过活疫苗的预防。比肯J 198023:157 – 61.
178.勒克莱尔JM,扎亚贾,莱文MJ,康东RG,戈德曼达。医院水痘的空气传播。英国医学杂志1980年;302:450 – 3.
179.Gustafson TL,Lavely GB,Brawner ER,哈奇森RH,Wright PF,Schaffner W .一次空气传播的院内水痘暴发。儿科学1982;70:550 – 6.
180.约瑟夫森A,冈伯特我。局部带状疱疹引起的院内水痘空气传播。j传染Dis 1988158:238 – 41.
181.Sawyer MH,Chamberlin CJ,Wu,Aintablian N,Wallace先生在医院病房空气样本中检测水痘带状疱疹病毒DNA。j传染疾病调查1994年;169:91 – 4.
182.斯坦伯格SP,格申AA。使用乳胶凝集试验测量水痘带状疱疹病毒抗体。临床微生物学杂志1991;29:1527 – 9.
183.格尔森AA,拉鲁萨PS,斯坦伯格SP。用乳胶凝集试验检测水痘带状疱疹病毒抗体。临床诊断病毒学1994;2:271 – 7.
184.Behrman A,Schmid DS,Crivaro A,Watson B .医护人员中水痘带状疱疹病毒滴度假阳性的原发性水痘病例群集传染病控制医院,2003年;24:202 – 6.
185.Hall S,Galil K,Seward J和Watson B .利用基于学校的疫苗接种诊所控制两所学校的水痘暴发。儿科2000;105:e17 – 20。
186.莱迪克E,库特BJ,扎亚茨巴,猜哈,国家过敏和传染病研究所水痘疫苗合作研究组。接受Oka/Merck水痘疫苗的急性淋巴细胞白血病儿童中类固醇治疗与疫苗相关皮疹的关系疫苗1989;7:549 – 53.
187.疾病控制中心。VARIVAX妊娠登记处的建立。MMWR 1996年;45:239.
188.Shields KE,Galil K,Seward J,Sharrar RG,Cordero JF,Slater E .妊娠期水痘疫苗暴露:妊娠登记前5年的数据。妇产科2001年;98:14 – 9.
189.Wilson E,Goss MA,Marin M,等。妊娠期水痘疫苗暴露:来自妊娠登记十年的数据。感染疾病。出版于2007年。
190.Dennehy PH,Saracen CL,Peter G .上呼吸道感染儿童接种麻疹-腮腺炎-风疹-水痘(MMRV)联合疫苗后的血清转换率。儿科学1994;94:514 – 6.
191.法里索公里,斯泰尔-格林宾夕法尼亚州,马科维兹勒,柏特莱卡宾夕法尼亚州。疫苗接种水平和麻疹疫苗接种的错失机会:一项公共儿科诊所的记录审计。儿科学1992;89:589 – 92.
192.免疫球蛋白对麻疹和风疹免疫的干扰。《儿科杂志》1993年;122:204 – 11.
193.浅野长晟Y,中山H,Yazaki T,等。通过立即接种水痘活疫苗预防家庭接触者感染水痘。儿科学1977;59:3 – 7.
194.活动性水痘患儿兄弟姐妹暴露后水痘疫苗接种。儿科传染病杂志1998;17:256 – 7.
195.沃森B,苏厄德J,杨A,等。水痘疫苗暴露后的有效性。儿科2000;105:84 – 8.
196.疾病控制中心。卫生保健工作者的免疫接种:免疫接种实践咨询委员会(ACIP)和医院感染控制实践咨询委员会(HICPAC)的建议。MMWR 1997年;46(编号RR-18)。
197.疾病控制中心。水痘带状疱疹免疫球蛋白用于预防水痘。MMWR 1984;33:84 – 90, 95 – 100.
198.水痘-带状疱疹免疫球蛋白的评估:家庭暴露于水痘后对免疫抑制儿童的保护。J Infect Dis 1983147:737 – 43.
199.莱文MJ,纳尔逊WL,普雷布鲁德老,扎亚JA。水痘带状疱疹免疫球蛋白的临床试验。静脉注射免疫球蛋白的临床应用。英国伦敦:学术出版社有限公司;1986:255 – 67.
200.Cangene公司。VariZIG[包装插页]。加拿大温尼伯:Cangene公司;2005.可从以下网址获得http://www.cangene.com/pdf/VariZIG_Monograph.English.pdf.
201.美国儿科学会。水痘带状疱疹感染。在:皮克林路,编辑。红皮书:传染病委员会2006年报告。第27版。伊利诺伊州埃尔克格罗夫村:美国儿科学会;2006:711 – 25.
202.疱疹病毒感染被动免疫的现状。载于:Alving BM,Finlayson JS,eds。免疫球蛋白:静脉注射制剂的特点和应用。马里兰州贝塞斯达:美国卫生与人类服务部;1980年(DHHS出版物编号[FDA] 80-9005):111 – 21。
203.华莱士先生,鲍勒瓦,默里NB,布罗丁SK,奥德菲尔德欧共体三。口服阿昔洛韦治疗成人水痘。安实习医师医学1992;117:358 – 63.
204.哈里斯河,罗迪斯河。妊娠合并水痘肺炎:病例报告及文献回顾。妇产科1965年;25:734 – 40.
205.疾病控制中心。一种用于水痘暴露后预防的新产品(VariZIG ),根据一项研究性新药申请扩大准入方案提供。MMWR 2006年;55:209 – 10.
*在编写本报告期间,Dalya Güris是美国疾病预防控制中心国家免疫和呼吸系统疾病中心病毒疾病部的一名员工。她目前受雇于新泽西州怀特豪斯站的默克公司。
†在本报告中,功效是指在理想条件下特定干预措施产生有益结果的程度。
§数字范围中的破折号用于表示包括年、小时、天、年龄、剂量或一系列编号项目。
¶ 在本报告中,有效性是指某一特定干预措施在实地部署时,对特定人群发挥预期作用的程度。
使用辅助技术的人可能无法完全访问此文件中的信息。如需帮助,请发送电子邮件至:mmwrq@cdc.gov。在电子邮件的主题行中键入508住宿和报告标题。
附录
水痘疫苗接种建议摘要
常规童年时间表
- 常规儿童期疫苗接种应为2剂。
- 学龄前儿童应在12 – 15个月时接种第一剂水痘疫苗。
- 学龄儿童应在4 – 6岁时接种第二剂疫苗(如果第一次接种后已经>3个月)
>13岁的人
>13岁的人应接种2剂疫苗,剂次(间隔4 – 8周)。
所有没有免疫证据的青少年和成人都应该接种疫苗。
由于其增加了向严重疾病高危人群传播的风险或增加了暴露风险,疫苗接种对于以下人群中无免疫证据的人尤其重要:
-与严重并发症高危人群有密切接触的人(例如,保健人员和免疫缺陷者的家庭接触者);
-在可能传播水痘带状疱疹病毒的环境中生活或工作的人(例如,教师、儿童保育工作者以及机构中的居民和工作人员);
-生活和工作在据报有传播的环境中的人(例如大学生、囚犯和教养机构工作人员、军事人员);
-育龄非怀孕妇女;
-生活在有子女家庭中的青少年和成人;和
-国际旅行者。
产前评估和产后疫苗接种
建议对妇女进行水痘免疫证据的产前评估。妊娠结束或终止后,没有水痘免疫证据的妇女应接种疫苗。
艾滋病毒感染者接种疫苗
应考虑对感染艾滋病毒的儿童进行疫苗接种,其CD4+ T淋巴细胞百分比具有年龄特异性>15%,可考虑用于CD4+ T淋巴细胞计数的青少年和成人>200个细胞/µ长度
爆发控制
两剂疫苗接种政策
暴露后预防
建议在3 – 5天内
进入儿童保育、学校、大学和其他中学后教育机构的要求
所有州应要求所有年级(包括大学)的学生和儿童保育中心的学生接种水痘疫苗,除非他们有水痘免疫的其他证据。
水痘免疫的证据
水痘免疫证据包括以下任何一种:
水痘疫苗适龄接种记录:
-学龄前儿童(即>12个月):1剂
-学龄儿童、青少年和成人:2剂*
免疫的实验室证据†或疾病的实验室确认;
1980年前在美国出生§;
保健提供者对水痘病史的诊断或验证¶;或者
保健提供者对带状疱疹病史的诊断或验证。
*适用于在13岁以下接受首剂注射的儿童,且两次注射的间隔时间为>28天,第二剂被认为有效。
†商业试验可用于评估疾病诱导的免疫,但它们缺乏总是检测疫苗诱导的免疫的灵敏度(即,它们可能产生假阴性结果)。
§对于卫生保健人员、孕妇和免疫缺陷者来说,1980年之前的出生不应被视为免疫的证据。
¶任何健康护理提供者(例如,学校或职业诊所护士、执业护士、医师助理或医师)都可以提供对典型疾病的病史或诊断的核实。对于报告有非典型或轻度病例史或报告有非典型或轻度病例的人,建议由医生或其指定人员进行评估,并应寻求以下之一:1)与典型水痘病例或实验室确认病例的流行病学联系,或2)实验室确认证据,如果是在急性疾病时进行的。当缺乏此类文件时,不应认为患者有有效的病史,因为其他疾病可能类似于轻度非典型水痘。
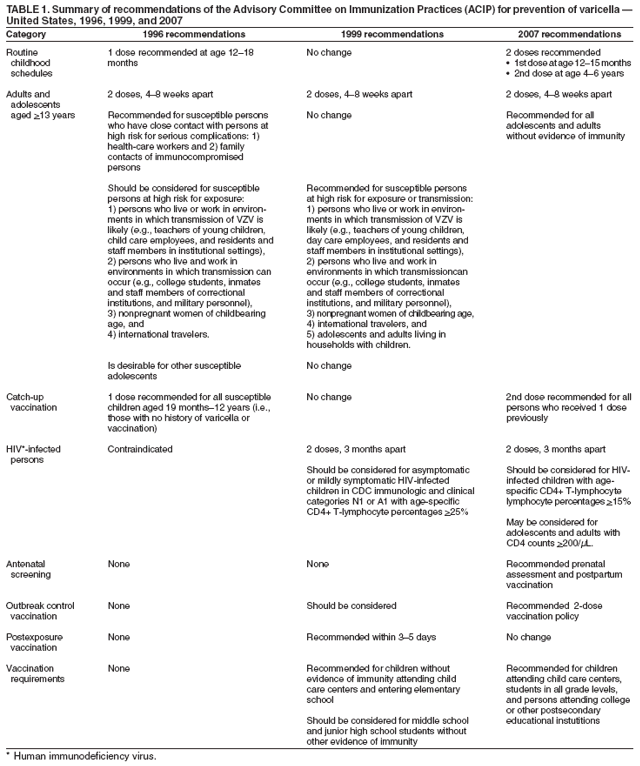
图1
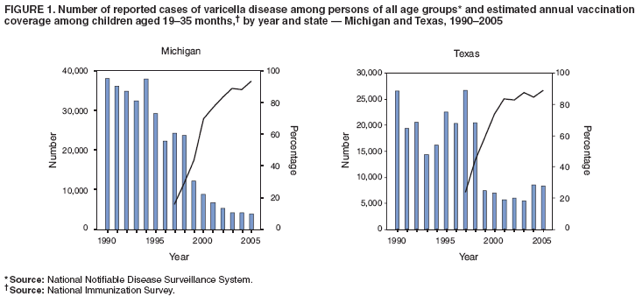
表2

盒子

最近检查日期:2007年4月6日
https://www.cdc.gov/mmwr/preview/mmwrhtml/rr5604a1.htm
Hits: 60
- 年龄≥60岁的成人使用呼吸道合胞病毒疫苗:美国免疫实践咨询委员会的最新建议,2024年
- JYNNEOS(活的、非复制的天花和猴痘疫苗)用于正痘病毒职业暴露危险人群的暴露前疫苗接种:美国免疫实践咨询委员会的建议,2022
- 黄热病疫苗:免疫实践咨询委员会(ACIP)的建议
- 美国成人中15价肺炎球菌结合疫苗和20价肺炎球菌结合疫苗的使用:美国免疫实践咨询委员会的最新建议,2022年
- ACIP建议:新冠肺炎疫苗
- 用疫苗预防和控制季节性流感:美国免疫实践咨询委员会的建议,2024-25流感季节
- ACIP建议:水痘疫苗
- 19岁以上免疫功能低下成年人使用重组带状疱疹疫苗的ACIP证据推荐框架
- ACIP建议:麻疹、腮腺炎和风疹疫苗
- ACIP建议:麻疹、腮腺炎、风疹和水痘疫苗
- ≥6月龄的人使用新冠肺炎疫苗:美国免疫实践咨询委员会的建议,2024–2025
- ACIP建议:白喉、破伤风和百日咳(DTaP/Tdap/Td)疫苗
- 19-59岁成年人普遍接种乙肝疫苗的最新建议——美国,2024年
- 对年龄≥65岁的成人和年龄≥6个月的中度或重度免疫缺陷者使用额外剂量的2024-2025新冠肺炎疫苗:美国免疫实践咨询委员会的建议,2024
- Bexsero MenB-4C疫苗的新接种间隔和时间表:美国免疫实践咨询委员会的最新建议,2024年10月
- 更新:免疫实践咨询委员会关于甲型肝炎疫苗用于国际旅行暴露后预防和暴露前预防的建议
- ACIP建议:甲肝疫苗
- ACIP:50岁以上成人使用肺炎球菌结合疫苗的扩展建议
- ACIP建议:人类乳头瘤病毒(HPV)疫苗
- 免疫接种实践咨询委员会推荐 18 岁或以下儿童和青少年的免疫接种计划 — 美国,2025 年
- 免疫接种实践咨询委员会建议 19 岁或以上成人的免疫接种计划 — 美国,2025 年
- ACIP关于常规脊髓灰质炎病毒免疫接种的最新建议
- 使用 23 价肺炎球菌多糖疫苗 (PPSV23) 预防成人侵袭性肺炎球菌疾病的最新建议
- 21价肺炎球菌结合疫苗在美国成人中的使用:美国免疫实践咨询委员会的建议,2024年
- ACIP 对 ≥65 岁成年人使用额外更新的 2023-2024 年 COVID-19 疫苗剂量 2024年
- ACIP 辉瑞五价脑膜炎球菌疫苗在 ≥10 岁人群中的使用,美国,2023 年
- ACIP美国成人使用灭活脊髓灰质炎疫苗的最新建议,2023年
- 蜱传脑炎疫苗(森林脑炎灭活疫苗):美国免疫实践咨询委员会的建议,2023年
- 妊娠期使用辉瑞呼吸道合胞病毒疫苗预防婴儿呼吸道合胞病毒相关下呼吸道疾病:美国免疫实践咨询委员会的建议,2023
- ACIP 演示幻灯片:2025 年 4 月 15 日至 16 日会议
- 在猴痘爆发期间,≥18 岁有猴痘风险的人使用 JYNNEOS(天花和猴痘疫苗,活疫苗,非复制性):免疫实践咨询委员会的建议 — 美国,2023 年
- ACIP建议:肺炎球菌疫苗
- 用于流感治疗和化学预防的抗病毒药物:免疫实践咨询委员会(ACIP)的建议
- ACIP建议:轮状病毒疫苗
- ACIP 建议:炭疽疫苗
- ACIP 疫苗建议和指南
- 美国免疫实践咨询委员会关于 10 岁及以上人群使用葛兰素史克 MenACWY-CRM/MenB-4C 五价脑膜炎球菌疫苗的建议——2025 年
- ACIP 建议:带状疱疹疫苗
- ACIP关于水痘预防的建议