Molecule helps vaccine to engage killer T cells
约翰·T·威尔逊
含有称为抗原的肽段的疫苗在刺激关键的免疫细胞——杀伤性T细胞方面表现不佳。现在有一种分子使抗原能够遇到这些T细胞。
表位)并加载到MHC-I分子上。对于附加了抗原的分子,作者选择了一个STING蛋白质的激活剂(激动剂)。STING位于内质网表面,能触发类似于病毒感染期间发生的炎症反应。因此,固定的STING激动剂(见图1)不仅将抗原引导至内质网表面以改善交叉呈递,还能推动炎症信号。这些包括表达称为细胞因子和共刺激分子的分子,它们对刺激T细胞和产生有效的T细胞反应至关重要。
作者展示了他们的策略,称为SABER(基于STING激动剂的ER靶向),显著增加了MHC-I上的抗原呈递。同时,SABER激活STING以增加共刺激分子的表达,从而在体外测试中导致CD8+ T细胞的激活增加。作者发现,这依赖于STING激动剂的存在。
被称为杀伤性T细胞(也称为细胞毒性CD8+ T细胞)的免疫细胞在抵御病毒感染和消除肿瘤中起着关键作用。当T细胞受体特异性地识别免疫系统视为外来的蛋白质中的肽段(称为抗原)时,这些T细胞能找到并摧毁它们的靶标。因此,能够引发CD8+ T细胞强烈反应的疫苗对于预防和治疗多种疾病具有希望。然而,临床上使用的绝大多数疫苗往往只能引起CD8+ T细胞的微弱反应,而是通过激活免疫系统的其他组成部分来提供保护。在《自然》杂志上发表的一篇文章中,王等人描述了一种刺激CD8+ T细胞的疫苗技术,并在癌症和SARS-CoV-2感染的小鼠模型中显示出希望。
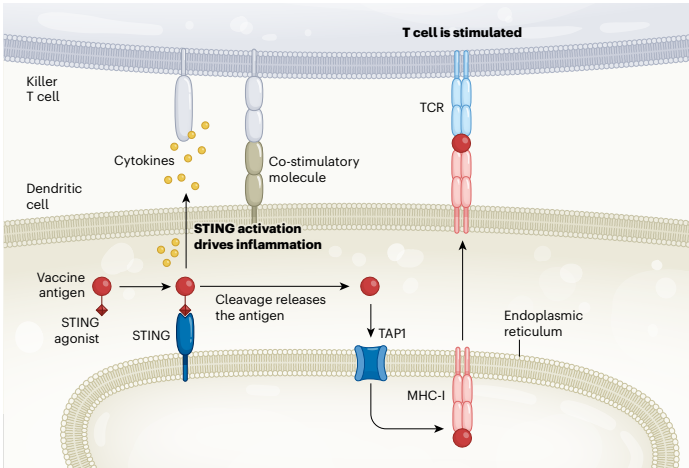
从CD8+ T细胞产生反应需要外源性抗原被免疫细胞(称为树突状细胞)摄取,分解成较小的肽片段,并在细胞表面结合主要组织相容性复合体I(MHC-I)分子呈现。这一过程称为交叉呈递,使CD8+ T细胞能够识别并与特定抗原结合,从而刺激T细胞获得其细胞杀伤能力。然而,交叉呈递效率低下,是从CD8+ T细胞对抗原产生反应的主要瓶颈。这一挑战激发了数十年的研究,致力于开发工程疫苗技术,将抗原导向称为淋巴结的免疫细胞刺激器官,将抗原靶向树突状细胞,或增加抗原向细胞质的传递,以便接触与生成抗原结合MHC-I复合物相关的机制。
以特定方向与抗原结合,使得激动剂能与内质网表面的STING结合,并且该肽段能被酶切割,以便在ER中加载到MHC-I分子上。
该研究还揭示了一种以前未知的促进交叉呈递的机制,该机制利用ER膜上STING的聚集来组装细胞内的“微型反应器”。这些微型反应器通过在小空间集中分子,从而增加抗原与MHC-I分子的相互作用以及与抗原处理和MHC-I加载所需的关键机制的相互作用。需要更多研究来进一步剖析这一机制,并确定肽类抗原的特定分子特征是否促进这一过程。此外,人类群体中存在几种版本的STING,因此在不同类型的STING中检验这一现象至关重要。
抗原体积小,因此在体内给药后通常会迅速被清除,导致树突状细胞的摄取极微。携带SABER结合抗原的小鼠产生了较弱的T细胞反应。为了克服这一障碍,作者将SABER抗原包装进脂质囊泡,即纳米颗粒,这些囊泡使用了与SARS-CoV-2信使RNA疫苗相同的脂质。这种包装使SABER抗原更好地进入淋巴结中的树突状细胞,并帮助SABER肽进入细胞质,从而更有效地接触STING。
通过使用脂质纳米颗粒,作者发现SABER疫苗能刺激CD8+T细胞对多种抗原产生强烈反应。这一结果仅在抗原与STING激动剂连接时实现。在小鼠测试中,SABER疫苗的表现优于几种已建立的疫苗配方。
刺激免疫细胞针对癌症的治疗方法彻底改变了癌症治疗。然而,许多人对临床批准的称为免疫检查点抑制剂(ICIs)的免疫疗法没有反应。在某些情况下,这可能是
部分原因是由于识别肿瘤细胞抗原的CD8+ T细胞数量不足,或者这些T细胞杀死靶细胞的能力受损。这些问题激发了人们对开发癌症疫苗的兴趣,以改善对免疫检查点抑制剂(ICIs)的反应。作者证明,SABER疫苗在小鼠模型中对肿瘤生长有显著的抑制作用,并增加了淋巴瘤、黑色素瘤和结肠癌的生存时间。王及其同事还报告称,使用他们的方法提高了小鼠黑色素瘤对免疫检查点抑制剂的反应。
SABER疫苗非常适合进行临床试验,作为癌症疫苗——它们在小鼠中安全,SABER肽可以按相关规模轻松生产,类似的STING激动剂正在进行临床试验,而且脂质纳米粒子被广泛使用。一个关键问题是,与其他新兴疫苗选择相比,SABER在驱动强效免疫反应、安全性以及制造便捷性方面的比较情况如何。
值得注意的是,目前mRNA癌症疫苗正在临床研究中,并且已经报告了令人满意的结果。因此,有必要对比不同技术的实际效果和免疫接种情况。此外,相比之下,mRNA提供了一个更为模块化的系统,编码多种癌症抗原的mRNA可以轻松用于个性化疫苗。相比之下,不同的抗原具有不同的化学性质,这可能会影响其驱动免疫反应的能力;尽管将SABER包装在脂质纳米粒子中可以改善其稳定性新型疫苗,纳米粒子制备过程可能需要进一步优化,以确保有效且一致地包封具有不同氨基酸组成的Saber连接抗原。
此外,作者仅用单一抗原免疫小鼠,而许多癌症疫苗使用多达20种独特抗原。评估Saber通过将多种肽载入脂质纳米粒子来扩大CD8+ T细胞反应的程度将是重要的。
尽管如此,与基于mRNA的疫苗相比,肽疫苗具有一些优势,对疫苗的结构和药理学特性有更好的控制。
可能影响免疫反应的因素包括脂质纳米粒子。因此,开发针对其独特作用机制优化的定制传递技术值得研究。
王等人提出了Saber疫苗作为分子工程和免疫学的融合,揭示了一种增强抗原交叉呈递的机制。开发一种创新的疫苗技术以刺激细胞毒性CD8+ T细胞的响应可能有助于设计更好的癌症和其他疾病的疫苗。
约翰·T·威尔逊在田纳西州纳什维尔的范德堡大学化学与生物分子工程系及生物医学工程系,以及病理学、免疫学与微生物学系和范德堡-英格拉姆癌症中心。电子邮件:john.t.wilson@vanderbilt.edu
Hits: 21
