Contents
Guideline for Hand Hygiene in Health-Care Settings
医疗保健感染控制实践的建议 咨询委员会和 HICPAC/SHEA/APIC/IDSA 手部卫生工作组
编撰者:
John M. Boyce, M.D.1
Didier Pittet, M.D.2
1康涅狄格
州纽黑文圣拉斐尔
医院 2日内瓦大学
瑞士日内瓦
本报告中的材料源自美国国家传染病中心主任 James M. Hughes 医学博士;以及医疗保健质量促进部,史蒂夫·所罗门 (Steve Solomon) 医学博士,代理主任。
总结
《卫生保健机构手部卫生指南》为医护人员 (HCW) 提供了 有关医疗保健环境中洗手和手部消毒的数据。此外,它还提供了具体的建议 促进改善手部卫生习惯,减少病原微生物向患者和工作人员的传播 在医疗保健环境中。本报告回顾了自 1985 年 CDC 指南(Garner JS, Favero MS. CDC 洗手和医院环境控制指南,1985 年)以来发表的研究。感染控制 1986;7:231–43)和 1995 年 APIC 指南(Larson EL,APIC 指南委员会。APIC 洗手和手部消毒指南 在医疗保健环境中。Am J 感染对照 1995;23:251–69) 发布,并提供了对 医护人员的手部卫生习惯、人员对推荐洗手习惯的依从性以及对依从性产生不利影响的因素。回顾了关于酒精洗手液体内疗效和与其使用相关的低皮炎发病率的新研究。最近的研究证明了多学科手部卫生促进计划的价值,以及 总结了含酒精的洗手液在改善手部卫生习惯方面的潜在作用。建议 关于相关问题(例如,使用外科手部消毒剂、护手霜或乳霜,以及佩戴人造指甲)也包括在内。
第一部分 手部卫生科学数据回顾
历史视角
正常皮肤细菌菌群
正常皮肤的生理机能
术语定义
实质性。吸附性是某些活性成分的一种属性,这些活性成分粘附在角质层上(即,在冲洗或干燥后仍留在皮肤上),以抑制残留在皮肤上的细菌的生长。
外科手部消毒剂。防腐灯手术人员在术前进行 Dwash 或消毒洗手液 消除短暂性并减少常驻手部菌群。消毒洗涤剂制剂通常具有持久性 抗菌活性。
手明显脏污。手上有可见的污垢或明显被蛋白质物质、血液或其他物质污染 体液(例如粪便或尿液)。
无水防腐剂。一种不需要使用外源性水的防腐剂。涂抹这种试剂后,将双手揉搓在一起,直到试剂干燥。
美国食品药品监督管理局 (FDA) 产品 类别。1994 年 FDA 暂定最终专论 保健消毒药品将产品分为三类,定义如下 (19):
- 患者术前皮肤 制备。一种速效、广谱且持久的含防腐剂制剂 这大大减少了完整皮肤上的微生物数量。
- 消毒洗手液或 HCW 洗手。一种专为频繁使用而设计的含防腐剂的制剂;它减少了 充分清洗、冲洗和干燥后,完整皮肤上的微生物数量达到初始基线水平;它 广谱、速效,并且尽可能持续存在。
- 外科洗手液。一种含防腐剂的制剂,可显著减少微生物的数量 在完整的皮肤上;它是广谱的、快速起效的和持久的。
病原体在手上传播的证据
与医疗保健相关的病原体通过 HCW 的手从一名患者传播到另一名患者需要 事件顺序如下:
- 存在于患者皮肤上的生物体,或脱落到靠近 患者,必须转移到 HCW 手中。
- 这些生物必须能够在人员的手中存活至少几分钟。
- 接下来,工人的洗手或手部消毒剂必须不充分或完全省略,或者用于 手部卫生必须不适当。
- 最后,护理人员受污染的手必须与其他患者直接接触,或者与 将与患者直接接触的无生命物体。
与医疗保健相关的病原体不仅可以从感染或引流的伤口中恢复,还可以从 正常、完整的患者皮肤经常定植区域 (20– 31)。会阴或腹股沟区域通常定植最严重, 但腋窝、躯干和上肢(包括手)也经常定植 (23,25,26,28,30–32)。生物体的数量 (例如,金黄色葡萄球菌、奇异变形杆菌、克雷伯菌属和不动杆菌属。存在于皮肤的完整区域 的某些患者的 100 到 106/cm2 (25,29,31,33)。糖尿病患者、接受透析的患者 慢性肾功能衰竭和慢性皮炎患者可能有完整的皮肤区域被金黄色葡萄球菌定植 (34–41)。因为大约 每天从正常皮肤上脱落106个含有活微生物的皮肤鳞屑 (42),患者病号服、床单、床头家具和患者周围环境中的其他物体很容易被患者菌群污染 (30,43–46)。这种污染特别可能是由葡萄球菌或肠球菌引起的,它们对干燥有抵抗力。
关于导致患者菌群传播到手部的患者护理活动类型的数据有限 人员 (26,45–51)。过去,曾尝试将患者护理活动分层为最有可能 导致手部污染 (52),但这种分层方案从未通过量化 发生的细菌污染。护士的手可能会被 100–1,000 CFU 的克雷伯氏菌感染。 “清洁”活动(例如,抬起患者;测量患者的脉搏、血压或口腔温度;或触摸患者的 手、肩或腹股沟)(48)。同样,在另一项研究中,对触摸奇异疟原虫严重定植患者的腹股沟的护士进行了手部培养 (25);从手套汁样品中回收 10–600 CFU/mL 的这种微生物 护士的手。最近,其他研究人员研究了在涉及直接接触患者伤口护理、血管内导管护理、 呼吸道护理和患者分泌物的处理 (51)。 琼脂指尖印模板用于培养细菌;从指尖回收的细菌数量从 0 到 300 CFU 不等。这项研究的数据表明,患者的直接接触和呼吸道护理最有可能污染手指 的照顾者。革兰阴性杆菌占分离株的 15%,金黄色葡萄球菌占 11%。患者护理活动的持续时间 与 HCW 手部细菌污染的强度密切相关。
医护人员的手可被革兰氏阴性杆菌、金黄色葡萄球菌、肠球菌或梭菌污染 通过执行“清洁程序”或触摸住院患者皮肤的完整区域来艰难 (26,45,46,53)。此外,人员 照护呼吸道合胞病毒 (RSV) 感染婴儿通过进行某些活动(例如 喂养婴儿、换尿布和与婴儿玩耍) (49)。 仅接触过被 婴儿的分泌物也通过用 RSV 污染他们的手并接种他们的口腔或 结膜粘膜。其他研究还证明,医护人员可能仅通过触摸病房中的无生命物体就污染他们的手(或手套) (46,53–56)。没有关于医院手部污染的研究 旨在确定污染是否导致病原体传播给易感患者。
其他研究记录了 HCW 的手被潜在的医疗保健相关病原体污染,但 没有将他们的发现与先前患者接触的特定类型联系起来 (15,17,57–62)。例如,在手套使用之前 在医护人员中很常见,在隔离病房工作的护士中,有 15% 的手上携带 1 x 104 CFU 的金黄色葡萄球菌 (61)。 在综合医院工作的护士中,29% 的手上有金黄色葡萄球菌(中位数:3,800 CFU), 而在皮肤病医院工作的人中有 78% 的手上有这种微生物(中位数:14.3 x 106 CFU)。同样,17%–30% 的护士手上携带革兰氏阴性杆菌(中位数:3,400–38,000 CFU)。一项研究发现,金黄色葡萄球菌可以从 21% 的重症监护病房人员手中回收,21% 的医生和 5% 的护士携带者手上有 >1,000 CFU 的金黄色葡萄球菌 (59)。 另一项研究发现,在神经外科病房工作的人员手上的定植水平较低,平均有 3 个 CFU 的金黄色葡萄球菌和 11 个 CFU 的革兰阴性杆菌 (16)。 系列培养显示,100% 的 HCW 至少携带一次革兰阴性杆菌,并且 64% 的人至少携带一次金黄色葡萄球菌。
手动传动模型
几位研究人员使用不同的实验模型研究了传染源的传播。合一 研究,护士被要求触摸革兰氏阴性杆菌严重定植患者的腹股沟 15 秒—就像 他们正在测量股动脉脉搏 (25)。然后,护士通过用普通肥皂和水洗手或使用酒精洗手液来清洁双手。清洁双手后,他们用手指触摸了一块导尿管材料,然后导尿管 段被培养。研究表明,触摸患者潮湿皮肤的完整区域会转移足够多 生物体到护士的手上,导致随后传播到导管材料,尽管用普通肥皂和水洗手。
还研究了生物体通过手接触从人工污染的“供体”织物传播到清洁的“受体”织物。结果表明,如果供体结构或 手接触时湿透 (63)。总体而言,从受污染的供体织物中获得的生物体中只有 0.06% 通过手接触转移到受体织物上。腐生葡萄球菌、铜绿假单胞菌和沙雷氏菌属在手接触后从受污染织物转移到清洁织物的数量也高于大肠杆菌 (64)。 生物体从湿手转移到各种类型的表面的数量(即 >104)比从彻底干燥的手转移的要多得多 (65)。
手部卫生与保健相关病原体的关系
手部消毒可降低医疗保健相关感染的发生率 (66,67)。 一项使用 1847 年的历史对照表明,在维也纳总医院第一产科诊所分娩的母亲的死亡率在医院工作人员用消毒剂洗手时比用普通肥皂和水洗手时要低得多 (3)。
在 1960 年代,由美国国立卫生研究院 (National Institutes of Health) 和美国联邦健康研究院 (Office of the Ltd) 赞助的一项前瞻性对照试验 外科医生证明,由护士照顾的婴儿在处理金黄色葡萄球菌定植的指示婴儿后不洗手的婴儿比由护士照顾的婴儿更频繁、更迅速地获得该微生物,后者使用六氯酚在婴儿接触之间清洁双手 (68)。该试验提供的证据证明,与 不洗手,在患者接触之间用消毒剂洗手可以减少与医疗保健相关的病原体的传播。
试验研究了用普通肥皂和水洗手与某种形式的手部消毒剂对医疗保健相关感染率的影响 (69,70)。 消毒洗手时,与医疗保健相关的感染率较低 由人员执行 (69)。在另一项研究中,消毒洗手与某些重症监护病房较低的医疗保健相关感染率有关,但在其他病房中则无关 (70)。
与使用普通肥皂洗手或使用含酒精的洗手液相比,使用含洗必泰的清洁剂进行消毒洗手后,与健康保健相关的感染率较低 (71)。 然而,因为在同时使用联合方案的期间只使用了最少量的酒精冲洗,并且因为当氯己定可用时,对政策的依从性更高,确定哪个因素(即手部卫生方案或 依从性差异)很难解释较低的感染率。研究人员还确定,当更换用于卫生洗手的抗菌肥皂时,与医疗保健相关的 MRSA 感染减少 (72,73)。
医院工作人员洗手频率的增加与克雷伯菌属在患者之间的传播减少有关 (48);然而,这些研究并未量化工作人员的洗手水平。在最近的一项研究中,当更多地进行手部消毒时,会减少各种与医疗保健相关的病原体的获取 经常由医院工作人员 (74);这项研究和另一项研究 (75) 记录了 随着对推荐手部卫生措施的依从性提高,与医疗保健相关的感染减少。
疫情调查表明,感染与人手不足或过度拥挤之间存在关联;这种关联一直与手部卫生依从性差有关。暴发期间:中心静脉导管相关血流感染危险因素调查 (76),在调整了混杂因素后,患者到护士 比率仍然是血流感染的独立危险因素,表明护理人员减少低于 Critical Threshold 可能通过危及适当的导管护理而导致此次爆发。护士人手不足会促进 MRSA 在重症监护环境中的传播 (77) 通过放松对基本控制措施(例如手部卫生)的关注。在肠杆菌爆发时 新生儿重症监护病房中的泄殖腔 (78),每天住院儿童的数量高于该病房的最大容量,导致每个儿童的可用空间低于当前的建议。与此同时,值班工作人员的人数大大少于 工作量,这也导致对基本感染控制措施的关注放松。坚持手部卫生 在工作负载高峰期,设备接触前的实践率仅为 25%,但在人员不足和过度拥挤期结束后增加到 70%。监测记录显示,在此期间住院与 四倍 获得医疗保健相关感染的风险增加。这项研究不仅证明了这种关联 在工作量和感染之间,但它也突出了抗菌药物传播的中间原因:对手部卫生政策的遵守不力。
用于评估手部卫生产品功效的方法
当前方法
研究人员采用不同的方法来研究洗手、抗菌洗手以及外科手部消毒规程在体内的功效。各项研究之间存在以下差异:1)在使用测试药剂之前,手部是否特意沾染细菌;2)用于污染手指或手部的方法;3)涂抹在手部的手部卫生产品的用量;4)产品与皮肤接触的时长;5)在使用测试溶液后,从皮肤上采集细菌的方法;6)表述产品功效的方法(即,从皮肤上采集到的细菌减少的百分比,或者从皮肤上释放的细菌的对数减少量)。尽管存在这些差异,大多数研究仍可归入两大类中的一类:专注于去除暂住菌的产品的研究,以及涉及用于去除手部常住菌的产品的研究。 大多数关于医护人员(HCW)手部去除暂住菌产品的研究,都涉及在志愿者使用普通肥皂、抗菌肥皂或无水抗菌剂之前,用特定接种量的测试微生物对志愿者的皮肤进行人为污染。相比之下,针对外科医生术前清洁手部(必须符合外科手部消毒规程)而测试的产品,是在不人为污染志愿者手部的情况下,测试其去除常住菌的能力。
在美国,供医护人员使用的抗菌洗手产品由美国食品药品监督管理局(FDA)的非处方药产品部门(OTC)监管。FDA的《医疗保健用抗菌药品暂定最终专著》(TFM)(19)中概述了医护人员洗手产品和外科术前刷手产品的体外和体内测试要求。供医护人员洗手使用的产品需使用标准化方法进行评估(19)。测试按照测试材料的使用说明进行。在进行基线细菌采样之前,以及在每次使用测试材料洗手之前,将5毫升的粘质沙雷氏菌标准化悬浮液涂抹在手上,然后在手部表面揉搓。将特定用量的测试材料挤到手上,并涂抹在手部和前臂下三分之一处。向手部加入少量自来水,然后在规定时间内充分揉搓出泡沫,覆盖手部和前臂下三分之一的所有表面。然后,志愿者在40摄氏度的自来水下冲洗手部和前臂30秒。需要用测试配方产品洗手十次。在第一次、第三次、第七次和第十次洗手后,将用于采样的橡胶手套或聚乙烯袋戴在左右手上,并向每只手套中加入75毫升采样溶液;手套需在手腕上方扎紧。按摩手部所有表面一分钟,然后无菌采集样本用于定量培养。通常不在采样溶液中添加抗菌剂的中和剂,但如果采样液中抗菌剂的稀释不能实现明显的中和效果,则需向采样溶液中添加针对测试配方的特定中和剂。对于无水配方产品,也采用类似的程序。TFM规定的功效标准如下:首次使用后5分钟内,每只手上的指示菌数量减少2个对数级(log10),第十次使用后5分钟内,每只手上的指示菌数量减少3个对数级(log10)(19)。
供外科术前刷手使用的产品也采用标准化方法进行评估(19)。志愿者需用指甲棒清洁指甲下的污垢,并修剪指甲。取下手上和手臂上的所有首饰。将手和三分之二的前臂在38摄氏度至42摄氏度的自来水中冲洗30秒,然后用不含抗菌成分的肥皂洗手30秒,再在自来水下冲洗30秒。然后就可以确定手部微生物的基线数量。接下来,按照制造商提供的说明,使用测试配方产品进行外科刷手操作。如果配方产品未附带说明,则需对手部和前臂进行两次各5分钟的刷洗,然后冲洗。在5天内进行的一系列11次刷手操作中,确定手部微生物数量相对于基线的减少量。在第1天、第2天和第5天的第一次刷手后1分钟、3小时和6小时对手部进行采样。洗手后,志愿者戴上橡胶手套;然后向其中一只手套中加入75毫升采样溶液,按摩手部所有表面一分钟。然后无菌采集样本并进行定量培养。另一只手套戴在另一只手上保持6小时,然后以同样的方式进行采样。TFM要求,配方产品需在使用后1分钟内使每只手上的细菌数量减少1个对数级(log10),并且在第1天的6小时内,每只手上的细菌细胞数量不得超过基线水平;到计数的第二天结束时,该配方产品必须在使用后1分钟内使每只手上的微生物菌群数量减少2个对数级(log10),到第五天结束时,与既定基线相比,必须在使用后1分钟内使每只手上的微生物菌群数量减少3个对数级(log10)(19)。
在欧洲,评估手卫生制剂功效最广泛使用的方法是欧洲标准1500-1997(EN 1500——化学消毒剂和防腐剂。卫生手部消毒测试方法和要求)(79)。该方法需要12至15名测试志愿者,以及培养18至24小时的大肠杆菌K12肉汤培养物。先用软皂洗手,擦干,然后将手浸入肉汤培养物中至掌骨中部,浸泡5秒钟。将手从肉汤培养物中取出,沥干多余液体,然后在空气中晾干3分钟。通过将每只手的指尖分别在10毫升不含中和剂的胰蛋白胨大豆肉汤(TSB)中揉搓60秒来获取初始细菌回收值。将手从肉汤中取出,按照设定方式用3毫升手部消毒剂进行30秒钟的消毒处理。重复相同操作,总消毒时间不超过60秒。双手在流动水中冲洗5秒钟,然后沥干水分。将每只手的指尖分别在添加了中和剂的10毫升TSB中揉搓。用这些肉汤来获取最终数值。制备回收培养基的10倍稀释液并进行平板接种。在3小时内,用参考消毒剂(60%的2-丙醇[异丙醇])和测试产品对相同的志愿者进行测试。在36摄氏度下培养24小时和48小时后进行菌落计数。使用左手和右手的平均菌落数进行评估。计算对数减少因子,并将其与初始值和最终值进行比较。测试产品的减少因子应优于或等同于参考含酒精手部消毒剂的减少因子,才可被接受。如果存在差异,则使用威尔科克森检验对结果进行统计分析。对数减少值明显低于参考含酒精手部消毒剂(即大约减少4个对数级)的产品被判定为不符合标准。
由于功效标准不同,美国食品药品监督管理局(FDA)的暂定最终专论(TFM)和欧洲EN 1500文件中确立含酒精手部消毒剂的标准也有所不同(1,19,79)。符合FDA TFM功效标准的含酒精手部消毒剂不一定符合EN 1500的功效标准(80)。此外,科学研究尚未确定为了最大限度减少医疗机构中病原体的传播,手上的细菌或其他微生物数量需要减少到何种程度(1,8);目前还不清楚手上的细菌数量必须减少1个对数级(减少90%)、2个对数级(减少99%)、3个对数级(减少99.9%)还是4个对数级(减少99.99%)。还有其他几种方法也被用于衡量消毒剂对各种病毒病原体的功效(81-83)。
传统方法的缺点
评估供 HCW 使用的手部卫生产品的公认方法要求测试志愿者清洗 他们的手用普通或抗菌肥皂 30 秒或 1 分钟,尽管在大多数研究中观察到 医院工作人员洗手的平均时间为 <15 秒 (52,84–89)。研究者数量有限 已使用 15 秒洗手或卫生洗手方案 (90–94)。因此,几乎没有关于 普通肥皂或抗菌肥皂在 HCW 实际使用的条件下的功效。同样,某些 评估用作消毒洗手液的无水消毒剂的公认方法要求将 3 mL 酒精揉入手中 30 秒,然后重复涂抹相同的时间。这种类型的协议也不 反映 HCW 的实际使用模式。此外,用于产品评估的志愿者通常是 HCW 的替代者,他们的手部菌群可能无法反映在卫生保健机构工作人员手上发现的菌群。应使用标准化方案在执业 HCW 中进行进一步研究,以获得更真实的看法 微生物定植和细菌转移和交叉传播的风险 (51)。
用于手部卫生的制剂回顾
普通(非抗菌)肥皂
肥皂是以洗涤剂为基础的产品,含有酯化脂肪酸以及氢氧化钠或氢氧化钾。它们有多种形式,包括块状肥皂、皂纸、皂片和液体制剂。肥皂的清洁作用源于其洗涤剂特性,能够去除手上的污垢、尘土和各种有机物质。普通肥皂即使有抗菌活性,也是微乎其微的。然而,用普通肥皂洗手可以去除附着不牢固的暂居菌。例如,用普通肥皂和水洗手15秒钟,皮肤上的细菌数量可减少0.6至1.1个对数级,而洗手30秒钟,细菌数量可减少1.8至2.8个对数级(1)。不过,在一些研究中,用普通肥皂洗手并未能去除医院工作人员手上的病原体(25,45)。用普通肥皂洗手可能会出现一种看似矛盾的情况,即皮肤上的细菌数量反而增加了(92,95-97)。非抗菌肥皂可能会对皮肤造成相当程度的刺激并导致皮肤干燥(92,96,98),不过在肥皂制剂中添加润肤剂或许可以降低其引起刺激的可能性。偶尔,普通肥皂也会受到污染,这可能会导致工作人员的手被革兰氏阴性杆菌定植(99)。
醇类
大多数含酒精的手部消毒剂含有异丙醇、乙醇、正丙醇,或者是其中两种成分的组合。尽管正丙醇在欧洲部分地区用于含酒精的手部消毒剂已有多年,但在美国,它并未被列入食品药品监督管理局(FDA)的暂定最终专论(TFM)中,作为被批准用于医护人员洗手或外科洗手制剂的有效成分。大多数关于酒精的研究评估了不同浓度的单一酒精。其他研究则集中于两种酒精的组合,或者是含有少量六氯酚、季铵化合物、聚维酮碘、三氯生或葡萄糖酸氯己定的酒精溶液(61,93,100 – 119)。
酒精的抗菌活性可归因于其使蛋白质变性的能力(120)。含有60% – 95%酒精的溶液效果最佳,而浓度更高的酒精效力反而较低(120 – 122),因为在没有水的情况下,蛋白质不易变性(120)。溶液中的酒精含量可以用重量百分比(w/w)表示,该表示方法不受温度或其他变量的影响;也可以用体积百分比(vol/vol)表示,而体积百分比会受到温度、比重和反应浓度的影响(123)。例如,按重量计算70%的酒精,如果在15摄氏度下配制,相当于按体积计算76.8%的酒精;如果在25摄氏度下配制,则相当于80.5%(123)。在手部消毒用的含酒精制剂中,酒精浓度通常用体积百分比表示(19)。
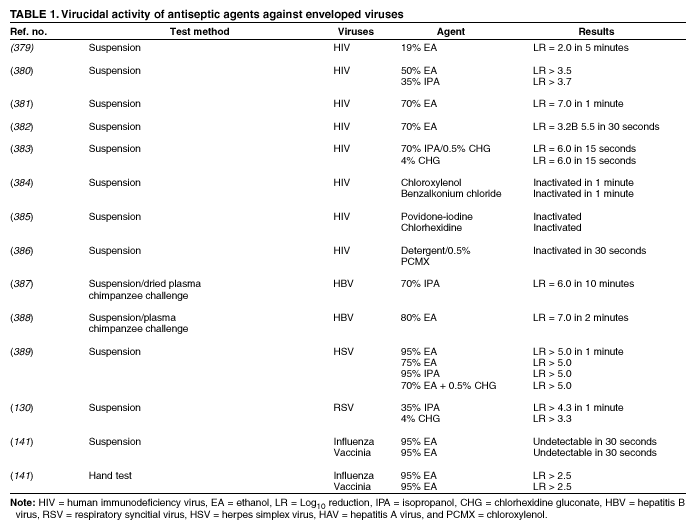
酒精在体外对革兰氏阳性和革兰氏阴性繁殖体细菌具有出色的杀菌活性,这些细菌包括多重耐药病原体(如耐甲氧西林金黄色葡萄球菌[MRSA]和耐万古霉素肠球菌[VRE])、结核分枝杆菌以及各种真菌(120 – 122,124 – 129)。某些有包膜(亲脂性)病毒(如单纯疱疹病毒、人类免疫缺陷病毒[HIV]、流感病毒、呼吸道合胞病毒和牛痘病毒)在体外测试时对酒精敏感(120,130,131)(表1)。乙肝病毒是一种有包膜的病毒,对酒精的敏感性稍低,但可被60% – 70%的酒精杀灭;丙肝病毒也很可能会被这个浓度的酒精杀死(132)。在一个用于研究消毒活性的猪组织载体模型中,发现70%的乙醇和70%的异丙醇比含有4%葡萄糖酸氯己定的抗菌肥皂更能有效地降低有包膜噬菌体的滴度(133)。尽管酒精对这些微生物有效,但它对细菌芽孢、原生动物卵囊以及某些无包膜(非亲脂性)病毒的活性非常差。
众多研究记录了酒精在体内的抗菌活性。酒精能有效地减少手上的细菌数量(14,121,125,134)。通常情况下,对于人工污染的手,涂抹30秒后,测试细菌释放量的对数减少值平均为3.5个对数级,涂抹1分钟后为4.0 – 5.0个对数级(1)。1994年,FDA的TFM将60% – 95%的乙醇归类为I类制剂(即通常认为在用于抗菌洗手或医护人员洗手产品时是安全且有效的)(19)。尽管TFM将70% – 91.3%的异丙醇归为IIIE类(即数据不足,无法归类为有效),但随后60%的异丙醇在欧洲被用作参考标准,用于与含酒精的手部消毒产品进行比较(79)。酒精涂抹在皮肤上时能迅速杀菌,但它没有明显的持续(即残留)活性。然而,使用含酒精的手部消毒剂后,皮肤上细菌的再生长速度较慢,大概是因为酒精对一些皮肤细菌产生了亚致死效应(135,136)。在含酒精的溶液中添加氯己定、季铵化合物、奥替尼啶或三氯生可以产生持续活性(1)。
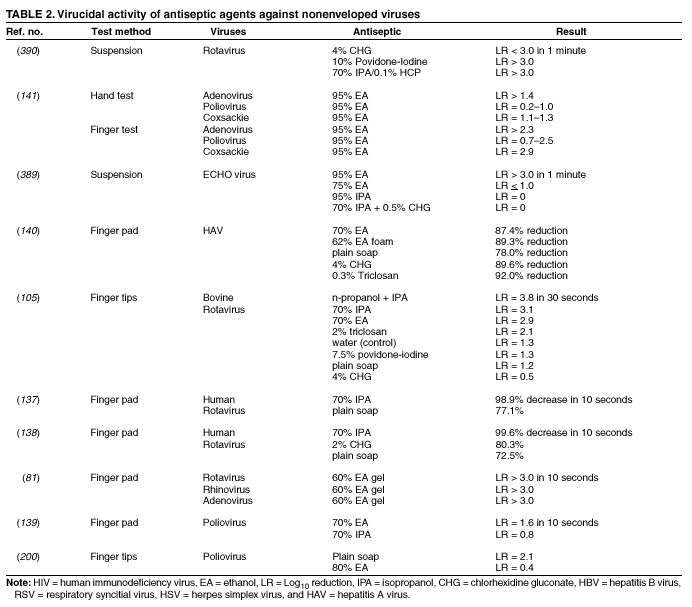
当以含酒精手部消毒剂中的浓度使用时,酒精在体内对几种无包膜病毒也有活性(表2)。例如,在降低指尖垫上轮状病毒滴度方面,70%的异丙醇和70%的乙醇比药皂或非药皂更有效(137,138)。最近一项使用相同测试方法的研究评估了一种市售的含有60%乙醇的产品,发现该产品使三种无包膜病毒(即轮状病毒、腺病毒和鼻病毒)的感染滴度降低了超过3个对数级(81)。其他无包膜病毒,如甲型肝炎病毒和肠道病毒(如脊髓灰质炎病毒)可能需要70% – 80%的酒精才能可靠地灭活(82,139)。然而,70%的乙醇和一种含有润肤剂的62%乙醇泡沫产品在降低整只手或指尖上的甲型肝炎病毒滴度方面,效果都优于非药皂;在降低手上的病毒数量方面,它们与含有4%葡萄糖酸氯己定的抗菌肥皂效果相当(140)。在同一项研究中,70%的乙醇和62%的乙醇泡沫产品对脊髓灰质炎病毒的杀灭活性都比非抗菌肥皂或含有4%葡萄糖酸氯己定的肥皂更强(140)。然而,根据酒精浓度、手接触酒精的时间以及病毒变种的不同,酒精可能对甲型肝炎病毒和其他非亲脂性病毒无效。无包膜病毒的灭活受到温度、消毒剂与病毒的体积比以及蛋白质负载的影响(141)。乙醇对病毒的活性比异丙醇更强。有必要进一步开展关于含酒精制剂和抗菌肥皂的体外和体内研究,以确定在医疗机构中中断病毒直接接触传播所需的最低杀病毒活性水平。
当手明显脏污或被蛋白质类物质污染时,不适合使用酒精。然而,当存在相对少量的蛋白质类物质(如血液)时,乙醇和异丙醇在减少手上存活细菌数量方面可能比普通肥皂或抗菌肥皂更有效(142)。
酒精可以防止医疗相关病原体的传播(25,63,64)。在一项研究中,护士使用含酒精的手部冲洗液进行抗菌手部消毒后,在只有17%的实验中,革兰氏阴性杆菌会从定植患者的皮肤通过护士的手转移到一块导管材料上(25)。相比之下,用普通肥皂和水洗手后,在92%的实验中都会发生细菌转移。这个实验模型表明,当医护人员的手严重污染时,使用含酒精的冲洗液进行抗菌手部消毒比用普通肥皂和水洗手更能有效地防止病原体传播。
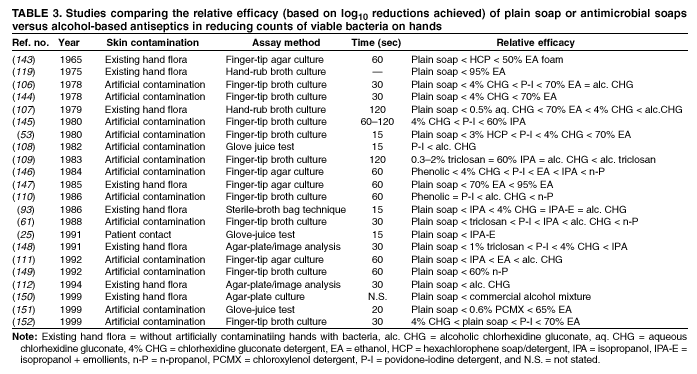
对于医护人员的标准洗手或手部消毒而言,含酒精的产品比普通肥皂或抗菌肥皂更有效(表3)(25,53,61,93,106 – 112,119,143 – 152)。在除了两项之外的所有比较含酒精溶液与抗菌肥皂或洗涤剂的试验中,酒精比使用含有六氯酚、聚维酮碘、4%氯己定或三氯生的肥皂或洗涤剂洗手更能减少手上的细菌数量。在研究对抗菌药物耐药的微生物的实验中,含酒精的产品比用肥皂和水洗手更能有效地减少从医护人员手上分离出的多重耐药病原体的数量(153 – 155)。
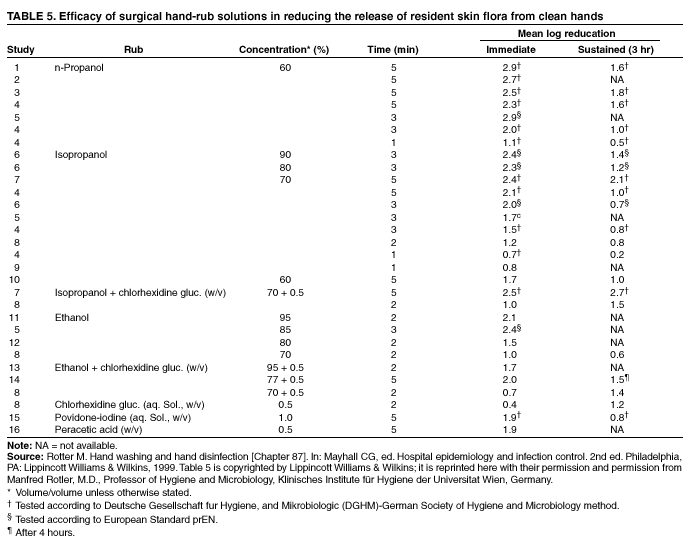
酒精对外科手术人员术前手部清洁有效(1,101,104,113 – 119,135,143,147,156 – 159)(表4和表5)。在多项研究中,在使用产品后立即测定手上的细菌数量,然后在1 – 3小时后再次测定;进行延迟测试是为了确定在手术过程中手上细菌的再生长是否受到抑制。在所有研究中,含酒精的溶液都比用普通肥皂洗手更有效,并且在大多数实验中,它们比抗菌肥皂或洗涤剂更能减少手上的细菌数量(101,104,113 – 119,135,143,147,157 – 159 )。此外,大多数含酒精制剂比聚维酮碘或氯己定更有效。
含酒精的手卫生产品的功效受几个因素影响,包括所用酒精的类型、酒精浓度、接触时间、酒精使用量以及涂抹酒精时手是否湿润。在手上面涂抹少量(即0.2 – 0.5毫升)的酒精并不比用普通肥皂和水洗手更有效(63,64)。一项研究记录表明,1毫升酒精的效果明显不如3毫升酒精(91)。涂抹在手上的理想产品用量尚不清楚,并且可能因不同配方而异。然而,如果在双手相互揉搓10 – 15秒后感觉手是干的,很可能是产品用量不足。由于浸有酒精的湿巾含有的酒精量有限,其效果与肥皂和水相当(63,160,161)。
医院中使用的含酒精手部消毒剂有低粘度冲洗液、凝胶和泡沫等形式。关于各种配方相对功效的数据有限。一项现场试验表明,在减少医护人员手上的细菌数量方面,乙醇凝胶比类似的乙醇溶液稍有效(162)。然而,最近的一项研究表明,冲洗液比所测试的凝胶更能减少手上的细菌数量(80)。有必要进一步开展研究,以确定含酒精冲洗液和凝胶在减少医疗相关病原体传播方面的相对功效。
如果不在含酒精的制剂中添加润肤剂、保湿剂或其他皮肤调理剂,频繁使用含酒精的制剂进行手部消毒会导致皮肤干燥。添加1% – 3%的甘油或其他皮肤调理剂可以减少或消除酒精的干燥作用(90,93,100,101,106,135,143,163,164)。此外,在最近的几项前瞻性试验中,含有润肤剂的含酒精冲洗液或凝胶比所测试的肥皂或抗菌洗涤剂对皮肤的刺激和干燥作用要小得多(96,98,165,166)。这些在临床环境中进行的研究,使用了各种主观和客观方法来评估皮肤刺激和干燥情况。有必要进一步开展研究,以确定不同配方的产品是否会产生类似的效果。
即使是耐受性良好且含有润肤剂的酒精手部消毒剂,在任何破损皮肤(如割伤和擦伤)处也可能会引起短暂的刺痛感。香味浓烈的含酒精手部消毒剂制剂可能会让有呼吸道过敏的医护人员难以忍受。由对酒精或某些含酒精手部消毒剂中存在的各种添加剂过敏引起的过敏性接触性皮炎或接触性荨麻疹综合征很少发生(167,168)。
酒精是易燃的。含酒精手部消毒剂的闪点在21摄氏度到24摄氏度之间,这取决于所含酒精的类型和浓度(169)。因此,应按照美国国家防火协会的建议,将含酒精手部消毒剂存放在远离高温或火焰的地方。在欧洲,含酒精手部消毒剂已被广泛使用多年,与之相关的火灾发生率一直很低(169)。美国最近的一份报告描述了一起闪燃事件,这是由一系列不寻常的事件导致的,其中包括一名医护人员在手上涂抹了酒精凝胶后,立即脱下了一件聚酯隔离服,然后在酒精尚未蒸发时触摸了一扇金属门(170)。脱下聚酯隔离服产生了大量静电,当医护人员触摸金属门时产生了可听见的静电火花,点燃了她手上未蒸发的酒精(170)。这一事件强调了在涂抹含酒精产品后,需要双手相互揉搓,直到所有酒精都蒸发。
由于酒精具有挥发性,容器的设计应尽量减少酒精的蒸发。含酒精溶液受污染的情况很少有报道。有一份报告记录了由蜡样芽孢杆菌芽孢污染乙醇而引起的一系列假感染事件(171)。
洗必泰
氯二甲酚
六氯酚
六氯酚是由两个酚基和三个氯基团组成的双酚。在 1950 年代和 1960 年代初,含有 3% 六氯酚的乳液被广泛用于卫生洗手、手术磨砂膏和 用于医院托儿所婴儿的常规洗澡。六氯酚的抗菌活性源于其能力 灭活微生物中的基本酶系统。六氯酚具有抑菌作用,对金黄色葡萄球菌活性好,对革兰氏阴性菌、真菌和分枝杆菌活性相对较弱 (7)。
将六氯酚作为卫生洗手液和手术擦洗的研究表明,在 单人洗手液 (53,143,188)。六氯酚在使用后数小时内具有残留活性,并逐渐降低 多次使用后手上的细菌计数(即具有累积效应) (1,101,188,189)。 反复使用 3% 六氯酚制剂后,药物通过皮肤吸收。用六氯酚洗澡的婴儿和经常使用 3% 六氯酚制剂洗手的人员血液中的六氯酚含量为 0.1–0.6 ppm (190)。 在 1970 年代初期,某些用六氯酚沐浴的婴儿出现神经毒性(空泡变性)(191)。因此,在 1972 年,FDA 警告说,六氯酚不应再常规用于婴儿洗澡。然而,在停止在托儿所常规使用六氯酚给婴儿洗澡后,研究人员指出,发病率 医院托儿所中与医疗保健相关的金黄色葡萄球菌感染大幅增加 (192,193)。 在一些情况下,当婴儿重新开始六氯酚洗澡时,感染频率降低。然而,目前的指南仍然建议不要用六氯酚对新生儿进行常规洗澡,因为其具有潜在的神经毒性作用 (194)。 该试剂被 FDA TFM 归类为通常不被认为是用作消毒洗手液安全有效的 (19)。六氯酚不应用于烧伤患者或大面积易感、敏感皮肤的沐浴。含有 3% 六氯酚的肥皂只能凭处方获得 (7)。
碘和碘伏
自 19 世纪以来,碘就被公认为是一种有效的消毒剂。然而,由于碘常常会导致皮肤刺激和变色,碘伏在很大程度上已取代碘,成为消毒剂中的活性成分。
碘分子能够迅速穿透微生物的细胞壁,并通过与氨基酸和不饱和脂肪酸形成复合物使细胞失活,从而导致蛋白质合成受损和细胞膜改变( 195)。碘伏由元素碘、碘化物或三碘化物,以及一种高分子量的聚合物载体(即络合剂)组成。存在的分子碘的量(即所谓的 “游离” 碘)决定了碘伏的抗菌活性水平。“有效” 碘是指可以用硫代硫酸钠滴定的碘的总量( 196)。典型的 10% 聚维酮碘配方含有 1% 的有效碘,游离碘浓度为 1 ppm( 196)。将碘与各种聚合物结合可增加碘的溶解度,促进碘的持续释放,并减少对皮肤的刺激。掺入碘伏中最常见的聚合物是聚乙烯吡咯烷酮(即聚维酮)和乙氧基化非离子洗涤剂(即泊洛沙姆)( 195、196)。碘伏的抗菌活性还可能受到 pH 值、温度、接触时间、总有效碘浓度,以及存在的有机和无机化合物的量和类型(如醇类和洗涤剂)的影响。
碘和碘伏对革兰氏阳性菌、革兰氏阴性菌以及某些产芽孢细菌(如梭菌属和芽孢杆菌属)具有杀菌活性,并且对分枝杆菌、病毒和真菌也有活性( 8、195、197 – 200)。然而,在消毒剂中使用的浓度下,碘伏通常不具有杀芽孢作用( 201)。体内研究表明,碘伏能减少从人员手上分离出的存活微生物的数量( 113、145、148、152、155)。5% – 10% 的聚维酮碘已被美国食品药品监督管理局(FDA)的暂定最终专论(TFM)暂时归类为 I 类制剂(即作为抗菌洗手剂和医护人员洗手剂使用时是安全有效的制剂)( 19)。碘伏从皮肤上冲洗掉后表现出的持续抗菌活性的程度尚不清楚。在一项研究中,观察到其持续活性可达 6 小时( 176);然而,其他几项研究表明,用碘伏洗手后,其持续活性仅为 30 – 60 分钟( 61、117、202)。在一些研究中,在洗手后戴手套 1 – 4 小时再获取细菌数量,结果显示碘伏的持续活性较差( 1、104、115、189、203 – 208)。在存在有机物质(如血液或痰液)的情况下,碘伏的体内抗菌活性会大幅降低( 8)。
大多数用于手部卫生的碘伏制剂含有 7.5% – 10% 的聚维酮碘。浓度较低的配方也具有良好的抗菌活性,因为稀释可以增加游离碘的浓度( 209)。然而,随着游离碘含量的增加,对皮肤的刺激程度也可能增加( 209)。与碘相比,碘伏对皮肤的刺激较小,过敏反应也较少,但与其他常用于手部卫生的消毒剂相比,它引起的刺激性接触性皮炎更多( 92)。偶尔,由于生产工艺不佳,碘伏消毒剂会被革兰氏阴性杆菌污染,并导致感染暴发或假暴发( 196)。
季铵化合物
季铵盐化合物由一个直接与四个烷基相连的氮原子组成,这些烷基的结构和复杂程度可能各不相同(210)。在这一大类化合物中,烷基苄基氯化铵是作为消毒剂使用最为广泛的。其他曾被用作消毒剂的化合物包括苄索氯铵、西曲溴铵和氯化十六烷基吡啶(1)。这类化合物的抗菌活性最早在 20 世纪初得到研究,早在 1935 年,就有一种用于外科医生术前手部清洁的季铵盐化合物投入使用(210)。这类化合物的抗菌活性很可能归因于它们吸附在细胞质膜上,随后导致低分子量的细胞质成分泄漏(210)。
季铵盐化合物主要具有抑菌和抑真菌的作用,不过在高浓度时对某些微生物也具有杀菌作用(1);它们对革兰氏阳性菌的活性比对革兰氏阴性杆菌的活性更强。季铵盐化合物对分枝杆菌和真菌的活性相对较弱,而对亲脂性病毒的活性更强。它们的抗菌活性会受到有机物质存在的不利影响,并且与阴离子洗涤剂不相容(1,210)。1994 年,美国食品药品监督管理局(FDA)的暂定最终专论(TFM)暂时将苄基氯化铵和苄索氯铵归类为 IIIS 类活性成分(即没有足够的数据将它们归类为用作抗菌洗手剂时是安全且有效的成分)(19)。FDA 正在对这些成分进行进一步评估。
季铵盐化合物通常耐受性良好。然而,由于对革兰氏阴性菌的活性较弱,苄基氯化铵容易被这类细菌污染。多起感染或假感染暴发事件都可追溯到被革兰氏阴性杆菌污染的季铵盐化合物(211 – 213)。出于这个原因,在过去的 15 至 20 年间,在美国这些化合物很少被用于手部消毒。不过,最近新推出了一些含有苄基氯化铵或苄索氯铵的洗手产品供医护人员使用。最近一项针对外科重症监护病房人员的研究发现,用含有季铵盐化合物的抗菌湿巾清洁手部,其效果与用普通肥皂和水洗手差不多;这两种方法的效果都不如使用含酒精的手部消毒剂对手部进行消毒(214)。一项基于实验室的研究报告称,一种含有季铵盐化合物的无酒精手部消毒剂在减少志愿者手上的微生物数量方面是有效的(215)。需要对这类产品进行进一步研究,以确定新配方在医疗保健环境中是否有效。
三氯生
三氯生(化学名称:2,4,4′- 三氯 – 2′- 羟基二苯醚)是一种非离子型的无色物质,于 20 世纪 60 年代研制而成。它已被添加到供医护人员和公众使用的肥皂中,以及其他消费品里。浓度在 0.2% 至 2% 之间的三氯生具有抗菌活性。三氯生能进入细菌细胞,影响细胞质膜以及 RNA、脂肪酸和蛋白质的合成(216)。最近的研究表明,这种物质的抗菌活性归因于它与烯酰基酰基载体蛋白还原酶的活性位点结合(217、218)。
三氯生具有广泛的抗菌活性,但通常表现为抑菌作用(1)。其最小抑菌浓度(MICs)范围在 0.1 至 10 微克 / 毫升之间,而最小杀菌浓度为 25 至 500 微克 / 毫升。三氯生对革兰氏阳性菌(包括耐甲氧西林金黄色葡萄球菌 [MRSA])的活性比对革兰氏阴性杆菌的活性更强,尤其是对铜绿假单胞菌(1、216)。该物质对分枝杆菌和念珠菌属具有一定的活性,但对丝状真菌的活性有限。用 0.1% 的三氯生进行 1 分钟的卫生洗手后,手上的细菌数量可减少 2.8 个对数级(1)。在多项研究中,使用三氯生后的细菌数量对数减少值低于使用氯己定、碘伏或含酒精产品后的减少值(1、61、149、184、219)。1994 年,美国食品药品监督管理局(FDA)的暂定最终专论(TFM)暂时将浓度低于 1.0% 的三氯生归类为 IIIS 类活性成分(即没有足够的数据将该成分归类为用作抗菌洗手剂时是安全且有效的成分)(19)。FDA 正在对该成分进行进一步评估。与氯己定一样,三氯生在皮肤上具有持续活性。它在手部护理产品中的活性受 pH 值、表面活性剂、润肤剂或保湿剂的存在,以及特定配方的离子性质的影响(1、216)。三氯生的活性基本不受有机物的影响,但它可能会因被螯合在某些配方中表面活性剂形成的胶束结构内而受到抑制。大多数含有低于 2% 三氯生的配方耐受性良好,很少引起过敏反应。某些报告指出,为医院工作人员提供含三氯生的手部消毒剂制剂可导致耐甲氧西林金黄色葡萄球菌感染的减少(72、73)。由于三氯生对革兰氏阴性杆菌的活性不强,偶尔会有关于其制剂受污染的报告(220)。
其他消毒剂
在塞麦尔维斯证明使用次氯酸盐洗手可降低与产褥热相关的产妇死亡率约 150 年后,人们再次研究了用次氯酸盐水溶液洗手 30 秒的效果(221)。结果表明,该溶液并不比蒸馏水更有效。塞麦尔维斯所采用的方法是用 4%(重量 / 重量)的次氯酸盐溶液搓洗双手,直至双手有滑腻感(约 5 分钟),其他研究人员重新审视了这一方法(222)。这项更新的研究表明,该方法的效果比用 60% 的异丙醇搓洗 1 分钟强 30 倍。然而,由于次氯酸盐溶液反复使用时常常会刺激皮肤,且气味浓烈,所以很少用于手部卫生。
美国食品药品监督管理局(FDA)正在评估某些其他制剂用于医疗保健相关消毒剂的可能性(19)。然而,对于这些制剂用于医护人员洗手制剂的效果,尚未进行充分评估。有必要对这些制剂进行进一步评估。可能会推出使用不同浓度传统消毒剂(如低浓度碘伏)或含有具有消毒特性新化合物的产品供医护人员使用。例如,初步研究表明,在乙醇载体中添加含银聚合物(即 Surfacine®)可制成一种在动物和人类皮肤上具有持续抗菌活性的制剂(223)。具有良好体外活性的新化合物必须进行体内测试,以确定它们减少医护人员手上暂居菌和常驻菌的能力。
消毒剂对产芽孢细菌的活性
由艰难梭菌引起的医疗保健相关腹泻的广泛流行,以及美国近期发生的与通过邮政系统寄送的受污染物品相关的人类炭疽芽孢杆菌感染事件,引发了人们对消毒剂对产芽孢细菌活性的担忧。用于抗菌洗手或抗菌手部消毒制剂中的任何一种消毒剂(包括醇类、氯己定、六氯酚、碘伏、对氯间二甲苯酚和三氯生),对梭菌属或芽孢杆菌属的杀菌效果都不可靠(120、172、224、225)。用非抗菌或抗菌肥皂和水洗手可能有助于从受污染的手表面物理去除芽孢。应鼓励医护人员在护理患有艰难梭菌相关腹泻的患者时戴手套(226)。摘下手套后,应用非抗菌或抗菌肥皂和水洗手,或使用含酒精的手部消毒剂进行消毒。在艰难梭菌相关感染暴发期间,摘下手套后用非抗菌或抗菌肥皂和水洗手是谨慎的做法。对于疑似或已证实接触过受炭疽芽孢杆菌污染物品的医护人员,也应鼓励他们用非抗菌或抗菌肥皂和水洗手。
细菌对消毒剂敏感性降低
细菌对消毒剂敏感性降低可能是一个菌种的固有特征,也可能是后天获得的特性(227)。有几份报告描述了一些细菌菌株,它们似乎对某些消毒剂(如氯己定、季铵盐化合物和三氯生)的敏感性有所降低(根据体外确定的最低抑菌浓度来定义)(227 – 230)。然而,由于医护人员实际使用的消毒剂浓度通常远高于对消毒剂敏感性降低的菌株的最低抑菌浓度,所以这些体外研究结果的临床相关性存在疑问。例如,某些耐甲氧西林金黄色葡萄球菌菌株的氯己定和季铵盐化合物的最低抑菌浓度,比甲氧西林敏感菌株高出数倍,某些金黄色葡萄球菌菌株对三氯生的最低抑菌浓度也有所升高(227、228)。然而,这些菌株很容易被实际工作中医护人员使用的这些消毒剂浓度所抑制(227、228)。对一种耐三氯生细菌酶的描述,引发了一个问题,即细菌对这种消毒剂的耐药性是否比其他消毒剂更容易产生(218)。此外,将含有 MexAB-OprM 外排系统的铜绿假单胞菌菌株暴露于三氯生,可能会筛选出对多种抗生素(包括氟喹诺酮类)耐药的突变株(230)。需要进一步研究来确定细菌对消毒剂敏感性降低是否具有流行病学意义,以及对消毒剂的耐药性是否对抗生素耐药菌株的流行有任何影响(227)。
外科手部消毒
自 19 世纪后期,李斯特提倡在手术前将石炭酸涂抹在外科医生手上以来,用消毒剂对双手和前臂进行术前清洁已成为一种被广泛接受的做法(231)。尽管尚未进行随机对照试验表明,使用消毒剂进行术前擦洗比使用非抗菌肥皂能显著降低手术部位感染率,但其他一些因素为这种做法提供了有力的依据。如果在手术过程中,外科医生手上的细菌被带入手术区域,就可能导致伤口感染(232);如果用非抗菌肥皂洗手,细菌会在外科手套内迅速繁殖。然而,用消毒剂进行术前擦洗后,细菌的生长会减缓(14、233)。在手术过程中,减少手术团队成员手上的常驻皮肤菌群,可降低手术中手套被刺破或撕裂时细菌释放到手术区域的风险(1、156、169)。最后,至少有一起手术部位感染暴发事件是由于通常使用抗菌外科擦洗制剂的外科医生开始使用非抗菌产品导致的(234)。
用于外科手部擦洗的抗菌制剂,需评估其在不同时间减少从手上释放细菌数量的能力,包括:1)擦洗后立即减少的数量;2)佩戴外科手套 6 小时后(即持续活性)减少的数量;3)连续 5 天多次使用后(即累积活性)减少的数量。在确定产品的功效时,即时活性和持续活性被认为是最重要的。美国的指南建议,用于外科手部擦洗的制剂应能大幅减少完整皮肤上的微生物数量,含有无刺激性的抗菌制剂,具有广谱抗菌活性,且起效快、活性持久(19、235)。
研究表明,含有 60% – 95% 的纯酒精,或含有 50% – 95% 酒精并与少量季铵盐化合物、六氯酚或葡萄糖酸氯己定结合的制剂,在擦洗后能比其他制剂更有效地立即降低皮肤上的细菌数量(表 4)。接下来活性较强的制剂(按活性递减顺序)是葡萄糖酸氯己定、碘伏、三氯生和普通肥皂(104、119、186、188、203、204、206、208、236)。由于关于对氯间二甲苯酚作为外科擦洗剂的研究结果相互矛盾,需要进一步研究来确定该化合物与其他制剂相比的功效(176、185、186)。
尽管醇类被认为不具有持久的抗菌活性,但用醇类进行外科擦洗后,细菌在手上的繁殖似乎较慢,并且佩戴手套 1 – 3 小时后手上的细菌数量很少超过基线(即擦洗前)值(1)。然而,最近一项研究表明,仅含有 61% 乙醇的制剂在擦洗后 6 小时未能达到足够的持续活性(237)。含有 0.5% 或 1% 葡萄糖酸氯己定的含酒精制剂具有持久活性,在某些研究中,其活性与含有葡萄糖酸氯己定的洗涤剂相当,甚至超过后者(1、118、135、237)。
含有 2% 或 4% 葡萄糖酸氯己定的基于洗涤剂的外科擦洗制剂的持久抗菌活性最强,其次是六氯酚、三氯生和碘伏(1、102、113 – 115、159、189、203、204、206 – 208、236)。由于六氯酚在反复使用后会被吸收入血液,所以很少被用作外科擦洗剂。
传统上,外科工作人员被要求在术前擦洗双手 10 分钟,这常常会导致皮肤损伤。多项研究表明,擦洗 5 分钟与擦洗 10 分钟一样能有效地减少细菌数量(117、238、239)。在其他研究中,擦洗 2 或 3 分钟可将细菌数量降低到可接受的水平(156、205、207、240、241)。
研究表明,分两步进行的外科擦洗方法是有效的,即先用抗菌洗涤剂擦洗,然后涂抹含酒精的制剂。例如,先用 4% 葡萄糖酸氯己定或聚维酮碘擦洗 1 或 2 分钟,然后涂抹含酒精的产品,其效果与用抗菌洗涤剂擦洗 5 分钟一样(114、242)。
外科手部消毒方案曾要求工作人员用刷子进行擦洗。但这种做法可能会损伤工作人员的皮肤,并导致手上细菌的脱落增加(95、243)。用一次性海绵或海绵 – 刷子组合进行擦洗,与用刷子擦洗一样能有效地减少手上的细菌数量(244 – 246)。然而,多项研究表明,无论是刷子还是海绵,对于将外科工作人员手上的细菌数量降低到可接受水平都不是必需的,尤其是在使用含酒精产品时(102、117、159、165、233、237、247、248)。这些研究中的一些是在擦洗后立即或 45 – 60 分钟进行培养(102、117、233、247、248),而在其他研究中,则是在擦洗后 3 小时和 6 小时进行培养(159、237)。例如,最近一项基于实验室的志愿者研究表明,与使用海绵 / 刷子涂抹含有 4% 葡萄糖酸氯己定的洗涤剂制剂相比,使用不含刷子的含有 1% 葡萄糖酸氯己定加 61% 乙醇的制剂,参与者手上的细菌数量更低(237)。
普通肥皂、抗菌肥皂 / 洗涤剂和醇类的相对功效
比较普通肥皂、抗菌肥皂和含酒精手部消毒剂的体内功效研究存在一定问题,因为有些研究用细菌数量减少的百分比来表示功效,而另一些研究则用细菌数量的对数减少值来表示。然而,总结每项研究中测试的药物的相对疗效可以 概述了用于洗手、卫生洗手、消毒手的各种配方的体内活性 摩擦或手术手部消毒剂(表 2–-4)。
手部卫生措施导致的刺激性接触性皮炎
刺激性接触性皮炎的发生频率和病理生理学
在某些调查中,约 25% 的护士报告了手部出现与皮炎相关的症状或体征,多达 85% 的护士有过皮肤问题的病史(249)。频繁且反复地使用手部卫生产品,尤其是肥皂和其他洗涤剂,是医护人员患上慢性刺激性接触性皮炎的主要原因(250)。洗涤剂对皮肤产生刺激的可能性差异很大,而添加润肤剂和保湿剂可以减轻这种刺激。与抗菌肥皂相关的刺激可能是由抗菌剂或配方中的其他成分引起的。受影响的人常常抱怨皮肤有干燥或灼烧感、感觉皮肤 “粗糙”,以及出现红斑、脱屑或皲裂。洗涤剂通过使角质层蛋白质变性、改变细胞间脂质(脂质成分的耗尽或重组)、降低角质形成细胞的凝聚力以及降低角质层的水结合能力来损伤皮肤(250、251)。皮肤受损还会改变皮肤菌群,导致葡萄球菌和革兰氏阴性杆菌更频繁地定植(17、90)。尽管醇类是现有的相对安全的消毒剂之一,但它们也会导致皮肤干燥和刺激(1、252)。乙醇通常比正丙醇或异丙醇的刺激性小(252)。
碘伏引发刺激性接触性皮炎的报告更为常见(92)。其他可能导致刺激性接触性皮炎的消毒剂(按发生频率递减顺序)包括氯己定、对氯间二甲苯酚、三氯生和含酒精的产品。因反复接触洗涤剂而受损的皮肤可能更容易受到含酒精制剂的刺激(253)。商业制备的手部卫生产品的潜在刺激性,通常通过测量经表皮水分流失来确定,制造商可能会提供这方面的信息。其他可能导致频繁洗手相关皮炎的因素包括用热水洗手、相对湿度低(冬季最为常见)、未使用额外的护手霜或乳液,以及纸巾的质量(254、255)。佩戴或摘下手套时产生的剪切力以及对乳胶蛋白的过敏也可能导致医护人员手部出现皮炎。
与手部卫生产品相关的过敏性接触性皮炎
对涂抹在皮肤上的产品产生的过敏反应(即接触性过敏)可能表现为迟发型反应(即过敏性接触性皮炎),较少情况下表现为速发型反应(即接触性荨麻疹)。接触性过敏最常见的原因是香料和防腐剂;乳化剂是不太常见的原因(256 – 259)。液体肥皂、护手霜或乳液以及 “护乳霜” 可能含有会导致医护人员发生接触性过敏的成分(257、258)。
已有报告显示,对消毒剂包括季铵盐化合物、碘或碘伏、氯己定、三氯生、对氯间二甲苯酚和醇类产生过敏反应(118、167、172、256、260 – 265)。与含酒精的手部消毒剂相关的过敏性接触性皮炎并不常见。瑞士一家大型医院对一款已使用超过 10 年的商用含酒精手部消毒剂进行监测,未发现一例有记录的对该产品过敏的病例(169)。2001 年末,根据信息自由法案要求,查询美国食品药品监督管理局(FDA)不良事件报告系统中关于美国流行的含酒精手部消毒剂不良反应的数据,仅发现一例归因于此类产品的红斑皮疹反应报告(约翰・M・博伊斯医学博士,康涅狄格州纽黑文市圣拉斐尔医院,个人交流,2001 年)。然而,随着医护人员对这类产品使用的增加,很可能会遇到真正对这类产品的过敏反应。
对含酒精产品的过敏反应可能是对酒精的真正过敏、对杂质或醛类代谢物的过敏,或者是对产品中其他成分的过敏(167)。乙醇或异丙醇可能导致过敏性接触性皮炎或即时接触性荨麻疹反应(167)。含酒精手部消毒剂中作为非活性成分存在的化合物,包括香料、苯甲醇、硬脂醇或异硬脂醇、苯氧乙醇、肉豆蔻醇、丙二醇、对羟基苯甲酸酯和苄基氯化铵,都可能引发过敏反应(167、256、266 – 270)。
减少消毒剂不良反应的建议方法
将医护人员因手部卫生导致的刺激性接触性皮炎降至最低的潜在策略包括:减少接触刺激性物质(尤其是阴离子洗涤剂)的频率;用对皮肤损伤较小的制剂替代潜在刺激性高的产品;对工作人员进行有关刺激性接触性皮炎风险的教育;为护理人员提供保湿护肤产品或防护霜(96、98、251、271 – 273)。减少医护人员接触手部卫生产品的频率被证明是困难的,而且由于大多数机构中医护人员对手部卫生政策的依从性较低,这也不是一个理想的方法。尽管医院为工作人员提供了非抗菌肥皂,希望能将皮炎降至最低,但频繁使用这类产品可能比抗菌制剂对皮肤造成更大的损伤、干燥和刺激(92、96、98)。减少工作人员接触刺激性肥皂和洗涤剂的一种策略是推广使用含有各种润肤剂的含酒精手部消毒剂。最近的几项前瞻性随机试验表明,含有润肤剂的含酒精手部消毒剂比用非抗菌肥皂或抗菌肥皂洗手更易被医护人员接受(96、98、166)。在使用含酒精手部消毒剂后立即用肥皂和水常规洗手可能会导致皮炎。因此,应提醒工作人员,在每次使用含酒精手部消毒剂后常规洗手既无必要,也不被推荐。
护手霜和乳液通常含有保湿剂以及各种脂肪和油脂,这些成分可以增加皮肤的水分含量,并补充改变或耗尽的皮肤脂质,而这些脂质有助于维持正常皮肤的屏障功能(251、271)。几项对照试验表明,定期(如每天两次)使用这类产品可以帮助预防和治疗由手部卫生产品引起的刺激性接触性皮炎(272、273)。在一项研究中,频繁且定时使用含油乳液改善了皮肤状况,从而使医护人员的洗手频率提高了 50%(273)。这些研究报告强调了对工作人员进行定期、频繁使用护手产品重要性教育的必要性。
最近,防护霜已推向市场,用于预防与手部卫生相关的刺激性接触性皮炎。这类产品会被吸收到表皮的表层,旨在形成一层不会被标准洗手去除的保护层。最近两项评估护理人员皮肤状况的随机对照试验表明,防护霜的效果并不比使用的对照乳液或基质更好(272、273)。因此,防护霜在预防医护人员的刺激性接触性皮炎方面是否有效仍不得而知。
除了评估护手产品的功效和可接受性外,产品选择委员会还应询问含油产品对橡胶手套完整性以及机构中使用的消毒剂功效可能产生的潜在有害影响(8、236)。
选择手部卫生产品时需考虑的因素
在评估手部卫生产品在医疗保健机构中使用的可能性时,管理人员或产品选择委员会必须考虑可能影响这类产品整体功效的因素,包括消毒剂对各种病原体的相对功效(附录)以及工作人员对手部卫生产品的接受程度(274、275)。医护人员不太接受的肥皂产品可能会阻碍他们频繁洗手(276)。产品(无论是肥皂还是含酒精的手部消毒剂)的特性,如气味、质地(即 “手感”)和颜色,会影响工作人员的接受程度(92、277、278)。对于肥皂来说,起泡的难易程度也可能影响使用者的偏好。
由于医护人员每班洗手的次数可能有限,也可能多达每班 30 次,产品导致皮肤刺激和干燥的倾向是影响其被接受以及最终使用的一个重要因素(61、98、274、275、277、279)。例如,对酒精干燥作用的担忧是美国医院中含酒精手部卫生产品接受度低的主要原因(5、143)。然而,多项研究表明,含有润肤剂的含酒精手部消毒剂是医护人员可以接受的(90、93、98、100、101、106、143、163、164、166)。对于含酒精产品,干燥所需的时间也可能影响使用者的接受程度。
研究表明,工作人员洗手或抗菌洗手的频率受到手部卫生设施可及性的影响(280 – 283)。在某些医疗保健机构中,收治多名患者的病房里只有一个洗手池,或者洗手池离病房门很远,这可能会使离开病房的工作人员不愿洗手。在重症监护病房,床边设备(如呼吸机或静脉输液泵)可能会阻挡通往洗手池的通道。与用于洗手或抗菌洗手的洗手池不同,含酒精手部消毒剂的分配器不需要管道设施,可以放置在每个患者的床边以及患者护理区域的许多其他位置。随身携带含酒精手部消毒剂溶液,再加上床边分配器的配备,与医护人员对手部卫生规程的依从性大幅提高有关(74、284)。为避免肥皂和含酒精手部消毒剂之间产生混淆,含酒精手部消毒剂分配器不应放置在洗手池旁边。应告知医护人员,每次使用含酒精手部消毒剂后用肥皂和水洗手既无必要,也不被推荐,因为这可能会导致皮炎。然而,由于工作人员在反复使用含酒精手部凝胶后会感觉手上有润肤剂 “堆积”,某些制造商建议在使用 5 – 10 次凝胶后用肥皂和水洗手。
自动洗手机尚未被证明能提高洗手的质量或频率(88、285)。尽管最近开发了技术先进的自动洗手设备和监测系统,但只有极少数研究表明,使用这些设备能使医护人员对手部卫生的依从性得到持久改善。有必要对自动洗手设施和监测系统进行进一步评估。
在评估手部卫生产品时,还必须考虑制造商或供应商提供的分配器系统。当分配器出现以下情况时,可能会阻碍医护人员使用:1)堵塞或部分堵塞,工作人员使用时无法挤出产品;2)无法将产品正确地挤出到手上。在一家提供粘性含酒精手部冲洗液的医院里,只有 65% 能正常使用的分配器在按压一次分配器杠杆时就能将产品挤出到护理人员手上,9% 的分配器完全堵塞(286)。此外,挤出的产品量往往不理想,有时产品会喷到墙上而不是护理人员手上。
关于医疗保健机构中使用的手部卫生产品的成本,目前信息有限(165、287)。在一家拥有 450 张床位的社区教学医院的患者护理区域对这些成本进行了评估(287);该医院在含有 2% 氯己定的制剂、普通肥皂和一种含酒精手部冲洗液上花费了 22000 美元(每位患者每天 0.72 美元)(287)。当包括诊所和非患者护理区域的手部卫生用品时,肥皂和手部消毒剂的年度总预算为 30000 美元(大约每位患者每天 1 美元)。其他机构的年度手部卫生产品预算差异很大,这是因为使用模式不同以及产品价格各异。一位研究人员(287)确定,如果将非抗菌液体肥皂的任意相对成本设定为 1.0,那么每升 2% 葡萄糖酸氯己定制剂的成本将是其 1.7 倍,含酒精手部消毒剂产品的成本高 1.6 – 2.0 倍,含酒精泡沫产品的成本高 4.5 倍。最近一项对抗菌肥皂用于外科擦洗与不含刷子的含酒精手部消毒剂用于外科擦洗的成本比较显示,含酒精产品用于术前擦洗的成本和所需时间更低(165)。在两个重症监护病房进行的一项试验中,使用含酒精手部消毒剂的成本是使用抗菌肥皂洗手成本的一半(每次使用分别为 0.025 美元和 0.05 美元)(166)。
为了正确看待手部卫生产品的支出,医疗保健机构应考虑将其手部卫生产品预算与因医疗保健相关感染导致的医院估计额外成本进行比较。仅四到五例平均严重程度的医疗保健相关感染所导致的医院额外成本,可能就等于住院患者护理区域使用的手部卫生产品的全年预算。仅一例严重的手术部位感染、下呼吸道感染或血流感染,给医院带来的成本可能就超过用于手部卫生的消毒剂的全年预算(287)。两项研究对促进手部卫生项目的益处进行了一定的量化估计(72、74)。一项研究表明,在观察到的 7 个月期间耐甲氧西林金黄色葡萄球菌(MRSA)发生率下降后,因减少了万古霉素的使用而节省了约 17000 美元(72)。在另一项研究中,既考虑了与促进手部卫生项目相关的直接成本(含酒精手部消毒剂溶液使用量增加和海报制作成本),也考虑了与医护人员时间相关的间接成本(74),该项目的成本估计每年不超过 57000 美元(平均每位入院患者 1.42 美元)。因增加使用含酒精手部消毒剂溶液而产生的额外成本平均每 100 个患者日为 6.07 美元。基于保守估计,即每避免一例感染可节省 2100 美元,并假设观察到的感染率下降中只有 25% 与手部卫生实践的改善有关,该项目具有显著的成本效益。因此,医院管理人员必须认识到,通过购买更有效或更易被接受的手部卫生产品来改善手部卫生实践,他们将避免医院感染的发生;每年仅预防有限数量的额外医疗保健相关感染,所节省的费用就将超过改进后的手部卫生产品的任何增量成本。
医护人员的手部卫生实践
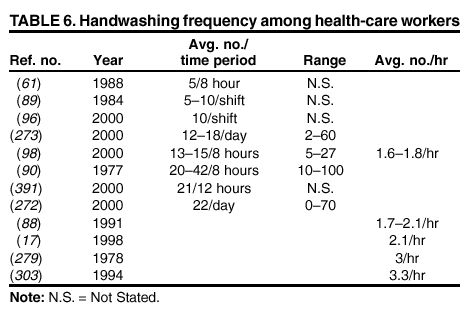
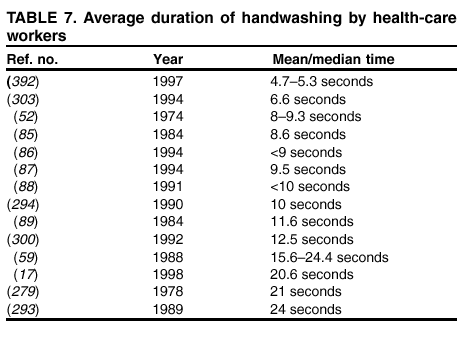
在医院进行的观察性研究中,医护人员每班平均洗手 5 次,最多可达每班 30 次(表 6)(17、61、90、98、274、288);某些护士每班洗手次数少于 100 次(90)。全院范围内对手部卫生的监测显示,不同医院病房之间平均的洗手机会数量差异显著。例如,儿科病房的护士每小时患者护理时间内平均有 8 次手部卫生机会,而重症监护病房的护士平均每小时有 20 次(11)。在观察性研究中,医护人员洗手或卫生洗手的时长平均为 6.6 至 24.0 秒(表 7)(17、52、59、84 – 87、89、249、279)。除了洗手时间有限外,工作人员常常未能清洗到手和手指的所有部位(288)。
医护人员对推荐手部卫生规范的依从性
手部卫生依从性的观察性研究
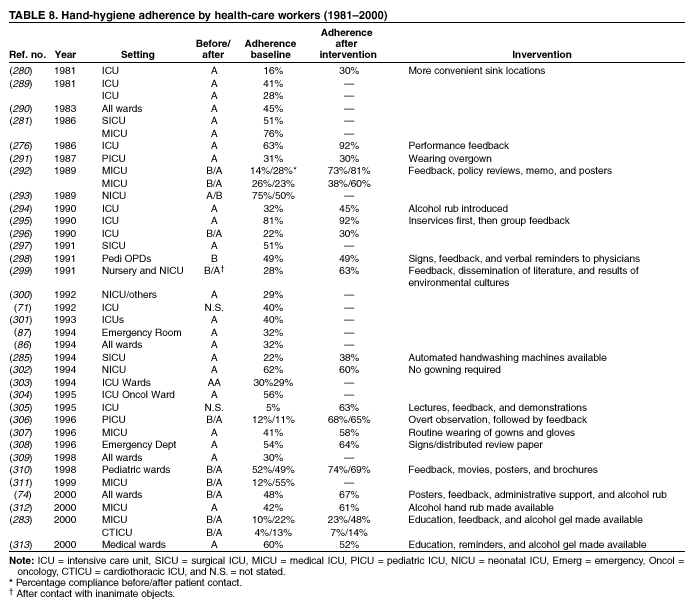
医护人员对推荐的手部卫生规程的依从性较差,平均基线依从率在 5% 至 81% 之间(总体平均:40%)(表 8)(71、74、86、87、276、280、281、283、285、289 – 313)。不同研究中用于定义依从(或不依从)的方法以及进行观察的方法差异很大,并且报告中未提供有关所使用方法和标准的详细信息。大多数研究将手部卫生依从性作为主要的观察结果指标,而少数研究将依从性作为更广泛调查的一部分进行测量。几位研究人员报告称,在实施各种干预措施后依从性有所提高,但大多数研究的随访期较短,并未证实行为改善是否具有持久性。其他研究表明,在一项旨在提高对手部卫生政策依从性的长期项目中,洗手行为得到了持续改善(74、75)。
影响依从性的因素
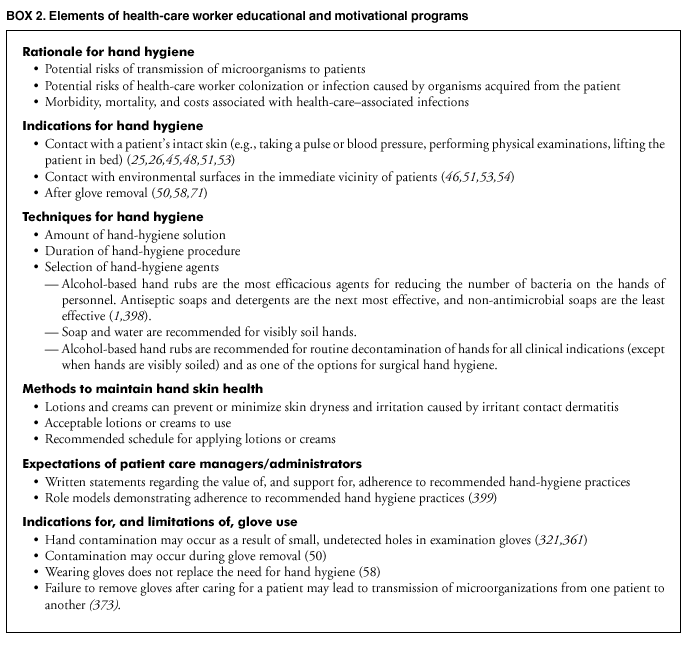
可能影响手部卫生的因素包括流行病学研究中确定的因素,以及医护人员报告的不遵守手部卫生建议的原因。在几项观察性研究或旨在提高依从性的干预措施中,已客观确定了手部卫生依从性差的风险因素(11、12、274、292、295、314 – 317)。其中,与护士相比,身为医生或护理助理一直与依从性降低相关(方框 1)。
在对医护人员手部卫生实践进行的最大规模的全院调查中(11),确定了不遵守推荐手部卫生措施的预测因素。预测变量包括专业类别、医院病房、一天 / 一周中的时间,以及患者护理的类型和强度,患者护理强度定义为每小时患者护理时间内的手部卫生机会数量。在观察到的 2834 次手部卫生机会中,平均依从率为 48%。在多变量分析中,护士和周末期间的不依从率最低(比值比 [OR]:0.6;95% 置信区间 [CI]=0.4 – 0.8)。与内科病房相比,重症监护病房的不依从率更高(OR:2.0;95% CI = 1.3 – 3.1);在细菌污染风险高的操作期间(OR:1.8;95% CI = 1.4 – 2.4),以及当患者护理强度较高时(21 – 40 次洗手机会 —— OR:1.3;95% CI = 1.0 – 1.7;41 – 60 次机会 —— OR:2.1;95% CI = 1.5 – 2.9;>60 次机会 —— OR:2.1;95% CI = 1.3 – 3.5),不依从率也更高。对手部卫生的需求越高,依从性越低;当患者护理强度超过每小时 10 次机会时,每增加 10 次机会,依从性平均下降 5%(±2%)。同样,依从率最低(36%)的是重症监护病房,那里对手部卫生的指示通常更为频繁(平均每患者小时 20 次机会)。依从率最高(59%)的是儿科病房,那里的患者护理平均强度低于医院的其他区域(平均每患者小时 8 次机会)。这项研究的结果表明,完全遵守先前的指南可能不太现实,而方便获取手部卫生用品有助于提高依从性(11、12、318)。
被认为妨碍遵守手部卫生实践建议的因素包括:手部卫生制剂引起的皮肤刺激、无法获取手部卫生用品、干扰医护人员与患者的关系、护理的优先级(即患者的需求优先于手部卫生)、戴手套、遗忘、不了解指南、手部卫生时间不足、工作量大且人员配备不足,以及缺乏科学信息表明改善手部卫生对医疗保健相关感染率有明确影响(11、274、292、295、315 – 317)。在观察性研究中,已对某些被认为妨碍遵守手部卫生指南的因素进行了评估或量化(12、274、292、295、314 – 317)(方框 1)。
手部卫生制剂引起的皮肤刺激是导致无法适当遵守手部卫生规范的一个重大障碍(319)。由于肥皂和洗涤剂定期使用会损伤皮肤,必须让医护人员更好地了解手部卫生制剂可能带来的不良影响。对这一主题缺乏了解和教育是影响积极性的一个障碍。在几项研究中,含有润肤剂的含酒精手部消毒剂(体积比为 60% – 90% 的异丙醇、乙醇或正丙醇)对皮肤的刺激性比所测试的肥皂或洗涤剂更小。此外,所测试的含有润肤剂的含酒精产品至少与所测试的洗涤剂一样耐受且有效。而且,研究表明,几种护手霜减少了皮肤脱屑和皲裂,这可能会减少手部微生物的脱落(67、272、273)。
无论是洗手池、肥皂、药用洗涤剂还是含酒精手部消毒剂溶液,方便获取手部卫生用品对于最佳地遵守手部卫生建议至关重要。护士离开患者床边、走到洗手池、洗手并擦干,然后再去照顾下一位患者所需的时间,会阻碍他们频繁洗手或进行手部消毒(11、318)。工程控制措施可以提高依从性,但应仔细监测手部卫生行为,以排除新引入的洗手设备可能带来的负面影响(88)。
戴手套对遵守手部卫生政策的影响尚未明确确定,因为已发表的研究得出了相互矛盾的结果(87、290、301、320)。无论是否使用或更换手套,都需要进行手部卫生。在接触患者后或在对同一患者进行 “脏” 和 “清洁” 身体部位护理之间未摘下手套,必须被视为不遵守手部卫生建议(11)。在一项实验条件接近临床实践的研究中(321),在接触患者之间清洗并重复使用手套,在摘下手套后观察到手上的细菌计数为 0 – 4.7 个对数级。因此,应不鼓励这种做法;摘下手套后应进行洗手或消毒。
- 缺乏对手部卫生指南的了解;
- 在患者护理过程中未识别出手部卫生的机会;
- 未意识到病原体交叉传播的风险,这些都是良好手部卫生实践的障碍。
此外,某些医护人员认为他们在必要时已经洗过手了,即使观察结果表明他们并没有(89、92、295、296、322)。
被认为妨碍手部卫生行为的因素不仅与机构有关,还与医护人员的同事有关。因此,在实施系统变革以确保改善医护人员的手部卫生实践时,需要同时考虑机构和小组层面的动态因素。
促进手部卫生的可能目标
促进手部卫生的目标源自评估不依从风险因素的研究、报告的不遵守建议的原因,以及被认为对促进医护人员适当行为很重要的其他因素。尽管某些因素无法改变(方框 1),但其他因素是可以改变的。
必须解决的一个因素是医护人员清洁双手所需的时间。传统洗手所需的时间可能使得完全遵守先前的指南不太现实(11、12、318),而更快速地获取手部卫生材料有助于提高依从性。在重症监护病房进行的一项研究表明,护士离开患者床边、走到洗手池、洗手,然后返回继续护理患者平均需要 62 秒(318)。相比之下,使用放置在每个患者床边的含酒精手部消毒剂估计只需要其四分之一的时间。方便获取手部卫生材料对于适当的手部卫生行为是必不可少的,并且在大多数医疗保健机构中是可以实现的(323)。特别是在高需求的情况下(例如,大多数重症监护病房)、繁忙的工作条件下,以及在人员拥挤或人员配备不足的时候,医护人员更可能使用含酒精手部消毒剂而不是洗手(323)。此外,使用含酒精手部消毒剂可能比用普通肥皂和水或抗菌肥皂进行传统洗手更好,因为它们不仅所需时间更少(166、318),而且起效更快(1),对手部的刺激也更少(1、67、96、98、166)。在唯一一个报告称手部卫生依从性持续改善且感染率下降的项目中,使用的就是含酒精手部消毒剂(74)。然而,如果在为工作人员提供含酒精手部消毒剂的同时,不进行持续的教育和激励活动,可能不会带来手部卫生实践的持久改善(313)。由于增加手部卫生制剂的使用可能会导致皮肤干燥,建议提供免费的护肤乳液。
教育是改善手部卫生实践的基石。教育项目必须涉及的主题包括:
- 缺乏关于改善手部卫生对医疗保健相关感染和耐药菌传播率的明确影响的科学信息;
- 对手部卫生指南缺乏认识,以及在日常患者护理中对手部卫生的适应症了解不足;
- 对大多数医护人员手部卫生平均依从率较低的认识;
- 对手部卫生和皮肤护理保护剂的适用性、功效以及使用方法的了解。
医护人员必然是在一个机构内的小组中工作。改善手部卫生行为的可能目标不仅包括与单个医护人员相关的因素,还包括与小组和整个机构相关的因素(317、323)。在小组层面促进手部卫生的可能目标示例包括:对手部卫生依从性进行教育和提供绩效反馈;努力防止高工作量、人员缩减和人员配备不足;鼓励工作单位的关键成员树立榜样并提供榜样。在机构层面,改善的目标包括:
- 书面指南、手部卫生制剂、皮肤护理推广和制剂,或手部卫生设施;
- 遵守的文化或传统;
- 行政领导的支持、制裁、支持和奖励。
在各种类型机构中进行的几项研究报告称,对推荐的手部卫生实践的依从性处于中等甚至较低水平,这表明这种依从性因医院病房和医护人员类型而异。这些结果表明,可能需要专门为某些类型的人员设计教育课程(11、289、290、294、317、323)。
从行为理论中吸取的教训
1998 年,研究人员回顾了当时流行的行为理论及其在卫生专业领域的应用,试图更好地理解如何针对更成功的干预措施设定目标(317)。研究人员提出了一个假设框架,以加强手部卫生实践,并强调在设计行为干预措施时考虑个人和机构因素的复杂性的重要性。
尽管行为理论和二级干预措施主要针对个体工作人员,但这种做法可能不足以产生持续的改变(317、324、325)。旨在改善手部卫生实践的干预措施必须考虑不同层面的行为相互作用(12、317、326)。因此,在手部卫生宣传活动的战略规划和制定过程中,必须考虑个人因素、环境限制和机构氛围的相互依存关系。在医院中促进手部卫生的干预措施应考虑所有这些层面的变量。手部卫生行为涉及的各种因素包括意图、对行为的态度、感知的社会规范、感知的行为控制、感知的感染风险、手部卫生实践、感知的榜样、感知的知识和动机(317)。实现改变所需的因素包括:
- 对当前情况的不满;
- 对替代方案的认知;
- 在个人和机构层面都认识到改变的能力和潜力。
尽管后者意味着教育和激励,但前两者需要进行系统变革。
在报告的不遵守手部卫生建议的原因中(方框 1),某些原因显然与机构或系统相关(例如,机构对手部卫生缺乏优先级、行政制裁和安全氛围)。尽管在大多数机构中,所有这些原因都需要进行系统变革,但第三个原因需要管理层的承诺、可见的安全项目、可接受的工作压力水平、对报告问题的宽容和支持态度,以及对预防策略功效的信任(12、317、325、327)。最重要的是,改善感染控制实践需要:
- 质疑基本信念;
- 持续评估小组(或个人)的行为改变阶段;
- 采用适当的变革过程进行干预;
- 支持个人和小组的创造力(317)。
由于变革过程的复杂性,单一的干预措施往往会失败。因此,多模式、多学科的策略可能是必要的(74、75、317、323、326)。
促进改善手部卫生的方法
150 多年来,促进手部卫生一直是一项具有挑战性的任务。在职教育、信息传单、研讨会和讲座、自动分配器以及对手部卫生依从率的绩效反馈,都曾带来短暂的改善(291、294 – 296、306、314)。
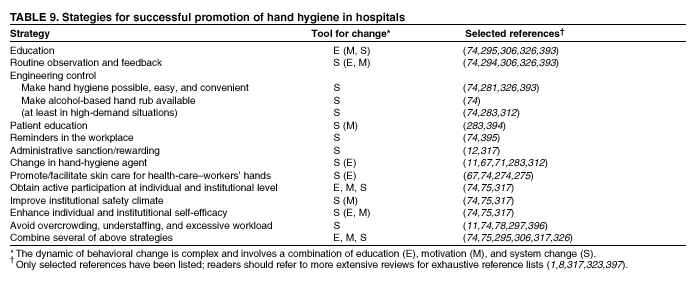
已经发表了几种在医院中促进手部卫生的策略(表 9)。这些策略需要教育、激励或系统变革。某些策略基于流行病学证据,其他策略则基于作者和其他研究人员的经验以及对当前知识的回顾。某些策略在某些情况下可能不必要,但在其他情况下可能会有所帮助。特别是,当无法使用含酒精手部消毒剂时,在工作量大且对手部卫生需求高的机构或医院病房中,更换手部卫生制剂可能是有益的(11、73、78、328)。然而,如果在冬季(手部皮肤更易受刺激的时候)更换推荐的手部卫生制剂,并且不提供皮肤护理产品(如防护霜和乳液),这种更换可能是有害的。在教育和激励项目中,还应考虑纳入其他特定要素(方框 2)。
几种可能与成功促进手部卫生相关的策略需要进行系统变革(方框 1)。手部卫生依从性和促进涉及个人和系统层面的因素。增强个人和机构对进行变革的可行性的态度(自我效能感)、获得两个层面人员的积极参与,以及营造机构安全氛围,这些挑战超出了目前对感染控制专业人员角色的认知。
增加教育、个人强化技术、适当的奖励、行政制裁、增强自我参与、更多组织领导者的积极参与、增强对健康威胁的感知、自我效能感和感知的社会压力(12、317、329、330),或者这些因素的组合,是否能够提高医护人员对手部卫生的依从性,还需要进一步研究。最终,遵守推荐的手部卫生实践应该成为患者安全文化的一部分,在这种文化中,一系列相互依存的质量要素相互作用,以实现共同的目标(331)。
基于这些假设性的考虑以及某些机构的成功实际经验,提高对手部卫生实践依从性的策略应该是多模式和多学科的。然而,在实施这些策略之前,必须进行进一步的研究。
促进手部卫生的效果以及改善手部卫生的影响
缺乏关于改善手部卫生对医疗保健相关感染率的确切影响的科学信息,这可能是妨碍人们适当遵守手部卫生建议的一个因素(方框 1)。然而,有证据支持这样一种观点,即改善手部卫生能够降低医疗保健相关感染率。未进行适当的手部卫生被认为是医疗保健相关感染以及多重耐药菌传播的主要原因,并且已被公认为是感染暴发的一个重要因素。
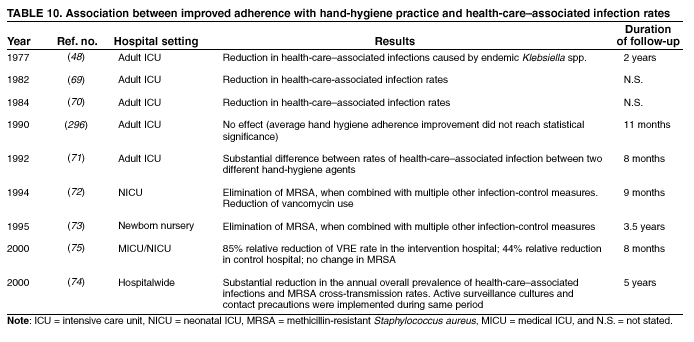
在九项基于医院的关于手部卫生对医疗保健相关感染风险影响的研究中(表 10)(48、69 – 75、296),大多数研究都表明,改善手部卫生实践与降低感染率之间存在时间上的关联。
在其中一项研究中,新生儿重症监护病房中的地方性耐甲氧西林金黄色葡萄球菌(MRSA)在引入一种新的手部消毒剂(1% 三氯生)7 个月后被消除;所有其他感染控制措施保持不变,包括通过采集培养样本进行每周主动监测的做法(72)。另一项研究报告称,一个新生儿病房发生了涉及 22 名婴儿的 MRSA 暴发(73)。尽管采取了大量措施,但在添加一种新的消毒剂(即 0.3% 三氯生)之前,疫情无法得到控制;所有先前使用的控制措施保持不变,包括戴手套和穿隔离衣、分组护理以及采集培养样本进行主动监测。
最近报告了日内瓦大学医院一项长期的全院性促进手部卫生项目的成效(74)。在全院性的观察性调查中,对常规患者护理期间遵守手部卫生指南的总体情况进行了监测。这些调查在 1994 年 12 月至 1997 年 12 月期间每半年进行一次,分别在实施一项特别强调床边使用含酒精手部消毒实践的手部卫生宣传活动之前和期间进行。向所有病房分发了个人装的手部消毒剂溶液瓶,并在所有病床上安装了定制的放置架,以方便进行手部消毒。还鼓励医护人员将消毒剂瓶放在口袋里,1996 年,推出了一种新设计的扁平(而非圆形)瓶子,以进一步方便放在口袋里携带。该宣传策略是多模式的,涉及一个由医护人员组成的多学科团队,使用墙上的海报,在整个机构的床边推广含酒精手部消毒剂,并定期向所有医护人员反馈表现情况(有关方法的更多详细信息,请访问http://www.hopisafe.ch)。对医疗保健相关感染率、MRSA 交叉传播的发病率以及手部消毒消毒剂的使用量进行了测量。遵守推荐的手部卫生实践的情况从 1994 年的 48% 逐步提高到 1997 年的 66%(P < 0.001)。在研究期间,使用肥皂和水洗手的频率保持稳定,而手部消毒的频率显著增加(P < 0.001),1993 – 1998 年期间,含酒精手部消毒剂溶液的使用量从每 1000 个患者日 3.5 升增加到 15.4 升(P < 0.001)。在对依从性差的已知风险因素进行调整后,手部消毒频率的增加情况没有改变。在同一时期,总体医疗保健相关感染率和 MRSA 传播率均下降(均 P < 0.05)。观察到的 MRSA 传播率的下降可能既受到手部卫生依从性改善的影响,也受到同时实施的用于检测和隔离 MRSA 定植患者的主动监测培养措施的影响(332)。日内瓦大学医院的经验是首个关于手部卫生宣传活动在数年时间里持续改善的报告。另外一个多模式项目也在较长时间内使手部卫生实践得到了持续改善(75);而大多数研究的观察期仅限于 6 至 9 个月。
尽管这些研究并非旨在评估手部卫生在预防医疗保健相关感染方面的独立作用,但结果表明,改善手部卫生实践可降低病原微生物传播的风险。在学校和日托中心(333 – 338)以及社区环境中(339 – 341)进行的调查也报告了促进手部卫生对降低交叉传播风险的有益影响。
与手部卫生相关的其他政策
指甲和假指甲
研究已证实,手部的指甲下区域存在高浓度的细菌,最常见的是凝固酶阴性葡萄球菌、革兰氏阴性杆菌(包括铜绿假单胞菌属)、棒状杆菌和酵母菌(14、342、343)。新涂的指甲油不会增加从指甲周围皮肤分离出的细菌数量,但剥落的指甲油可能会促使指甲上生长更多的微生物(344、345)。即使经过仔细洗手或使用外科擦洗剂,工作人员的指甲下空间通常仍会携带大量潜在病原体(346 – 348)。
假指甲是否会导致医疗保健相关感染的传播尚不清楚。然而,无论是洗手前还是洗手后,佩戴假指甲的医护人员的指尖携带革兰氏阴性病原体的可能性都比留自然指甲的医护人员更高(347 – 349)。自然指甲或假指甲的长度是否是一个重要的风险因素尚不清楚,因为大多数细菌生长在指甲靠近指甲下皮肤的近端 1 毫米处(345、347、348)。最近,一个新生儿重症监护病房发生的铜绿假单胞菌感染暴发被归因于两名护士(一名留着长的自然指甲,另一名戴着长的假指甲),她们的手上携带了相关的铜绿假单胞菌菌株(350)。在暴露期间,患者由这两名护士护理的可能性明显高于对照组,这表明长指甲或假指甲被铜绿假单胞菌定植可能是导致感染暴发的一个因素。从流行病学角度来看,佩戴假指甲的工作人员还与其他几起由革兰氏阴性杆菌和酵母菌引起的感染暴发有关(351 – 353)。尽管这些研究提供了佩戴假指甲存在感染风险的证据,但仍需要更多的研究。
手套使用政策
美国疾病控制与预防中心(CDC)建议医护人员佩戴手套,目的是:1)降低工作人员从患者处感染疾病的风险;2)防止医护人员的菌群传播给患者;3)减少工作人员的手部因可能从一名患者传播给另一名患者的菌群而受到的短暂污染(354)。在获得性免疫缺陷综合征(艾滋病)疫情出现之前,主要是护理定植或感染某些病原体的患者的工作人员,或者接触乙肝高风险患者的工作人员会佩戴手套。自 1987 年以来,为了防止人类免疫缺陷病毒(HIV)和其他血源性病原体从患者传播给医护人员,手套的使用量大幅增加(355)。美国职业安全与健康管理局(OSHA)规定,在所有可能接触到血液或可能被血液污染的体液的患者护理活动中,必须佩戴手套(356)。
手套在防止医护人员手部污染方面的有效性已在多项临床研究中得到证实(45、51、58)。一项研究发现,在接触患者时佩戴手套的医护人员,每护理患者一分钟,手上平均仅被污染 3 个菌落形成单位(CFU),而不戴手套的医护人员每护理患者一分钟,手上平均被污染 16 个 CFU(51)。另外两项涉及护理艰难梭菌或耐万古霉素肠球菌(VRE)感染患者的研究表明,佩戴手套可防止大多数直接接触患者的工作人员手部受到污染(45、58)。佩戴手套还能防止工作人员在接触受污染的环境表面时手上沾染 VRE(58)。防止手部严重污染被认为很重要,因为当手部严重污染时,洗手或手部消毒可能无法去除所有潜在病原体(25、111)。
多项研究提供的证据表明,佩戴手套有助于减少医疗保健环境中病原体的传播。在一项前瞻性对照试验中,要求工作人员在处理任何人体物质时常规佩戴乙烯基手套,患者中艰难梭菌腹泻的发生率从干预前的每 1000 例患者出院 7.7 例下降到干预期间的每 1000 例出院 1.5 例(226)。在 “戴手套” 病房中,无症状艰难梭菌携带率也大幅下降,而在对照病房中则没有下降。在耐万古霉素肠球菌或耐甲氧西林金黄色葡萄球菌流行的重症监护病房中,要求所有医护人员在护理病房中的所有患者时都佩戴手套(即普遍使用手套),这很可能有助于控制疫情暴发(357、358)。
手套的使用对工作人员手部卫生习惯的影响尚不清楚。几项研究发现,佩戴手套的工作人员离开患者房间时洗手的可能性较小(290、320)。相比之下,另外两项研究发现,佩戴手套的工作人员在护理患者后洗手的可能性要大得多(87、301)。
关于医护人员使用手套,必须考虑以下注意事项。应告知工作人员,手套并不能完全防止手部污染。在接触患者时佩戴手套的医护人员中,不到 30% 的人的手上可分离出定植在患者身上的细菌菌群(50、58)。此外,佩戴手套并不能完全防止感染乙肝病毒和单纯疱疹病毒(359、360)。在这种情况下,病原体大概是通过手套的小破损,或者在脱手套时手部受到污染而接触到护理人员的手部(50、321、359、361)。
医护人员使用的手套通常由天然橡胶乳胶和合成非乳胶材料(如乙烯基、丁腈橡胶和氯丁橡胶 [氯丁二烯的聚合物和共聚物])制成。由于医护人员和患者中对乳胶过敏的情况日益普遍,美国食品药品监督管理局(FDA)已批准了几种蛋白质含量较低的有粉和无粉乳胶手套,以及医疗保健机构可为对乳胶过敏的员工提供的合成手套。在已发表的研究中,手套的屏障完整性因手套材料的类型和质量、使用强度、使用时间长短、制造商、手套是在使用前还是使用后进行测试以及检测手套泄漏的方法而异(359、361 – 366)。在已发表的研究中,乙烯基手套出现破损的频率比乳胶手套更高,使用后破损频率的差异最大(359、361、364、367)。然而,完好无损的乙烯基手套提供的防护效果与乳胶手套相当(359)。有限的研究表明,丁腈手套的泄漏率与乳胶手套相近(368 – 371)。准备多种类型的手套是可取的,因为这样工作人员可以选择最适合其患者护理活动的手套类型。尽管最近的研究表明手套的质量有所提高(366),但摘下手套后仍应对手部进行消毒或洗手(8、50、58、321、361)。手套不应清洗或重复使用(321、361)。使用含石油的护手霜或乳液可能会对手套的完整性产生不利影响(372)。使用有粉手套后,某些含酒精的手部消毒剂可能会与工作人员手上残留的粉末发生反应,导致手部有沙砾感。在经常使用有粉手套的机构中,应在摘下有粉手套后对各种含酒精的手部消毒剂进行测试,以避免选择会产生这种不良反应的产品。应提醒工作人员,在接触不同患者之间不摘手套可能会导致微生物传播(358、373)。
首饰
多项研究表明,戒指下方的皮肤比没有戴戒指的手指上的相同部位皮肤定植的细菌更多(374 – 376)。一项研究发现,40% 的护士的戒指下方皮肤上携带革兰氏阴性杆菌(如阴沟肠杆菌、克雷伯菌和不动杆菌),并且某些护士的戒指下方连续几个月携带相同的细菌(375)。在最近一项涉及 60 多名重症监护病房护士的研究中,多变量分析显示,戒指是携带革兰氏阴性杆菌和金黄色葡萄球菌的唯一重要风险因素,并且分离出的细菌浓度与佩戴戒指的数量相关(377)。佩戴戒指是否会导致病原体的传播增加尚不清楚。两项研究确定,洗手后戴戒指的人和不戴戒指的人手上的平均细菌菌落数相似(376、378)。需要进一步研究来确定在医疗保健环境中佩戴戒指是否会导致病原体的传播增加。
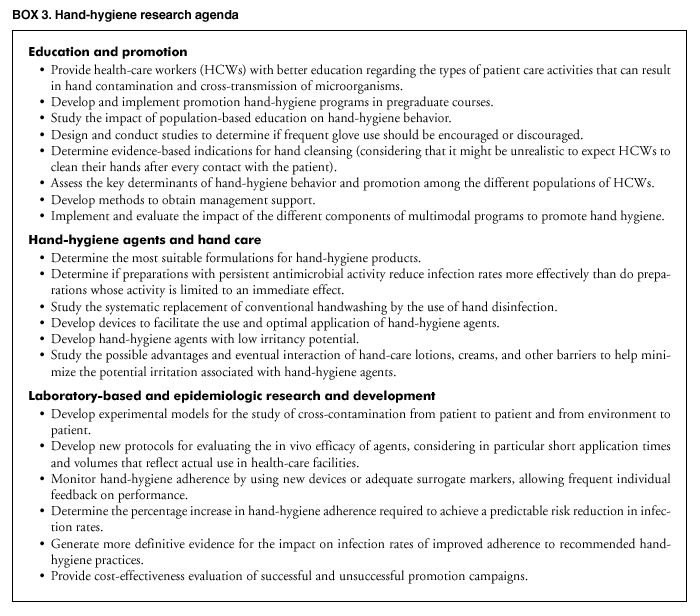
手部卫生研究议程
尽管近年来关于手部卫生的已发表研究数量大幅增加,但关于手部卫生产品以及提高工作人员对推荐政策依从性的策略,仍有许多问题尚未得到解答。工业界的研究人员和临床研究人员仍需解决几个问题(方框 3)。
基于 Web 的手部卫生资源
有关改善手部卫生的更多信息,请访问瑞士
日内瓦日内瓦 http://www.hopisafe.ch
大学医院 http://www.cdc.gov/ncidod/hip
佐治亚州
亚特兰大疾病预防控制中心 http://www.jr2.ox.ac.uk/bandolier/band88/b88-8.html
英国
Bandolier 杂志 http://www.med.upenn.edu
宾夕法尼亚大学,宾夕法尼亚州费城
第二部分.建议
分类
这些建议旨在改善医护人员的手部卫生习惯,并减少医疗保健环境中病原微生物向患者和工作人员的传播。本指南及其建议不适用于食品加工或餐饮服务场所,也无意取代美国食品药品监督管理局(FDA)《食品法典范本》所提供的指导意见。
与美国疾病控制与预防中心 / 医院感染控制实践咨询委员会(CDC/HICPAC)先前的指南一样,每条建议都基于现有的科学数据、理论依据、适用性和经济影响进行分类。CDC/HICPAC 对建议的分类系统如下:
- IA 类:强烈建议实施,且得到精心设计的实验、临床或流行病学研究的有力支持。
- IB 类:强烈建议实施,得到某些实验、临床或流行病学研究以及有力理论依据的支持。
- IC 类:根据联邦或州法规或标准的规定,必须实施。
- II 类:建议实施,得到有启发性的临床或流行病学研究或理论依据的支持。
- 无建议:未解决的问题。对于这些做法,存在证据不足或对其有效性尚未达成共识的情况。
建议
洗手和手部消毒的适用情况
- 当手部明显脏污、被蛋白质类物质污染,或明显被血液或其他体液弄脏时,使用非抗菌肥皂和水或抗菌肥皂和水洗手(IA 类)(66)。
- 如果手部没有明显脏污,在 1C – J 项所述的所有其他临床情况下,使用含酒精的手部消毒剂对手部进行常规去污(IA 类)(74、93、166、169、283、294、312、398)。或者,在 1C – J 项所述的所有临床情况下,使用抗菌肥皂和水洗手(IB 类)(69 – 71、74)。
- 在直接接触患者之前对手部进行去污(IB 类)(68、400)。
- 在插入中心血管内导管之前,在戴上无菌手套之前对手部进行去污(IB 类)(401、402)。
- 在插入留置导尿管、外周血管导管或其他无需手术操作的侵入性器械之前,对手部进行去污(IB 类)(25、403)。
- 在接触患者的完整皮肤后(例如,在测量脉搏或血压以及抬起患者时),对手部进行去污(IB 类)(25、45、48、68)。
- 如果手部没有明显脏污,在接触体液或排泄物、黏膜、非完整皮肤和伤口敷料后,对手部进行去污(IA 类)(400)。
- 在患者护理过程中,从污染的身体部位移动到清洁的身体部位时,对手部进行去污(II 类)(25、53)。
- 在接触患者附近的无生命物体(包括医疗设备)后,对手部进行去污(II 类)(46、53、54)。
- 摘下手套后,对手部进行去污(IB 类)(50、58、321)。
- 在进食前和使用卫生间后,使用非抗菌肥皂和水或抗菌肥皂和水洗手(IB 类)(404 – 409)。
- 可以考虑使用浸渍抗菌剂的湿巾(即湿纸巾)作为使用非抗菌肥皂和水洗手的替代方法。由于它们在减少医护人员手上的细菌数量方面不如含酒精的手部消毒剂或使用抗菌肥皂和水洗手有效,因此它们不能替代含酒精的手部消毒剂或抗菌肥皂(IB 类)(160、161)。
- 如果怀疑或证实接触了炭疽芽孢杆菌,使用非抗菌肥皂和水或抗菌肥皂和水洗手。在这种情况下,建议采用洗手和冲洗的物理动作,因为醇类、氯己定、碘伏和其他消毒剂对芽孢的活性较差(II 类)(120、172、224、225)。
- 对于在医疗保健环境中常规使用非酒精类手部消毒剂进行手部卫生,无法给出建议。这是一个未解决的问题。
手部卫生技术
- 当使用含酒精的手部消毒剂对手部进行去污时,将产品挤到一只手的手掌上,然后双手相互揉搓,覆盖手部和手指的所有表面,直到手部干燥(IB 类)(288、410)。按照制造商关于使用产品量的建议操作。
- 当使用肥皂和水洗手时,先用水将手浸湿,取制造商建议量的产品涂在手上,然后用力揉搓双手至少 15 秒,覆盖手部和手指的所有表面。用水冲洗双手,并用一次性纸巾彻底擦干。用纸巾关闭水龙头(IB 类)(90 – 92、94、411)。避免使用热水,因为反复接触热水可能会增加患皮炎的风险(IB 类)(254、255)。
- 使用非抗菌肥皂和水洗手时,液体肥皂、块状肥皂、片状肥皂或粉状肥皂都是可以接受的。使用块状肥皂时,应使用便于排水的肥皂架,并使用小块的肥皂(II 类)(412 – 415)。
- 不建议在医疗保健场所使用悬挂式或卷式的多次使用布质毛巾(II 类)(137、300)。
外科手部消毒
- 在开始外科手部擦洗之前,取下戒指、手表和手镯(II 类)(375、378、416)。
- 在流水下使用指甲清洁器清除指甲下的污垢(II 类)(14、417)。
- 在进行外科手术之前,在戴上无菌手套之前,建议使用抗菌肥皂或具有持久活性的含酒精手部消毒剂进行外科手部消毒(IB 类)(115、159、232、234、237、418)。
- 当使用抗菌肥皂进行外科手部消毒时,按照制造商建议的时间擦洗双手和前臂,通常为 2 – 6 分钟。长时间的擦洗(例如 10 分钟)是没有必要的(IB 类)(117、156、205、207、238 – 241)。
- 当使用具有持久活性的含酒精外科手部擦洗产品时,按照制造商的说明操作。在涂抹酒精溶液之前,先用非抗菌肥皂预洗双手和前臂,并将双手和前臂彻底擦干。按照建议涂抹含酒精产品后,在戴上无菌手套之前,让双手和前臂彻底干燥(IB 类)(159、237)。
手部卫生制剂的选择
- 为工作人员提供有效且潜在刺激性低的手部卫生产品,尤其是当这些产品每班需要多次使用时(IB 类)(90、92、98、166、249)。本建议适用于临床区域中在患者护理前后用于手部消毒的产品,以及外科人员用于外科手部消毒的产品。
- 为了最大限度地提高医护人员对手部卫生产品的接受度,就正在考虑使用的任何产品的手感、香味和皮肤耐受性,征求这些员工的意见。手部卫生产品的成本不应是影响产品选择的主要因素(IB 类)(92、93、166、274、276 – 278)。
- 在选择非抗菌肥皂、抗菌肥皂或含酒精的手部消毒剂时,向制造商索取有关用于清洁手部的产品、护肤产品以及机构中使用的手套类型之间的已知相互作用的信息(II 类)(174、372)。
- 在做出购买决策之前,评估各种产品制造商或经销商的分配器系统,以确保分配器功能正常,并能挤出适量的产品(II 类)(286)。
- 不要向部分已使用的肥皂分配器中添加肥皂。这种 “加满” 分配器的做法可能会导致肥皂受到细菌污染(IA 类)(187、419)。
皮肤护理
- 为医护人员提供护手霜或乳液,以尽量减少与手部消毒或洗手相关的刺激性接触性皮炎的发生(IA 类)(272、273)。
- 向制造商索取有关护手霜、乳液或含酒精的手部消毒剂可能对机构中正在使用的抗菌肥皂的持久效果产生的任何影响的信息(IB 类)(174、420、421)。
手部卫生的其他方面
- 在直接接触高风险患者(例如,重症监护病房或手术室的患者)时,不要佩戴人造指甲或指甲延长器(IA 类)(350 – 353)。
- 保持自然指甲尖端长度不超过 1/4 英寸(II 类)(350)。
- 当可能接触到血液或其他潜在传染性物质、黏膜和非完整皮肤时,佩戴手套(IC 类)(356)。
- 在护理完一名患者后摘下手套。不要佩戴同一副手套护理多名患者,并且在不同患者之间使用手套后不要清洗手套(IB 类)(50、58、321、373)。
- 在患者护理过程中,如果从污染的身体部位移动到清洁的身体部位,更换手套(II 类)(50、51、58)。
- 对于在医疗保健场所佩戴戒指,无法给出建议。这是一个未解决的问题。
医护人员的教育和激励计划
- 作为改善医护人员手部卫生习惯的整体计划的一部分,对工作人员进行教育,让他们了解哪些患者护理活动可能导致手部污染,以及各种清洁手部方法的优缺点(II 类)(74、292、295、299)。
- 监测医护人员对推荐的手部卫生规范的依从情况,并向工作人员提供有关他们表现的信息(IA 类)(74、276、292、295、299、306、310)。
- 鼓励患者及其家属提醒医护人员对手部进行去污(II 类)(394、422)。
管理措施
- 将提高手部卫生依从性作为机构的优先事项,并提供适当的管理支持和财政资源(IB 类)(74、75)。
- 实施一个多学科计划,旨在提高卫生人员对推荐的手部卫生规范的依从性(IB 类)(74、75)。
- 作为提高手部卫生依从性的多学科计划的一部分,为医护人员提供易于获取的含酒精手部消毒剂产品(IA 类)(74、166、283、294、312)。
- 为了提高在预计工作量大且患者护理强度高的区域工作的人员的手部卫生依从性,在患者房间入口处或床边、其他方便的位置以及医护人员随身携带的个人口袋大小的容器中提供含酒精手部消毒剂(IA 类)(11、74、166、283、284、312、318、423)。
- 将含酒精手部消毒剂的储备存放在经批准可存放易燃材料的柜子或区域内(IC 类)。
第三部分.绩效指标
引用
- Rotter M. 洗手和手消毒 [第 87 章]。在:Mayhall CG,编辑。医院流行病学和感染控制。 第 2 版费城,宾夕法尼亚州:Lippincott Williams & Wilkins,1999年。
- 拉巴拉克公司。关于使用苏打水和石灰氯化物的说明和观察。Porter J, ed. [法语] 康涅狄格州纽黑文: 鲍德温和特雷德韦,1829 年。
- Semmelweis I. 产褥热的病因、概念和预防。卡特 KC,编辑。 第1 版。威斯康星州麦迪逊:威斯康星大学出版社,1983 年。
- 患者护理中的洗手 [动态图片]。华盛顿特区:美国公共卫生服务局,1961 年。
- Steere AC,Mallison GF。预防院内感染的洗手做法。Ann 实习医生 1975;83:683–90.
- Garner JS, Favero MS. CDC 洗手和医院环境控制指南,1985 年。感染控制 1986;7:231–43.
- Larson E. 局部抗菌剂使用指南。Am J 感染控制 1988;16:253–66.
- Larson EL,APIC 指南委员会。APIC 医疗保健环境中洗手和手部消毒指南。Am J 感染 对照 1995;23:251–69.
- 医院感染控制实践咨询委员会 (HICPAC)。防止万古霉素耐药性扩散的建议。 感染控制医院流行病学 1995;16:105–13.
- Garner JS,医院感染控制实践咨询委员会。医院隔离预防措施指南。感染控制中心 流行病学 1996;17:53–80.
- Pittet D、Mourouga P、Perneger TV、感染控制计划的成员。在教学医院遵守洗手规定。安 实习医学 1999;130:126–30.
- 博伊斯 JM。现在是采取行动的时候了:改善医院的手部卫生。Ann 实习医学 1999;130:153–5.
- Selwyn S. 人体皮肤的微生物学和生态学。从业者 1980 年;224:1059–62.
- 价格 PB。正常皮肤的细菌学:一种新的定量测试,应用于细菌菌群和消毒作用的研究 机械清洁。J Infect Dis 1938;63:301–18.
- Larson E. 洗手剂、洗手频率和临床区域对手部植物群群的影响。Am J 感染控制 1984;11:76–82.
- Maki D. 控制医院病原菌的定植和传播。Ann 实习医生 1978;89(第 2 部分):777–80。
- Larson EL、Norton Hughes CA、Pyrak JD、Sparks SM、Cagatay EU、Bartkus JM。与手部皮肤损伤相关的细菌菌群变化 的医护人员。Am J 感染控制 1998;26:513–21.
- Sprunt K, Redman W, Leidy G. 常规洗手的抗菌效果。儿科 1973;52:264–71.
- 美国食品和药物管理局。医疗保健消毒药品暂定最终专论;建议的规则。联邦公报 1994;59:31441–52.
- 洛布里 EJL。皮肤上的革兰氏阴性杆菌。Br J Dermatol 1969;81(增刊 1):55–61。
- 高贵的 WC。微球菌科的分布。Br J Dermatol 1969;81(增刊 1):27–31。
- McBride ME、Duncan WC、Bodey GP、McBride CM. 选定的癌症患者和医院人员的微生物皮肤菌群。J Clin 微生物学 1976;3:14–20.
- 凯斯韦尔 MW。手在医院革兰氏阴性菌感染中的作用。在:Maibach HI, Aly R, eds.皮肤微生物学:与临床的相关性 感染。纽约州纽约市:Springer-Verlag,1981 年。
- Larson EL, McGinley KJ, Foglia AR, Talbot GH, Leyden JJ. 住院和健康皮肤菌群的组成和抗菌素耐药性 成年人。J Clin Microbiol 1986;23:604–8.
- 新泽西州埃伦克兰茨,阿方索 BC。未能使用温和的肥皂洗手液来防止患者细菌转移到尿道导管。感染控制 Hosp Epidemiol 1991 年;12:654–62.
- Sanderson PJ, Weissler S. 从护士和患者手中回收大肠菌群:导致污染的活动。J Hosp 感染 1992;21:85–93.
- Coello R、Jiménez J、García M 等人。在影响 990 名患者的疫情中耐甲氧西林金黄色葡萄球菌感染、定植和携带的前瞻性研究。Eur J Clin Microbiol Infect Dis 1994;13:74–81.
- 桑福德 MD、Widmer AF、贝尔 MJ、琼斯 RN、温泽尔 RP。有效检测和长期持续携带 耐甲氧西林金黄色葡萄球菌。Clin Infect Dis 1994;19:1123–8.
- Bertone SA、Fisher MC、Mortensen JE。新生儿潜在导管部位的定量皮肤培养。感染控制中心 流行病学 1994;15:315–8.
- Bonten MJM、Hayden MK、Nathan C、VanVoorhis J 等人。患者和环境定植的流行病学 耐万古霉素肠球菌。柳叶刀 1996;348:1615–9.
- Larson EL, Cronquist AB, Whittier S, Lai L, Lyle CT, Della Latta P. 住院患者和慢性病患者之间皮肤菌群的差异。 心肺 2000;29:298–305.
- Polakoff S, Richards IDG, Parker MT, Lidwell OM. 接受外科手术的患者对金黄色葡萄球菌的鼻腔和皮肤携带。J Hyg (Lond) 1967;65:559–66.
- 莱顿 JJ、麦金利 KJ、诺德斯特龙 KM、韦伯斯特 GF。皮肤微生物群落。J Invest Dermatol 1987;88:65 秒–72 秒。
- Tuazon CU、Perez A、Kishaba T、Sheagren JN。胰岛素注射糖尿病患者的金黄色葡萄球菌。美国医学会 1975;231:1272。
- 卡普洛维茨 LG、康斯托克 JA、兰德维尔 DM、道尔顿 HP、梅霍尔 CG。鼻子和皮肤微生物定植的前瞻性研究 血液透析患者血管通路部位感染。J Clin Microbiol 1988;26:1257–62.
- Aly R, Maibach HI, Shinefield HR. 特应性皮炎的微生物菌群。Arch Dermatol 1977 年;113:780–2.
- Kirmani N、Tuazon CU、Murray HW、Parrish AE、Sheagren JN。接受长期血液透析的患者金黄色葡萄球菌携带率。 Arch 实习医生 1978;138:1657–9.
- Goldblum SE、Ulrich JA、Goldman RS、Reed WP。血液透析患者和工作人员的鼻腔和皮肤菌群:定量和 葡萄球菌携带的定性特征和模式。Am J Kidney Dis 1982 年;11:281–6.
- Boelaert JR, Van Landuyt HW, Gordts BZ, De Baere YA, Messer SA, Herwaldt LA.血液透析患者金黄色葡萄球菌的鼻腔和皮肤携带:鼻腔莫匹罗星的作用。感染控制医院流行病学 1996;17:809–11.
- Zimakoff J, Pedersen FB, Bergen L, et al. 四个血液和腹膜透析中心患者金黄色葡萄球菌携带和感染 在丹麦。J Hosp 感染 1996;33:289–300.
- Bibel DJ、Greenbert JH、Cook JL。金黄色葡萄球菌和特应性皮炎的微生物生态学。Can J Microbiol 1997;23:1062–8.
- 高贵的 WC。皮肤微生物的扩散。Br J Dermatol 1975;93:477–85.
- 葡萄球菌向环境的传播。抗生素年鉴 1959:952–7。
- Boyce JM、Opal SM、Chow JW 等人。具有可转移性 vanB 级万古霉素耐药性的多重耐药屎肠球菌暴发。J Clin Microbiol 1994;32:1148–53.
- McFarland LV, Mulligan ME, Kwok RYY, Stamm WE.艰难梭菌感染的院内获得性。N Engl J Med 1989 年;320:204–10.
- Samore MH, Venkataraman L, DeGirolami PC, Levin E, Arbeit RD, Karchmer AW.散发性和 院内梭菌的聚集性病例 艰难腹泻。美国医学杂志 1996;100:32–40.
- Lidwell OM, Towers AG, Ballard J, Gladstone B. 在清洁空气环境中护士和患者之间微生物的转移。J 应用细菌 1974;37:649–56.
- Casewell M, Phillips I. 手作为克雷伯氏菌物种的传播途径。Br Med J 1977 年;2:1315–7.
- Hall CB,道格拉斯 RG。呼吸道合胞病毒的传播方式。儿科杂志 1981;99:100–2.
- 奥尔森 RJ、林奇 P、科伊尔 MB、卡明斯 J、博克特 T、斯塔姆 WE。检查手套在临床实践中作为手部污染的屏障。 美国医学会 1993;270:350–3.
- 皮特 D、达兰 S、图韦诺 S、索万 V、佩内格电视台。在常规患者护理期间,医院工作人员的手受到细菌污染。 Arch Intern Med 1999 年;159:821–6.
- 福克斯 MK、朗纳 SB、威尔斯 RW。洗手习惯有多好?Am J 护理学 1974;74:1676–8.
- Ojajärvi J. 洗手和消毒方法在患者护理后去除短暂细菌的有效性。J Hyg (伦敦) 1980;85:193–203.
- Boyce JM, Potter-Bynoe G, Chenevert C, King T. 耐甲氧西林金黄色葡萄球菌引起的环境污染:可能的感染控制影响。感染控制医院流行病学 1997;18:622–7.
- Hayden, MK, Blom, DW, Lyle, EA 等人。医护人员 (HCW) 在接触 VRE 后感染手和手套的风险 (+) 患者 (pt) 或 pts 环境 (env) [摘要 K-1334]。在 第 41届抗菌剂 Interscience 会议 和芝加哥化疗:美国微生物学会,2001 年。
- 斯科特 E,布卢姆菲尔德 SF。微生物污染通过布、手和器皿的存活和转移。J Appl Bacteriol 1990;68:271–8.
- 鲍尔 TM, Ofner E, Just HM, Just H, Daschner FD.一项评估空气传播和直接传播相对重要性的流行病学研究 内科重症监护病房中微生物的接触传播。J Hosp 感染 1990;15:301–9.
- Tenorio AR、Badri SM、Sahgal NB 等人。手套在患者护理后预防医护人员手携带耐万古霉素肠球菌的有效性。Clin Infect Dis 2001;32:826–9.
- 达施纳 FD.目前使用防腐剂的成本效益如何?J Hosp 感染 1988;11(增刊 A):227–35。
- Knittle MA, Eitzman DV, Baer H. 人员手部污染在革兰氏阴性院内感染流行病学中的作用。J 儿科 1975;86:433–7.
- 艾利夫 GAJ、巴布 JR、戴维斯 JG、莉莉 HA。手部消毒:实验室和病房研究中各种药物的比较。J 医院 感染 1988;11:226–43.
- Strausbaugh LJ、Sewell DL、Ward TT、Pfaller MA、Heitzman T、Tjoelker R. 医院工作人员手上酵母携带频率高。J Clin Microbiol 1994 年;32:2299–300.
- Marples RR,Towers AG。用于研究微生物接触转移的实验室模型。J Hyg (Lond) 1979;82:237–48.
- 麦金托什 CA,霍夫曼 PN。微生物通过手转移的扩展模型:生物之间的差异和效果 酒精消毒。J Hyg (Lond) 1984;92:345–55.
- 帕特里克 DR,芬顿 G,米勒 TE。残留水分决定了手部后触摸接触相关细菌转移的水平 洗涤。流行病菌感染 1997;119:319–25.
- 拉森 E.洗手与感染风险之间的因果关系?证据审查。感染控制医院流行病学 1988;9:28–36.
- Larson E. 皮肤卫生和感染预防:更多相同或不同的方法?Clin Infect Dis 1999;29:1287–94.
- Mortimer EA Jr, Lipsitz PJ, Wolinsky E, Gonzaga AJ, Rammelkamp CH Jr. 葡萄球菌在新生儿之间的传播。敌法师 J Dis Child 1962 年;104:289–95.
- 真希 DG.医务人员使用消毒剂洗手。J Chemother 1989 年;1(增刊 1):3–11。
- Massanari RM, Hierholzer WJ Jr.消毒肥皂对重症监护病房医院感染率的交叉比较。敌法师 J 感染控制 1984;12:247–8.
- Doebbeling BN、Stanley GL、Sheetz CT 等人。替代洗手剂在减少 重症监护病房。N Engl J Med 1992 年;327:88–93.
- Webster J, Faoagali JL, Cartwright D. 术后从新生儿重症监护病房中消除耐甲氧西林金黄色葡萄球菌 用三氯生洗涤。J 儿科儿童健康 1994;30:59–64.
- Zafar AB、Butler RC、Reese DJ、Gaydos LA、Mennonna PA。使用 0.3% 三氯生 (Bacti-Stat*) 根除 新生儿托儿所中的耐甲氧西林金黄色葡萄球菌。Am J 感染控制 1995;23:200–8.
- Pittet D, Hugonnet S, Harbarth S, Mourouga P, Sauvan V, Touveneau S. 全院计划提高依从性的有效性 手部卫生。柳叶刀 2000;356:1307–12.
- Larson EL, Early E, Cloonan P, Sugrue S, Parides M.与增加洗手相关的组织气候干预 减少院内感染。Behav Med 2000;26:14–22.
- Fridkin SK、Pear SM、Williamson TH、Galgiani JN、Jarvis WR。人手不足在中心静脉导管相关血流中的作用 感染。感染控制医院流行病学 1996;17:150–8.
- 维卡 AF。护理人员的工作量是耐甲氧西林金黄色葡萄球菌在成人重症治疗病房中传播的决定因素。J Hosp Infect 1999 年;43:109–13.
- Harbarth S, Sudre P, Dharan S, Cadenas M, Pittet D. 与人手不足、过度拥挤和不良卫生习惯有关的泄殖腔肠杆菌爆发。感染控制医院流行病学 1999;20:598–603.
- 欧洲标准化委员会。化学消毒剂及防腐剂—卫生搓手液—测试方法及要求 (阶段 2/步骤 2)[欧洲标准 EN 1500]。比利时布鲁塞尔:中央秘书处:1997 年。
- Kramer A, Rudolph P, Kampf G, Pittet D. 酒精类洗手液的有限功效。柳叶刀 2002;359:1489–90.
- Sattar SA, Abebe M, Bueti AJ, Jampani H, Newman J, 华 S. 酒精基手凝胶对人腺、鼻和 使用指垫法的轮状病毒。感染控制医院流行病学 2000;21:516–9.
- Wolff MH, Schmitt J, Rahaus M, König A. 甲型肝炎病毒:一种检测 杀病毒活性的方法。J Hosp 感染 2001;48(增刊 A):S18–S22。
- 斯坦曼 J.杀病毒测试的一些原则。J Hosp 感染 2001;48(增刊 A):S15–S17。
- Gould D, Ream E. 评估护士的手部净化表现。护理时报 1993;89:47–50.
- Quraishi ZA、McGuckin M、Blais FX。重症监护病房洗手的持续时间:一项描述性研究。Am J 感染控制 1984;11:83–7.
- Lund S, Jackson J, Leggett J, Hales L, Dworkin R, Gilbert D. 社区医院手套使用和洗手的现实情况。Am J 感染 Control 1994 年;22:352–7.
- Meengs MR, Giles BK, Chisholm CD, Cordell WH, Nelson DR. 急诊科的洗手频率。安·埃默格 Med 1994 年;23:1307–12.
- Larson E、McGeer A、Quraishi ZA 等人。自动水槽对高风险单元洗手习惯和态度的影响。感染控制 Hosp Epidemiol 1991 年;12:422–8.
- Broughall JM、Marshman C、Jackson B、Bird P.用于测量洗手频率的自动监控系统。J Hosp 感染 1984;5:447–53.
- Ojajärvi J, Mäkelä P, Rantasalo I. 经常洗手时手消毒失败:需要长时间的实地研究。海杰 (隆德) 1977 年;79:107–19.
- Larson EL、Eke PI、Wilder MP、Laughon BE。肥皂的数量是洗手中的变量。感染控制 1987;8:371–5.
- 拉森 E、莱顿 JJ、麦金利 KJ、格罗夫 GL、塔尔博特 GH。与频繁洗手相关的皮肤生理和微生物学变化。 感染控制 1986;7:59–63.
- Larson EL、Eke PI、Laughon BE。酒精洗手液在频繁使用条件下的功效。抗菌剂 Chemother 1986;30:542–4.
- 拉森 EL,劳伦 BE。四种含有葡萄糖酸氯己定的防腐剂产品的比较。抗菌剂 Chemother 1987;31:1572–4.
- Meers PD, Yeo GA. 洗手后细菌和皮肤鳞屑脱落。J Hyg (Lond) 1978;81:99–105.
- Winnefeld M, Richard MA, Drancourt M, Grobb JJ. 日常两种手部去污程序的皮肤耐受性和有效性 医院使用。Br J Dermatol 2000;143:546–50.
- Maki DG、Zilz MA、Alvarado CJ。四种洗手剂的抗菌效果评估。在:Nelson JC, Grassi C, eds.目前的化疗和传染病会议记录 第 11届国际化疗和化学大会 第 19届 ICACC.华盛顿特区:美国微生物学会,1979 年。
- Boyce JM, Kelliher S, Vallande N. 与两种手部卫生方案相关的皮肤刺激和干燥:肥皂和水洗手与 使用酒精洗手液进行手部消毒。感染控制医院流行病学 2000;21:442–8.
- Sartor C, Jacomo V, Duvivier C, Tissot-Dupont H, Sambuc R, Drancourt M. 与以下相关的院内粘质沙雷氏菌感染 液体非药物肥皂的外源性污染。感染控制医院流行病学 2000;21:196–9.
- 社论:手部消毒。美国外科杂志 1965;109:691–3.
- Gravens DL、Butcher HR Jr、Ballinger WF、Dewar NE. 用于手术室人员手部的 Septisol 消毒泡沫:一种有效的 抗菌剂。外科 1973;73:360–7.
- Eitzen HE, Ritter MA, 法国 MLV, Gioe TJ.外科洗手剂的微生物使用比较。J 骨关节外科 Am 1979;61–A:403–6.
- Minakuchi K、Yamamoto Y、Matsunaga K 等人。速干摩擦型聚维酮碘酒精消毒剂的防腐效果 溶液。研究生医学杂志 1993;69(增刊 3):S23–S26。
- 巴布 JR,戴维斯 JG,艾利夫 GAJ。评估外科手部消毒的测试程序。J Hosp 感染 1991;18(增刊 B):41–9。
- 贝拉米 K、阿尔科克 R、巴布 JR、戴维斯 JG、艾利夫 GA。使用轮状病毒评估“卫生”手部消毒的测试。J 医院 感染 1993;24:201–10.
- Ayliffe GAJ, Babb JR, Quoraishi AH.“卫生”手部消毒测试。J Clin Pathol 1978;31:923–8.
- Lilly HA、Lowbury EJL、Wilkins MD。洗涤剂彼此比较,并与作为皮肤“去菌”剂的防腐剂进行比较。海杰 (隆德) 1979;82:89–93.
- 乌尔里希 JA。比较 hibistat(0.5% 葡萄糖酸氯己定溶于 70% 异丙醇溶液中)和优碘手术擦洗膏(7.5% 聚维酮碘)对人体皮肤的实验性污染有疗效。Curr Ther Res 1982 年;31:27–30.
- Bartzokas CA、Gibson MF、Graham R、Pinder DC。三氯生和洗必泰制剂与 60% 异丙醇的比较 用于卫生的手部消毒。J Hosp 感染 1983;4:245–55.
- Rotter ML, Koller W, Wewalka G, Werner HP, Ayliffe GAJ, Babb JR. 卫生手部消毒程序的评估:受控 Vienna 测试模型的并行实验。J Hyg (Lond) 1986 年;96:27–37.
- Kjrlen H, Andersen BM. 洗手和消毒严重污染的手—有效还是无效?J Hosp 感染 1992;21:61–71.
- Namura S, Nishijima S, 浅田 Y.抗菌洗手液残留活性的评估:“使用中”环境研究。J 皮肤醇 1994;21:481–5.
- 贾维斯 JD、Wynne CD、Enwright L、Williams JD。在医院洗手和含消毒肥皂。J Clin Path 1979 年;32:732–7.
- 佩雷拉 LJ、李 GM、韦德 KJ。与皮肤状况和微生物计数相关的五种手术洗手方案的评估。J Hosp Infect 1997 年;36:49–65.
- 拉森 EL、Butz AM、Gullette DL、劳伦 BA。用于手术擦洗的酒精?感染控制医院流行病学 1990;11:139–43.
- Aly R,迈巴赫 HI。0.5% 葡萄糖酸氯己定和 70% 异丙醇对正常抗菌效果的比较研究 手的植物群。应用环境微生物学 1979;37:610–3.
- Galle PC, Homesley HD, Rhyne AL. 重新评估手术擦洗。Surg Gynecol Obstet 1978 年;147:215–8.
- 罗森伯格 A,阿拉塔里 SD,彼得森 AF。安全性和有效性 抗菌葡萄糖酸氯己定。Surg Gynecol Obstet 1976 年;143:789–92.
- Ayliffe GAJ、Babb JR、Bridges K 等人。评估从皮肤中去除总生物体和病原体的两种方法的比较。J Hyg (Lond) 1975;75:259–74.
- 拉尔森 EL,莫顿 HE。醇类 [第 11 章]。在:Block SS,编辑。消毒、灭菌和保存。 第 4 版。宾夕法尼亚州费城:Lea 和 Febiger,1991:642-54。
- 价格 PB。乙醇作为杀菌剂。Arch Surg 1939 年;38:528–42.
- 哈灵顿 C,沃克 H.酒精的杀菌作用。波士顿医学和外科杂志 1903 年;148:548–52.
- 价格 PB。外科细菌学和外科技术的新研究。美国医学会 1938 年;111:1993–6.
- 库特哈德 CE,赛克斯 G.酒精的杀菌作用,特别提到它对细菌孢子的作用。药学杂志 1936;137:79–81.
- Pohle WD,斯图尔特 LS。清洁的杀菌作用 agents—对 Price 程序修改的研究。J Infect Dis 1940;67:275–81.
- Gardner AD. 清洁未洗过的皮肤的快速消毒:进一步的实验。柳叶刀 1948:760–3。
- Sakuragi T, Yanagisawa K, Dan K. 皮肤消毒剂对耐甲氧西林金黄色葡萄球菌的杀菌活性。阿内斯·阿纳尔格 1995;81:555–8.
- Kampf G, Jarosch R, Rüden H. 基于洗必泰的手消毒剂对耐甲氧西林金黄色葡萄球菌 (MRSA) 的有效性有限。J Hosp 感染 1998;38:297–303.
- Kampf G, Höfer M, Wendt C. 手消毒剂在体外对耐万古霉素肠球菌的疗效。J Hosp 感染 1999;42: 143–50.
- 普拉特 J,巴克纳尔 RA。用异丙醇和洗必泰洗涤剂洗手液对呼吸道合胞病毒进行消毒。J Hosp 感染 1985;6:89–94.
- Krilov LR, Harkness SH. 洗涤剂和消毒剂灭活呼吸道合胞病毒。儿科感染病 1993;12:582–4.
- Sattar SA, Tetro J, Springthorpe VS, Giulivi A. 防止乙型和丙型肝炎病毒的传播:杀菌剂在哪里相关?Am J 感染 Control 2001 年;29:187–97.
- 伍尔万 JD,Gerberding JL。检测方法对抗病毒消毒剂和防腐剂表观活性的影响。抗菌剂 Chemother 1995 年;39:921–3.
- Pillsbury DM、Livingood CS、Nichols AC. 正常皮肤的细菌菌群:报告各种软膏和溶液的效果,包括 评论本研究的临床意义。Arch Dermatol 1942 年;45:61–80.
- Lowbury EJL、Lilly HA、Ayliffe GAJ。外科医生手部的术前消毒:酒精溶液的使用和手套对皮肤菌群的影响。 Br Med J 1974 年;4:369–72.
- Lilly HA、Lowbury EJL、Wilkins MD、Zaggy A. 酒精消毒的延迟抗菌作用。J Hyg (Lond) 1979;82: 497–500.
- Ansari SA、Springthorpe VS、Sattar SA、Tostowaryk W、Wells GA. 布、纸和暖风干燥在消除病毒方面的比较 以及洗手时的细菌。Am J 感染控制 1991;19:243–9.
- Ansari SA, Sattar SA, Springthorpe VS, Wells GA, Tostowaryk W.测试洗手剂对病毒功效的体内方案 和细菌:轮状病毒和埃希菌属的实验 大肠杆菌。应用环境微生物学 1989;55:3113–8.
- 斯坦曼 J、尼尔科恩 R、迈耶 A、贝克尔 K。两种体内方案,用于测试洗手和手消毒的杀病毒功效。 Zentralbl Hyg Umweltmed.1995;196:425–36.
- Mbithi JN, Springthorpe VS, Sattar SA.洗手剂对甲型肝炎病毒 (HM-175) 的体内效率比较 1 型脊髓灰质炎病毒 (Sabin)。应用环境微生物学 1993;59:3463–9.
- 舒尔曼 W,艾格斯 HJ。酒精手消毒剂的抗病毒活性:体外悬浮试验与体内实验的比较 在手上,以及在每个指尖上。抗病毒研究 1983;3:25–41.
- Larson E, Bobo L. 在有血的情况下进行有效的手部去菌。J Emerg Med 1992 年;10:7–11.
- Dineen P, Hildick-Smith G. 手部的消毒护理 [第 21 章]。在:Maibach HI,Hildick-Smith G,编辑。皮肤细菌及其作用 在感染中。纽约:麦格劳-希尔,1965 年。
- Lilly HA,洛布里 EJL。短暂的皮肤菌群:根据其沉积方式通过清洁或消毒来去除它们。J Clin 路径 1978;31:919–22.
- Rotter M、Koller W、Wewalka G. 用于手部消毒的含聚维酮碘和葡萄糖酸氯己定的洗涤剂。J 医院 感染 1980;1:149–58.
- 卫生手部消毒。感染控制 1984;1: 18–22.
- Blech MF、Hartemann P、Paquin JL。非消毒肥皂和乙醇的手部消毒活性。Zentralbl Bakteriol Hyg [B] 1985;181:496–512.
- Leyden JJ、McGinley KJ、Kaminer MS 等人。全手触摸板的计算机图像分析:一种表面定量方法 手上的细菌和抗菌剂的作用。J Hosp 感染 1991;18(增刊 B):13–22。
- Rotter ML, Koller W. 卫生洗手液和卫生洗手液的测试模型:两种不同污染和采样的影响 技术。J Hosp 感染 1992;20:163–71.
- Zaragoza M, Sallés M, Gomez J, Bayas JM, Trilla A. 用肥皂或酒精溶液洗手?其 有效性。Am J 感染控制 1999;27:258–61.
- 保尔森 DS、芬德勒 EJ、多兰 MJ、威廉姆斯 RA。仔细观察酒精凝胶作为抗菌消毒剂。Am J 感染对照 1999;27:332–8.
- Cardoso CL, Pereira HH, Zequim JC, Guilhermetti M. 手部清洁剂从受污染的手上去除鲍曼不动杆菌菌株的有效性。Am J 感染控制 1999;27:327–31.
- Casewell MW, Law MM, Desai N.卫生手部消毒剂测试剂的实验室模型:洗手和洗必泰 去除克雷伯氏菌。J Hosp 感染 1988;12:163–75.
- 韦德 JJ,德赛 N,凯斯韦尔 MW。用于去除流行性耐万古霉素的屎肠球菌和对庆大霉素的阴沟肠杆菌的卫生手部消毒。J Hosp 感染 1991;18:211–8.
- Huang Y, Oie S, Kamiya A. 手部清洁效果比较 去除耐甲氧西林葡萄球菌的药物 来自实验污染指尖的金黄色葡萄球菌。Am J 感染控制 1994;22:224–7.
- Lowbury EJL,Lilly HA。外科医生和护士的手部消毒。Br Med J 1960;1:5184。
- 伯曼 RE,奈特 RA。手部消毒液的评估。Arch Environ Health 1969 年;18:781–3.
- Rotter ML、Simpson RA、Koller W. 使用不同浓度的醇类进行外科手部消毒:使用新型 提议的欧洲标准方法。感染控制医院流行病学 1998;19:778–81.
- Hobson DW, Woller W, Anderson L, Guthery E. 一种新的酒精基外科洗手液配方的开发和评估 持久的抗菌特性和无刷应用。Am J 感染控制 1998;26:507–12.
- 琼斯 MV,罗 GB,杰克逊 B,新泽西州普里查德。使用酒精纸湿巾进行常规手部清洁:两家医院的试验结果。J Hosp Infect 1986 年;8:268–74.
- Butz AM, Laughon BE, Gullette DL, Larson EL. 酒精浸渍湿巾作为手部卫生的替代品。Am J 感染控制 1990;18:70–6.
- Ojajärvi J. 芬兰的洗手。J Hosp 感染 1991;18(增补) B): 35–40.
- 纽曼 JL,塞茨 JC。间歇性使用抗菌洗手液,以减少肥皂对医护人员的刺激。敌法师 J 感染控制 1990;18:194–200.
- 罗特 ML, 科勒 W, 诺伊曼 R.化妆品添加剂对酒精类手部消毒剂可接受性的影响。J 医院 感染 1991;18(增刊 B):57–63。
- Larson EL、Aiello AE、Heilman JM 等人。手术手部准备不同方案的比较。AORN J 2001 年;73:412–20.
- Larson EL、Aiello AE、Bastyr J 等人。重症监护病房人员的两种手部卫生方案评估。Crit Care Med 2001 年;29;944–51.
- Ophaswongse S, 迈巴赫 HI.酒精性皮炎:过敏性接触性皮炎和接触性荨麻疹综合征:综述。接触性皮炎 1994;30:1–6.
- Rilliet A, Hunziker N, Brun R. 酒精接触性荨麻疹综合征(速发型超敏反应):病例报告。皮肤病菌 1980;161:361–4.
- Widmer AF.用无水酒精搓手液代替洗手?Clin Infect Dis 2000;31:136–43.
- Bryant KA, Pearce J, Stover B. 与使用酒精类防腐剂相关的闪火 [信件]。Am J 感染控制 2002;30:256–7.
- Hsueh PR, Teng LJ, Yang PC, Pan HL, Ho SW, Luh KT. 蜡样芽孢杆菌引起的院内假性流行病可追溯到受污染的乙基 来自酒类工厂的酒精。J Clin Microbiol 1999;37:2280–4.
- 丹顿 GW。洗必泰 [第 16 章]。在:Block SS,编辑。消毒、灭菌和预订。 第 4 版。宾夕法尼亚州费城:Lea 和 Febiger,1991 年。
- Narang HK,Codd AA。常用消毒剂对肠道病毒的作用。J Hosp 感染 1983;4:209–12.
- 沃尔什 B、布莱克莫尔 PH、德拉布 YJ。护手霜对葡萄糖酸氯己定抗菌活性的影响。J Hosp 感染 1987;9:30–3.
- Lowbury EJL,Lilly HA。使用 4% 洗必泰洗涤剂溶液 (Hibiscrub) 和其他皮肤消毒方法。Br Med J 1973 年;1:510–5.
- 保尔森 DS.五种外科洗手液制剂的比较评价。AORN J 1994 年;60:246–56.
- Stingeni L, Lapomarda V, Lisi P. 医院环境中的职业性手部皮炎。接触性皮炎 1995;33:172–6.
- Marrie TJ, Costerton JW.粘质沙雷氏菌在洗必泰中的存活时间延长。应用环境微生物学 1981;42:1093–102.
- McAllister TA, Lucas CE, Mocan H, et al. 儿科肿瘤病房粘质沙雷氏菌爆发,可追溯到受污染的洗必泰。斯科特 医学杂志 1989;34:525–8.
- Vigeant P、Loo VG、Bertrand C 等人。与受污染的洗必泰有关的粘质沙雷氏菌感染暴发。感染控制 Hosp Epidemiol 1998;19:791–4.
- Vu-Thien H、Darbord JC、Moissenet D 等人。调查烧伤病房中氯己定传播的 Alcaligenes xylosoxidans 引起的伤口感染爆发。Eur J Clin Microbiol 1998;17:724–6.
- 拉森 E,塔尔博特 GH。选择医护人员洗手剂的方法。感染控制 1986;7:419–24.
- 戴维斯 J、巴布 JR、艾利夫 GAJ、威尔金斯医学博士。腹部皮肤消毒。Br J 外科杂志 1978;65:855–8.
- Larson E、Mayur K、Laughon BA。两种洗手频率对 3 种洗手产品减少定植菌群的影响 供医护人员使用。Am J 感染控制 1988;17:83–8.
- Soulsby ME, Barnett JB, Maddox S. 简要报告:含氯二甲酚与含葡萄糖酸氯己定的防腐功效 手术擦洗制剂。感染控制 1986;7:223–6.
- Aly R,迈巴赫 HI。用葡萄糖酸氯己定、聚维酮碘和 氯二烯醇海绵刷。Am J 感染控制 1988;16:173–7.
- Archibald LK, Corl A, Shah B, et al. 粘质沙雷氏菌爆发与 1% 氯二酚肥皂的外源性污染有关。感染 Control Hosp Epidemiol 1997;18:704–9.
- Lowbury EJL, Lilly HA, Bull JP.手部消毒:去除常驻细菌。Br Med J 1963 年;1:1251–6.
- 昆辛 RB,沃尔特 CW。手术擦洗—实际考虑。Arch Surg 1973 年;107:75–7.
- 洛克哈特 J.六氯酚的毒性有多大?儿科 1972;50:229–35.
- Shuman RM, Leech RW, Alvord EC Jr. 六氯酚对人类的神经毒性:II.对 46 名早产儿的临床病理学研究。 Arch Neurol 1975 年;32:320–5.
- Dixon RE、Kaslow RA、Mallison GF、Bennett JV。美国医院托儿所葡萄球菌病暴发—12月 1971 年至 1972 年 3 月。儿科 1973;51:413–6.
- Kaslow RA、Dixon RE、Martin SM 等人。与医院托儿所沐浴做法相关的葡萄球菌病—全国 流行病学调查。儿科 1973;51:418–29.
- 美国儿科学会,美国妇产科医师学会。围产期护理指南。 第 4 版伊利诺伊州 Elk Grove Village:美国儿科学会;华盛顿特区:美国妇产科医师学会,1997 年。
- Gottardi W. 碘和碘化合物 [第 8 章]。在:Block SS,编辑。消毒、灭菌和保存。 第 4 版。费城,宾夕法尼亚州:Lea & Febiger;1991.
- 安德森 RL。碘伏防腐剂:内在微生物污染 与耐药菌。感染控制医院流行病学 1989;10:443–6.
- 戈尔登海姆警察局。聚维酮碘溶液和乳膏对耐甲氧西林金黄色葡萄球菌的体外疗效。研究生医学杂志 1993;69(增刊 3):S62–S65。
- 特拉奥雷 O, 法亚德 SF, 拉韦兰 H.聚维酮碘对医院细菌菌株活性的体外评估。J 医院 感染 1996;34:217–22.
- McLure AR, Gordon J. 聚维酮碘和 洗必泰抗耐甲氧西林葡萄球菌 金黄色葡萄球。J Hosp 感染 1992;21:291–9.
- 戴维斯 JG、巴布 JR、布拉德利 CR、艾利夫 GAJ。使用评估皮肤消毒剂杀病毒活性的测试方法的初步研究 脊髓灰质炎病毒和噬菌体。J Hosp 感染 1993;25:125–31.
- 第 79 章/洗手和手消毒。在:Mayhall CG,编辑医院流行病学和感染控制。巴尔的摩 MD:Williams & Wilkins,1996年。
- 韦德 JJ,凯斯韦尔 MW。手上残留抗菌活性的评估及其临床相关性。J Hosp 感染 1991;18(增刊 B):23–8。
- Aly R,迈巴赫 HI。葡萄糖酸氯己定的比较评价 (Hibiclens®) 和聚维酮碘 (EZ) 擦洗®)用于术前手部擦洗的海绵/刷子。Curr Ther Res 1983 年;34:740–5.
- Herruzo-Cabrera R, Vizcaino-Alcaide MJ, Fdez-AciZero MJ.N-双丙烯胺醇溶液对手术消毒的有用性 用碘聚维酮和洗必泰洗手的比较:临床论文。J 外科研究 2000;94:6–12.
- Hingst V, Juditzki I, Heeg P, Sonntag HG.减少 3 次应用后手术手部消毒的疗效评价 5 分钟 J Hosp 感染 1992;20:79–86.
- Faoagali J, Fong J, George N, Mahoney P, O’Rourke V. Novaderm 的即时、残留和累积抗菌效果的比较 R、Novascrub R、Betadine 手术磨砂膏、Hibiclens 和液体肥皂。Am J 感染控制 1995;23:337–43.
- 佩雷拉 LJ、李 GM、韦德 KJ。手术洗手程序对手术室护士微生物计数的影响。Am J 感染 Control 1990 年;18:354–64.
- Peterson AF, Rosenberg A. 手术擦洗制剂的比较评估。Surg Gynecol Obstet 1978 年;146:63–5.
- 伯克尔曼 RL,荷兰 BW,安德森 RL。聚维酮碘溶液的稀制剂的杀菌活性增加。J Clin 微生物学 1982;15:635–9.
- 季铵盐抗菌化合物 [第 13 章]。在:Block SS,编辑消毒、灭菌和保存。 第 4 版。宾夕法尼亚州费城:Lea 和 Febiger;1991.
- Dixon RE、Kaslow RA、Mackel DC、Fulkerson CC、Mallison GF。季铵盐水溶液防腐剂和消毒剂:使用 和 滥用。美国医学会 1976 年;236:2415–7.
- Sautter RL, Mattman LH, Legaspi RC.粘质沙雷氏菌脑膜炎与受污染的苯扎氯铵溶液有关。感染 Control 1984 年;5:223–5.
- Oie S, Kamiya A. 防腐剂和消毒剂的微生物污染。Am J 感染控制 1996;24:389–95.
- Hayes RA、Trick WE、Vernon MO 等人。外科重症监护病房 (SICU) 中三种手部卫生 (HH) 方法的比较 [摘要 K-1337]。在第 41届抗菌剂和化疗 Interscience 会议上发表伊利诺伊州芝加哥:美国学会 微生物学,2001 年。
- Dyer DL、Gerenraich KB、Wadhams PS. 测试一种新的无酒精洗手液以对抗感染。AORN J 1998 年;68:239–51.
- 琼斯 RD、Jampani HB、纽曼 JL、李 AS。三氯生:医疗保健环境中的有效性和安全性综述。Am J 感染对照 2000;28:184–96.
- Ward WH、Holdgate GA、Rowsell S 等人。烯酰基(酰基载体蛋白)还原酶抑制的动力学和结构特征 三氯生。生物化学 1999;38:12514–25.
- 希思 RJ、李 J、罗兰 GE。三氯生对金黄色葡萄球菌 NADPH 依赖性烯酰酰基载体蛋白还原酶的抑制作用 和六氯酚。J Biol Chem 2000;275:4654–9.
- Faoagali JL, George N, Fong J, Davy J, Dowser M. 4% 葡萄糖酸氯己定和 1% 的抗菌效果比较 急性临床病房中的三氯生洗手液产品。Am J 感染控制 1999;27:320–6.
- Barry MA, Craven DE, Goularte TA, Lichtenberg DA.含三氯生的消毒肥皂对粘质沙雷氏菌的污染:影响 用于医院感染。感染控制 1984;5:427–30.
- Lowbury EJL, Lilly HA, Bull JP.手部消毒:去除短暂微生物。Br Med J 1964 年;2:230–3.
- Rotter ML. Semmelweis 的 sesquicentennial:一个鲜为人知的周年纪念日 洗手。传染病最新观点 1998;11:457–60.
- Manivannan G、Brady MJ、Cahalan PT 等人。Surfacine™ 洗手液的即时、持续和残留抗菌效果 [摘要].感染控制医院流行病学 2000;21:105。
- Gershenfeld L. 聚维酮碘作为杀孢子剂。Am J Pharm 1962 年;134:79–81.
- 化学杀孢子剂和孢子抑制剂 [第 22 章]。在:Block SS,编辑。消毒、灭菌和保存。 第 4 版。宾夕法尼亚州费城:Lea 和 Febiger,1991 年。
- Johnson S、Gerding DN、Olson MM 等人。使用乙烯基手套中断艰难梭菌院内的前瞻性对照研究 传输。美国医学杂志 1990;88:137–40.
- 细菌对杀菌剂不敏感的机制。Am J 感染控制 2001;29:259–61.
- 库克森 BD,博尔顿 MC,普拉特 JH。耐甲氧西林金黄色葡萄球菌对洗必泰的耐药性还是只是 MIC 升高?体外和 体内评估。抗菌剂 Chemother 1991;35:1997–2002.
- MarA、soxS 或 acrAB 的过表达在实验室和临床菌株中产生对三氯生的耐药性 大肠杆菌。FEMS Microbiol Lett 1998;166:305–9.
- Chuanchuen R, Beinlich K, Hoang TT, et al.铜绿假单胞菌三氯生和抗生素之间的交叉耐药是由 多药外排泵:暴露于三氯生的易感突变菌株选择过表达 MexCD-OprJ 的 nfxB 突变体。抗菌剂 Chemother 2001 年;45:428–32.
- Gröschel DHM, Pruett TL.手术消毒 [第 36 章]。在:Block SS,编辑。消毒、灭菌和保存。 第 4 版。宾夕法尼亚州费城:Lea 和 Febiger,1991 年。
- 博伊斯 JM、波特-拜诺 G、欧泊 SM、Dziobek L、Medeiros AA。表皮葡萄球菌感染的常见来源暴发 接受心脏手术的患者。J Infect Dis 1990;161: 493–9.
- 杜瓦 NE,Gravens DL。septisol 消毒泡沫作为手术擦洗剂的有效性。应用微生物学 1973;26:544–9.
- Grinbaum RS, de Mendonça JS, Cardo DM.血管外科手术中爆发与手搓相关的手术部位感染。 感染控制医院流行病学 1995;16:198–202.
- AORN 推荐实践委员会。外科洗手液的推荐做法。在:Fogg D、Parker N、Shevlin D、eds。 标准、推荐做法和指南。科罗拉多州丹佛:AORN,2001 年。
- Larson E, Anderson JK, Baxendale L, Bobo L. 保护泡沫对擦洗和手套的影响。Am J 感染控制 1993;21: 297–301.
- Mulberry G、Snyder AT、Heilman J、Pyrek J、Stahl J. 无水、无磨砂葡萄糖酸氯己定/乙醇手术擦洗的评估 抗菌功效。Am J 感染控制 2001;29:377–82.
- 迪内恩 P.手术擦洗持续时间的评估。Surg Gynecol Obstet 1969 年;129:1181–4.
- O’Farrell DA、Kenny G、O’Sullivan M、Nicholson P、Stephens M、Hone R. 总手部擦洗时间前最佳手部擦洗持续时间的评估 髋关节置换术。J Hosp 感染 1994;26:93–8.
- O’Shaughnessy M、O’Malley 副总裁、Corbett G、Given HF。 手术擦洗时间的持续时间 [简短说明]。Br J 外科杂志 1991;78:685–6.
- Wheelock SM, Lookinland S. 手术手部擦洗时间对后续细菌生长的影响。AORN J 1997 年;65:1087–98.
- Deshmukh N, Kjellberg SI, Kramer JW.5 分钟聚维酮碘擦洗液和 1 分钟聚维酮碘擦洗液的比较,然后 酒精泡沫。军事医学 1998;163:145–7.
- Kikuchi-Numagami K, Saishu T, Fukaya M, Kanazawa E, Tagami H. 用刷子或不刷子擦洗手术的刺激性。学报 Derm Venereol 1999;79:230–2.
- 迪内恩 P.在手术擦洗中使用聚氨酯海绵。Surg Gynecol Obstet 1966 年;123:595–8.
- 博恩赛德 GH、小克劳德 VH、小科恩 I使用一次性碘伏肥皂浸渍手术擦洗的细菌学评价 聚氨酯擦洗海绵。外科 1968;64:743–51.
- 麦克布莱德 ME,邓肯 WC,诺克斯 JM。手术擦洗刷的评估。Surg Gynecol Obstet 1973 年;137:934–6.
- 伯曼 RE,奈特 RA。手部消毒液的评估。Arch Environ Health 1969 年;18:781–3.
- Loeb MB, Wilcox L, Smaill F, Walter S, Duff Z.一项用刷子手术擦洗与单独使用消毒肥皂进行比较的随机试验。敌法师 J 感染控制 1997;25:11–5.
- Larson E, Friedman C, Cohran J, Treston-Aurand J, Green S. 护士手部皮肤损伤的患病率和相关性。心 肺 1997;26:404–12.
- 图普克 RA。洗涤剂和清洁剂 [第 7 章]。在:van der Valk PGM,Maibach HI,编辑。刺激性接触性皮炎综合征。新增功能 纽约州约克:CRC 出版社,1996 年。
- 威廉 KP。预防表面活性剂诱导的刺激性接触性皮炎。Curr Probl Dermatol 1996;25:78–85
- de Haan P, Meester HHM, Bruynzeel DP.醇类的刺激性 [第 6 章]。在:van der Valk PGM,Maibach HI,编辑。刺激性接触 皮炎综合征。纽约州纽约市:CRC 出版社,1996 年。
- Lübbe J, Ruffieux C, van Melle G, Perrenoud D. 皮肤消毒剂 n-丙醇的刺激性。接触性皮炎 2001;45:226–31.
- qhlenschlaeger J, Friberg J, Ramsing D, Agner T. 皮肤对水和洗涤剂的敏感性的温度依赖性。Acta Derm Venereol 1996 年;76:274–6.
- 埃米尔森 A, 林德伯格 M, 福斯林德 B.十二烷基硫酸钠和氯化镍体外渗透人的温度效应 皮肤。Acta Derm Venereol 1993 年;73:203–7.
- 对化妆品的接触过敏:致病成分。接触性皮炎 1987;17:26–34.
- Schnuch A, Uter W, Geier J, Frosch PJ, Rustemeyer T. 医护人员的接触过敏— IVDK 的结果。Acta Derm Venereol 1998;78:358–63.
- Rastogi SC, Heydorn S, Johansen JD, Basketter DA.家用和职业产品中的香料化学品。接触性皮炎 2001;45:221–5.
- Uter W, Schnuch A, Geier J, Pfahlberg A, Gefeller O. 职业与对香料混合物的接触过敏之间的关联:一个 国家监测数据的多因素分析。占领环境医学 2001;58:392–8.
- Perrenoud D、Bircher A、Hunziker T 等人。瑞士对 13 种常见防腐剂的致敏频率。接触性皮炎 1994;30:276–9.
- Kiec-Swierczynska M, Krecisz B. 罗兹地区护士的职业性皮肤病。Int J Occup Med Environ Health 2000;13:179–84
- Garvey LH、Roed-Petersen J 和 Husum B. 麻醉患者的过敏反应—四例洗必泰过敏。学报 麻醉剂 Scand 2001;45:1290–4.
- 新罕布什尔州 Pham、Weiner JM、Reisner GS 和 Baldo BA。对洗必泰的过敏反应。案例报告。免疫球蛋白 E 抗体的意义 以及确定过敏原决定因素。Clin Exp 过敏 2000;30:1001–7.
- Nishioka K, Seguchi T, Yasuno H, Yamamoto T, 富永 K.接触性皮炎成分斑贴试验的结果 聚维酮碘制剂。接触性皮炎 2000;42:90–4.
- Wong CSM,贝克 MH。抗菌洗手液中三氯生引起的过敏性接触性皮炎。接触皮炎 2001;45:307。
- Guin JD, Goodman J. 苯甲醇引起的接触性荨麻疹表现为对盐水浸泡不耐受。接触性皮炎 2001;45:182–3.
- Podda M, Zollner T, Grundmann-Kollmann M, Kaufmann R, Boehncke WF.期间苯甲醇引起的过敏性接触性皮炎 局部抗真菌治疗。接触性皮炎 1999;41:302–3.
- Yesudian PD, King CM. 硬脂醇引起的过敏性接触性皮炎 Efudix® 霜。接触性皮炎 2001;45:313–4.
- Aust LB,Maibach HI。两组独立的小组成员中人体皮肤对异硬脂醇敏感的发生率。接触性皮炎 1980;6:269–71.
- Funk JO,迈巴赫 HI。丙二醇皮炎:重新评估一个老问题。接触性皮炎 1994;31:236–41.
- Hannuksela M. 保湿剂预防接触性皮炎。Curr Probl Dermatol 1996;25:214–20.
- Berndt U, Wigger-Alberti W, Gabard B, Elsner P. 隔离霜及其载体作为职业保护措施的功效 刺激性接触性皮炎。接触性皮炎 2000;42:77–80.
- McCormick RD、Buchman TL、Maki DG。双盲 / 预定使用新型隔离霜和含油化妆水保护医护人员双手的随机试验。Am J 感染控制 2000;28:302–10.
- Larson E, Killien M. 影响患者护理人员洗手行为的因素。Am J 感染控制 1982;10:93–9.
- Zimakoff J, Kjelsberg AB, Larsen SO, Holstein B.由工作人员评估的对手部卫生态度的多中心问卷调查 在丹麦和挪威的 15 家医院。Am J 感染控制 1992;20:58–64.
- Mayer JA, Dubbert PM, Miller M, Burkett PA, Chapman SW. 在重症监护病房增加洗手。感染控制 1986;7:259–62.
- Ojajärvi J.选择肥皂对医院常规手部卫生的重要性。J Hyg (Lond) 1981 年;86:275–83.
- 斯科特 D、巴恩斯 A、李斯特 M、阿克尔 P.用户对洗必泰洗手液配方的可接受性的评估。J Hosp 感染 1991;18(增刊 B):51–5。
- 泰勒 LJ.洗手技术评估—2.护理时报 1978 年;74:108–10.
- 普雷斯顿 GA,拉尔森 EL,斯塔姆 WE。私人隔离室对患者护理实践、定植和感染的影响 护理单位。美国医学杂志 1981;70:641–5.
- Kaplan LM, McGuckin M. 使用更方便的水槽提高洗手依从性。感染控制 1986;7:408–10.
- Freeman, J. 通过在床边放置洗手水槽来预防医院感染 [摘要 60]。在: 程序和 第 33届抗菌剂和化疗国际科学会议摘要。华盛顿特区:美国微生物学会,1993:130。
- Bischoff WE、Reynolds TM、Sessler CN、Edmond MB、Wenzel RP。医护人员遵守洗手规定。引入 一种可获得的含酒精的手部消毒剂。Arch Intern Med 2000 年;160:1017–21.
- Pittet D. 手消毒的依从性及其对医院获得性感染的影响。J Hosp 感染 2001;48(增刊 A):S40–S46。
- Wurtz R、Moye G、Jovanovic B. 洗手机、洗手合规性和交叉污染的可能性。Am J 感染 Control 1994 年;22:228–30.
- 科汉 C,利吉 C,杜米根 DG,博伊斯 JM。选择含酒精的洗手液时评估产品分配器的重要性。敌法师 J 感染控制 2002 年(出版中)。
- 博伊斯 JM。消毒技术:可及性、可负担性和接受度。新兴感染疾病 2001;7:231–3.
- 泰勒 LJ.洗手技巧评估—1.护理时报 1978:54–5。
- Albert RK, Condie F. 医疗重症监护病房的洗手模式。N Engl J Med 1981 年;304:1465–6.
- Larson E. 对隔离技术的依从性。Am J 感染控制 1983;11:221–5.
- 儿科重症监护病房的洗手技术。Am J Dis Child 1987 年;141:683–5.
- Conly JM、Hill S、Ross J、Lertzman J、Loule TJ。重症监护病房的洗手习惯:教育计划的效果 及其与感染率的关系。Am J 感染控制 1989;17:330–9.
- DeCarvalho M, Lopes JMA, Pellitteri M. 新生儿重症监护病房洗手的频率和持续时间。儿科感染病 J 1989;8:179–80.
- Graham M. 重症监护病房洗手的频率和持续时间。Am J 感染控制 1990;18:77–80.
- Dubbert PM, Dolce J, Richter W, Miller M, Chapman SW. 增加 ICU 工作人员洗手:教育和小组反馈的影响。 感染控制医院流行病学 1990;11:191–3.
- 西蒙斯 B、布莱恩特 J、内曼 K、斯宾塞 L、阿哈特 K。洗手在预防地方性重症监护病房感染中的作用。 感染控制医院流行病学 1990;11:589–94.
- Pettinger A,Nettleman 医学博士。隔离预防措施的流行病学。感染控制医院流行病学 1991;12:303–7.
- Lohr JA、Ingram DL、Dudley SM、Lawton EL、Donowitz LG。儿科门诊环境中的洗手:不一致的做法。敌法师 J Dis Child 1991 年;145:1198–9.
- Raju TNK, Kobler C. 改善新生儿托儿所的洗手习惯。美国医学杂志 1991;302:355–8.
- Larson EL、McGinley KJ、Foglia A 等人。洗手习惯以及两个儿科病房的细菌手部菌群的抵抗力和密度 秘鲁利马。Am J 感染控制 1992;20:65–72.
- Zimakoff J, Stormark M, 拉森 SO.重症监护病房医护人员使用手套和洗手的行为。一个 在丹麦和挪威的四家医院进行多中心调查。J Hosp 感染 1993;24:63–7.
- Pelke S, Ching D, Easa D, Melish ME.穿防护服不会影响新生儿重症监护病房的定植或感染率。Arch 儿科 Adolesc Med 1994 年;148:1016–20.
- Gould D. 护士的手部消毒实践:当地研究的结果。J Hosp 感染 1994;28:15–30.
- Shay DK、Maloney SA、Montecalvo M 等人。耐万古霉素肠球菌血流感染的流行病学和死亡风险。J 感染 Dis 1995;172:993–1000.
- Berg DE, Hershow RC, Ramirez CA. 危地马拉城重症监护病房院内感染的控制。Clin Infect Dis 1995;21:588–93.
- Tibballs J. 教医院医务人员洗手。Med J Aust 1996 年;164:395–8.
- Slaughter S、Hayden MK、Nathan C 等人。普遍使用手套和防护服与单独使用手套对 在内科重症监护病房收购耐万古霉素肠球菌。Ann 实习医学 1996;125:448–56.
- Dorsey ST, Cydulka RK, Emerman CL.Is handwash teachable?:在城市紧急情况下未能改善洗手行为 部门。Acad Emerg Med 1996 年;3:360–5.
- Watanakunakorn C, Wang C, Hazy J.一项关于医护人员洗手和感染控制做法的观察性研究。感染 Control Hosp Epidemiol 1998;19:858–60.
- Avila-Agüero ML, UmaZa MA, Jiménez AL, Faingezicht I, París MM. 三级儿科医院的洗手习惯及其对 一个教育计划。Clin Perform Qual Health Care 1998;6:70–2.
- 柯克兰 KB,韦恩斯坦 JM。触点隔离的不利影响。柳叶刀 1999;354:1177–8.
- Maury E、Alzieu M、Baudel JL 等人。酒精溶液的可用性可以提高重症监护病房的手部消毒依从性。是 J Respir Crit Care Med 2000;162:324–7.
- Muto CA, Sistrom MG, Farr BM. 手部卫生率不受安装快速起效手部消毒剂分配器的影响。Am J 感染 对照 2000;28:273–6.
- 贾维斯 WR。洗手—忘记了 Semmelweis 的教训?柳叶刀 1994;344:1311–2.
- Larson E, Kretzer EK.遵守洗手和屏障预防措施。J Hosp 感染 1995;30(增刊):88–106。
- 斯普罗特 LJ,英格利斯 TJJ。重症监护病房手部卫生习惯的多中心调查。J Hosp 感染 1994;26:137–48.
- Kretzer EK, Larson EL. 改善感染控制实践的行为干预。Am J 感染控制 1998;26:245–53.
- 沃斯 A,威德默 AF。没时间洗手!?洗手与酒精擦牙:我们能承受 100% 的依从性吗?感染控制中心 流行病学 1997;18:205–8.
- Larson E. 洗手和皮肤生理和细菌学方面。感染控制 1985;6:14–23.
- Thompson BL、Dwyer DM、Ussery XT、Denman S、Vacek P、Schwartz B. 在长期护理机构中使用洗手和手套。感染 Control Hosp Epidemiol 1997;18:97–103.
- Doebbeling BN、Pfaller MA、休斯顿 AK、Wenzel RP。从受污染的手套中去除院内病原体。安·实习生 Med 1988;109:394–8.
- 麦克兰 C、切内利 S、西尔韦斯特拉克 ML、基尔霍夫 KT。护理实践问题:未能遵守无菌技术。Am J 感染 Control 1983 年;11:178–82.
- Pittet D. 提高医院手部卫生的依从性。感染控制医院流行病学 2000;21:381–6.
- Teare L,洗手联络小组。洗手:适度的措施—效果大。Br Med J 1999;318:686。
- Teare EL、Cookson B、French GL 等人。英国洗手倡议。J Hosp 感染 1999;43:1–3.
- 拉尔森 EL、布莱恩 JL、阿德勒 LM、布兰 C。改变洗手行为的多方面方法。Am J 感染控制 1997;25:3–10.
- 第 A 周。为什么我在每次患者接触之间不洗手 [信]。Br Med J 1999;319:518。
- Webster J. 新生儿重症监护室洗手:葡萄糖酸氯己定 4% 和三氯生的产品可接受性和有效性 1%.J Hosp 感染 1992;21:137–41.
- Kelen GD、Green GB、Hexter DA 等人。急诊科对通用预防措施的依从性有显著改善 遵循政策机构。Arch Intern Med 1991 年;151:2051–6.
- 改变医生订购诊断测试的行为 [社论]。美国医学会 1998;280:2036。
- 菲利普斯 DF。“新面貌”反映了患者安全增强风格的变化。美国医学会 1999;281:217–9.
- Harbarth S, Martin Y, Rohner P, Henry N, Auckenthaler R, Pittet D. 延迟感染控制措施对医院暴发的影响 耐甲氧西林葡萄球菌 金黄色葡萄球。J Hosp 感染 2000;46:43–9.
- Early E, Battle K, Cantwell E, English J, Lavin JE, Larson E. 几种干预措施对洗手频率的影响 小学公立学校的孩子。Am J 感染控制 1998;26:263–9.
- Butz AM, Larson E, Fosarelli P, Yolken R. 日托所儿童感染症状的发生。Am J 感染控制 1990;18:347–53.
- 基梅尔 LS。洗手教育可以减少疾病缺勤。J Sch Nurs 1996 年;12:14–6, 18.
- Master D, Hess Longe S, Dickson H. 小学人口的定时洗手。Fam Med 1997 年;29:336–9.
- Roberts L, Smith W, Jorm L, Patel M, Douglas RM, McGilchrist C. 感染控制措施对上部频率的影响 儿童保育中的呼吸道感染:一项随机对照试验。儿科 2000;105:738–42.
- Roberts L, Jorm L, Patel M, Smith W, Douglas RM, McGilchrist C. 感染控制措施对腹泻发作频率的影响 在儿童保育中:一项随机对照试验。儿科 2000;105:743–6.
- 可汗穆。通过洗手中断志贺菌病。Trans R Soc Trop Med Hyg 1982 年;76:164–8.
- Shahid NS, Greenough WB, Samadi AR, Huq MI, Rahman N. 用肥皂洗手可减少腹泻和细菌病原体的传播 孟加拉国的一个村庄。J 腹泻 Dis Res 1996;14:85–9.
- 斯坦顿 BF,克莱门斯 JD。一项改变水卫生行为以减少孟加拉国城市儿童腹泻的教育干预措施。是 J 流行病学杂志 1987;125:292–301.
- McGinley KJ, Larson EL, Leyden JJ. 手甲下间隙微生物群落的组成和密度。J Clin Microbiol 1988;26:950–3.
- Hedderwick SA, McNeil SA, Lyons MJ, Kauffman CA. 与医护人员佩戴的人造指甲相关的病原微生物。 感染控制医院流行病学 2000;21:505–9.
- Baumgardner CA, Maragos CS, Larson EL. 指甲油对指甲微生物生长的影响:驱散圣牛。AORN J 1993 年;58:84–8.
- Wynd CA、Samstag DE、Lapp AM。手术室护士指甲上的细菌携带。AORN J 1994 年;60:796–805.
- 手术擦洗对指甲下微生物种群的影响美国外科杂志 1979;138:463–7.
- Pottinger J, Burns S, Manske C. 人工钉子与天然钉子的细菌携带。Am J 感染控制 1989;17:340–4.
- McNeil SA, Foster CL, Hedderwick SA, Kauffman CA. 用抗菌肥皂或酒精凝胶清洁手部的效果 医护人员佩戴的人造指甲的微生物定植。Clin Infect Dis 2001;32:367–72.
- 手术室中的假指甲 Rubin DM.AORN J 1988 年;47:944–5, 948.
- Moolenaar RL、Crutcher M、San Joaquin VH 等人。新生儿重症监护病房铜绿假单胞菌的长期暴发:确实 员工的指甲在疾病传播中发挥作用?感染控制医院流行病学 2000;21:80–5.
- Passaro DJ、Waring L、Armstrong R 等人。术后粘质沙雷氏菌伤口感染可追溯到院外来源。J 感染 Dis 1997 年;175:992–5.
- Foca M、Jakob K、Whittier S 等人。新生儿重症监护病房的地方性铜绿假单胞菌感染。N Engl J Med 2000;343: 695–700.
- Parry MF, Grant B, Yukna M, et al. 脊柱手术后念珠菌骨髓炎和椎间盘炎:涉及使用人造指甲的爆发。临床 感染 Dis 2001;32:352–7.
- Garner JS, Simmons BP. 医院隔离预防措施指南。感染控制 1983;4(增刊 4):245–325。
- CDC. 在医疗保健环境中预防 HIV 传播的建议。MMWR 1987 年;36(增刊 2S):3S–18S。
- 职业安全与健康管理局。29 CFR 第 1910.1030 部分。职业暴露于血源性病原体:最终规则。 联邦公报 1991 年;29CFR 第 1910:1030 部分。
- Hartstein AI、Denny MA、Morthland VH、LeMonte AM、Pfaller MA。在医院和重症监护病房控制耐甲氧西林金黄色葡萄球菌。感染控制医院流行病学 1995;16:405–11.
- Maki DG、McCormick RD、Zilz MA、Stolz SM、Alvarado CJ。普遍预防措施期间 SICU 中 MRSA 暴发:新的流行病学 对于院内 MRSA:普遍预防措施的缺点 [摘要 473]。在:程序和摘要 第 30届抗菌剂和化疗科学间会议。华盛顿特区:美国微生物学会,1990 年。
- Kotilainen HR、Brinker JP、Avato JL、Gantz NM。乳胶和乙烯基检查手套:质量控制程序和对健康的影响 护理人员。Arch 实习医生 1989;149:2749–53.
- Reingold AL, Kane MA, Hightower AW.未能佩戴手套和其他防护装置以防止乙型肝炎病毒经口传播 外科 医生。美国医学会 1988;259:2558–60.
- Korniewicz DM, Laughon BE, Butz A, Larson E. 乙烯基和乳胶手术手套的完整性。Nurs Res 1989;38:144–6.
- DeGroot-Kosolcharoen J,琼斯 JM。乳胶和乙烯基手套对水和血液的渗透性。Am J 感染控制 1989;17:196–201.
- Korniewicz DM, Kirwin M, Cresci K, Markut C, Larson E. 乳胶手套在两个高风险病房中的使用比较:外科重症监护 和获得性免疫缺陷综合征。心肺 1992;21:81–4.
- Korniewicz DM、Kirwin M、Cresci K 等人。检查手套的屏障保护:双层与单层。Am J 感染控制 1994;22:12–5.
- 手套泄漏率与乳胶含量和品牌的关系:购买者警告 [摘要 24]。 在:美国医疗保健流行病学学会第 10届年会的议程和摘要,佛罗里达州奥兰多,1998 年。
- Flanagan H, Farr B. 继续评估弗吉尼亚大学的手套泄漏率。在 美国医疗保健流行病学学会第 11届年会,加拿大多伦多,2001 年 4 月 1 日。
- Korniewicz DM、Laughon BE、Cyr WH、Lytle CD、Larson E. 病毒通过用过的乙烯基和乳胶检查手套泄漏。J Clin 微生物学 1990;28:787–8.
- Rego A, Roley L. 手套的使用屏障完整性:乳胶和丁腈优于乙烯基。Am J 感染控制 1999;27:405–10.
- Fisher MD、Reddy VR、Williams FM、Lin KY、Thacker JG、Edlich RF. 无粉检查手套的生物力学性能。J Emerg Med 1999 年;17:1011–8.
- Edlich RF, Suber F, Neal JG, Jackson EM, Williams FM. 无粉检查手套对噬菌体渗透的完整性。J 生物医学 Mater Res 1999 年;48:755–8.
- 默里 CA, 伯克 FJT, 麦克休 S.常规乳胶和非乳胶牙科检查手套穿刺发生率的评估 临床实践。Br 牙科杂志 2001;190:377–80.
- Jones RD、Jampani H、Mulberry G、Rizer RL。用于外科手部准备的保湿酒精洗手液。AORN J 2000 年;71:584–99.
- Patterson JE、Vecchio J、Pantelick EL 等人。受污染的手套与重症监护病房中醋酸不动杆菌变种的传播的关联。美国医学杂志 1991;91:479–83.
- 洛布里 EJL。手术室中的无菌方法。柳叶刀 1968;1:705–9.
- 霍夫曼 PN、库克 EM、麦卡维尔 MR、埃默森 AM。从医院工作人员佩戴的结婚戒指下的皮肤中分离出的微生物。BR Med J 1985 年;290:206–7.
- Jacobson G, Thiele JE, McCune JH, Farrell LD. 洗手:戒指佩戴和微生物数量。Nurs Res 1985;34:186–8.
- Hayes RA、Trick WE、Vernon MO 等人。在外科重症监护病房 (SICU) 中使用环作为手定植的危险因素 (RF) [摘要 K-1333]。在:程序和摘要 第 41届抗菌剂和化疗跨科学会议。华盛顿: 美国微生物学会,2001 年。
- 索尔兹伯里 DM、Hutfilz P、Treen LM、Bollin GE、Gautam S。戒指对医护人员手部微生物负荷的影响。Am J 感染 Control 1997 年;25:24–7.
- Spire B, Barré-Sinoussi F, Montagnier L, Chermann JC.化学消毒剂灭活淋巴结病相关病毒。 柳叶刀 1984;2:899–901.
- Martin LS, McDougal JS, Loskoski SL. 人类嗜 T 淋巴细胞病毒 III 型/淋巴结病相关的消毒和灭活 病毒。J Infect Dis 1985;152:400–3.
- Resnick L, Veren K, Salahuddin SZ, Tondreau S, Markham PD. HTLV-III/LAV 在临床和 实验室环境。美国医学会 1986;255:1887–91.
- van Bueren J、Larkin DP、Simpson RA。醇类灭活 1 型人类免疫缺陷病毒。J Hosp 感染 1994;28:137–48.
- Montefiori DC, Robinson WE Jr, Modliszewski A, Mitchell WM. 用 含有洗涤剂和酒精的洗必泰防腐剂。J Hosp 感染 1990;15:279–82.
- 伍德 A,佩恩 D.三种防腐剂/消毒剂对包膜和非包膜病毒的作用。J Hosp 感染 1998;38:283–95.
- Betadine 产品和洗必泰灭活人类免疫缺陷病毒。J Acquir 免疫缺陷 Syndr 1989 年;2:16–20.
- Lavelle GC, Gubbe SL, Neveaux JL, Bowden BJ.抗菌肥皂配方体外杀病毒功效评价 血液-病毒混合物中的人类免疫缺陷病毒。抗菌剂 Chemother 1989;33:2034–6.
- 邦德 WW、法韦罗 MS、彼得森新泽西州、埃伯特 JW。用中度至高浓度消毒化学品灭活乙型肝炎病毒。J Clin 微生物学 1983;18:535–8.
- Kobayashi H、Tsuzuki M、Koshimizu K 等人。乙型肝炎病毒对消毒剂或热的易感性。J Clin Microbiol 1984;20:214–6.
- 库尔茨 JB。醇类对埃可病毒 11 号的杀病毒作用 [信]。柳叶刀 1979;1:496–7.
- Sattar SA, Raphael RA, Lochnan H, Springthorpe VS.通过医院使用的化学消毒剂和防腐剂灭活轮状病毒。能 微生物学杂志 1983;29:1464–9.
- Larson E、Silberger M、Jakob K 等人。评估替代手部卫生方案以改善新生儿重症监护患者的皮肤健康 单位护士。心肺 2000;29:136–42.
- 古尔德 D,张伯伦 A.使用以病房为基础的教育教学包,以提高护士对感染控制程序的依从性。 J Clin 护理学 1997;6:55–67.
- Aspöck C, Koller W.简单的手部卫生练习。Am J 感染控制 1999;27:370–2.
- McGuckin M、Waterman R、Porten L 等人。提高洗手依从性的患者教育模式 [实践论坛]。Am J 感染 Control 1999 年;27:309–14.
- Khatib M, Jamaleddine G, Abdallah A, Ibrahim Y. 在管理接受机械通气的患者时洗手和使用手套 重症监护室。胸部 1999;116:172–5.
- 海莉 RW,布雷格曼 DA。人手不足和过度拥挤在新生儿葡萄球菌感染复发中的作用 特殊护理病房。J Infect Dis 1982;145:875–85.
- 皮特 D,博伊斯 JM。手部卫生和患者护理:追求 Semmelweis 的遗产。柳叶刀传染病 2001;4 月:9 日至 20 日。
- 博伊斯 JM。用酒精和其他无水防腐剂洗手的科学依据。在:Rutala WA,编辑。消毒、灭菌 和防腐剂:医疗机构的原则和实践。华盛顿特区:感染控制和流行病学专业人士协会, Inc,2001 年。
- 奥博伊尔 CA,亨利 SJ,达克特 LJ。护士洗手的动机:一种标准化的测量方法。应用护理学 研究 2001;14:136–45.
- 塞梅尔维斯 IP.Die aetiologie, der begriff und die prophylaxis des kindbettfiebers.佩斯、维也纳和莱比锡:CA Hartleben 的 Verlags-Expedition 1861 年。
- Eggimann P, Harbarth S, Constantin MN, Touveneau S, Chevrolet JC, Pittet D. 针对血管通路护理的预防策略的影响 关于重症监护病房感染的发生率。柳叶刀 2000;355:1864–8.
- Bull DA、Neumayer LA、Hunter GC 等人。改进的无菌技术降低了心血管患者阳性线培养的发生率。 J 外科研究 1992;52:106–10.
- Hirschmann H、Fux L、Podusel J 等人。插入外周静脉导管前手部卫生对频率的影响 的并发症。J Hosp 感染 2001;49:199–203.
- Drusin LM、Sohmer M、Groshen SL、Spiritos MD、Senterfit LB、Christenson WN。儿科重症监护室的甲型肝炎感染 护理单位。Arch Dis Child 1987 年;62:690–5.
- Doebbeling BN、Li N、Wenzel RP。医护人员中甲型肝炎疫情:传播的危险因素。Am J Public 健康 1993;83:1679–84.
- Standaert SM, Hutcheson RH, Schaffner W. 沙门氏菌胃肠炎的院内传播给疗养院的洗衣工人。 感染控制医院流行病学 1994;15:22–6.
- 罗德里格斯 EM、帕罗特 C、罗尔卡 H、门罗 SS、德怀尔 DM。疗养院病毒性胃肠炎暴发:排除的重要性 病员工。感染控制医院流行病学 1996;17:587–92.
- Schaffner W, Lefkowitz LB Jr, Goodman JS, Koenig MG. 医院感染暴发,A 组链球菌可追溯至无症状 肛门携带者。N Engl J Med 1969 年;280:1224–5.
- Viglionese A, Nottebart VF, Bodman HA, Platt R. 医护人员的复发性 A 组链球菌携带与广泛相关 分离的院内爆发。美国医学杂志 1991;91(增刊 3B):329S–33S。
- Ojajärvi J.病房手部消毒所用消毒剂的评估。J Hyg (Lond) 1976 年;76:75–82.
- Mermel LA, Josephson SL, Dempsey J, Parenteau S, Perry C, Magill N. 临床微生物学实验室中志贺氏菌的爆发。J Clin Microbiol 1997 年;35:3163–5.
- 麦克布莱德 ME.正在使用的肥皂产品的微生物菌群。应用环境微生物学 1984;48:338–41.
- Kabara JJ,布雷迪 MB。在“使用”状态下肥皂受到污染。J Environ Pathol Toxicol Oncol 1984;5:1–14.
- Heinze JE, Yackovich F. 用受污染的肥皂洗涤不太可能传播细菌。Epidem Inf 1988 年;101:135–42.
- Bannan EA,LF 法官。与洗手有关的细菌学研究: 1. 肥皂条无法传播细菌。Am J Public 健康 1965 年;55:915–21.
- 场 EA,麦高恩 P,皮尔斯 PK,马丁 MV。戒指和手表:是否应该在牙科手术前取下它们?J 登特 1996;24:65–9.
- Lowbury EJL,Lilly HA。戴手套的手作为手术部位消毒剂的涂抹器。柳叶刀 1975;2:153–6.
- AORN 推荐实践委员会。外科洗手液的推荐做法。AORN J 1999 年;69:842–50.
- Grohskopf LA, Roth VR, Feikin DR, et al. 血液透析中心促红细胞生成素 α 污染引起的液化沙雷氏菌血流感染。 N Engl J Med 2001 年;344:1491–7.
- Dharan S、Hugonnet S、Sax H、Pittet D. 手部护理霜与酒精手部消毒干扰的评估。占用 Environ Dermatol 2001;49:81–4.
- 希格 P.手部护理会破坏手部消毒吗?J Hosp 感染 2001;48(增刊 A):S37–S39。
- McGuckin M、Waterman R、Storr J 等人。英国 J Hosp Infect 2001 年患者赋权手部卫生计划的评估;48:222–7.
- Girou E, Oppein F. 法国大学医院的洗手依从性:引入手揉的新视角 无水醇基溶液。J Hosp 感染 2001;48(增刊 A):S55–S57。
* 在最近的一项随机临床试验中,监测了由手术人员进行手术的患者的手术部位感染率,这些手术人员在术前使用 4% 聚维酮碘或 4% 抗菌肥皂进行传统的 5 分钟手术手部擦洗,或 用非抗菌肥皂洗手 1 分钟,然后使用含酒精的洗手液进行 5 分钟的手部摩擦技术 含 0.2% 乙硫酸镁铵。两组患者的手术部位感染发生率几乎相同。 (来源:Parienti JJ、Thibon P、Heller R 等人,用于防腐 Chirurgicale des Mains 研究组的成员。用酒精水溶液搓手与传统手术手擦洗和 30 天手术部位感染率:一项随机等效研究。美国医学会 2002;288:722–7).


| 使用商品名称和商业来源仅用于识别身份,并不意味着美国国务院认可 卫生与公众服务部。 互联网上对非 CDC 站点的引用包括 作为一项服务提供给 MMWR 读者,不构成或暗示 CDC 或美国对这些组织或其计划的认可 卫生与公众服务部。CDC 不对内容负责 在这些网站上找到的页面。MMWR 中列出的 URL 地址是截至 发布日期。 |
免责声明 所有 MMWR HTML 版本的文章都是从 ASCII 文本的电子转换而来的 转换为 HTML。此转换可能导致 HTML 版本中出现字符转换或格式错误。 用户不应依赖此 HTML 文档,但应参考电子 PDF 版本和/或 官方文本、图表和表格的原始 MMWR 纸质副本。 本期的纸质原件可从文件总监处获得, 美国政府印刷局 (GPO),华盛顿特区 20402-9371;电话:(202) 512-1800。 请联系 GPO 了解当前价格。
**有关格式错误的问题或消息应发送给 mmwrq@cdc.gov。
页面转换时间: 10/17/2002
Hits: 98
- 心脏病成人的疫苗接种指南
- 用于检测治疗性蛋白制品的免疫原性的检测法开发和验证行业指南
- 肺部疾病成人的疫苗接种指南
- 快速响应:截至 2024 年 12 月在非大流行背景下人类接种禽流感疫苗的初步指南
- 糖尿病成人的疫苗接种指南
- 慢性肝病或慢性肝脏感染成人的疫苗接种指南
- 人类免疫缺陷病毒(HIV)感染者成人疫苗接种指南
- 65 岁及以上成人流感疫苗接种补充指南
- 2013 年美国感染病学会(IDSA)免疫功能低下人群疫苗接种临床实践指南
- 针对公共卫生紧急情况的猴痘检测政策
- 卫生保健机构手部卫生指南
- 环境感染控制指南 保健设施
- 2025 年 4 月 30 日的 NACI 声明摘要:关于 2025-2026 年季节性流感疫苗的声明
- 更新了老年人呼吸道合胞病毒 (RSV) 疫苗指南,包括扩大 RSVPreF3 在 50-59 岁人群中的使用以及使用新的 mRNA-1345 疫苗
- 孕期梅毒感染筛查:美国预防服务工作组重申建议声明
- 2025 年 5 月 14 日的 NACI 声明摘要:关于免疫功能低下成人带状疱疹疫苗接种的最新建议
- 2022 美国动物卫生协会犬类疫苗接种指南(2024年更新)
- 2020 年 AAHA/AAFP 猫科动物疫苗接种指南
- 2025 年 5 月 15 日的 NACI 声明摘要:关于使用 Imvamune 预防 mpox 的更新指南的快速响应
- 2025 年 2 月 13 日 NACI 声明摘要:关于麻疹暴露后预防的更新建议
- 从 2025 年 7 月 1 日起完成常规免疫接种计划(英国)
- 2025 年 1 月 10 日的 NACI 声明摘要:2025 年至 2026 年夏季 COVID-19 疫苗使用指南
- 麻疹暴露后预防更新建议的增编
- 使用 Imvamune 预防猴痘的更新指南
- 免疫功能低下成人带状疱疹疫苗接种的最新建议
- 推荐使用帕利珠单抗减少婴儿呼吸道合胞病毒感染的并发症
- 登革热防控方案(2025年版)
- 关于防止节肢动物叮咬的个人防护措施的声明 – 更新
- CATMAT 关于在 65 岁或以上人群中使用基孔肯雅热减毒活疫苗 (IXCHIQ) 的指南
- 关于在授权旅行者使用 QDENGA(登革热疫苗)的司法管辖区使用的建议
- 基于暴露的干预措施,用于管理整个生命周期中高度针头恐惧的个体:临床实践指南,呼吁进一步研究
- mRNA COVID-19 疫苗接种后患有心肌炎和心包炎的青少年的临床指南
- 归国国际旅客发热初步评估指南
- NACI 快速响应:在持续的猴痘疫情背景下更新了关于 Imvamune 的临时指南
- 关于管理耐多药沙门氏菌感染的临时指南
- 家长免疫接种指南
- 英国旅行者接种基孔肯雅热疫苗:JCVI 建议
- 针对 80 岁及以上成年人的呼吸道合胞病毒 (RSV) 免疫计划:JCVI 建议,2025 年 7 月 16 日
- JCVI 关于 2026年秋季和 2027 年春季 COVID-19 疫苗接种的声明
- CATMAT 关于播散性类圆线虫病的声明
- 成人免疫接种指南
- 针对呼吸道合胞病毒感染住院高风险婴幼儿的帕利珠单抗预防更新指南
- 针对呼吸道合胞病毒感染住院高风险婴幼儿的帕利珠单抗预防
- JCVI 关于 2026 年至 2027 年流感疫苗的声明
- 有关打算探亲访友的国际旅客的声明摘要
- 青少年疫苗接种指南
- 免疫接种状态不确定或不完全的个人疫苗接种:2025 年 7 月 1 日起
- 从 2025 年 7 月 1 日起进行常规儿童免疫接种(2024 年 7 月 1 日出生的婴儿)
- 加拿大关于在疫苗短缺期间使用分次剂量黄热病疫苗的临时建议
- 寨卡病毒预防和治疗建议
- 带状疱疹免疫接种计划:医护人员资讯
- 带状疱疹疫苗接种指南
- 儿童和青少年接种COVID-19疫苗
- 印度旅行疫苗接种:2025 年循证健康指南
- 旅行者疟疾预防和治疗指南
- 登革热:给明智旅行者与移居者的详尽旅行指南
- 旅行者伤寒:预防和保护完整指南
- 美国儿科学会 2025 年 8 月 19 日发布的推荐18 岁及以下儿童与青少年免疫接种程序
- 隐藏的敌人:旅行者立克次体感染完整指南
- 心脏病发作症状:旅行者的基本医疗指南
- 真菌性皮肤感染:类型、治疗和预防完整指南
- 热带医学和旅行咨询委员会 (CATMAT) 关于国际旅行者和伤寒的声明
- 2025 年简明临床指南:ACC 关于成人免疫接种作为心血管护理一部分的专家共识声明:美国心脏病学会解决方案集监督委员会的报告
- 产科-妇科护理中的 COVID-19 疫苗接种注意事项
- 妊娠期流感:预防和治疗
- 母体呼吸道合胞病毒疫苗接种
- 疫苗预防和控制季节性流感:免疫实践咨询委员会的建议——美国,2025-26 年流感季节
- 用Clesrovimab预防婴儿严重呼吸道合胞病毒相关下呼吸道感染:免疫实践咨询委员会的建议 — 美国,2025年
- 健康怀孕指南
- 关于预防婴幼儿呼吸道合胞病毒感染的建议:政策声明
- 过敏反应定义、概述和临床支持工具:2024 年共识报告 – GA2LEN项目
- 人狂犬病免疫球蛋白(human rabies immunoglobulin, HRIG)使用临时建议
- 如何与我们的心脏病患者讨论成人疫苗接种
- 2025 年秋季疫苗指南
- 疫苗佐剂非临床研究技术指导原则
- 完整的常规免疫接种计划 英国 2025年9月1日期
- 2025 年至 2026 年国家流感免疫接种计划信函
- 恰加斯病:基本旅行指南
- 创新型疫苗临床试验申请申报资料要求
- 远离结核病的旅行者指南
- 更顺畅的免疫接种体验指南
- 您的免疫预约指南:充满信心地完成整个过程
- 联合疫苗临床前和临床研究技术指导原则
- 疫苗接种预约指南:预期事项与准备方法
- 旅行时如何保护儿童免受水痘侵害:专家指南
- 家长互联网免疫接种信息指南
- 您的无缝免疫接种与健康服务指南
- 2025年病毒爆发与旅行警告:专家友好指南
- 结合疫苗质量控制和临床研究技术指导原则
- 预防用含铝佐剂疫苗技术指导原则
- 生物制品稳定性研究技术指导原则(试行)
- 常见传染病的暴露后预防
- 无缝接种预约指南
- 开发用于预防全球传染病的疫苗的一般原则
- 关于预防性疾病的联合疫苗评估:生产、测试和临床研究
- 关于组合疫苗及免疫学兽用药品(IVMPs)联合使用的指导原则
- 世界卫生组织关于疫苗非临床评价的指南
- 确保基于DT的组合疫苗的质量、安全和有效性的建议
- 沙特 疫苗生产和质量控制指南
- 疫苗接种预约指南:流程与准备事项
- 儿童与青少年疫苗接种时间指南
- 聚焦预防 | 美国心脏病学会简化心血管疾病免疫接种建议
- 精通疫苗接种诊所:提高效率与优化患者护理的内部指南
- 临床医生呼吸道疫苗共同临床决策指南
- 你的疫苗接种顺利体验指南
- 美国传染病学会关于A组链球菌性咽炎的临床实践指南更新
- 更顺畅疫苗接种体验终极指南
- 婴幼儿和青少年COVID-19疫苗接种建议:政策声明
- IDSA 2025年关于在免疫功能低下患者中使用疫苗预防季节性新冠病毒、流感和呼吸道合胞病毒感染的指南
- 无脾成人的疫苗接种指南
- 花生过敏预防的积极趋势:预防指南的实际影响
- 2025–2026年儿童流感预防与控制建议:技术报告
- 您的疫苗诊所指南:像专业人士一样导航系统
- 带状疱疹疫苗临床试验技术指导原则
- PIDS/IDSA 2023年儿童急性细菌性关节炎诊断和管理指南
- 预防节肢动物叮咬的个人防护措施声明
- 异维甲酸与疫苗诊所:保持防护的内部指南
- IDSA 2024年抗微生物药物耐药革兰氏阴性菌感染治疗指南
- 重组糖蛋白激素类产品药学研究与评价技术指导原则
- 流感病毒疫苗临床试验技术指导原则(征求意见稿)
- 重组表达单克隆抗体类生物制品制造及检定规程撰写指南(征求意见稿)
- 归国国际旅行者发热初始评估指南
- 中国流感疫苗预防接种技术指南(2025—2026)
- 成人癌症相关免疫抑制患者抗菌药物预防临床实践指南:ASCO/IDSA更新版
- 免疫功能低下旅行者
- 全国镰状细胞中心联盟关于镰状细胞病健康维护的共识建议共识声明
- 多联疫苗临床试验技术指导原则
- 曲霉病诊断和管理临床实践指南:IDSA 2016年更新版
- 养老院感染预防与控制多学会指南
- 关于跨国收养的声明
- 美国传染病学会 (IDSA) 发布的《念珠菌病管理临床实践指南:2016 年更新版》
- 流感疫苗完全指南
- IWGDF/IDSA糖尿病相关足部感染诊疗指南
- 热带病与旅行咨询委员会:老年旅行者声明
- 疫苗临床试验不良事件分级标准指导原则(修订版)
- ATS/CDC/IDSA临床实践指南:成人和儿童结核病的诊断
- 用于人乳头瘤病毒检测的自行收集阴道标本及筛查终止指南:美国癌症协会宫颈癌筛查指南更新
- 热带医学与旅行咨询委员会关于儿童旅行者的声明
- 成人导管相关性尿路感染的诊断、预防和治疗:美国传染病学会2009年国际临床实践指南
- HIVMA/IDSA 2014年更新版:HIV感染患者慢性肾病管理临床实践指南
- 对免疫状况不明或未完成的人员进行疫苗接种:自2026年1月1日起
- SHEA/IDSA 发布的《成人艰难梭菌感染管理临床实践指南:2021 年更新》
- 加拿大传染病报告:孕期旅行声明
- 成人和儿童艰难梭菌感染临床实践指南:美国医疗保健流行病学学会/美国感染病学会2017年更新版
- 关于旅行者与狂犬病疫苗的声明
- IDSA 2016 年球孢子菌病治疗临床实践指南
- 免疫接种者袖珍指南:孕期与哺乳期
- 成人社区获得性肺炎的诊断和治疗:美国胸科学会和美国传染病学会官方临床实践指南
- CATMAT 关于播散性粪类圆线虫病的声明:预防、评估和管理指南
- 3个月以上婴幼儿社区获得性肺炎的管理:儿科传染病学会和美国传染病学会临床实践指南
- 复杂性尿路感染(cUTI):治疗和管理临床指南
- 自行采集阴道标本用于人乳头瘤病毒检测及筛查退出指南:美国癌症协会宫颈癌筛查指南更新
- 旅行者结核病风险评估与预防
- IDSA 新型冠状病毒肺炎患者治疗和管理指南
- 热带病与旅行咨询委员会(CATMAT) 致旅行者及关于黄热病的声明
- 预防用疫苗佐剂药学研究技术指导原则(试行 )
- 隐球菌病治疗临床实践指南: 美国感染病学会2010年更新
- 儿童常规免疫接种计划
- ASM/ECMM/ISHAM 隐球菌病诊断和治疗全球指南
- 加拿大各省及地区婴幼儿常规(及补种)疫苗接种时间表(截至2025年12月)
- 美国儿科学会推荐的青少年及年轻成人疫苗
- IDSA 脑炎管理指南
- 加拿大各省和地区针对健康且先前已接种疫苗的成年人的常规疫苗接种计划
- 美国2026年儿童和青少年免疫接种计划建议
- 美国心脏协会成人感染性心内膜炎指南:诊断、抗菌治疗和并发症处理
- IDSA 2008 年老年长期护理机构居民发热和感染评估临床实践指南更新
- 癌症成人患者的疫苗接种:ASCO指南
- 癌症患者治疗前的乙型肝炎病毒筛查与管理:美国临床肿瘤学会临时临床意见更新
- CEPI 生物安全政策
- IDSA 关于 A 组链球菌(GAS)咽炎的临床实践指南更新
- 2026 年美国 18 岁及以下儿童和青少年推荐免疫接种程序
- 2025-2030 年美国人膳食指南
- AASLD/IDSA 2023 年丙型肝炎病毒感染检测、管理和治疗临床实践指南更新
- 关于接受度普利尤单抗治疗的患者使用疫苗的系统评价和专家德尔菲共识建议:美国过敏、哮喘和免疫学会立场文件
- 常规推荐的孕产妇疫苗接种汇总
- SHEA/APIC/IDSA/PIDS 多学会联合立场文件:提高标准——有效医疗机构感染预防和控制计划所需的资源和结构
- 美国医疗机构中感染乙型肝炎、丙型肝炎或人类免疫缺陷病毒的医护人员管理办法
- 医护人员疫苗接种咨询四步法指南
- IDSA 2017 年医疗相关性脑室炎和脑膜炎临床实践指南
- AASLD ISDA 慢性乙型肝炎治疗实践指南
- 美国传染病学会 2025 年组织胞浆菌病临床实践指南更新:成人、儿童和孕妇无症状组织 胞浆菌肺结节(组织胞浆菌瘤)及轻度或中度急性肺组织胞浆菌病的治疗
- 呼吸中心:您的 GoodRx 指南
- 2017 年 HIVMA/IDSA 艾滋病毒感染者慢性疼痛管理临床实践指南
- 人乳头瘤病毒疫苗临床试验技术指导原则 (修订版)
- 流感病毒疫苗临床试验技术指导原则(试行)
- 美国传染病学会和美国胸科学会2016年临床实践指南:成人医院获得性肺炎和呼吸机相关性肺炎的管理
- 美国内科医师学会免费提供的 2025-2026 年成人新冠疫苗接种快速实践指南(适用于非孕妇或免疫功能低下成人)
- 美国传染病学会发布的《婴幼儿、儿童、青少年和成人免疫接种计划:临床实践指南》
- SHEA/IDSA 实施抗菌药物管理计划的临床实践指南
- IDSA 2017 年感染性腹泻诊断和治疗临床实践指南
- IDSA 2018 年季节性流感诊断、治疗、化学预防和机构暴发管理临床实践指南更新
