Gap junctions in the immune system
介绍
间隙连接(GJs)是细胞间紧密接触通讯中最受关注的机制。尽管免疫细胞在组织内通常分布稀疏,但在正常的免疫反应或病理条件下(例如白血病),当淋巴器官被克隆相同的增殖细胞密集浸润时,它们可以通过间隙连接相互接触。
什么是间隙连接?
间隙连接通道(GJ 通道)由两个对接的连接子(半通道)组成,每个连接子分别由相邻细胞提供。单个半通道由六个寡聚化的连接蛋白(Cx)亚基组成,这些亚基属于结构相关的跨膜蛋白家族。所有 Cx 都具有相似的结构,其特征在于四个α螺旋跨膜疏水结构域(见图)。目前,人类和小鼠基因组中分别存在 20 个和 21 个高度保守的 Cx 家族成员,其中一些在免疫细胞上表达(见表 1)。GJ 的形成允许相邻细胞之间直接转移离子、小分子和 miRNA。心肌细胞通过 GJ 连接,从而实现同步极化。已知有三种不同类型的 GJ:同源/同型、异源/异型和异型连接。同型 GJ 由两个相同的连接子形成,而异型 GJ 由不同的连接子形成。同源或异源半通道由一种或多种 Cx 同工型组成。
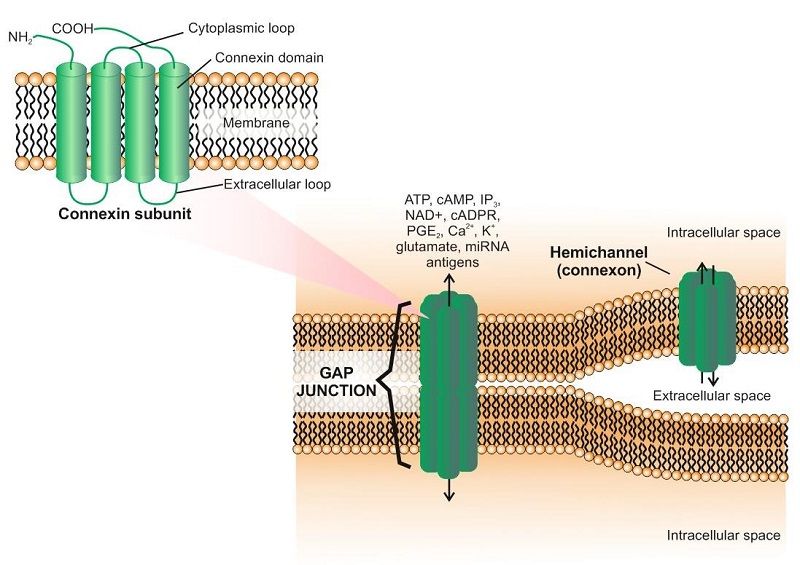
连接蛋白的作用有时仅限于细胞内信号传导,而这并不一定需要形成功能性间隙连接(图)。在这种情况下,细胞内信号通路被激活,涉及 ZO-1 等分子。这种机制在正常和病理状态下均可发挥作用。
最近,另一类名为 Pannexins (Panxs) 的蛋白质家族被认为能够形成缝隙连接,该家族仅包含三个成员 (Panx1–3)。然而,功能性 Panx 缝隙连接的表达仍然存在争议。
间隙连接在免疫系统中发挥什么作用?
许多免疫相关分子可以穿过缝隙连接,包括小肽、IP3 和 cAMP。Ca2+ 信号在免疫细胞中发挥着重要作用,参与细胞迁移、成熟和死亡。几年前,人们已经证实了与 Ca2+ 信号相关的第二信使(例如 IP3)可以通过缝隙连接进行转移。
当抗原呈递细胞(APC)中的缝隙连接(GJs)介导的抗原转移被证实后,缝隙连接在免疫学领域引起了广泛关注。这种通过缝隙连接的直接抗原转移使得抗原能够与主要组织相容性复合体(MHC)I 类分子形成复合物并进行交叉呈递。在此过程中,抗原呈递细胞从感染细胞或肿瘤细胞获取抗原,并通过将抗原呈递给 T 细胞来启动有效的免疫应答。事实上,所有类型的抗原呈递细胞都表达连接蛋白。此外,极化 T 细胞(Th1 或 Th2)之间的缝隙连接也已被证实。
滤泡树突状细胞(FDC)是能够保留抗原并参与免疫应答形成和维持的特化细胞。研究表明,Cx43 与 FDC 标志物(CD21 和 CD35)在人扁桃体和脾脏的生发中心共定位。此外,FDC 之间以及 FDC 与 B 细胞之间的缝隙连接通讯已在功能和超微结构水平上得到证实。
NAD+是一种能够穿过缝隙连接和半通道的小分子;可以预见,NAD+通过这些通道的转移或释放可能有助于不同免疫细胞之间的细胞间通讯。例如,CD38 是髓系和淋巴系细胞表达的一种分子,它们利用 NAD+生成 cADPR 和 ADP 核糖,而 cADPR 和 ADP 核糖参与多种免疫细胞反应。
ATP 可激活免疫细胞,并从细胞释放后促进自分泌和旁分泌激活。Cx 和 Panx 半通道参与嘌呤能信号传导已有报道,且近期有研究对其进行了修订。因此,Cx 和 Panx 半通道介导的 ATP 释放可能在免疫应答的各个阶段发挥作用。cAMP 也可通过缝隙连接传递;当调节性 T 细胞(Treg)与初始 T 细胞接触时,cAMP 可促进 Treg 介导的免疫抑制。
CD8+ T 细胞利用缝隙连接(GJs)进行激活,这已在体外实验中得到证实:初始 CD8+ T 细胞与黑色素瘤靶细胞建立缝隙连接。CD8+ T 细胞不利用缝隙连接进行杀伤;然而,NK 细胞通过 Cx43 依赖性过程与树突状细胞(DCs)和肿瘤细胞建立缝隙连接,从而促进 NK 细胞介导的细胞溶解和进一步的抗肿瘤免疫。
缝隙连接(GJs)允许单链和双链 RNA 以及特定的单链 microRNA 在细胞间穿梭,这对免疫反应具有重要影响。最近的研究表明,同种免疫细胞之间可以转移不同的 microRNA(miR-142、-223 和-155)。同样,巨噬细胞也被发现可以通过缝隙连接转移 miRNA 来抑制肝癌细胞的增殖。有趣的是,只有特定的 miRNA 会在细胞间交换,这表明缝隙连接对某些 miRNA 具有选择性通透性。这些数据提示,miRNA 转移可能是免疫系统抑制癌症的一种机制。
在疾病中,缝隙连接(GJs)已被证实与白血病密切相关。在包括急性淋巴细胞白血病(ALL)、急性髓系白血病(AML)和慢性骨髓增生性疾病在内的血液系统疾病中,骨髓基质细胞中 Cx43 表达上调。然而,在急性白血病中,也有证据表明 Cx43 表达降低,并且基质细胞和白血病细胞之间的缝隙连接通讯丧失。此外,研究表明缝隙连接对某些类型白血病细胞的存活至关重要,特别是为白血病干细胞(LSCs)提供存活信号。因此,白血病细胞的活性显然强烈依赖于细胞间以及细胞与基质细胞之间通过缝隙连接的通讯,然而,Cx43 表达变化在这些疾病发病机制中的意义仍有待进一步研究。
间隙连接是如何调控的?
缝隙连接(GJs)能够快速形成、开放/关闭和解离。这种可塑性使其能够介导缓慢和快速的细胞间通讯,但同时也意味着 GJs 的功能必须受到精确调控。通常情况下,半通道在内质网膜上完全形成,并通过高尔基体运输至细胞表面。连接蛋白(Cxs)在通过内吞作用进入细胞后,会不断更新并被溶酶体降解。GJ 斑块的降解受泛素化和磷酸化调控,并且在某些细胞类型中还依赖于蛋白酶体。
Cxs 的表达受多种细胞因子调控,这些细胞因子通常不会单独发挥作用,而是具有协同作用(见表 2)。

GJ 研究的临床意义是什么?
利用特异性药物递送抑制缝隙连接和半通道具有潜在可能。这可以通过使用非特异性缝隙连接阻断剂(例如辛醇或卡贝诺酮)或使用更具特异性的分子(例如模拟肽)来实现。一些新的方法正在涌现,例如使用抗连接蛋白抗体。关于 miRNA 通过缝隙连接转移的数据为特异性靶向 microRNA 和 siRNA 开辟了新的可能性。总而言之,这可能为调节先天性和适应性免疫反应以及治疗某些疾病(例如白血病)开辟新的途径。
参考
1. 细胞因子对抗原呈递细胞中半通道和间隙连接通道的调控。Saez PJ、Shoji KF、Aguirre A 等。炎症介质。2014;2014:742734。
2. 细胞间隙连接的通讯:历史回顾与当前进展。Evans WH. Biochem Soc Trans. 2015;43(3):450-9。
3. Cx25 参与白血病细胞通讯和化疗敏感性。Sinyuk M、Alvarado AG、Nemiyanov P 等。Oncotarget. 2015;6(31):31508-21。
4. ZO-1 表达在慢性 B 细胞白血病中具有预后价值。Nesmiyanov PP、Tolkachev BE、Strygin AV。免疫生物学。2016;221(1):6-11。
5. miRNA 的间隙连接穿梭——一种新的细胞间基因调控途径及其临床应用前景。Lemcke H.、Steinhof G.、David R. Cellular Signalling.2015;27:2506-2514。
© 本作品的版权归英国标准协会 (BSI) 所有。
免疫系统中的间隙连接 | 英国免疫学会 — Gap junctions in the immune system | British Society for Immunology
Hits: 9
