Contents
Mucosal vaccination clears Clostridioides difficile colonization
自然 volume 652, pages1289–1297 ( 2026 )
抽象的
艰难梭菌感染 (CDI) 是医疗相关感染和抗生素相关感染的主要原因,复发率高达 30% 1,2,3,4,5 。以往针对 CDI 的疫苗策略未能降低病原体负荷,而降低病原体负荷是预防艰难梭菌传播和复发的先决条件 6,7,8,9,10,11 。这些疫苗采用肠外途径给药,诱导的是全身性免疫反应,而非结肠黏膜(感染部位)的免疫反应。本研究比较了一种多价佐剂疫苗(包含灭活的艰难梭菌毒素和新型表面抗原)经黏膜(直肠)和肠外(腹腔)途径给药后的保护效果和定植负荷。我们发现,黏膜免疫而非肠外途径能够清除宿主体内的艰难梭菌 。去定植的独特相关因素包括粪便中针对植物表面抗原的 IgG 反应,以及结肠中针对孢子抗原的、以 T 辅助细胞 17 型(Th17)为主的组织驻留记忆 T 细胞反应。重要的是,黏膜疫苗接种可预防发病、死亡、组织损伤和复发。我们的研究结果揭示了不同疫苗接种途径在保护性和病原体清除相关因素方面的显著差异,并强调了一种可诱导针对艰难梭菌感染(CDI)的完全免疫的黏膜免疫方案。
其他人也在浏览类似内容
主要的
艰难梭菌是一种产孢厌氧菌,是医院感染的主要病原体之一,也是抗生素相关性腹泻的主要病原体 1 。仅在美国, 艰难梭菌感染(CDI)每年就导致约 50 万例病例、2.9 万例死亡和 48 亿美元的医疗保健费用 2,3,4 。因此,人们已投入大量精力研发针对艰难梭菌感染的疫苗。
以往针对艰难梭菌感染 (CDI) 的疫苗策略主要针对其主要毒力因子,即毒素 TcdA 和 TcdB 6,7,8,9,10 。辉瑞公司一项二价 TcdA/TcdB 疫苗的 III 期临床试验显示,该疫苗能够预防严重感染,但并未达到预防感染的主要终点( ClinicalTrials.gov:NCT03090191 )。而赛诺菲公司的一项疫苗试验则因达到无效标准而终止( ClinicalTrials.gov:NCT01887812 )。近期,一种针对 CDI 的多价 mRNA-脂质纳米颗粒候选疫苗在临床前研究中显示出良好的前景,能够保护小鼠免受严重感染和死亡 11 。然而,这些策略以及其他一些策略在清除结肠中的细菌方面效果甚微或无效 6,7,8,9,10,11,12 ——考虑到艰难梭菌孢子通过粪-口途径传播,这是一个至关重要的终点。 30% 的复发性 CDI 发病率 5 以及健康成年人中社区获得性 CDI 病例的记录增加 3 凸显了优先清除艰难梭菌的免疫策略的必要性。
我们建立了一种疫苗接种策略,旨在增强艰难梭菌的清除能力,同时增强对艰难梭菌感染症状的保护作用。该策略结合了以下几个方面:(1) 选择新型营养体和孢子抗原以促进艰难梭菌的清除;(2) 对艰难梭菌毒素抗原进行点突变,使其失活,同时保留天然结构以识别广泛的表位;(3) 使用大肠杆菌热不稳定毒素双突变体 (dmLT) 作为黏膜佐剂;(4) 采用直肠给药途径,并与肠外给药途径进行比较;(5) 评估体液和细胞免疫反应指标,以确定症状减轻和艰难梭菌清除的相关因素。我们证明了一种具有保护作用的黏膜疫苗制剂,可提供彻底清除宿主体内艰难梭菌的免疫力。
NTA 诱导非典型清除
计算机模拟预测,16 种与细胞表面功能相关的艰难梭菌非毒素抗原(NTA)具有低致敏性、高抗原性、B 细胞线性表位和 MHC-II 结合位点、在不同艰难梭菌菌株间高度保守,以及与宿主(小鼠和人)和共生微生物蛋白的低同源性 13 。我们重组表达并纯化了其中 13 种蛋白,并根据每种蛋白或蛋白复合物的总产量和溶解度(补充表 1 )筛选出几种进行抗原性测试。我们优先考虑了 FlgGEK(一种由 FlgG、FlgE 和 FlgK 鞭毛基体杆状结构组成的三元复合物, 见补充信息 )、C40 肽酶 2(一种细胞壁修饰酶)、多糖脱乙酰酶(一种肽聚糖脱乙酰酶)以及 CspC(一种孢子外壳结合的萌发受体) 14 。
疫苗诱导的结肠细菌清除是由肠系膜淋巴结反应介导的。因此,我们推测在感染部位接种 NTA 混合物可诱导黏膜免疫反应,从而降低细菌负荷。我们在 28 天内对小鼠进行了 3 次免疫接种,接种方式分别为直肠灌注(ri;模拟灌肠黏膜免疫)或腹腔注射(ip;模拟肠外免疫)(图 1a )。所有免疫接种均包含 dmLT 作为佐剂,dmLT 可诱导全身和黏膜体液免疫以及肠道 Th17 反应[1]。无论是直肠灌注还是腹腔注射 NTA 混合物,均能提高小鼠对野生型(WT) 艰难梭菌 R20291 致死性攻击的存活率(图 1b )。然而,只有腹腔注射疫苗的小鼠在感染后 2 天体重减轻得到显著保护(图 1c-e )。为了在不造成动物死亡的情况下评估定植负荷,我们用艰难梭菌 R20291 ∆A∆B(以下简称∆A∆B,一种毒素缺失的菌株)对不同组别的疫苗接种小鼠进行了攻击。与仅注射 dmLT 的对照组相比,添加 NTA 混合物的小鼠显著降低了∆A∆B 的定植负荷(图 1f )。在添加 NTA 混合物的小鼠中,部分小鼠在感染后第 5 天开始定植量降至检测限以下(每克粪便 500 个菌落形成单位(CFU)),并一直保持未定植状态直至实验结束。相比之下,腹腔注射疫苗对定植负荷没有影响(图 1g )。这表明,NTA 的黏膜疫苗接种可以降低定植负荷,同时对严重疾病和死亡提供一定的保护作用。
a ,实验示意图。该图使用 BioRender 软件绘制。b – e ,存活率 ( b ) 和相对于第 0 天的体重损失百分比 ( c ),以及感染后 2 天 (dpi) ( d ) 和 3 天 ( e ) 的体重定量 。f 、 g ,通过 ri ( f ) 和 ip ( g ) 疫苗接种后,通过 CFU 滴定法对粪便中的艰难梭菌进行计数。检测限用虚线表示:500 CFU/g 粪便。对于 c – e ,数据为平均值 ± 标准误。统计学显著性采用对数秩 Mantel-Cox 检验 ( b )、Tukey 校正的单因素方差分析 ( d 和 e ) 以及双侧 Student’s t 检验 ( f 和 g ) 计算,每天的数据分别进行分析。 * P ≤ 0.05,** P ≤ 0.01,*** P ≤ 0.001,**** P ≤ 0.0001;NS,无统计学意义。对于 b – g ,每组 n = 10; n 的减少是由于动物在感染期间死亡所致。图中所示为来自两个独立实验的个体数据点,并已进行合并。
为了确定每种 NTA 对 NTA 混合物经 ri 途径免疫后产生的保护作用和定植减少作用的单独贡献,我们在用 WT R20291 或∆A∆B 菌株进行攻击前,分别通过 ri 途径或腹腔注射(ip)用单一 NTA 免疫小鼠(扩展数据图 1a )。ri 途径给予的每种 NTA 以及 ip 途径给予的 C40 肽酶 2 均能提高小鼠的存活率(扩展数据图 1b,c )。重要的是,与仅注射 dmLT 的对照组相比,ri 途径接种 CspC、C40 肽酶 2 和 FlgGEK 显著降低了∆A∆B 菌株攻击小鼠的定植负荷(扩展数据图 1d )。单独 ip 途径接种 NTA 对定植没有影响(扩展数据图 1e )。
尽管疫苗能够清除细菌,但接受 ri 疫苗接种的小鼠并未表现出全身性抗 NTA IgG 或粪便 IgA 水平升高,这与典型的 dmLT 佐剂黏膜体液免疫反应不符 15 。事实上,与 ri 疫苗接种的小鼠相比,腹腔注射疫苗的小鼠血清中抗 NTA IgG(扩展数据图 1f )和粪便中抗 NTA IgA(扩展数据图 1g )的滴度显著更高。相反,ri 疫苗接种的小鼠粪便中针对 FlgGEK、C40 肽酶 2 和多糖脱乙酰酶的 IgG 滴度升高(扩展数据图 1h )。虽然与腹腔注射疫苗的小鼠相比,注射疫苗的小鼠粪便中抗 NTA IgA 或血清 IgG 没有统计学意义上的显著增加,但这些滴度与单 NTA 注射疫苗的小鼠降低艰难梭菌负荷的能力呈正相关,但与腹腔注射疫苗的小鼠则不然(扩展数据图 1i,j )。
ri 疫苗接种可提供完全免疫力
以往的艰难梭菌疫苗包含化学交联或甲醛灭活的艰难梭菌毒素 TcdA 和 TcdB 类毒素抗原 6,7,8,9,10 。虽然这些方法可以安全注射,但它们可能会破坏毒素上相关的中和表位 16,17 。为了避免这种情况,我们对 TcdA 和 TcdB 构建体进行了最小程度的突变,以阻止两种毒素的糖基转移酶活性(GTX) 18 。为了解决 TcdB 的残余毒性,我们引入了额外的突变,以消除孔形成(L1106K) 19 和 CSPG4 受体结合(D1812G) 20 。这些突变毒素经验证具有天然折叠结构,在细胞变圆试验中无活性,并且在与 dmLT 偶联后可安全用于体内免疫( 见补充信息 )。
由于第三次经腹腔注射(ri)和腹腔注射(ip)免疫并未提高黏膜体液抗体滴度(扩展数据图 1f-h ),我们采用两剂初免-加强免疫方案,用 NTAs 和灭活艰难梭菌毒素的组合免疫小鼠(图 2a )。此外,我们还优化了 ri 和 ip 免疫中 dmLT 的用量,以最大限度地延长体液免疫的持续时间,分别将 dmLT 用量降低至每剂 15 µg 和 1 µg(扩展数据图 2 )。
a ,实验示意图。小鼠感染 10 天或 15 天,各组之间未观察到差异。该图使用 BioRender 软件绘制。b 、 c ,小鼠感染野生型艰难梭菌 R20291 后,经腹腔注射(RI)( b )和腹腔注射(ip)( c )疫苗接种后的存活率。括号内为毒素+dmLT 组和毒素+NTA+dmLT 组的曲线。 d 、 e :接种后第 2 天( d )和第 3 天( e )相对于第 0 天的体重减轻情况。数据为平均值±标准误 。f – q :分别通过 ri( f – k) 和 ip (l – q )途径接种 dmLT( f 、 i 、 l 、 o )、毒素+dmLT( g 、 j 、 m 、 p )和毒素+NTAs+dmLT( h 、 k 、 n 、 q )后,对粪便中艰难梭菌 R20291 的总菌数(营养细胞和孢子( f -h 和 l-n))和孢子数(i-k 和 o – q ) 进行计数。P 值相对于同一时间点的对照组计算。每条线代表一只小鼠。检测限以虚线表示:每克粪便 500 CFU。统计学显著性采用对数秩 Mantel-Cox 检验( b 和 c )和 Tukey 校正的单因素方差分析( d – g 和 f – q ,每日数据单独分析)进行计算。对于 b – q ,每组 n = 20; n 的减少是由于感染期间动物死亡所致。图中展示了来自两个独立实验的个体数据点,这些数据点是合并后的。
毒素和 NTA 制剂的 ri 和 ip 疫苗接种均能提高小鼠在野生型艰难梭菌 R20291 攻击后的存活率(图 2b,c )。单独接种毒素或毒素联合 NTA 制剂,无论采用何种给药途径,均能保护小鼠在疾病的关键时间点免于体重下降(图 2d,e )。重要的是,与未接种疫苗的小鼠相比,ri 疫苗接种在感染后第 3 天可保护小鼠免于结肠和盲肠上皮损伤(扩展数据图 3a,b )。
为了确定在 NTA 配方中添加毒素是否能减少 ri 和 ip 疫苗接种小鼠的定植,我们在感染后 10 天或 15 天对粪便中的总菌落形成单位(CFU,反映孢子和营养型细菌)或仅耐热孢子进行计数。ri 疫苗接种后,小鼠在感染后第 9 天清除艰难梭菌 (图 2f-h ),并在第 8 天清除孢子(图 2i-k )。在这些动物的结肠和盲肠组织中未检测到孢子或营养型细菌(扩展数据图 4a-d ),16S PCR(扩展数据图 4e )和定量 PCR(qPCR;扩展数据图 4f,g )检测也未发现艰难梭菌 。这些结果与腹腔注射疫苗的小鼠形成鲜明对比,后者未能清除艰难梭菌 (图 2l-q 和扩展数据图 4a-g ),且艰难梭菌定植水平与未感染小鼠相似(扩展数据图 4h )。这些数据表明,肠内(ri)而非腹腔注射(ip)非活性毒素和 NTA 配方能够清除粪便和组织中的艰难梭菌 ,同时还能防止体重减轻、上皮损伤和死亡。
由于灭活毒素+NTA 配方能够清除 ri 疫苗接种小鼠体内的艰难梭菌感染(CDI),我们接下来研究了该给药途径和配方是否能够预防万古霉素诱导的复发模型中的复发感染(图 3a )。与仅使用 dmLT 和毒素+dmLT 配方的小鼠相比,ri 疫苗接种并同时使用毒素+NTA 配方的小鼠在 CDI 复发期间的死亡率显著降低(图 3b )。毒素+NTA 疫苗接种的小鼠在初次感染和复发感染期间的体重减轻和腹泻也显著减少(图 3c,d )。这些小鼠在万古霉素治疗期间也清除了艰难梭菌 ,并且在感染后 30 天内未复发(图 3i,j ),而对照组则出现复发(图 3e-h )。因此,ri 疫苗接种诱导的艰难梭菌从宿主体内的清除通过提供完全免疫力来预防复发。
a ,实验示意图。该图使用 BioRender 软件绘制。b , 小鼠感染野生型艰难梭菌 R20291 并复发后 30 天的存活率 。c ,体重减轻 。d ,粪便评分。e- j ,分别对接种 dmLT(e、f)、毒素 + dmLT(g、h)和毒素 + NTAs + dmLT(i、j)后,粪便中艰难梭菌 R20291 总菌数(营养细胞和孢子;e 、 g 、 i ) 和孢子数 ( f 、 h 、 j )进行计数。P 值相对于同一时间点的对照组计算。每条线代表一只小鼠。检测限用虚线表示:500 CFU/g 粪便。对于 c 和 d ,数据以均值 ± 标准误表示。统计学显著性采用对数秩 Mantel-Cox 检验 ( b ) 和 Tukey 校正的单因素方差分析 ( c 和 d ,以及 e – j ,其中每天的数据单独分析) 计算。对于 b – j ,每组 n = 15; n 的减少是由于动物在感染期间死亡所致。
粪便 IgG 可清除增殖性艰难梭菌
在艰难梭菌感染前,我们检测了血清和粪便中针对疫苗的黏膜和全身抗体反应,以研究细菌清除的体液免疫机制。虽然两种给药途径均能诱导血清中抗 TcdA IgG 的产生,但其他所有抗原的全身体液免疫反应仅在腹腔注射后出现(图 4a-e )。除 TcdA 外,ri 疫苗接种未诱导粪便中针对其他抗原的 IgA 反应(图 4f-j )。然而,ri 疫苗接种显著提高了粪便中抗 TcdA、抗 C40 肽酶 2 和抗 FlgGEK IgG 的水平(图 4k、n、o )。
a – e ,第 28 天攻击前血清中针对抗原的 IgG 反应。f – j ,第 28 天攻击前粪便中针对抗原的 IgA 反应。k – o ,第 28 天攻击前粪便中针对抗原的 IgG 反应。p – s ,感染后第 3 天结肠 IEL 和 LPL 区室中 T 细胞的百分比。t – v ,体外共培养接种疫苗小鼠的 T 细胞与 CspC 致敏的树突状细胞后,对离体 T 细胞产生的细胞因子进行计数。对于 a – v ,数据为平均值 ± 标准误。统计学显著性采用 Tukey 校正的单因素方差分析 (ANOVA) 计算( a – v )。图中展示了来自两个独立实验的单个数据点。对于 a – o ,每组 n = 5–15(取决于样本收集能力)。 p – s ,每组 n = 4–10(取决于感染后第 3 天是否有死亡); t – v ,每组/每组 n = 3 个重复。C40 pep 2,C40 肽酶 2;N,未感染/无抗原小鼠。
接种疫苗的小鼠在感染艰难梭菌 3 天后处死,并评估其体液免疫的细胞学指标。值得注意的是,毒素+NTA 配方的 ri 处理增加了肠系膜淋巴结中抗 C40 肽酶 2 和抗 FlgGEK 记忆 B 细胞(扩展数据图 5b )以及浆细胞(扩展数据图 5c )的数量。因此,ri 疫苗接种可增强针对 C40 肽酶 2 和 FlgGEK 营养抗原的黏膜 IgG 反应和记忆。
为了进一步评估抗营养性黏膜 IgG 在艰难梭菌清除中的作用,并确定这些 IgG 是否能从血清渗出至感染部位,我们进行了一项被动转移实验。供体小鼠通过 RI 途径分别接种 dmLT 或 C40 肽酶 2、FlgGEK 和 dmLT,以诱导产生抗营养性抗原黏膜 IgG。加强免疫 2 周后收集粪便,分离并过滤除菌粪便 IgG。在艰难梭菌攻击期间,通过腹腔注射或 RI 途径,将供体粪便 IgG 注射到先前已接种过灭活毒素和 CspC 疫苗的受体小鼠体内 ,共注射三次(见扩展数据图 6a )。
无论采用何种途径,接受对照或抗营养型抗原粪便 IgG 的各组小鼠的存活率和体重减轻均无差异(扩展数据图 6c、d )。然而,经 ri 途径接受抗营养型抗原粪便 IgG 的小鼠腹泻程度显著低于接受对照的小鼠(扩展数据图 6e )。与各自的 ri 途径 dmLT 对照组相比,这些小鼠的总艰难梭菌负荷也显著降低(扩展数据图 6f、g )。腹腔注射任一组黏膜 IgG 的小鼠的总菌落形成单位(CFU)负荷均未受到影响(扩展数据图 6j、k )。各组的艰难梭菌孢子计数均无统计学差异,表明总 CFU 负荷的差异是由对营养型艰难梭菌的影响所致(扩展数据图 6h、i、l、m )。体外功能分析显示,抗 C40 肽酶 2 和抗 FlgGEK 黏膜 IgG 可破坏艰难梭菌的游动能力(扩展数据图 6b )。综上所述,这些数据表明,抗 C40 肽酶 2 和抗 FlgGEK 粪便 IgG 可降低艰难梭菌的增殖负荷并抑制其运动。这些结果进一步表明,腹腔注射抗增殖粪便 IgG 并不能降低定植负荷,提示全身循环 IgG 对艰难梭菌清除的贡献微乎其微。
ri 诱导抗孢子 T H 17 反应
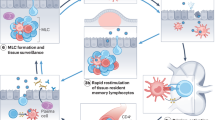
尽管尚未在直肠免疫的背景下研究针对艰难梭菌的细胞保护机制,但其他黏膜疫苗可在感染部位诱导组织驻留记忆(T0;CD1031CD692)细胞 3。因此,我们假设 ri 产生的免疫记忆也能在肠上皮内淋巴细胞 (IEL) 和固有层淋巴细胞 (LPL) 中诱导 T4 细胞反应。
在接受单毒素或毒素+NTA 制剂的小鼠中,肠上皮内淋巴细胞(IEL)(图 4p )和淋巴浆细胞(LPL)(图 4q )中的 CD80T1 细胞显著增加。此外,ri 给药显著诱导了 IEL 和 LPL 中的 CD42T3 细胞(图 4r,s )。为了确定 T4 细胞对特定抗原的分子反应,我们将从腹腔注射(ip)和 ri 免疫小鼠中分离的结肠 CD45 或 CD86T7 细胞与来自用单一疫苗抗原致敏的未免疫小鼠的骨髓来源树突状细胞(BMDC)进行共培养。3 天后分析共培养物的细胞因子谱。在接受 ri 疫苗接种的小鼠的 T 细胞中,CspC 诱导了 TH817 细胞反应相关细胞因子(包括 IL-1β、IL-6 和 IL-1α)的显著增加(图 4t–v )。与用其他疫苗抗原致敏的 BMDC 共培养的 CD49 和 CD810 T 细胞未产生这些细胞因子反应(扩展数据图 7a–c )。未观察到针对其他抗原的其他显著细胞因子反应,包括 TH11 和 TH12 通路中的经典细胞因子反应(扩展数据图 7 )。
为了确定在疫苗配方中添加 CspC 是否是清除艰难梭菌的必要条件,研究人员对小鼠进行了重复免疫接种,分别接种了灭活毒素、CspC 和 dmLT 的混合疫苗,以及灭活毒素、C40 肽酶 2、FlgGEK 和 dmLT 的混合疫苗。结果显示,接种毒素和 CspC 的疫苗显著降低了小鼠的死亡率和体重下降(扩展数据图 8a-c ),而未接种 CspC 的疫苗则导致 40% 的死亡率和显著的体重下降。与仅接种 dmLT 的对照组相比,未接种 CspC 的疫苗组小鼠的菌落形成单位 (CFU) 显著增加(扩展数据图 8e,g )。相反,接种毒素 + CspC 混合疫苗的小鼠在感染后第 10 天清除了艰难梭菌孢子,但并未清除全部细菌(扩展数据图 8d,f )。
黏膜疫苗具有持久性
尽管目前肠外途径的艰难梭菌疫苗能够诱导长期的抗毒素保护性免疫,但这种免疫反应在结肠黏膜疫苗模型中的持久性尚未得到研究。为了检验 ri 给药是否能够持久地预防疾病并清除艰难梭菌 ,我们在末次给药后 60 天或 200 天对小鼠进行免疫接种,并用野生型艰难梭菌 R20291 进行攻击(图 5a )。在两个延长的感染时间点,使用毒素和 NTA 配方进行免疫均能保护小鼠免于死亡和体重减轻(图 5b-e )。与仅使用 dmLT(图 5i 、l、o、r)和仅使用毒素+dmLT(图 5j、 m、p、s)的配方相比,这些免疫小鼠在两个时间点均能清除营养型艰难梭菌和孢子(图 5k、n、 q、t )。
a ,实验示意图。该图使用 BioRender 软件绘制。b 、 c ,野生型小鼠在加强免疫后 60 天( b )和 200 天( c )感染艰难梭菌 R20291 后的存活率。d 、 e ,加强免疫后 60 天和 200 天感染后 2 天( d )和 3 天( e )的体重变化。f – h ,结肠 LPL 区室中 T 细胞(CD80( f )、CD81T2( g )和 CD43T4( h )LPL)的百分比。 i – t ,分别计数加强免疫后 60 天( i – n )和 200 天(o – t ) 小鼠粪便中艰难梭菌 R20291 的总菌数 (营养细胞和孢子; i – k 和 o – q )和孢子数( l – n 和 r – t ),分为仅注射 dmLT 组( i 、 l 、 o 、 r )、毒素+dmLT 组( j 、 m 、 p 、 s )和毒素+NTAs+dmLT 组( k 、 n 、 q 、 t )。对于 i – t , P 值是相对于同一时间点的对照组计算的。每条线代表一只小鼠。检测限用虚线表示:500 CFU/g 粪便。对于 d – h ,数据以均值 ± 标准误表示。统计学显著性采用对数秩 Mantel-Cox 检验( b 和 c )和 Tukey 校正的单因素方差分析( d – t ;对于 i – t ,每天的数据均单独分析)进行计算。对于 b – e ,每组 n = 15;对于 f – h ,每组 n = 5;对于 i – t ,每组 n = 10; n 的减少是由于动物在感染期间死亡所致。图中展示了来自两个独立实验的个体数据点,这些数据点是合并后的。 FACS,荧光激活细胞分选。
为了探究体液免疫表型是否持久,我们检测了第 14、74、134 和 214 天血清和粪便中抗原特异性抗体的滴度(图 5a )。加强免疫后 60 天和 120 天(分别为第 74 天和第 134 天),血清中抗 TcdA 和抗 TcdB IgG、粪便中 IgA 和 IgG 均显著升高(扩展数据图 9a-c)。加强免疫后 120 天,血清中抗 CspC 和 C40 肽酶 2 的 IgG 升高,抗 FlgGEK 的滴度也呈现类似的趋势(扩展数据图 9a )。加强免疫后 74 天,粪便中抗 C40 肽酶 2 和 FlgGEK 的 IgG 升高(扩展数据图 9c ) , 随后在 120 天时下降。因此,在 ri 加强免疫数月后,抗 NTA 和抗毒素体液反应,特别是粪便 IgG 会增强。
我们进一步比较了感染后 3 天的细胞反应,以确定在 ri 加强免疫后 60 天和 200 天的时间点是否存在 T0 细胞。在这些延长的时间点,接种疫苗的小鼠肠上皮内淋巴细胞(IEL)中的总 T 细胞反应增加,但 T1 细胞没有增加(扩展数据图 10c、e-h )。我们还发现接种疫苗的小鼠固有层淋巴细胞(LPL)中的 CD82 T 细胞(图 5f )、CD83 T4 细胞(图 5g )和 CD45 T6 细胞(图 5h )均显著增加。综上所述,这些数据突显了 ri 诱导的抗 NTA 粪便 IgG 和固有层中 T7 细胞的持久性和长期存在——这些反应与针对艰难梭菌的清除性免疫相关。
讨论
本文描述了一种多价黏膜疫苗的临床前开发,该疫苗包含灭活毒素、新型表面相关 NTA 和 dmLT 佐剂,可诱导针对急性及复发性艰难梭菌感染(CDI)的完全免疫。除了降低疾病严重程度外,直肠给药还能减少艰难梭菌毒素造成的组织损伤(扩展数据图 3a、b )——这是其他临床前疫苗 11 和抗毒素疗法 23,24 所不具备的保护作用。我们预期该策略在开发针对 CDI 及其他肠道病原体的人用疫苗方面具有重要的转化价值。我们设想将有效的 ri 疫苗以灌肠剂的形式给药,类似于最初的粪便微生物移植给药途径。最近的一项调查显示,只要疫苗有效,公众愿意接受艰难梭菌疫苗,无论给药途径如何 25 。
鉴于艰难梭菌感染(CDI)主要发生于老年人群 26 ,我们希望评估免疫接种或攻毒年龄是否会影响 ri 疫苗诱导的清除性免疫。我们分别在小鼠 6 周龄和 12 周龄时接种疫苗,发现其对艰难梭菌攻毒的反应无差异(合并数据见图 2 )。我们还检测了免疫反应的持久性,并在最后一次 ri 加强免疫后 14 天、60 天和 200 天用艰难梭菌攻毒小鼠。观察到小鼠在加强免疫后 200 天仍能保持 T RM 细胞反应并清除病原体(图 5g、h、q、t ),这为将 ri 疫苗应用于老年人群的临床转化提供了积极的信号。下一步的关键步骤是在老年小鼠(3-18 个月) 27 中开展 ri 免疫试验。
以往的艰难梭菌毒素疫苗均采用肠外途径给药 6,7,8,9,10,11 。我们的研究结果与这些研究一致,表明肠外接种疫苗可降低发病率和死亡率(图 2b-e ),但即使添加了艰难梭菌表面抗原,也无法降低细菌载量(图 2n,q )。这些小鼠的经典黏膜 IgA 反应上调(图 4f-j ),但与细菌清除率无关(图 2n,q )。研究肠外接种疫苗获得的黏膜 IgA 为何无法提供完全清除细菌的免疫力,或许能够阐明未来临床前艰难梭菌疫苗研发中克服这些缺陷的策略。
我们的研究结果表明,ri(而非 ip)疫苗接种能够诱导产生针对艰难梭菌 NTA C40 肽酶 2 和 FlgGEK 的强效粪便 IgG(图 4n,o ),从而清除营养型细菌(扩展数据图 6f,g )并限制其运动能力(扩展数据图 6b )。其他肠道病原体已被证实能够以粪便 IgG 依赖的方式从肠道中清除 28,29 。尽管粪便 IgG 的含量通常低于粪便 IgA,但其浓度会因肠道感染而升高 30 。肠道分泌 IgG 的浆细胞可以归巢至骨髓 31 ,这进一步提示了一种维持免疫记忆的机制。综上所述,这些数据表明,ri 诱导的局部抗表面抗原粪便 IgG 反应是限制艰难梭菌营养型定植的关键因素。
我们将 CspC 作为疫苗抗原,旨在靶向感染期间的孢子。包含 CspC 的配方组(图 2h、k 和扩展数据图 8d-g )比单独使用毒素 + dmLT 配方组(图 2g )更快地降低了总定植负荷。然而,缺乏抗 CspC 抗体反应(图 4c、h、m )提示孢子清除机制可能涉及细胞层面。事实上,在共培养过程中,经 CspC 预处理的 BMDC 可诱导 CD41 和 CD82 T3 细胞产生与 T017 细胞反应相关的细胞因子(图 4t-v )。值得注意的是,我们的细胞因子检测结果中未检测到 IL-17a(扩展数据图 7g )。先前的报告强调了使用 Luminex 分析对人类血清样本中的 IL-17a 进行定量时存在低限度的困难,这可能解释了我们的结果 32,33 。
此外,T017 细胞驱动的免疫应答中 IL-17a 的减少或缺失与肠道内的细菌感染有关 1。这与 ri 疫苗接种小鼠中 CD82T3 细胞的显著增加(图 4p,q )相结合,颇为有趣,因为艰难梭菌是一种胞外病原体。最近的两项研究表明,肠道上皮细胞对孢子的内吞作用可能是复发性艰难梭菌感染(CDI)的机制之一 4。这一观点得到了以下事实的支持:在健康个体中,携带产毒性艰难梭菌的个体可能无法通过 16S rRNA 粪便测序检测到 5;83-88%的复发性 CDI 患者是由其最初感染的菌株再次感染 6。综上所述,这些数据可能表明,肠道中隐藏的孢子库可以萌发并在易感宿主中重新引发感染。
因此,我们推测 CD80T1 细胞促进宿主体内隐匿孢子库的清除。这一理论或许可以解释在接种 ri 疫苗且已清除感染的小鼠中观察到的孢子和营养细胞数量的波动(图 2h、k 和图 5k、n、q、t ),因为孢子可能在营养细菌清除后萌发,直至所有孢子库都被清除。结肠驻留的 CD82T3 细胞以极低的稳态周转率维持,且不会从循环中重新增殖 4,这验证了我们模型中长寿命的 CD85T6 细胞(图 5g、h )和清除表型(图 5k、n、q、t )。未来阐明孢子清除机制的研究对于艰难梭菌免疫接种以阻止传播和复发至关重要。
方法
蛋白质表达和纯化
如前所述 18,19,20 ,对野生型 VPI10463 TcdA 和 TcdB2 进行了点突变。引物信息见补充表 2。TcdA 、TcdB 和 CspC 的重组表达和纯化方法如前所述 18,41 。所有抗原的质粒信息见补充表 2。 编码 NTA 的质粒是来自艰难梭菌 R20291 背景的候选 NTA 的密码子优化版本,由金斯瑞生物技术公司合成到 pET47b(+)载体中,并包含用于蛋白纯化的 C 端 6×组氨酸标签。C40 肽酶 2、FlgG、FlgE、FlgK、CspC 和多糖脱乙酰酶转化到大肠杆菌 BL21(DE3) STAR 菌株中(补充表 2 )。为了表达每个 NTA,将 12 升添加了 50 mg/L 卡那霉素的溶菌肉汤培养基接种过夜培养物,使 600 nm 处的光密度(OD600)达到 0.1。细胞在 37℃和 220 rpm 下培养。当细胞的 OD600 达到 0.4-0.6 时,用 1 mM 异丙基-β- D -1-硫代半乳糖苷(IPTG)诱导表达。 4 小时后,离心收集细胞,并将沉淀物重悬于 20 mM Tris (pH 8.0)、500 mM NaCl、2% 裂解液(苯甲基磺酰氟 (0.1 mM)、亮抑蛋白酶肽 (2 mg/ml −1 )、胃蛋白酶抑制剂 (2 mg/ml −1 )、2% DNase (2 mg/ml −1 ) 和 2% 溶菌酶 (10 mg/ml −1 ))中。使用 EmulsiFlex C3 微射流均质机 (Avestin) 在 15,000 lb 的压力下裂解细菌悬液三次 −2 。裂解液在 4 °C 下以 40,000 g 离心 45 分钟。首先使用 Ni 2+ 亲和柱 (HisTrap FastFlow Crude; GE Healthcare) 从上清液中分离 NTA。 使用 S-200 尺寸交换柱(GE Healthcare)在 ÄKTA Pure 快速蛋白质液相色谱系统(Cytiva)上,以 20 mM HEPES(pH 6.9)和 50 mM NaCl 进一步纯化 NTA 洗脱液。所有样品均使用内毒素去除试剂盒(Thermo Fisher Scientific)进行处理,并通过 0.22 µm 滤膜进行无菌过滤,然后分装用于免疫研究,并储存在 -80 °C 下。
FlgGEK 三元复合物是通过共纯化 FlgG、FlgE 和 FlgK 制备的。简而言之,将三种蛋白质的上清液按 1:1:1 的比例混合,然后裂解并离心,再通过 Ni 2+ 亲和层析和 S-200 尺寸交换层析进行纯化,随后去除内毒素,过滤并冷冻,如上所述。
dmLT 由 PATH 提供(致谢和数据可用性),溶于 1× PBS 中,并添加 0.05% Tween-20(0.6 mg ml −1 )。
动物和研究设计
所有研究均使用雄性和雌性 C57BL/6J 小鼠(Jackson Laboratories,000664)。小鼠在免疫接种前 1 周适应新设施。小鼠饲养于范德比尔特大学医学中心,光照/黑暗周期为 12 小时/12 小时,环境温度为 23℃(±3℃),湿度为 50%(±20%),并可自由摄取饲料和水。这些研究已获得范德比尔特大学医学中心机构动物护理和使用委员会的批准,并按照 M2200087-00 号方案进行。所有动物均随机分配至各实验组。在整个动物实验过程中,研究人员未采用盲法,以便根据机构安乐死指南,在艰难 梭菌感染期间准确监测个体体重减轻和发病率。
在 NTA 混合制剂和单个 NTA 研究中,6 周龄的雄性和雌性小鼠在 28 天内接受三次免疫,每次注射间隔 14 天。腹腔注射组小鼠接受 5 µg dmLT 佐剂,佐剂中包含 5 µg FlgGEK、C40 肽酶 2、CspC 和/或多糖脱乙酰酶,溶于无菌 PBS 中,每次注射总体积为 100 µl。ri 处理组小鼠接受 25 µg dmLT 佐剂,佐剂中包含 5 µg FlgGEK、C40 肽酶 2、CspC 和/或多糖脱乙酰酶,溶于 200 µl PBS 中。收集粪便后,对小鼠进行直肠灌注以排空结肠。ri 处理在麻醉下进行,使用经消毒的金属球头灌胃针插入直肠。疫苗制剂以脉冲式注入结肠,给药后手动挤压直肠 15 秒以防止渗漏,如前所述 42 。所有疫苗均在抗原解冻后 2 小时内接种。每次接种和攻毒前均采集粪便和血清样本。小鼠在最后一次加强免疫后 14 天进行攻毒,如前所述 43,44 。抗生素治疗通过在饮用水中添加 0.5 mg/ml 头孢哌酮 −1 ,小鼠可自由饮用 5 天,随后进行 2 天的恢复期,恢复期期间提供普通饮用水,之后通过灌胃进行艰难梭菌感染(CDI)感染。在指定情况下使用两种不同的艰难梭菌菌株:野生型 R20291 和 R20291 ∆A∆B 45 ,两种菌株的给药剂量均为每只小鼠 1 × 104 个孢子。每日监测小鼠的存活率和体重变化。在整个感染过程中,动物笼保持不变。当小鼠体重下降超过其初始体重的 20%时,对其进行安乐死。在攻毒期间,每日采集粪便样本进行菌落形成单位(CFU)计数。
为了分析各种 TcdA 和 TcdB 点突变体的毒性,我们按照上述方法,对 6 周龄小鼠进行腹腔注射,注射液为 5 µg dmLT,以及以下毒素/毒素组合中的 1 µg 或 5 µg:TcdA GTX ;TcdB2 GTX,L1106K ;TcdA GTX + TcdB2 GTX,L1106K ;TcdB2 GTX,L1106K,D1812G ;或 TcdB2 GTX,L1106K + TcdB2 GTX,L1106K,D1812G 。对于含有两种抗原的联合疫苗,分别注射 1 µg 或 5 µg 的每种抗原,总抗原量为 2 µg 或 10 µg。注射后 7 天内,对小鼠的发病率和死亡率进行监测。
为了优化疫苗中 dmLT 的用量,研究人员对 6 周龄小鼠分别进行腹腔注射或直肠灌注,注射剂量为不同水平的 dmLT。小鼠腹腔注射 dmLT 0、0.5、1、2.5 或 5 µg,持续 2 周,同时注射 5 µg TcdA GTX ;或直肠灌注 dmLT 0、10、15、20 和 25 µg,持续 2 周,同时灌注 5 µg TcdA GTX 。分别于第 0 天(首次接种)、第 14 天(第二次接种)、第 28 天、第 58 天和第 88 天采集血清和粪便样本,用于酶联免疫吸附试验(ELISA)分析疫苗诱导的体液免疫反应。
为了比较单独使用 dmLT 佐剂接种毒素突变体与使用 dmLT 佐剂接种毒素突变体以及使用 NTA 混合物和 dmLT 佐剂接种毒素突变体的效果,我们对两组 6 周龄和 12 周龄的小鼠进行了两次免疫接种,两次接种间隔 14 天。腹腔注射的小鼠分别接受 1 µg dmLT;1 µg dmLT 与 5 µg 的 TcdA GTX 、TcdB2 GTX,L1106K 和 TcdB2 GTX,L1106K,D1812G 联合;或 1 µg dmLT 与 5 µg 的 TcdA GTX 、TcdB2 GTX,L1106K 、TcdB2 GTX,L1106K,D1812G 、CspC、C40 肽酶 2 和 FlgGEK 联合。接受 ri 处理的小鼠接受:15 µg dmLT;将 15 µg dmLT 与 5 µg 的 TcdA GTX 、TcdB2 GTX,L1106K 和 TcdB2 GTX,L1106K,D1812G 混合;或将 15 µg dmLT 与 5 µg 的 TcdA GTX 、TcdB2 GTX,L1106K 、TcdB2 GTX,L1106K,D1812G 、CspC、C40 肽酶 2 和 FlgGEK 混合。按上述方法收集血清和粪便样本。小鼠按上述方法感染野生型艰难梭菌 R20291。感染后第 3 天处死小鼠进行组织病理学分析和流式细胞术分析,或按上述方法在感染后监测 10 天(6 周龄小鼠)或 15 天(12 周龄小鼠)。
在复发感染研究中,6 周龄小鼠采用与上述相同的实验分组和相同剂量的佐剂和抗原进行免疫(ri)。随后,在最后一次加强免疫 2 周后,小鼠按照上述方法用野生型艰难梭菌 R20291 进行攻击。感染两天后,小鼠在饮用水中添加 0.5 mg/ml 的万古霉素,自由饮用 10 天以清除感染,具体方法见文献[1]。接受万古霉素治疗 10 天后,小鼠恢复饮用普通饮用水,并监测 30 天以记录复发感染情况。粪便样本的颜色和成分按 1-5 分进行评分,评分方法与我们之前的研究[2]类似,具体如下:5 分,正常、成形的粪便;4 分,成形良好、略微湿润或略微变色的粪便;3 分,湿润且变色的粪便;2 分,软便,无湿尾; 1. 湿尾、水样腹泻和空肛。为降低交叉感染风险,在整个感染期间,动物笼子、食物和水瓶每天都会更换。
在被动转移研究中,6 周龄供体小鼠经直肠灌注免疫,分别灌注 15 µg dmLT;或灌注 15 µg dmLT 联合 5 µg C40 肽酶 2 和 FlgGEK。加强免疫 2 周后,收集供体小鼠的粪便样本,并在死后收集结肠和盲肠内容物。将每组的粪便和盲肠内容物混合,并在 1:1 (w/v) PBS 中加入 2%裂解液(如上所述)进行匀浆,然后在 10,000 g 下离心 10 分钟。将所得上清液移除,用 0.22 µm 滤膜进行无菌过滤,并与抗小鼠 IgG 微珠(Miltenyi Biotech)孵育,使用 LS 柱(Miltenyi Biotech)和 MidiMACS 磁珠系统(Miltenyi Biotech)提取粪便 IgG。分别从仅接种 dmLT 和接种 C40 肽酶 2 及 FlgGEK 疫苗的供体中获得了 3.8 mg/ml −1 和 3.3 mg/ml −1 的粪便 IgG。浓度使用 Nanodrop One C 微量紫外分光光度计(Thermo Fisher Scientific)测定。同时,一组 6 周龄受体小鼠接种了 15 µg dmLT 以及 5 µg TcdA GTX 、TcdB2 GTX,L1106K 、TcdB2 GTX,L1106K,D1812G 和 CspC 进行二次免疫。如上所述,受体小鼠接受野生型艰难梭菌 R20291 的攻击。感染后第 1、4 和 7 天,通过腹腔注射(ip,100 µl)或腹腔注射(ri,200 µl)的方式,将来自供体小鼠的经分离、无菌过滤的粪便 IgG 被动转移至受体小鼠体内。如上所述,感染后对受体小鼠进行为期 10 天的监测。在整个感染期间,每天更换动物笼。
为了比较含 CspC 和不含 CspC 的疫苗配方,将 6 周龄小鼠经直肠灌注 15 µg dmLT;或 15 µg dmLT 联合 5 µg TcdA GTX 、TcdB2 GTX,L1106K 、TcdB2 GTX,L1106K,D1812G 和 CspC;或 15 µg dmLT 联合 5 µg TcdA GTX 、TcdB2 GTX,L1106K 、TcdB2 GTX,L1106K,D1812G 、C40 肽酶 2 和 FlgGEK。如上所述,用野生型艰难梭菌 R20291 对小鼠进行攻击。感染后,按照上述方法对动物进行 10 天的监测,并在整个感染期间每天更换笼子。
为了进行寿命研究,我们使用相同的实验分组和相同剂量的佐剂和抗原,通过 ri 免疫接种两组 6 周龄小鼠。一组小鼠在加强免疫后 60 天,按照先前所述方法用野生型艰难梭菌 R20291 进行攻击;另一组小鼠则在加强免疫后 200 天进行攻击。小鼠在感染后第 3 天被安乐死用于流式细胞术分析,或按照上述方法在感染后监测 10 天。在两次感染期间,动物笼均每日更换。
抗原特异性抗体测量
进行 ELISA 检测。将 Nunc MaxiSorp 384 孔板(Thermo Fisher Scientific)用 30 µl/孔的 1 µg/ml 重组 TcdA、TcdB2、CspC、C40 肽酶 2、FlgGEK 或多糖脱乙酰酶包被。4℃过夜孵育后,用含 0.1% Tween-20 的 PBS 缓冲液(PBS-T)洗涤三次(每次 100 µl/孔),然后换用封闭液(含 0.1% Tween-20 和 2% (w/v) BSA 的 PBS 缓冲液)。之后,将孔板在室温下摇动孵育 1 小时。将粪便样本在 1:1 (w/v)的 PBS 缓冲液中加入 2%裂解液(如上所述)进行匀浆,并在 10,000 g 下离心 10 分钟。将血清样本用含 2%裂解液的 PBS 缓冲液稀释 1:100。用 PBS-T 缓冲液洗涤板三次后,每孔加入 20 µl 稀释后的样本,室温摇动孵育 2 小时。再次用 PBS-T 缓冲液洗涤板三次后,每孔加入 30 µl 辣根过氧化物酶(HRP)标记的特异性山羊抗小鼠 IgG(Jackson ImmunoResearch;1:2000)或山羊抗小鼠 IgA-HRP(Southern Biotech;1:2000),溶于含 2% BSA 的 PBS-T 缓冲液中,孵育 1 小时。用 PBS-T 缓冲液洗涤板四次。然后,每孔加入 30 µl TMB 底物试剂(Thermo Fisher Scientific),底物显色 3 分钟后,加入 30 µl 2 M 硫酸。使用 BioTek Cytation 5 酶标仪(安捷伦公司)在 450 nm 波长下记录吸光度值。粪便抗体滴度以每毫克粪便进行标准化。使用 GraphPad Prism v.10.4.2 生成图表,并使用单因素方差分析和 Tukey’s HSD 检验评估组间统计学差异。
艰难梭菌计数
粪便中艰难梭菌的含量通过以下方法进行定量:将粪便样本在 1× PBS(pH 7.4)中进行系列稀释,然后接种于牛磺胆酸-环丝氨酸-头孢西丁-果糖琼脂糖(TCCFA)半选择性培养基上,并计数菌落形成单位(CFU) 49 。粪便样本在接种于 TCCFA 培养基上计数孢子之前,先在 75 °C 下加热处理 20 分钟以杀死营养细胞 50 。同样,盲肠和结肠组织中的细菌含量也通过以下方法进行定量:将解剖的组织在 1× PBS 中研磨成悬液,然后接种于 TCCFA 琼脂培养基上,以计数细菌总数和孢子总数。使用 GraphPad Prism v.10.4.2 生成图表,并使用单因素方差分析和 Tukey’s HSD 检验评估各组之间每天的统计学差异。
对于 PCR 分析,使用 QIAamp PowerFecal Pro DNA 试剂盒(Qiagen)提取盲肠和结肠组织(已按上述方法研磨以检测细菌载量)的 DNA。采用艰难梭菌特异性 16S rRNA 编码基因 PCR 来验证组织样本中是否存在该细菌。PCR 反应体系与先前发表的方案 51,52 相同,所有样本的模板 DNA 量均标准化为 50 ng。使用的引物如下(购自 IDT):正向引物 5′-TTGAGCGATTTACTTCGGTAAAGA-3′(25 nmol,标准脱盐纯化);反向引物 5′-CCATCCTGTACTGGCTCACCT-3′(25 nmol,标准脱盐纯化) 53 。PCR 产物在 1%琼脂糖凝胶上进行电泳,并使用 ChemiDoc MP(Bio-Rad)成像。
对于 qPCR 分析,反应体系的设置严格按照文献 53 所述进行,使用与上述 PCR 相同的引物和 TaqMan Fast Advanced Master Mix for qPCR(Thermo Fisher Scientific)。从盲肠和结肠组织中提取的模板 DNA 在所有样本中均标准化至 50 ng。使用艰难梭菌特异性 16S 探针(购自 IDT)鉴定引物扩增产物:5′-6-FAM-CGGCGGACGGGTGAGTAACG-MBG-3′(100 nmol,HPLC 纯化)。反应在 QuantStudio 6 Flex qPCR 系统(Thermo Fisher Scientific)上进行。使用 GraphPad Prism v.10.4.2 生成图表,并使用单因素方差分析和 Tukey’s HSD 检验评估组间统计学差异。
差示扫描荧光法
将 0.1 mg ml −1 的重组 WT VPI TcdA、VPI TcdA GTX 、WT TcdB2、TcdB2 GTX,L1106K 和 TcdB2 GTX,L1106K,D1812G 分别装入玻璃毛细管中,并按照制造商的说明使用 Tycho 差示扫描荧光计 (NanoTemper) 进行测试。
细胞圆化试验
将 Vero-GFP 细胞 54 以每孔 25,000 个细胞的浓度接种于黑色透明底 96 孔板中,并过夜培养。将重组野生型 TcdB2、TcdB2 GTX 、TcdB2 L1106K 、TcdB2 GTX,L1106K, 、TcdB2 GTX,L1106K 和 TcdB2 GTX,L1106K,D1812G 在培养基中进行十倍系列稀释,并将每种样品 100 μl 加入到每个孔中,每个样品设置两个技术重复。将培养板置于 BioTek Cytation 5 多功能酶标仪(Agilent)中,在 37 °C、5% CO₂ 2 条件下静置培养,并在 20 倍放大倍率下,每 45 分钟在明场和 GFP 通道下成像,持续 24 小时。该实验重复两次。计算并分析了选定时间点浓度为 1 pM 时,圆形细胞数量与每张图像中细胞总数的归一化值,如前所述 54 。使用 GraphPad Prism v.10.4.2 生成图表,并使用双因素方差分析和 Tukey’s HSD 检验评估组间统计学差异。
组织病理学
盲肠和结肠用 10%中性缓冲福尔马林固定,经梯度乙醇脱水,二甲苯透明,石蜡包埋。组织块用 HM 335E 切片机(Microm 公司)切成 5 µm 厚的切片,贴于 Superfrost Plus 载玻片(Thermo Fisher Scientific 公司)上。为评估组织病理学,盲肠和结肠切片用苏木精-伊红染色(Vector Labs 公司),并由一位经认证的胃肠病理学家和一位经认证的兽医病理学家分别对水肿、炎症和上皮损伤进行盲法评分,评分标准参照已发表的标准(每组 n =5) 55,56 。报告两位病理学家评分的平均值。组织学评分用 GraphPad Prism v.10.4.2 软件作图,统计学差异采用单因素方差分析和 Tukey’s HSD 检验进行分析。所展示的图像均使用 BioTek Cytation 5 全自动数字成像系统(安捷伦公司)采集。整张玻片以 10 倍放大倍率成像,分辨率为 0.25 µm px −1 。
艰难梭菌运动性测定
将野生型艰难梭菌 R20291 在 BHIS 培养基(37 g/L 脑心浸液肉汤,添加 5 g/L 酵母提取物)中于 37 °C 下,在 COY 厌氧培养箱(COY Laboratory Products)中厌氧培养至对数生长期中期。取 1 ml 艰难梭菌菌液 ,以 10,000 g 离心 5 分钟,弃去上清液。将菌体沉淀重悬于 1 ml 1× PBS(pH 7.4)、经无菌过滤的 dmLT 粪便 IgG 或经无菌过滤的抗 FlgGEK 和抗 C40 肽酶 2 粪便 IgG(制备方法见上文被动转移小鼠实验)中,孵育 30 分钟。然后,将 10 µl 细菌-粪便 IgG 混合物点样至含有 0.3%琼脂的 BHIS 平板上,如前所述 57 。平板在厌氧条件下于 37 °C 培养 8 小时,然后在室温下培养 16 小时。用尺子测量每个点样菌落最宽处的直径。PBS 培养的艰难梭菌在 BHIS 平板上会形成菌苔,因此测量直至菌苔形成之前,即菌落开始游动的边缘。
脾脏和肠系膜淋巴结采集
收集脾脏,研磨成单细胞悬液,并用 70 µm 细胞筛在 1× Hank’s 平衡盐溶液 (1× HBSS)(Thermo Fisher Scientific)中过滤。使用 ACK 裂解缓冲液(Thermo Fisher Scientific)裂解红细胞,得到单细胞悬液。将细胞离心后重悬于 500 µl 1× HBSS 中,计数后立即使用。收集肠系膜淋巴结,并按上述方法处理(不使用 ACK)。
制备结肠以获取 IEL 和 LPL
IEL 和 LPL 组分的获取和验证方法如前所述 58,59 。简而言之,收集结肠,清除脂肪残留和粪便,纵向切开,然后用冰冷的 1× HBSS 缓冲液连续洗涤两次。将结肠切成约 0.7 cm 的小块,放入装有 2 ml 冰冷 HBSS 缓冲液的 15 ml 锥形瓶中。向其中加入 5 ml DTT 混合液(1× HBSS 缓冲液,添加 20 mM HEPES,pH 8.0、1 mM 丙酮酸钠和 1 mM DTT),并在 37 °C 下孵育 15 分钟。然后将锥形瓶手动摇晃 2 分钟。将上清液转移至含有 5 ml cRPMI-10% FCS(RPMI-GlutaMax 培养基,添加 10% FBS 和 10 mM HEPES,pH 8.0)的 15 ml 锥形瓶中,而组织则保留用于 LPL 提取(见下文)。使用 Percoll 密度梯度离心(Sigma-Aldrich)进一步富集上清液中的 IEL。将 IEL 在 4 °C、650 g 下离心 20 分钟。吸出上清液,并将 IEL 重悬于 250 µl 含 0.5% BSA 和 1 mM EDTA 的 1× PBS(构成 PBE 缓冲液)中。立即对细胞进行染色,用于流式细胞术分析。
对于 LPL 组,剩余的结肠组织保留在原有的 15 ml 锥形瓶中。然后,加入 5 ml 仅含 EDTA 的混合液(1× HBSS,补充 20 mM HEPES,pH 8.0,1 mM 丙酮酸钠和 0.5 mM EDTA)。样品在 37 °C 下孵育 10 分钟。之后,手动摇晃锥形瓶 2 分钟,弃去上清液。用镊子取出组织,并用剪刀将其剪碎,放入含有 3 ml 消化混合液(1× HBSS,补充 20% FBS,3 mg 胶原酶 D 和 0.06 mg DNase I)的新 15 ml 锥形瓶中。样品在 37 °C 下孵育 30 分钟。将试管手动摇晃 1 分钟,然后用移液器将上清液转移至含有 2 ml cRPMI-10% FCS(RPMI-GlutaMax 培养基,添加 10% FBS 和 10 mM HEPES,pH 8.0)的 15 ml 锥形瓶中。将 LPL 细胞在 4 °C、650 g 下离心 20 分钟。吸出上清液,并将 LPL 细胞重悬于 250 µl 1× PBE 缓冲液中。立即对细胞进行染色,用于流式细胞术分析。
生产用于抗原特异性 B 细胞的荧光标记重组蛋白
使用 EZ-Link Sulfo-NHS-LC-Biotinylation 试剂盒(Thermo Fisher Scientific,21435)对重组 TcdA、TcdB、CspC、C40 肽酶 2 和 FlgGEK 进行生物素化,并分别与链霉亲和素偶联的 BV650(BioLegend,405231)、Alexa Fluor 568(Thermo Fisher Scientific,S11226)、FITC(BioLegend,405201)、APC-Cy7(BioLegend,405208)和 Alexa Fluor 680(Thermo Fisher Scientific,S32358)偶联。标记反应的荧光染料与蛋白质的比例为 1:1。标记后的蛋白质经液氮速冻后,储存于 -80 °C 直至使用,以防止降解。
B 细胞和 T 细胞的流式细胞术分析
将单细胞悬液与 Zombie 近红外细胞活力染料(BioLegend,423105)在室温下孵育 30 分钟。用 1× PBE 洗涤细胞,以 650 g 离心 10 分钟,然后重悬于含 5% 正常山羊血清(60 mg ml −1 ,Thermo Fisher Scientific)的 1× PBE 中,在室温下封闭 30 分钟。对于 T 细胞分析,细胞用以下抗体染色:抗 CD45(eFluor 450,30-F11,1:600,Thermo Fisher Scientific,50-112-9409)、抗 ∆yTCR(PerCP-Cy5.5,GL3,1:600,BioLegend,118117)、5-OP-RU 四聚体(PE,1:1,500,NIH 四聚体核心设施;数据可用性)、抗 TCRβ(Alexa Fluor 594,H57-597,1:600,BioLegend,109238)、抗 B220(FITC,RA3-6B2,1:600,BioLegend,103205)、抗 CD4(BV570,RM4-5,1:150,BioLegend)。将抗 CD8 (Alexa Fluor 532, 53-6.7, 1:300, Thermo Fisher Scientific, 58-0081-80)、抗 CD69 (APC, H1.2F3, 1:300, BioLegend, 104513) 和抗 CD103 (PE-Fire 810, QA17A24, 1:300, BioLegend, 156919) 在室温下孵育 30 分钟。对于 B 细胞分析,将细胞用抗 CD45 (eFluor 450, 30-F11, 1:600, Thermo Fisher Scientific, 50-112-9409)、抗 B220 (BV480, RA3-6B2, 1:300, BD Biosciences, 565631)、抗 CD27 (BV510, LG.3A10, 1:300, BD Biosciences, 563605)、抗 CD138 (BV785, 281-2, 1:300, BioLegend, 142534) 和上述荧光标记的重组疫苗抗原在室温下染色 30 分钟。细胞用 1×PBE 缓冲液洗涤,并在 650 g 下离心 10 分钟,然后在室温下用 4%多聚甲醛固定 30 分钟。之后,细胞再次离心,用 1×PBE 缓冲液洗涤,并重悬于 250 µl 1×PBE 缓冲液中。流式细胞术数据采集使用 Cytek Aurora Spectral 流式细胞仪(Cytek 公司),并使用 SpectroFlow 软件(v.3.3.0,Cytek 公司)进行分析。 在进行流式细胞术分析之前,使用荧光减一(FMO)对照确定细胞群的设门。FMO 对照的制备方法是:将重复的细胞样本和微珠(Thermo Fisher Scientific,U20250)用一组荧光染料标记的抗体进行染色,但要分析的抗体除外。这样可以消除荧光溢出和跨通道扩散的影响,从而精确确定阳性和阴性细胞群。设门策略详见补充信息 。图表使用 GraphPad Prism v. 生成。10.4.2,采用单因素方差分析和 Tukey’s HSD 检验评估各组之间的统计学差异。
用抗原激活幼稚树突状细胞并与 T0 细胞共培养
从未经免疫的 C57BL/6J 小鼠中分离骨髓来源树突状细胞(BMDC),并使用粒细胞-巨噬细胞集落刺激因子(GM-CSF,Thermo Fisher Scientific,315-03-50UG)、白细胞介素-4(IL-4,Thermo Fisher Scientific,214-14-50UG)和 Flt3L(Thermo Fisher Scientific,250-31L-50UG)进行分化,具体方法如前所述 60,61 。在与 TH 细胞共培养的前一天,用 10 ng/ml 脂多糖(LPS,Thermo Fisher Scientific) −1 和 1 µM 的单个抗原或单独的 LPS 激活 BMDC。将 BMDC 与抗原在 37℃、5% CO2 条件下孵育 24 小时 2 。
在共培养当天,收集经腹腔注射(ip)或经呼吸道途径(ri)接种 dmLT(仅接种)或 dmLT、毒素和 NTAs(联合接种)的小鼠结肠(每组 n =3)。如上所述,从结肠中提取 LPL,将各组 LPL 混合,并进行 T 细胞标记染色。使用 Cytek Aurora CS 细胞分选仪(Cytek),按照补充信息中提供的设门策略,对 CD40 和 CD81 T2 细胞进行流式分选。
将骨髓来源树突状细胞 (BMDC) 重悬,洗涤去除脂多糖 (LPS) 和生长因子后,以每孔 5,000 个细胞的密度接种于 12 孔组织培养板(Thermo Fisher Scientific),每孔加入 2 ml 培养基。根据细胞分选仪的计数结果,向每个含有树突状细胞的孔中加入 1,000 个 CD40 或 CD81 T2 细胞。将细胞在 37 °C 下共培养 72 小时,然后取出 1 ml 共培养上清液,并在 -80 °C 下速冻,用于液相微珠细胞因子分析。
液珠细胞因子阵列
使用两套定制的 12 重小鼠 Luminex Discovery Assay 试剂盒(BioTechne)定量检测 IL-7、IL-12 p70、IL-1β/IL-1F2、IL-2、IL-4、IL-5、IL-6、IL-10、IL-13、IL-17/IL-17a、IFNγ和 IL-1α/IL-1F1。所有检测均按照制造商提供的方案进行三次重复。数据采集使用 Luminex FlexMap 3D(Luminex)。使用 Millipore Belysa(v.1.0.19)软件分析数据,并采用四参数 logistic 回归模型计算各标准曲线的浓度。使用 GraphPad Prism v.10.4.2 软件绘制图表,并使用单因素方差分析(ANOVA)和 Tukey’s HSD 检验评估组间统计学差异。
统计学和可重复性
数据以均值±标准误(SEM)的形式呈现(如适用)。定量变量采用 D’Agostino-Pearson 正态性检验进行正态分布检验。若不符合正态分布,则采用非参数统计检验。各实验的统计检验方法(参数检验或非参数检验)均列于图例和相应的 “方法” 部分。除非另有说明,各组样本方差均相似。实验中样本量 n 的范围取决于样本采集时间;例如,感染后第 2-3 天 n 值较低可能是由于动物因病死亡,导致无法提供粪便样本。图表使用 GraphPad Prism v.10.4.2 生成。
报告摘要
有关研究设计的更多信息,请参阅本文链接的《 自然投资组合报告摘要》 。
黏膜疫苗接种可清除艰难梭菌定植 | 自然 — Mucosal vaccination clears Clostridioides difficile colonization | Nature
Hits: 2