Bracketing and Matrixing Designs for Stability Testing of New Drug Substances and Products
新原料药和制剂稳定性试验的括号法和矩阵法设计
Step 5
2002/2/7
目 录
- 前言
- 1.1本指导原则的目的
- 1.2背景
- 1.3本指导原则涉及的范围
- 指导原则
- 2.1 总则
- 2.2 简化设计的适用性
- 2.3 括号法
- 2.4 矩阵法
- 2.5 数据评估
新原料药和制剂稳定性试验的括号设计法和矩阵设计法
1、前言
1.1 本指导原则的目的
本指导原则的目的是:在按照ICH Q1A(R)新原料药和制剂稳定性试验三方协调指导原则(下文”)进行稳定性研究时,如何应用括号设计法(括号法)及矩阵设计法(矩阵法)。
1.2 背景
Q1A指出了矩阵法和括号法在经过验证的情况下可以应用于新原料药及制剂的稳定性试验,但并未提供进一步的指南。
1.3 本指导原则涉及的范围
本文件阐述了括号法与矩阵法研究设计的指导原则。在可以应用括号法和矩阵法时,本指导原则给出了专门的规则。指导原则中提到的设计样例仅仅是用来举例说明,不应当认为是唯一或最佳的设计。
2、指导原则
2.1 总则
一项完整的设计方案就是在所有时间点对样品的全部设计因子的每个组合都进行试验。简化的设计方案则是在所有的时间点并非对每个因子组合的样品都进行试验。当涉及到多种因子时,简化的设计方案可替代完整设计方案。任何一种简化设计方案必须具备足够的预测重检期或有效期的能力。在考虑一种简化设计方案以前,需要评估和验证相关的假设。还需要考虑由于数据收集量的减少而得出与完整设计方案比较相对短的重检期或有效期的潜在风险。
在进行简化设计研究期间,如果有合理的依据,并且试验仍符合完整设计和简化设计的原则,可将简化方案改为完整的试验方案,或者改为简化程度少的设计方案。然而,如果因为设计的改变而造成样本量的增加,则应对统计分析作合理的调整。一旦改变了设计方案,在稳定性研究的剩余时间点,就应该采用改变后的完整试验方案或简化程度少的方案进行试验。
2.2 简化设计的适用性
简化设计可应用于绝大多数药物制剂的正式稳定性研究。对于某些复杂的给药系统,因为有很多潜在的药物与装置的相互作用,则应提供进一步的合理性验证后才可应用。对原料药而言,矩阵法的应用有一定的限制,而括号法则通常不适用。
在什么情况下可以使用括号法与矩阵法,取决于下文所述的条件。任何简化设计方案都需要验证。某些情况下,本指导原则中描述的条件已经为应用提供了足够的验证。但有些情况下,则应提供进一步的验证。进行验证的类型和程度,取决于可得到的支持性数据。应用矩阵法时,应当考虑由支持性数据所显示的的数据波动性和产品的稳定性。
括号法与矩阵法是基于不同原理的简化设计法。因此,若在一个设计方案中同时使用括号法与矩阵法,需谨慎考虑并进行科学验证。
2.3 括号法
如同Q1A(R)中术语所定义的,括号法是一种稳定性试验的设计方案,它仅对某些设计因子(如规格、包装容器大小和/或装量)处在极端状态的样品,与完整设计方案一样,在所有时间点进行试验。这种方案假设:任何中间状态样品的稳定性可以用被试验的极端状态样品的稳定性所代表。
如果无法确证被选择受试的规格、容器尺寸和/或装量确实是处在极端状态,那么使用括号法是不适当的。
2.3.1 设计因子
设计因子是需要在稳定性研究中评估其对产品稳定性影响的变量(如规格、容器大小和/或装量)。
2.3.1.1 规格
括号法可用于处方相同或相近的多个规格样品稳定性研究中。例子包括但不限于(1)由相同粉末混合物、不同填充量制成的不同规格的胶囊;(2)由不等量的同种颗粒压制成的不同规格的片剂;和(3)处方仅在某些微量辅料(如着色剂、矫味剂)上有差别的不同规格的口服溶液剂。
经过验证,可将括号法应用于处方中原辅料比例不同的多个规格的研究中。这样的验证可以包括在临床试验或产品研发中所用批次的产品不同规格间稳定性情况的比较结果。
如果各规格之间使用了不同的辅料,就不能应用括号法。
2.3.1.2 容器大小和/或装量
可将括号法应用于容器大小或者装量不同而其他保持不变的同种包装容器系列的研究。但是,如果在容器大小和装量均发生变化的情况下考虑使用括号法,就不能假设最大和最小的容器代表了所有包装形态的极端状态。应通过比较包装容器系统中可能影响产品稳定性的各种特性来仔细选择包装形态的极端状态。这些特性包括容器壁厚度、闭塞物的几何形状,表面积与体积之比,上部空间与总体积之比,每个剂量单位或单位装量体积的水蒸气透过率或氧气透过率等。
经过验证,括号法可以用于同种容器、不同闭塞物的研究。验证内容可以包括该系列容器密闭系统的相对通透率的讨论。
2.3.2 设计上的考虑和潜在风险
在研究工作开始以后,如果其中一种极端状态样品不再打算用于上市销售,那么该研究方案可以维持下去用以支持中间状态样品。还应承诺获得批准后,继续对已上市的极端状态样品进行稳定性研究。
在应用括号设计法前,应评估它对判断重检期或有效期的影响。如果极端状态样品的稳定性不同,就不能认为中间样品比最不稳定的极端样品更稳定(即,中间样品的有效期不应超过最不稳定的极端样品的有效期)。
2.3.3 设计示例
在表1中给出了一个括号法的设计示例。该实例为某种有三个规格和三种容器大小的制剂。在本例中,应证明15mL和500mL 高密度聚乙烯(HDPE)容器确实代表了极端状态。对于每一选定组合的批次,应如同在完整设计中一样,在每个时间点都进行试验。
表1:括号设计法示例
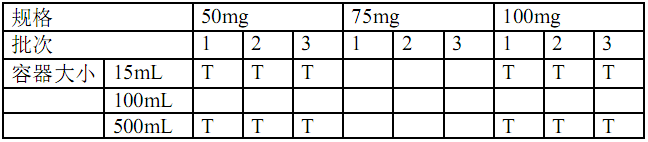
注: T=进行测试的样品
2.4 矩阵设计法
如同Q1A(R)中词汇表定义的一样,矩阵法是一种稳定性试验的设计方案,它在指定的某些时间点对所有具有全部因子组合的总样品中的一个选定子集进行试验。在后续的时间点,对另一个具有全部因子组合的样品子集进行试验。该设计方案假设受试的每个样品子集的稳定性代表着所给时间点上所有样品的稳定性。对于同一种制剂,受试样品间的各种差异应一一确定,如:批次不同,规格不同,包装容器相同但大小不同,在某些情况下,可能包装容器也不同。
当一种次级包装系统影响到制剂的稳定性时,可以将该包装系统归入矩阵。
每个贮存条件都应该在它自身的矩阵设计中分别设置。不能对试验项目进行矩阵设计。但是,经过验证后,对于不同试验项目,可选用另外的矩阵设计方案。
2.4.1 设计因子
可将矩阵设计法应用到具有相同或相似处方的不同规格。例子包括但不限于:(1)由相同的粉末混合物用不同的填充量制成的不同规格的胶囊;(2)由不等量的同种颗粒压制成的不同规格的片剂;以及(3)处方中仅在某些微量辅料(如着色剂或矫味剂)上有差别的口服溶液剂。
可以应用矩阵设计的其他例子有:使用相同的工艺和设备制成的、采用相同包装的不同批次产品。
经过验证,可以把矩阵设计运用到原辅料比例不同的、使用不同辅料的、或使用不同包装的不同规格制剂。验证通常应有相关数据的支持。例如,针对两种不同的闭塞物或包装容器应用矩阵法时,就应提供它们相对的水气透过率或具有相似的避光保护措施的数据。或者,可以提供制剂不受氧气,湿度和光照影响的相关数据。
2.4.2 设计上需考虑的因素
矩阵方案的设计应尽可能均衡,以使每个因子组合在整个拟定的研究期间和在申报前最后一个时间点能被试验到同等的程度。然而,如下所述,推荐的完全试验是在那些固定的时间点进行的,所以在对时间点进行矩阵的设计方案中,要达到完全的均衡可能是困难的。
在对时间点进行矩阵设计的方案中,应该在起始和结束的时间点对所有选定的因子组合进行测定,而在每个中间时间点仅仅对某些指定组合进行试验。如果在申报时无法提供用来确定有效期的完整的长期试验数据,则关于批次、规格、容器大小和装量以及其他因子的所有选定组合,应该在第12个月或在申报前的最后一个时间点均进行试验。而且,对于每个选定的组合,应申报在研究的前12个月中至少3个时间点(包括起始时间点)的数据。在加速试验条件或中间储存条件下进行矩阵设计时,对于每个选定的因子组合,应注意确保进行最少三个时间点的试验,包括最初和最终时间点。
当已进行关于设计因子的矩阵时,如果某个规格或容器尺寸和/或装量不再打算用于上市销售,对该规格或容器尺寸和/或装量的稳定性试验可继续下去,以支持设计方案中的其他规格或容器尺寸和/或装量。
2.4.3 设计实例
表2为某种两个规格(S1和S2)制剂的针对时间点的矩阵设计示例。术语“1/2简化”和“1/3简化”,是指对完整研究设计进行的简化策略。比如,1/2简化是在完整研究设计的每两个时间点中去掉一个,而1/3简化则是在每三个时间点去掉一个。在表2的示例中,其简化程度少于1/2或1/3。这是因为如同2.4.2节所述,所有因子组合在某些时间点要进行完全试验。这些示例包括在起始、结束和第12个月时间点的完全试验。所以最终的简化要比1/2(24/48)或1/3(16/48)少,实际上分别是15/48和10/48。
表2 某制剂两个规格关于时间点的矩阵设计示例
“二分之一简化”
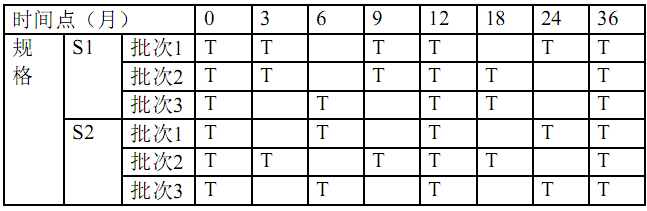
注:T=进行测试的样品
“三分之一简化”
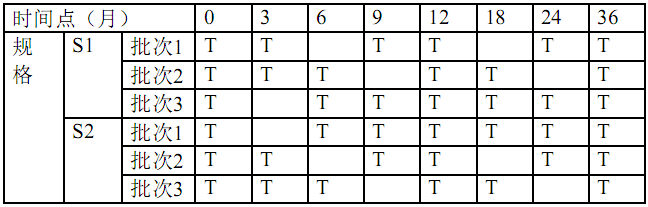
注:T=进行测试的样品
表3a、3b给出了另一个有3种规格、3种容器尺寸的某种制剂的矩阵设计示例。表3a是一种仅对时间点进行矩阵的设计,而表3b则是对时间点和因子均进行矩阵的设计方案。在表3a中,批次、规格以及容器尺寸的所有组合都被试验;而在表3b中,某些组合不被试验。
表3a和3b:某种三个规格三种容器尺寸制剂的矩阵设计示例
3a.对时间点的矩阵设计
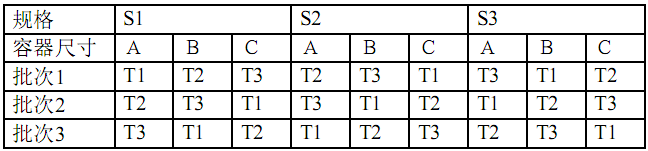
3b.对时间点和因子的矩阵设计
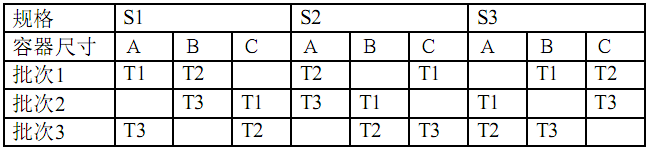
试验安排:
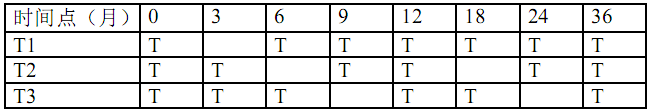
S1、S2和S3代表不同规格。A、B和C 代表不同的容器尺寸。
T=进行测试的样品
2.4.4 简化的适用性和程度
设计一个矩阵方案时,应考虑如下因素,虽然它们还不够全面:
- (1)了解数据的变异性;
- (2)产品预期的稳定性;
- (3)支持性数据的有效性;
- (4)在一个因子之内或多个因子之间产品稳定性的差异,和/或
- (5)研究中因子组合的数量。
一般来说,如果支持性数据指示了产品有可以预见的稳定性,则可采用矩阵设计。如果支持性数据变异性很小,则说明运用矩阵是适当的。但是,如果支持性数据显示了中等的波动性,就应该通过统计分析验证矩阵设计的合理性。如果支持性数据显示了很大的波动性,就不能采用矩阵设计方案。
所谓统计方法验证,即对该矩阵设计检测因子间降解速率差异的能力或其估计有效期的准确程度进行评估。
如果一个矩阵设计被认为是可采用的,那么其简化程度可根据被评估的因子组合的数量来决定。与产品相关的因子越多,每个因子的层次越多,可以考虑简化的程度就越大。然而,任何简化的设计都应有足够的预测产品有效期的能力。
2.4.5 矩阵设计的潜在风险
一个仅对因子而非对时间点的矩阵设计,与相应的完整设计方案相比,由于数据收集量的减少,通常在估测有效期的准确性上要差一些,得出的有效期要短一些。而且,这样的矩阵设计方案也许没有足够的能力检测出某些主要因子或因子间相互作用的影响,因此在评估有效期时,会导致将不同设计因子得来的数据进行不正确的合并。如果在因子组合的试验数量上简化过度,这些实验数据就不能合并以建立一个有代表性的有效期,也就不可能估测那些缺失的因子组合的有效期。
一个仅对时间点进行的矩阵研究设计,在检测各因子之间变化率的差异和建立一个可靠的有效期方面,常常与完整设计方案有相似的能力。这是因为假设这些变化存在线性关系,而且还因为所有因子组合在起始时间点和申报前的最后时间点都仍然进行完全试验。
2.5 数据评估
简化设计研究获得的稳定性数据的处理和评估方式与完整试验设计相同。
Hits: 59
- 新原料药和制剂的稳定性试验
- 稳定性试验: 新原料药和制剂的光稳定性试验
- 稳定性试验:新剂型的要求
- 新原料药和制剂稳定性试验的括号法和矩阵法设计
- 稳定性数据的评价
- 分析方法验证:文本及方法学
- 新原料药中的杂质
- 新药制剂中的杂质
- 元素杂质指南
- 关于在ICH区域内评估并推荐采用药典相关要求的指导原则
- 关于ICH区域内药典附录的评价及建议-注射剂装量检查法
- 关于ICH区域内药典附录的评价及建议-不溶性微粒检查法
- 关于ICH区域内药典附录的评价及建议-非无菌产品的微生物检查:微生物计数法
- 关于ICH区域内药典附录的评价及建议-非无菌产品的微生物检查:控制菌检查法
- 关于ICH区域内药典附录的评价及建议-非无菌产品的微生物检查:原料药及其制剂的判定标准
- 关于ICH区域内药典附录的评价及建议 -崩解时限检查法
- 关于ICH区域内药典附录的评价及建议 -溶出度检查法
- 关于ICH区域内药典附录的评价及建议 —无菌检查法
- 关于ICH区域内药典附录的评价及建议 -片剂脆碎度检查法
- 关于ICH区域内药典附录的评价及建议 —聚丙烯酰胺凝胶电泳法通则
- 关于ICH区域内药典附录的评价及建议 —毛细管电泳法
- 关于ICH区域内药典附录的评价及建议 —筛分法
- 关于ICH区域内药典附录的评价及建议 —粉末的散装密度和振实密度测定法
- 来源于人或动物细胞系的生物技术产品的病毒安全性评价
- 生物技术产品的质量:rDNA衍生蛋白质产品生产细胞的表达构建体分析
- 质量标准 新原料药和制剂的检测以及可接受标准:化学物质
- 质量风险管理
- 药品研发
- 药物致癌试验的必要性
- 人用药物的遗传毒性试验和数据分析指导原则
- 毒代动力学指导原则:毒性研究中全身暴露的评价
- 动物慢性毒性试验的周期(啮齿类和非啮齿类)
- 药代动力学:重复给药的组织分布研究指导原则
- 药物生殖毒性和雄性生育力毒性的检测
- 生物技术药品的临床前安全性试验
- 人用药延迟心室复极化(QT间期延长)潜在作用的非临床评价指导原则
- 人用药物的安全性药理学研究
- 人用药品的免疫毒性研究
- 抗癌药物的非临床评价
- 药物的光安全性评价
- 对非危及生命的疾病的长期治疗药物进行临床安全性评估的人群暴露程度
- 临床安全性数据管理:快速报告的定义和标准
- 药物警戒计划
- 研发安全性更新报告
- 临床研究报告的结构与内容
- 新药注册所需的量-效关系资料
- 引入海外临床数据时要考虑的种族因素
- 老年人群的临床研究
- 临床试验的一般考虑
- 临床试验统计原则
- 儿童用药品的临床调查
- 新抗高血压药的临床评价原则
- 基因组生物标记物、药物基因组学、遗传药理学、基因组数据和样本编码分类的定义
