NIH-Funded Clinical Trial Will Evaluate New Dengue Therapeutic
2月 11, 2025
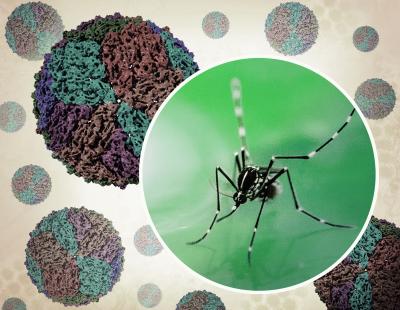 创意布局,其中包含可以传播登革热病毒的伊蚊照片,以及成熟登革热病毒颗粒的冷冻电子显微镜效果图。通过透射电子显微镜捕获的登革热病毒颗粒群(米色)(由 CDC 提供)在外部背景中微弱显示。
创意布局,其中包含可以传播登革热病毒的伊蚊照片,以及成熟登革热病毒颗粒的冷冻电子显微镜效果图。通过透射电子显微镜捕获的登革热病毒颗粒群(米色)(由 CDC 提供)在外部背景中微弱显示。
由美国国立卫生研究院 (NIH) 支持的一项临床试验正在测试一种实验性疗法,旨在帮助遭受登革热(一种蚊媒病毒性疾病)影响的人。该研究得到了 NIH 国家过敏和传染病研究所 (NIAID) 的支持,将涉及将成年志愿者暴露于一种导致轻度疾病的弱化登革热病毒株,并施用不同剂量的研究性治疗药物,以评估其安全性和减轻症状的能力。
根据美国疾病控制和预防中心的数据,登革热通过受感染的伊蚊传播,每年导致多达 4 亿人患病,主要在世界的热带和亚热带地区。2024 年,美洲的登革热病例激增至创纪录水平,亚利桑那州、加利福尼亚州、佛罗里达州、夏威夷州和德克萨斯州报告了美国本地传播。登革热在波多黎各流行,去年报告了近 1,500 例病例。大多数登革热患者不会出现症状,但那些会出现症状的人通常会出现严重的头痛和身体疼痛、恶心和呕吐、发烧和皮疹。每 20 名登革热患者中就有 1 人会发展为严重疾病,这可能导致休克、内出血和死亡。目前没有美国食品和药物管理局批准的登革热治疗方法。
“在照顾登革热危重患者时,医疗保健提供者除了提供支持性护理外别无选择,”NIAID 主任 Jeanne Marrazzo 医学博士、公共卫生硕士说,“我们必须找到安全有效的治疗方法,为登革热患者提供急需的缓解。
新的临床试验将测试 AV-1 的能力,AV-1 是由 AbViro(马里兰州贝塞斯达)开发的研究性人单克隆抗体治疗药物,在登革热病毒感染前后给药时缓解临床症状。先前完成的一项由 NIAID 支持的 1 期试验的结果表明,AV-1 在人体中是安全的,为新的临床试验测试其安全性和有效性提供了基础。
2 期临床试验将在两个地点招募至少 84 名健康成年志愿者:位于巴尔的摩的约翰霍普金斯大学彭博公共卫生学院免疫研究中心和位于伯灵顿的佛蒙特大学疫苗检测中心。在初步筛选和体格检查后,志愿者将被随机分配到两组中的一组。一组将在感染轻度登革热病毒株前一天接受 AV-1,另一组将在感染登革热病毒 4 天后接受 AV-1。每组将被进一步细分以接受 100 毫克、300 毫克或 900 毫克的 AV-1,以 60 分钟的静脉输注给药。对于三个剂量水平中的每一个,12 名参与者将接受研究性单克隆抗体,2 名参与者将接受安慰剂。
在 AV-1 给药之前或之后,每个志愿者都将接受减毒(减毒)登革热病毒注射。在使用这种攻击病毒的早期研究中,大多数志愿者出现皮疹,一些志愿者还出现了其他轻微的登革热症状,例如关节和肌肉疼痛或头痛。没有志愿者患上登革热或重症登革热。
志愿者将参加与研究人员的定期随访至少 155 天,以仔细监测研究性单克隆抗体的效果。通过身体检查、日记卡和血液样本,研究人员将记录志愿者的免疫系统对登革热病毒挑战的反应、病毒从血液中消失的速度以及他们可能出现的任何症状。研究人员将使用这些信息来确定与安慰剂相比,AV-1 如何影响志愿者从登革热中恢复的能力,并确定 AV-1 可能有效的剂量。
如果 AV-1 在这项临床试验中显示出有希望的结果,研究人员可能会对其对登革热病毒的安全性和有效性进行进一步的临床评估。有关该研究的更多信息,请访问 ClinicalTrials.gov 并搜索标识符NCT06799741。
Hits: 79
