Contents
Contrary to viral claim, regulatory agencies knew of residual DNA in COVID-19 mRNA vaccines; no evidence this poses health concern
关键要点
监管机构对疫苗等生物制品中残留 DNA 对健康的潜在影响的担忧并不新鲜或不陌生。事实上,在 COVID-19 大流行之前,世界卫生组织和美国食品药品监督管理局已经制定了可接受残留 DNA 水平的推荐指南。含有 DNA 的疫苗,例如水痘疫苗(一种含有 DNA 病毒的减毒活疫苗)在大流行之前也已被广泛使用,并已被证明是安全的。
审阅的内容
判决详细信息
事实不准确:加拿大卫生部表示,在疫苗获得授权之前,它就知道 COVID-19 mRNA 疫苗中存在残留的 DNA。BioNTech 于 2020 年向欧洲药品管理局提交的一份档案也显示,监管机构已获知残留 DNA 的数据。
不支持:没有可靠的证据表明疫苗中的 DNA 整合到我们的 DNA 中或会增加患癌症的风险。事实上,在 COVID-19 疫苗之前有几种含有 DNA 的疫苗,例如水痘疫苗。这些已被证明是安全的。
完整索赔
“您现在可以起诉 mRNA COVID 疫苗制造商要求赔偿损失,并且 FDA 必须将 COVID 疫苗从市场上撤下。为什么?掺杂。质粒生物活性污染物序列未向监管机构指出。加拿大卫生部周四证实辉瑞 COVID-19 疫苗中存在 DNA 污染,并证实辉瑞没有向公共卫生当局披露污染情况”
回顾
2023 年 10 月 20 日发布到 OSF 预印本服务器的预印本声称,某些批次的辉瑞和莫德纳 COVID-19 疫苗中存在 DNA 片段。它还声称残留 DNA 的数量与与特定疫苗批次相关的严重不良事件的数量相关,这表明不良事件可能是由残留 DNA 引起的。
这是对早先声称 COVID-19 mRNA 疫苗中的 DNA 污染构成癌症风险的最新解释,该说法于 2023 年 6 月在网上疯传。这一说法基于 2023 年 4 月的预印本,声称表明辉瑞 COVID-19 mRNA 疫苗含有来自 SV40 病毒的 DNA 序列。已发现 SV40 病毒会导致仓鼠等一些动物患癌症。4 月的预印本在之前的评论中已经详细讨论过。根据现有证据,Health Feedback 得出结论,这些说法未经证实。
顺便说一句,就在 2023 年 10 月预印本前一天出现的一篇大纪元时报文章声称,加拿大药品监管机构加拿大卫生部“表示辉瑞没有披露猿猴病毒 40 (SV40) DNA 序列的存在”,并引用了 4 月预印本的说法。大纪元时报曾多次发布有关 COVID-19 和疫苗的错误信息。
这两篇预印本与《大纪元时报》的文章相结合,在社交媒体上重新引发了关于疫苗中残留 DNA 的潜在影响的讨论。
不出所料,已知反对接种疫苗的个人和团体的社交媒体帖子——例如企业家史蒂夫·基尔施 (Steve Kirsch) 的这条推文、儿童健康保护组织的这篇文章以及 Rebel News 的这篇文章——抓住这篇文章声称疫苗制造商没有披露残留的 DNA 污染,并暗示 COVID-19 疫苗中的残留 DNA 是有害的。一些相关帖子被标记为 #PlasmidGate——这意味着预印本关于 COVID-19 疫苗中残留 DNA 的发现具有启示性和丑闻。
为了帮助读者了解这些说法是否得到证据支持,本综述将讨论 2023 年 10 月预印本中所做的工作、其发现的意义,以及是否有理由相信疫苗中残留的 DNA 会构成重大健康问题,正如一些社交媒体帖子所暗示的那样。
2023 年 10 月预印本的作者做了什么?
2023 年 10 月的预印本是 McKernan 等人在 2023 年 4 月预印本中报告的结果的后续。它着手测量几瓶辉瑞和莫德纳 COVID-19 疫苗中的 DNA 水平,这些疫苗属于加拿大使用的不同批次。
COVID-19 mRNA 疫苗中存在的残留 DNA 是用于制造疫苗的过程的结果。辉瑞 COVID-19 mRNA 疫苗是通过在大肠杆菌中大规模生产 SARS-CoV-2 刺突蛋白的遗传物质来制造的。这是通过将刺突蛋白的遗传物质放入质粒中来实现的,质粒是一个环状 DNA 分子,由大肠杆菌复制。
如果实验室条件最佳,大肠杆菌每 20 分钟分裂一次,这意味着可以在相对较短的时间内产生非常大量的质粒[3]。
然后从细菌中收集 DNA 并切割,以便分离包含刺突蛋白遗传物质的片段,以便将其转录成 mRNA。
预印本的作者使用了两种不同的方法来测量 DNA 水平:定量 PCR(这也是检测 SARS-CoV-2 感染的金标准)和荧光测定(使用与 DNA 等核酸结合的荧光标记物)。预印本的主要发现集中在插入质粒中的刺突蛋白 DNA 的测量,以及质粒上标记复制起点 (ori) 的 DNA。
作者还想探讨残留 DNA 水平是否与美国疫苗不良事件报告系统中的不良事件数量相关的问题。
根据预印本的方法部分,他们收集了与他们分析的疫苗批次相关的 VAERS 数据,尽管他们将报告仅限于来自美国以外的疫苗批次。将他们的分析仅限于美国境外报告的原因是,由于美国境内外潜在的漏报和强制性报告要求,他们希望降低不良事件报告率差异导致的混杂水平。没有给出为什么作者认为来自美国以外的数据受报告率差异的影响较小。
预印本没有发现 COVID-19 疫苗中残留 DNA 的水平令人担忧
预印本的主要结论之一是,使用 qPCR 在疫苗瓶中检测到的残留 DNA 水平实际上远低于世界卫生组织和美国食品药品监督管理局建议的 10 ng DNA/剂量限值。预印本承认了这一点,并指出“所有疫苗中的 qPCR 残留 DNA 含量均低于 [FDA 和 WHO 设定的 10 ng/剂量指南]”。
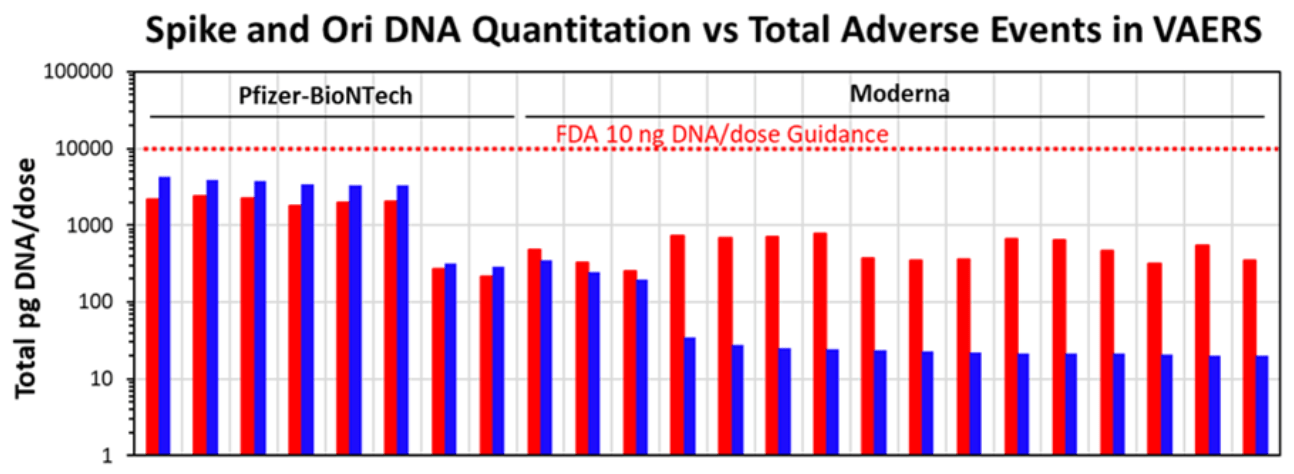
图 1 – 每个测试的小瓶中对应于复制起点(质粒上 DNA 复制开始的区域)的刺突 DNA(红色)和质粒 DNA(蓝色)的数量 。一皮克 (pg) 是一纳克的千分之一。请注意,y 轴位于对数刻度上,而不是线性刻度上。
然而,使用荧光法测量 DNA 水平似乎与 qPCR 测试的结果形成鲜明对比。作者报告说,这种方法表明疫苗中的 DNA 数量比 WHO 和 FDA 指南高出 188 到 509 倍以上。
虽然这似乎令人担忧,但需要注意的是,荧光测定的特异性不如 qPCR,因为作者使用的荧光标记物也可以结合 RNA 和 DNA。考虑到疫苗瓶含有 DNA 和 RNA 的混合物,这种限制很重要。
在这篇文章中,韦恩州立大学的外科肿瘤学家和癌症研究员 David Gorski 指出,在 DNA 定量之前,疫苗样本必须在 95°C 下用高温处理。热量会破坏包裹 RNA 的脂质纳米颗粒,将 RNA 释放到溶液中。“当 RNA 比 [双链 DNA] 多得多时,即使是高选择性的检测也可能受到 RNA 的影响,”他总结道。
赫尔辛基大学研究宿主-微生物相互作用的高级大学讲师 Mikael Niku 在 X/Twitter 上写信给预印本作者之一 Kevin McKernan,提出了同样的问题:“您使用的荧光测定试剂盒对 DNA 不具有特异性。Biotium 技术支持表示,它对 DNA 的选择性仅为 RNA 的 10 倍或更高,您应该将其用于*干净* dsDNA 制备”。
预印本的作者之一凯文·麦克南 (Kevin McKernan) 回应了这一批评,指出辉瑞如何使用荧光法来测量其疫苗中的 RNA 水平。
Niku 反驳说“当您测量溶液中 MAJOR 核酸的浓度时,荧光测定法是完全有效的,在 [辉瑞] 的情况下,这显然是 RNA”。
简而言之,荧光法检测到的明显大量 DNA 可能是由于样品中游离 RNA 水平高(正如 mRNA 疫苗所预期的那样),而不是 DNA。
Gorski 建议,作者可以通过用分解 RNA 的 RNase 酶处理样品,然后用荧光法测量 DNA 水平来检查是否是这种情况。但作者没有报告这样做,因此我们不能排除这种可能性。
接下来,作者试图将 VAERS 的严重不良事件报告数量与测试的疫苗批次中检测到的 DNA 数量联系起来,这也提出了一些问题。
正如 Gorski 指出的那样,数据点太少(大多数情况下是 4 或 5 个),因此无法首先得出可靠的相关性。
例如,显示辉瑞数据的图表被解释为显示严重不良事件的比例随着 qPCR 检测到的 DNA 量而增加,即使人们不应该相信数据点如此之少的相关性(图 2)。但在 Moderna 的情况下,具有更多的刺突 DNA 的行显示更多的 SAE,而来自质粒复制起点 (ori) 的 DNA 较多的行显示较少的 SAE 来解释。
因此,除了不可靠之外,因为它们基于的数据点太少,这些趋势线彼此不一致。
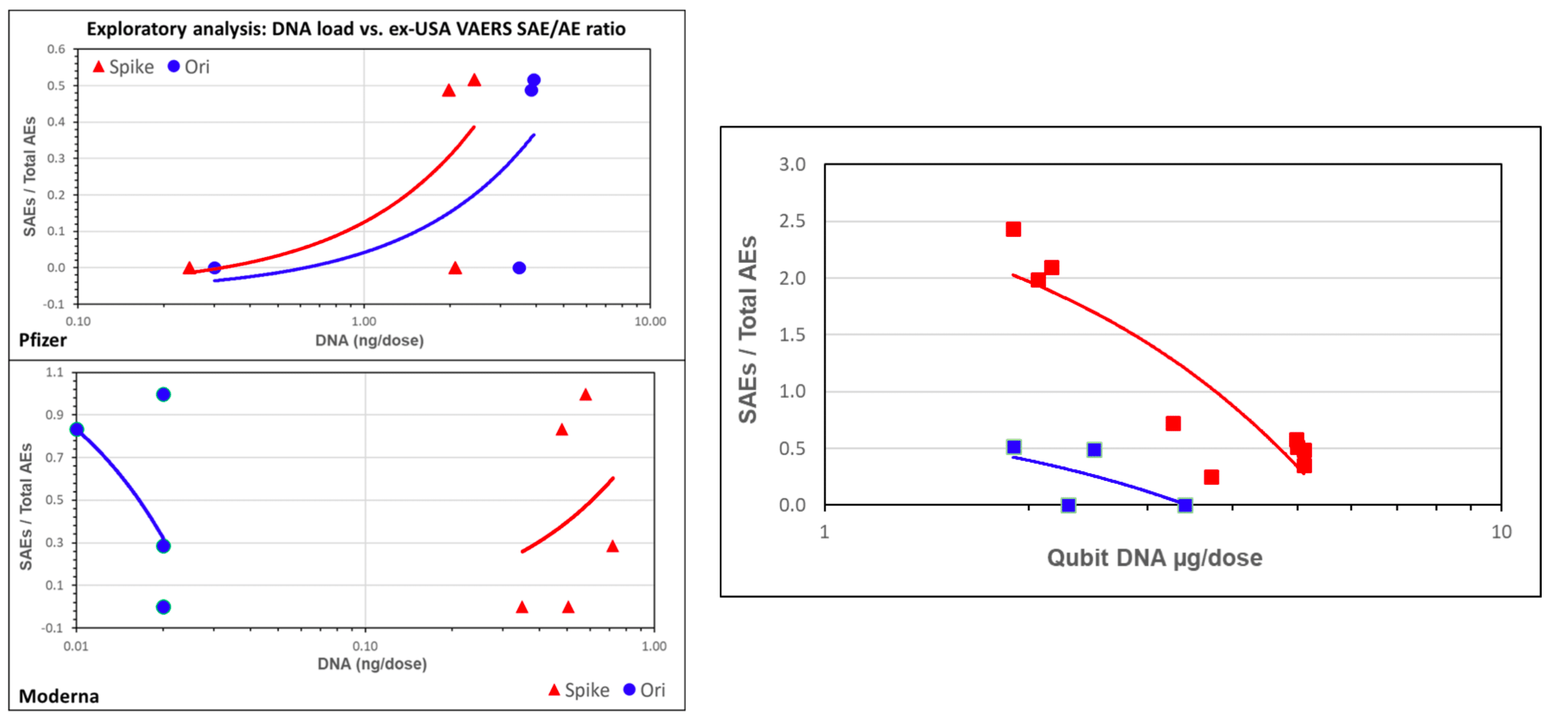
图 2 – 据称显示 qPCR(左)和 Qubit 荧光测定(右)检测到的 DNA 量与严重不良事件数量(占总不良事件的比例)的相关性的数据。左:红线对应于刺突 DNA,而蓝线对应于质粒 DNA。上图显示了辉瑞疫苗的结果,下图显示了莫德纳疫苗的结果。右:蓝线对应辉瑞,红线对应 Moderna。来源:Speicher 等人。
使用荧光法衍生的 DNA 测量的相关性表明,疫苗中存在的残留 DNA 越多,严重不良事件就越少。社交媒体帖子中没有承认这一结果,这些帖子依赖预印本声称残留 DNA 是有害的。
我们通过电子邮件联系了预印本的作者,询问他们使用的方法。在他的电子邮件回复中,预印本的通讯作者、圭尔夫大学的高级研究助理大卫·斯派歇尔 (David Speicher) 没有以书面形式回答我们的问题,而是提出通过 Zoom 电话回答。他补充说,作者将 “考虑 [我们] 有趣的问题,以便在手稿的未来版本中进行澄清”。
监管机构在预印本之前就知道 COVID-19 疫苗中存在残留的 DNA,没有发现令人担忧的证据
尽管某些社交媒体帖子做出了假设,但正如 COVID-19 大流行之前的各种出版物所表明的那样,监管机构对疫苗中 DNA 的潜在健康影响的担忧既不新鲜也不陌生。
根据 BioNTech 于 2021 年 2 月 19 日向欧洲药品管理局 (EMA) 提交的公开文件,我们知道疫苗生产过程的一部分涉及用一种称为 DNase 的酶处理所得 RNA 的批次。这种酶消化 DNA,将其分解成片段。因此,BioNTech 和 EMA 都知道疫苗中的 DNA 杂质以及为减少这种杂质而采取的措施。
声称监管机构直到现在才知道 COVID-19 mRNA 疫苗中的残留 DNA 是不正确的,因为提交给欧洲药品管理局的同一文件表明残留 DNA 是制造商量化的杂质之一(“与工艺和产品相关的杂质,包括宿主细胞基因组 DNA、RNA、蛋白质、内毒素、生物负荷和质粒亚型, 对于质粒 DNA,则常规定量”)。
《大纪元时报》发布的电子邮件还显示,加拿大卫生部“在审查期间和授权 mRNA COVID-19 疫苗之前意识到残留质粒 DNA 的存在是一种与过程相关的杂质”。
然而,加拿大卫生部的这一部分回应并未出现在《大纪元时报》的文章中,该文章为监管机构不知道 COVID-19 疫苗中残留 DNA 的不准确说法提供了空间,该声明由 Kirsch、Children’s Health Defense、Rebel News 等提出。
在对《大纪元时报》的回应中,加拿大卫生部还补充说,“对投放到加拿大市场的每批 COVID-19 疫苗的放行测试数据进行了审查,并被认为符合加拿大卫生部批准的要求”。
简而言之,声称加拿大卫生部等监管机构不知道 COVID-19 疫苗中存在残留 DNA 或疫苗制造商没有披露疫苗中存在残留 DNA 的说法是不准确的。
我们联系了加拿大卫生部和 FDA 就这些声明发表评论。
在回答我们关于 COVID-19 疫苗中 DNA 污染的问题时,加拿大卫生部在一份声明中说:
“作为监管机构,加拿大卫生部为制造商设定了要遵循的质量标准和要求,包括提供有关疫苗本身和制造过程的全面和详细信息。在任何疫苗的制造过程中,作为标准制造过程一部分的残留元素可能会残留。对这些残留片段的存在有严格的限制和控制,以确保对疫苗的安全性或有效性没有影响。
辉瑞-BioNTech COVID-19 疫苗不含猿猴病毒 40 (SV40)。SV40 启动子增强子序列的存在与整个病毒本身的存在不同。
发现 SV40 启动子增强子序列是辉瑞-BioNTech COVID-19 疫苗中的残留 DNA 片段。该片段无活性,没有功能作用,并且经测量始终低于加拿大卫生部和其他国际监管机构要求的限值。
“它还补充说,”任何关于 SV40 启动子增强子序列的存在与癌症风险增加有关的说法都是没有根据的”。我们在审核结束时提供了加拿大卫生部的完整声明。
FDA 通过电子邮件通知我们,我们的问题已转发给生物制品评估和研究中心 (CBER),该中心负责监管包括疫苗在内的生物衍生产品,并将尽快跟进回复。如果有新信息,我们将更新本综述。
没有证据表明 COVID-19 mRNA 疫苗中的残留 DNA 会构成健康风险
关于疫苗中残留 DNA 对健康的潜在影响的许多讨论都围绕着 DNA 可能整合到我们的基因组中并导致癌症等疾病的可能性。然而,这并没有得到证据的证实。
加拿大卫生部对《大纪元时报》的回应称,“用于辉瑞疫苗生产的 DNA 质粒通过额外的步骤线性化、降解和数量减少。没有同行评审的证据表明线性化或片段化的 DNA 能够易位到细胞核”。这部分回应没有包含在 Epoch Times 的文章中。
在一条推文中,McKernan 引用了 FDA 指南[4],指出即使是来自监管元件(如 SV40 启动子)的少量 DNA,也仍然可能构成 DNA 整合的风险。但是,这错过了指南中给出的重要背景:
“在评估质粒整合的潜在危害时,应该注意的是,将具有强调节区域的质粒引入宿主基因组的风险远远超过与随机点突变相关的风险 […]在这种情况下,短至 7 bp 的 DNA 片段会影响整合或重组的速率。示例包括 VDJ 重组信号序列和相关序列、气样元件和小卫星、ALU 序列、乙型肝炎和哺乳动物基因组中存在的重组酶信号以及拓扑异构酶 II 识别位点。“ [强调后加]
这些给定的例子中的几个都与一开始就非常简短的监管要素有关。例如,V(D)J 重组序列的长度在 7 到 9 个碱基对之间[5]。微型卫星的数位在 10 到 50 个碱基对之间。另一方面,SV40 启动子跨越 300 多个碱基对。在被分解成更小的碎片后,它是否仍能保持生物活性是值得怀疑的。
此外,即使残留的 DNA 进入我们的细胞,也没有证据表明这会导致整合。里斯本大学免疫学家兼教授 Marc Veldhoen 在 X/Twitter 上强调,已经有许多含有 DNA 的疫苗正在使用,例如 COVID-19 腺病毒载体疫苗,以及水痘疫苗(水痘病毒是一种 DNA 病毒)。没有证据表明这些疫苗与患癌症的风险增加有关。
他补充说:
“与 DNA 或 RNA 疫苗一样,使用减毒或灭活病原体的疫苗的工作原理类似。DNA/RNA 进入您的细胞,并从病原体中制造蛋白质。重要的是(原文如此),DNA/RNA 疫苗不能扩增,也不会产生传染性物质。
在所有这些情况下,DNA 都会进入我们的细胞。然而,我们的细胞有多种方法可以检测外源 DNA 并破坏它,因为我们的免疫系统将外源 DNA 视为感染的迹象[6-8]。这最终会导致受影响的细胞通过程序性细胞死亡(细胞凋亡)和去除留下的细胞、蛋白质、DNA 和 RNA 而死亡。
“所以不,即使有关于 SV40 增强子的恐怖故事,DNA 或 RNA 也不会进入细胞核,它肯定不会整合,细胞会死亡。它检测 DNA 或 RNA,然后死亡。它产生外来蛋白质,然后死亡。即;无论如何,细胞都会死亡,“他总结道。
加拿大卫生部在回应健康反馈关于 COVID-19 疫苗中 DNA 污染的问题时的声明
“加拿大卫生部最初于 2020 年 12 月批准了辉瑞-BioNTech COVID-19 mRNA 疫苗,随后又授权了更新版本,包括 2023 年 9 月针对 XBB Omicron 亚变体的最新疫苗。每项评估都包括确定疫苗符合该部门在加拿大使用的严格监管安全性、有效性和质量要求。
作为监管机构,加拿大卫生部为制造商制定了要遵循的质量标准和要求,包括提供有关疫苗本身和制造过程的全面和详细信息。在任何疫苗的制造过程中,作为标准制造过程一部分的残留元素可能会残留。对这些残留片段的存在有严格的限制和控制,以确保对疫苗的安全性或有效性没有影响。
辉瑞-BioNTech COVID-19 疫苗不含猿猴病毒 40 (SV40)。SV40 启动子增强子序列的存在与整个病毒本身的存在不同。
发现 SV40 启动子增强子序列是辉瑞-BioNTech COVID-19 疫苗中的残留 DNA 片段。该片段无活性,没有功能作用,经测量始终低于加拿大卫生部和其他国际监管机构要求的限值。
任何关于 SV40 启动子增强子序列的存在与癌症风险增加有关的说法都是没有根据的。也没有证据支持任何疫苗中存在完整的 SV40 会增加个体患癌症的风险或加速患癌症。
加拿大卫生部继续监测 COVID-19 疫苗,以确保它们继续满足安全性、有效性和质量的最高标准,并且其益处继续大于任何潜在风险。
更新(2023 年 10 月 28 日):
我们更新了我们的系统综述,纳入了预印本通讯作者加拿大卫生部和 FDA 的回复。此信息被添加到第 27 段和第 36 段中。加拿大卫生部的完整声明也附在审查的末尾。
引用
- 1 – Girardi 等人 (1962) 新生儿期接种液泡病毒 SV40 的仓鼠肿瘤的发展。实验生物学和医学。
- 2 – Cicala et al. (1993) SV40 诱导仓鼠间皮瘤。美国病理学杂志。
- 3 – Gibson et al. (2018) 野外细菌倍增时间的分布。伦敦皇家学会论文集。B 系列。
- 4 – Klinman 等人 (2010) FDA 预防性 DNA 疫苗指南:分析和建议。疫苗。
- 5 – Bassing 等人 (2000) 重组信号序列将染色体 V(D)J 重组限制在 12/23 规则之外。自然界。
- 6 – Briard 等人 (2020) 先天免疫反应中的 DNA 感应。生理学。
- 7 – 帕鲁丹和鲍伊。(2013) DNA 的免疫感应。免疫。
- 8 – Motwani 等人 (2019) 健康和疾病中 cGAS-STING 通路的 DNA 传感。自然评论遗传学。
Hits: 30