Stem cell transplantation
干细胞移植(SCT) 广泛用于治疗血液系统恶性肿瘤,例如淋巴瘤、 多发性骨髓瘤和髓系/淋巴母细胞白血病 。它也可能适用于治疗某些实体器官肿瘤,例如乳腺癌和肾细胞癌 ,并且越来越多地用于治疗非恶性疾病。其原理是清除患者的免疫系统,并用来自患者自身( 自体干细胞移植 )或 HLA 匹配供体 ( 异基因干细胞移植 )的造血干细胞进行替代。
干细胞采集方法有多种。可以直接从供者的骨髓腔中抽取细胞,也可以先给供者注射粒细胞集落刺激因子 ( G-CSF ) ,使干细胞动员到外周血,然后从外周血中采集。脐带血也可以作为干细胞来源。患者接受预处理后,将供者的干细胞输注到患者体内,干细胞会迁移到骨髓腔,通过稳态机制重建免疫系统。完全重建所需的时间因人而异,通常取决于预处理方案。
清髓性预处理通过高剂量放疗和免疫抑制剂(如环磷酰胺或白消安) 联合使用来清除患者的免疫系统。这种治疗毒性极大,因此只有身体状况较好且通常较年轻的患者才能耐受预处理,从而接受干细胞移植(SCT)。近年来,人们开发了其他强度较低的预处理方案(非清髓性或减低强度预处理[RIC] ),这些方案使用不同的化疗药物和/或较低剂量的放疗,从而增加了可选择 SCT 治疗的患者数量。
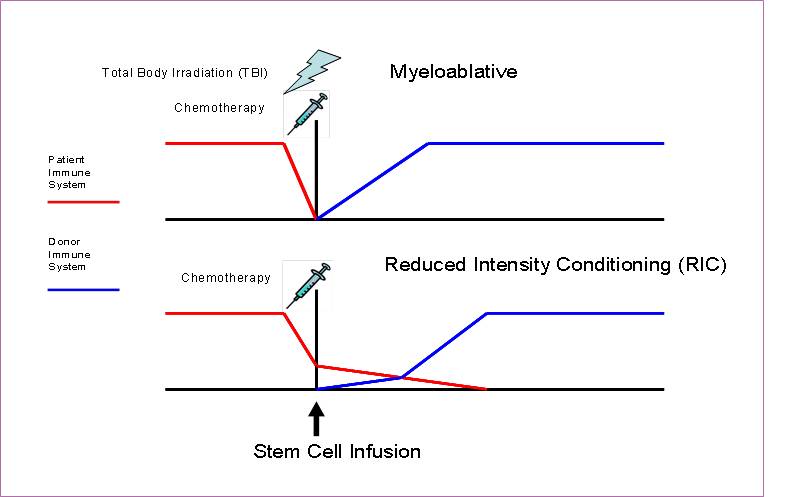
由于减低强度预处理方案不具有清髓性,输注后会出现一段混合嵌合期,其中同时存在患者细胞和供体细胞。最终,供体细胞会占据优势,使免疫系统完全由供体细胞组成( 图 1 )。
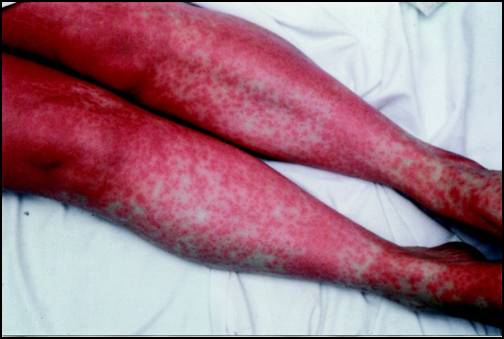
供体是根据 HLA 相容性选择的。供体和受体的 HLA 匹配度越高,发生可能危及生命的移植物抗宿主病 ( GvHD )的风险就越低。GvHD 是指新的供体免疫细胞攻击受体组织,通常是皮肤、肠道和肝脏( 图 2 )。这种情况可能导致严重的身体虚弱,甚至死亡。
造血干细胞移植(SCT)后的一个重要效应是移植物抗白血病(GvL) ,这对于治疗恶性肿瘤时预防复发至关重要。这两种效应被认为主要由 T 细胞介导,移植物抗宿主病(GvHD)的发生率与复发风险降低相关。研究表明,造血系统表达的次要组织相容性抗原 ( mHAg ),例如 HA-1,是 GvL 的重要靶点之一。然而,也有研究观察到,同基因移植后出现的 GvL 反应不太可能是由 mHAg 不匹配引起的,这表明 GvL 可能也具有肿瘤特异性成分。这种特异性成分可能针对肿瘤特异性抗原,例如癌睾丸抗原 ( CTAg )家族的肿瘤蛋白,或者像 PRAME 这样在肿瘤中过度表达的抗原。尽管癌症患者可能会对肿瘤相关抗原产生耐受性,但 SCT 可以促进有效免疫反应的产生,因为供体系统不太可能对这些癌症蛋白产生耐受性。
移植物抗宿主病(GvHD)的发生会带来一些问题,但它与复发风险的降低有关,这可能归因于移植物抗白血病(GvL)效应。因此,目前的研究主要集中在如何增强 GvL 效应并同时降低 GvHD 的发生率上。
© 本作品的版权归作者所有。
Hits: 16
