Contents
孕妇接种百日咳疫苗对预防婴儿百日咳风险分析
目标:
在澳大利亚引入管辖范围内的孕产妇百日咳疫苗接种计划后,我们评估了孕产妇疫苗的有效性(VE ),以及孕产妇百日咳疫苗接种是否改变了前3剂含百日咳疫苗的有效性。
方法:
我们对279 418对母婴进行了一项基于人群的队列研究,采用了3个澳大利亚管辖区的行政健康记录的概率联系。如果婴儿的母亲在出生前≥14天接种过百日咳疫苗,则婴儿可以通过母亲接种疫苗。管辖范围内的免疫记录用于确认婴儿接种了前3剂含百日咳疫苗。婴儿百日咳感染是使用应报告的疾病记录确定的。使用Cox比例风险模型估计VE。
结果:
51.7% 的孕妇(n = 144 429/279 418)在怀孕期间接种了百日咳疫苗,主要是在妊娠 28-31 周时。产妇接种百日咳疫苗的 VE 从 2 个月以下婴儿的 70.4%(95% 置信区间 [CI],50.5-82.3)下降到 7-8 个月婴儿的 43.3%(95% 置信区间 [CI],6.8-65.6),8 个月后则没有显著下降。虽然我们观察到,与未接种疫苗的婴儿相比,接种过母体疫苗的婴儿接种第三剂百日咳疫苗的 VE 点估计值略低(76.5% vs 92.9%,P = .002),但我们并未观察到更高的百日咳感染率(危险比为 0.70;95% CI 为 0.61-3.39)。
结论:
孕28周左右接种百日咳疫苗与8个月大婴儿感染风险较低相关。尽管有一些证据表明,在母亲接种疫苗的婴儿中,婴儿疫苗的有效性较低,但这似乎并没有转化为更大的疾病风险。
主题:
百日咳, 百日咳疫苗, 接种疫苗, 免疫
关于这个主题的已知信息:
怀孕期间接种百日咳疫苗可在6个月内预防百日咳感染。然而,母亲抗体对婴儿初次免疫应答的可能“钝化”效应仍然是一个重要的临床问题。
这项研究补充道:
尽管有证据表明,第3剂婴儿无细胞百日咳疫苗在母亲接种的婴儿中的有效性较低,但与没有母亲百日咳疫苗接种史的婴儿相比,这与百日咳发病率较高无关。
百日咳是一种传染性很强、可能很严重的呼吸道疾病。尽管自从引入全细胞和无细胞儿童期疫苗后,百日咳的负担有所减轻,但幼儿的发病率和死亡率仍然很高,占所有百日咳住院和死亡的70%至90%。婴儿的高发病率和死亡率导致许多高收入国家引入了孕产妇疫苗接种计划,以防止婴儿感染。在2012年至2013年百日咳流行后,美国和英国提出了为孕妇接种百日咳疫苗(孕产妇疫苗)的建议。2014年至2015年间,澳大利亚各州和地区通过了孕产妇百日咳疫苗接种计划,实施了辖区资助的计划,用于在妊娠约28周时进行白喉-破伤风-无细胞百日咳(dTpa)加强疫苗接种。2018年7月,根据国家免疫计划,孕产妇疫苗接种在澳大利亚获得了联邦资助。
虽然有强有力的数据支持母亲百日咳疫苗接种计划的有效性,但关于保护的持续时间、接种疫苗时胎龄的重要性以及对婴儿初次百日咳疫苗接种免疫应答的潜在影响仍有争议。先前在英国、美国和澳大利亚的研究已经证明在小于2个月的婴儿中,母亲dTpa疫苗接种对百日咳感染有43%至93%的有效性。然而,这些研究中很少考虑到怀孕期间接种疫苗的怀孕时间对疫苗效力(VE)的影响,也很少基于人群的研究评估了母亲接种婴儿疫苗的影响。
先前的研究已经确定了对母亲抗体干扰婴儿对含百日咳和其他疫苗的初次免疫反应的潜在担忧,这种机制被称为“钝化”。尽管一些临床试验和前瞻性队列研究已经观察到,与母亲未接种疫苗的婴儿相比,母亲接种疫苗的婴儿的免疫应答和血清转化较低,很少有大规模的观察性研究调查了母亲接种疫苗对婴儿百日咳疫苗抵抗临床疾病的效果的影响。
我们的目的是(1)根据婴儿年龄和接种疫苗时的孕龄,为预防婴儿百日咳感染提供可靠的母亲百日咳VE估计值;( 2)利用真实世界的数据在人群水平研究可能的钝化效应。
方法
…………………………………
统计分析
…………….
结果
在18个月大的婴儿队列中,共发现331例已报告的百日咳病例,相当于每100 000名婴儿中有118例;在接种疫苗的母亲的婴儿中发现了119例病例(每100 000名婴儿中有82例),在未接种疫苗的母亲的婴儿中发现了212例病例(每100 000名婴儿中有157例)。在331例百日咳病例中,49例(14.8%)是在小于2个月的婴儿中诊断的,124例(37.5%)是在小于6个月的婴儿中诊断的; 12.9% (n= 16/124)的病例与住院时间一致,4.8%(n= 6/124)与ICU入院相吻合,1.6%(n= 2/124)有后来的死亡记录。
小于6个月的婴儿中,母亲对已知百日咳感染的预防率为65.1% (95%可信区间[CI],49.5-76.0),对住院百日咳感染的预防率为60.2% (95% CI,18.3-86.6)图1)。没有足够的数据来评估VE对因百日咳入院ICU和死亡的影响。限于2个月以下婴儿的分析结果与6个月以下婴儿的分析结果相似。
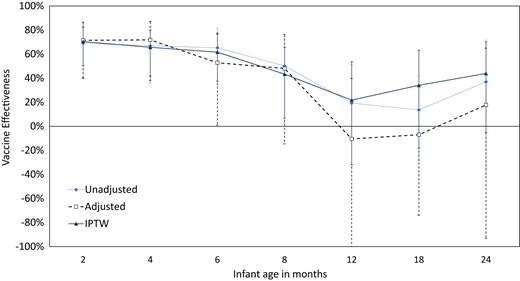
图1
按年龄组划分,小于2个月的婴儿的母亲dTpa VE为70.4% (95% CI,50.5–82.3),3至4个月的婴儿为65.7% (95% CI,41.8–79.8),5至6个月的婴儿为61.6% (95% CI,37.5–76.4),7至8个月的婴儿为43.3% (95% CI,6.8–65.6)图1)。8个月大后,VE不显著(9-12个月:VE,21.8% [95% CI,31.8-53.6%];13-18个月:34.1% [95%可信区间为18.1-63.2];19至24个月:44.0% [95%可信区间为5.0至70.1])。在母亲接种疫苗的婴儿中,报告百日咳感染的中位年龄(中位:11个月;四分位数间距,8.75个月)大于母亲未接种疫苗婴儿百日咳感染的中位年龄(中位:7.5个月;四分位距,10个月;P < .001), although this was predominantly obserVEd in QLD。6个月以下婴儿的VE从西澳大利亚的11.6% (95%可信区间为–57.9至50.5)到昆士兰的76.0% (95%可信区间为63.6–84.2)。不考虑接种疫苗时的胎龄和接种疫苗与出生之间的时间,6个月以下婴儿的VE相似。
共有171 840名婴儿在新界和九龙城区出生,并有免疫接种记录。其中,85 166人(49.6%)在子宫内接受了母亲疫苗接种,86 674人(50.4%)没有母亲疫苗接种记录。大多数接受母亲疫苗接种或未接受至少1剂含百日咳疫苗的婴儿(分别为93.4%和84.8%);87.3%母亲接种疫苗的婴儿完成了3剂DTaP系列,76.6%没有母亲接种疫苗的婴儿完成了3剂系列(表3)。
表3婴儿百日咳疫苗接种的估计效果,按母亲百日咳免疫状态
| 接受含百日咳疫苗的婴儿剂量数 | 母亲接种疫苗的婴儿(n= 85 166) | 没有母亲疫苗接种记录的婴儿(n= 86 674) | 母亲接种疫苗与未接种疫苗的母亲中的百日咳感染aHR (95% CI)b | |||||
|---|---|---|---|---|---|---|---|---|
| N (%) | 百日咳感染 | N (%) | 百日咳感染 | |||||
| n/总数(每10万名婴儿的病例数) | 价值工程(95%置信区间)a | n/总数(每10万名婴儿的病例数) | 价值工程(95%置信区间)a | |||||
| 从未接种过疫苗 | 5594 (6.6%) | 9/85 124 (10.6) | 参考 | 13 202 (15.2%) | 80/86 353 (92.6) | 参考 | 0.21 (0.10–0.45) | |
| 剂量1 | 79 572 (93.4%) | 8/79 548 (10.1) | 62.5% (15.5–83.3) | 73 472 (84.9%) | 22/73 389 (30.0) | 71.2% (52.7–82.4) | 0.34 (0.12–0.97) | |
| 剂量2 | 77 641 (91.2%) | 4/77 367 (5.2) | 83.2% (43.7–95.0) | 70 692 (81.6%) | 11/70 416 (15.6) | 83.6% (67.7–91.7) | 0.19 (0.05–0.71) | |
| 剂量3 | 74 358 (87.3%) | 14/67 518 (20.7) | 76.5% (32.8–91.8) | 66 432 (76.6%) | 15/64 835 (23.1) | 92.9% (86.4–96.3) | 0.70 (0.61–3.39) | |
aHR,调整后的危险比;CI,置信区间;VE,疫苗效力。
a疫苗有效性被估计为1-从Cox比例风险模型得出的风险比,其中婴儿月龄作为潜在的时间变量,婴儿百日咳疫苗接种作为随时间变化的暴露变量。模型根据母亲的社会经济地位、儿童的第一民族地位、早产、母亲开始产前护理(用作家庭获得保健服务的替代措施)和出生年份进行了调整。
b以婴儿月龄为潜在时间变量,比较每剂婴儿百日咳疫苗的母亲百日咳疫苗暴露导致的百日咳感染率的风险比。模型根据母亲的社会经济地位、儿童的第一民族地位、早产、母亲开始产前护理(用作家庭获得保健服务的替代措施)和出生年份进行了调整。
虽然1剂和2剂DTaP的婴儿VE对于母亲接种疫苗的婴儿和没有母亲接种疫苗的婴儿是相似的(1剂:62.5%对71.2%,P交互作用的值= . 32;剂量2: 83.2%对83.6%,P相互作用值= .46),第三剂DTaP的婴儿VE较低(第3剂:76.5%对92.9%,P交互作用的值= .002)(表3)。
尽管如此,接种过3剂DTaP疫苗的婴儿和未接种过疫苗的婴儿的百日咳发病率相似(每100,00 0名婴儿中有20.7例,每100,00 0名婴儿中有23.1例;调整后HR 0.7095%可信区间为0.61–3.39)。存活曲线表明,在没有母亲疫苗接种记录的婴儿中,无论DTaP免疫接种(图2)。
图2
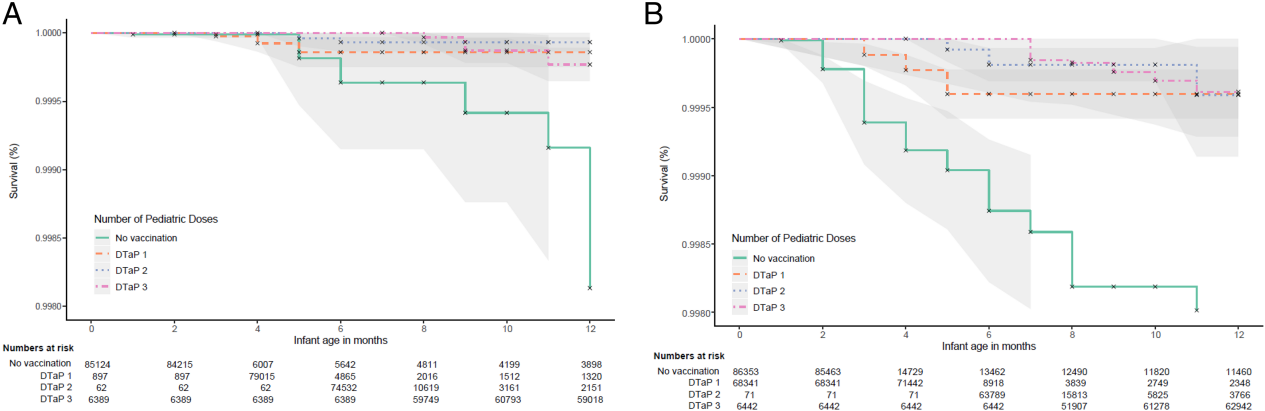
(A)母亲接种疫苗的婴儿和(B)没有母亲接种疫苗记录的婴儿中抗百日咳感染的存活率,按白喉-破伤风-无细胞百日咳(DTaP)疫苗剂量数。
讨论
在澳大利亚3个管辖区实施的母亲百日咳免疫计划的前3年中,我们估计52%的孕妇接种了无细胞百日咳疫苗,并且疫苗接种与6个月大的婴儿百日咳感染总体下降66%相关。母亲百日咳疫苗接种的这种保护作用直到8个月龄都是显著的。虽然我们观察到一些证据支持在母亲免疫接种的婴儿中,3剂DTaP免疫接种可降低婴儿VE,但这似乎并未转化为与无母亲免疫接种记录的婴儿相比更大的疾病风险。这些结果支持在怀孕期间进行百日咳疫苗接种,以预防婴儿百日咳相关的发病率。
由于我们队列的规模,我们能够通过接种疫苗的妊娠时间和婴儿的年龄来特异性地评估VE对百日咳的疗效。尽管免疫原性研究已经观察到在妊娠27至30周之间(与妊娠后期相比)接种疫苗的母亲所生婴儿的脐带血中具有更高的抗体亲和力并且最近的研究报道了在接种疫苗和分娩之间较长的间隔后母亲抗体的半衰期增加,我们没有观察到疫苗接种时间对VE的显著影响。类似地,最近在英国进行的一项开放标记随机对照试验比较了16-23周、24-27周和28-31周的百日咳疫苗接种,发现接种疫苗的妊娠时间对婴儿出生时的抗体没有影响。其他基于监测的母亲在出生前≥17周、13至16周、8至12周、1至7周接种百日咳疫苗的研究也表明,时间对VE预防婴儿疾病的作用有限。虽然我们的研究结果支持在妊娠中期和晚期接种无细胞百日咳疫苗的潜在有效性,但值得注意的是,由于研究期间的建议(即在妊娠28周接种疫苗),很少有母亲在妊娠25周之前接种疫苗。
我们对18个月大的婴儿进行了评估,以评价母亲接种疫苗对百日咳的保护时间,以及婴儿对初次百日咳疫苗接种的反应可能减弱。我们观察到至少在8个月大之前对疾病有显著的保护作用;比先前研究报告的时间长2个月。我们观察到一些证据表明,与没有母亲疫苗暴露的婴儿相比,母亲接种的婴儿第三剂婴儿DTaP疫苗的VE较低。这一发现与之前的随机对照试验结果一致和非随机研究,这些研究一致证明,在先前接受过母亲百日咳免疫接种的婴儿中,对婴儿百日咳疫苗的免疫应答较低。
很少有研究通过母亲疫苗接种状况直接测量婴儿免疫的VE。最近发表的一项对376名2至11个月大婴儿的多中心监测研究表明,至少1剂含百日咳疫苗预防住院百日咳感染的VE在母亲接种疫苗的婴儿中为74%,在无母亲接种史的婴儿中为68%。然而,作者承认他们受到小样本量的限制,无法进行分层分析来正式调查母亲接种疫苗是否改变VE。在我们更大规模的基于人群的研究中,我们确定了第三剂DTaP的效果改变,但在18个月龄时百日咳发病率较低。结合已发表的文献,我们对这些发现的解释是,母亲抗体可能“减弱”婴儿对初次免疫的反应,但母亲和/或婴儿抗体足以保护母亲接种疫苗的婴儿免受感染。然而,需要进一步的研究来证实我们的发现。
优势和劣势
我们的研究有几个优点和局限性。首先,使用澳大利亚的数据链接系统,我们能够构建一个大型的、基于人口的、跨越多个司法管辖区的母婴配对队列,其中包含关于母婴健康的全面纵向信息,有助于提高研究结果的可推广性并减少选择偏差。然而,这些数据是观察性的,和任何此类研究一样,结果可能会受到混杂因素的影响。为了限制这种影响,我们应用了几种技术,包括调整一系列可用的协变量,并通过疫苗接种的逆概率拟合加权模型。尽管如此,我们不能完全排除不受控制的混杂的可能性,特别是对于未观察到的或潜在的变量。我们研究的另一个重要限制是结果识别的方法和婴儿百日咳病例的数量少,这使我们无法对< 2个月的婴儿进行一些分析,对ICU入院和死亡进行VE估计,进行调整后的敏感性分析,并降低了我们按辖区进行估计的精确度。虽然案件是通过采用标准化案件定义的国家法定数据收集来确定的,我们不能排除队列中一些无症状病例未被识别的可能性,从而导致一些结果的错误分类。尽管如此,考虑到大多数病例都是聚合酶链反应检测到的(具有高特异性和敏感性),在我们的队列中不太可能出现假阳性,我们也不期望接种疫苗的母亲和未接种疫苗的婴儿之间会出现不同的结果错误分类。最后,尽管我们的免疫数据来源于具有高度特异性的医疗记录和登记,有可能一些接种了疫苗的人被错误地归类为未接种疫苗的人。因为我们没有理由相信这种错误分类会导致不同的结果,这可能会使我们的VE估计偏向于零,表明我们的估计可能低估了真实的VE。
结论
从这个基于人群的大型队列中,我们估计在怀孕期间接种无细胞百日咳疫苗可预防6个月大婴儿65%的百日咳感染。尽管第三剂DTaP疫苗的VE值可能比母亲接种疫苗的婴儿低,但我们没有观察到证据支持18个月龄内母亲接种疫苗导致百日咳感染率升高。这些结果表明,母亲接种百日咳疫苗可保护婴儿在最易发生严重发病和死亡的时期免受百日咳感染。我们的发现支持在孕28周左右给予百日咳疫苗加强剂量对婴儿健康有益的建议。
全文进行了浓缩,详细可以参见原文。
Regan AK, Moore HC, Binks MJ, McHugh L, Blyth CC, Pereira G, Lust K, Sarna M, Andrews R, Foo D, Effler PV, Lambert S, Van Buynder P. Maternal Pertussis Vaccination, Infant Immunization, and Risk of Pertussis. Pediatrics. 2023 Oct 9:e2023062664. doi: 10.1542/peds.2023-062664. Epub ahead of print. PMID: 37807881.
Hits: 96
