Contents
Group B Streptococcal Disease
卡伦・M・普奥波洛 医学博士、哲学博士 ¹⁻³
摘要
B 族链球菌为人体胃肠道和泌尿生殖道的常见定植菌,也是美国新生儿侵袭性感染最常见的单一致病菌。目前临床采用产时抗生素预防方案,降低孕产妇和新生儿的 B 族链球菌病发病风险,但尚无有效策略预防婴儿晚期发病及非妊娠成人感染。由荚膜多糖与蛋白抗原偶联制成的 B 族链球菌病疫苗正处于研发阶段,或可为所有高危人群提供预防手段。
B 族链球菌(无乳链球菌)可感染各年龄段人群,但其疾病负担主要集中于新生儿、小婴儿及 65 岁以上老年人。侵袭性感染的诊断标准为从无菌部位分离出 B 族链球菌。美国疾病控制与预防中心(CDC)的主动细菌核心监测系统持续追踪各年龄段人群的 B 族链球菌感染发病率,表 1 为 2020-2022 年的汇总数据 ¹⁻³。1 岁以下婴儿的 B 族链球菌感染率最高,该菌是美国所有新生儿侵袭性感染最常见的致病菌,也是早产儿侵袭性感染的第二大常见致病菌⁵⁻⁶。围产期 B 族链球菌感染的全球疾病负担同样沉重,2020 年全球范围内,该菌造成约 40 万例婴儿感染、5 万至 10 万例婴儿死亡、4 万例孕产妇感染,以及 4 万至 5 万例死产⁷。高收入国家在围产期感染预防方面已取得成效,但也导致约半数新生儿在出生前暴露于产时抗生素⁸⁻⁹。多价荚膜多糖偶联 B 族链球菌疫苗正研发中,有望改变该病的流行态势,在中低收入国家的意义尤为重大。本文将阐述 B 族链球菌病的微生物学与流行病学特征、发病机制、治疗及预防措施。
微生物学、免疫学及毒力特征
B 族链球菌为兼性革兰氏阳性双球菌,可在有氧和厌氧环境下生长。1933 年,丽贝卡・兰斯菲尔德采用甲醛灭活菌的酸提取物与兔抗血清,对溶血性链球菌菌株进行分型,将该菌归为 B 族 ¹⁰。2002 年完成 B 族链球菌的基因组测序,其约 50% 的基因与 A 族链球菌和肺炎链球菌的基因同源 ¹¹。B 族抗原是与细胞壁肽聚糖相连的多糖结构,无法在人体内诱导产生保护性抗体 ¹²。
B 族链球菌依据 10 种荚膜多糖抗原分为 Ia 至 IX 血清型,这些具有免疫学差异的抗原,其结构、遗传学特征、在毒力中的作用及免疫原性均已得到充分阐释 ¹²。链球菌荚膜是主要的毒力决定因子,可抵抗宿主白细胞的吞噬和杀伤,还可能促进其在肠道的定植 ¹³⁻¹⁵。荚膜多糖由重复糖基单元以不同方式组合而成,均带有末端唾液酸残基。唾液酸是 B 族链球菌逃避免疫攻击的关键,可抑制补体在细菌表面沉积,并通过补体旁路途径抑制细菌被杀伤。因此,中性粒细胞介导的 B 族链球菌杀伤作用,需要荚膜特异性抗体及补体经典途径的激活 ¹²¹⁶。
血清型特异性荚膜抗体对感染具有保护作用,母体抗体水平与新生儿的感染保护力相关,这也使 B 族链球菌荚膜成为疫苗研发的主要靶点 ¹⁴¹⁷¹⁸。
多种 B 族链球菌表面蛋白也参与疾病发病机制,在细胞黏附、器官定植、上皮侵袭、免疫逃逸和细胞毒性中发挥作用。该菌的主要毒力因子包括:与细胞侵袭相关的 α 样蛋白、与细胞黏附相关的菌毛蛋白、高毒力克隆复合体 17 中存在的高毒力 B 族链球菌黏附素,以及 β- 溶素 – 细胞溶素(该因子可使 B 族链球菌在血琼脂平板上生长时出现溶血性)¹²¹⁹²⁰。毒力因子的表达由多种双组分调控信号转导系统调控,该系统可响应 pH、氧含量、温度等环境因素 ²¹。
已有多种蛋白被列为潜在疫苗靶点,基于 α 样表面蛋白的疫苗已完成 Ⅰ 期临床试验 ²²。
B 族链球菌感染
B 族链球菌可在多种物种中分离得到。在发现其可导致人类疾病前,19 世纪末研究者已鉴定出牛源 B 族链球菌菌株可引发奶牛乳腺炎 ²³。其学名Streptococcus agalactiae(无乳链球菌)便源于该菌感染奶牛乳腺后会导致产奶量下降的现象。B 族链球菌还可感染并致死养殖鱼类,尤以淡水罗非鱼多见 ²³²⁴。在人体中,该菌可在健康成人的体内定植且无临床症状,但可引发新生儿、小婴儿、孕产妇及老年人的感染性疾病。
新生儿及小婴儿感染
美国于 20 世纪 60 年代首次发现新生儿 B 族链球菌病,至 70 年代,该菌的感染率迅速超过其他常见新生儿致病菌,其快速传播的原因至今尚未完全阐明 ²⁵⁻²⁷。新生儿 B 族链球菌感染分为早发型和晚发型:早发型发病于出生至 6 日龄,晚发型发病于 7 至 89 日龄。该分型与两种感染的独特临床特征相符,且与多数新生儿队列研究中针对其他致病菌采用的 3 日龄分界标准不同 ²⁸。超晚发型则定义为 3 月龄及以上婴儿的感染。
母体直肠阴道内 B 族链球菌定植是新生儿早发型感染最重要的危险因素。B 族链球菌并非人体胃肠道和泌尿生殖道菌群中的常驻菌,也非优势菌。美国任意时点的孕产妇定植率为 20%~30%,全球孕产妇定植率约为 18%,且存在地域差异⁷²⁹。美国孕产妇发生 B 族链球菌定植的相关因素包括:年龄偏小、肥胖、性生活活跃及吸烟 ²⁹⁻³²。孕产妇的 B 族链球菌定植状态(定植 / 未定植)可在孕期发生变化,妊娠 36 周及以后行直肠阴道培养检测 B 族链球菌,结果与分娩时的定植状态相关性最高 ²⁹³⁰。
早发型感染的发病机制为:母体胃肠道和下泌尿生殖道的 B 族链球菌上行定植,蔓延至子宫上生殖道、子宫腔(包括羊水),最终定植于胎儿和新生儿体内。胎儿和新生儿的黏膜、皮肤定植,以及吸入或吞咽受感染的羊水,均可促使感染进展为侵袭性疾病。若无产时抗生素预防,定植产妇分娩的婴儿中,约半数会发生体表部位定植,其中 1%~2% 会发展为侵袭性疾病 ²⁹³³³⁴。表 2 列出了早发型感染的其他独立危险因素,包括促进发病的因素(如胎膜早破时间延长)、导致基础易感性的因素(如早产儿的新生儿免疫防御功能低下),以及提示感染正在发生的因素(如母体发热)。
晚发型感染的发病机制尚未完全明确。婴儿可通过非母体途径感染 B 族链球菌,但母体定植和早产是晚发型感染最强的预测因素 ²⁹³⁵³⁶。婴儿口咽和胃肠道定植是晚发型感染的重要发病因素,且晚发型感染与母体 B 族链球菌乳腺炎相关 ³⁷。受感染的母乳是否为 B 族链球菌的感染源,或定植量较高的婴儿是否会将该菌传播至母乳中,目前尚无定论;但母乳中的 B 族链球菌抗体可能在预防婴儿定植和感染中发挥作用 ³⁸。
表 1 美国特定人群的 B 族链球菌病发病率 *
| 人群 | 发病率 |
|---|---|
| 新生儿(0~6 日龄) | 0.20/1000 活产儿 |
| 婴儿(7~89 日龄) | 0.25/1000 活产儿 |
| 孕产妇 | 0.12/1000 活产儿 |
| 年龄分组 – | |
| <1 岁 | 49.0/10 万 |
| 1~17 岁 | 0.2/10 万 |
| 18~49 岁 | 4.0/10 万 |
| 50~64 岁 | 14.0/10 万 |
| 65~84 岁 | 22.0/10 万 |
| ≥85 岁 | 39.0/10 万 |
| 美国总体人群 | 9.0/10 万 |
- 汇总数据除孕产妇来自法雷斯等人的研究⁴外,其余均来自美国疾控中心主动细菌核心监测报告 ¹⁻³。
美国疾控中心 2006-2015 年的报告共收录 1277 例早发型和 1387 例晚发型 B 族链球菌病病例 ³⁹。约 75% 的早发型感染在出生当日确诊,94%~95% 的病例在出生后 48 小时内发病。美国早产儿(妊娠<37 周)占总活产数的 10%~11%,但占早发型感染病例的 27%~28%。约 10% 的早发型感染合并脑膜炎 ³⁹。早发型感染婴儿的临床表现缺乏特异性,轻者仅出现呼吸急促、喂养困难、皮肤花斑等轻微症状,重者可发展为严重脓毒症综合征,伴代谢性酸中毒、肺炎、肺表面活性物质缺乏、持续性肺动脉高压或全身性低血压。美国早发型感染的病死率为 4%~6%,且过去 30 年无明显变化 ³⁹⁴⁰,死亡病例主要为早产儿(病死率 19%),足月儿病死率仅为 2%³⁹。一项针对欧洲 8 个国家 2008-2010 年 82 例早发型感染的研究显示,其早产率、临床表现及病死率与美国数据相近⁴¹。
美国晚发型感染婴儿的中位发病日龄为 34 天(四分位距 20~49 天)³⁹,超 40% 的病例为早产儿。早产儿的 B 族链球菌定植状态、母源抗体水平及免疫保护应答的差异,可能是其易感性更高的原因。约 30% 的晚发型感染合并脑膜炎,肺炎、化脓性关节炎、骨髓炎和腹膜炎的合并率相对较低。与早发型感染不同,晚发型感染常以发热为首发症状,但其他全身感染症状的发生率与早发型相近。美国晚发型感染的病死率约为 5%~6%,早产儿及合并脑膜炎的病例病死率更高,约为 8%~10%³⁹。欧洲多家中心对 71 例晚发型感染的分析结果显示,其发病日龄、早产率、临床表现、脑膜炎发生率及病死率均与美国数据一致⁴¹。
超晚发型感染的发病率约为晚发型的 1/10,现有有限数据显示,存在基础疾病的婴儿发病风险更高⁴⁴²⁴³。
中低收入国家的新生儿和婴儿 B 族链球菌感染病死率显著高于高收入国家,尤其是在缺乏专业助产人员的地区⁷。无论在何种地区,足月和早产的 B 族链球菌感染存活者均可能出现永久性神经损伤,合并脑膜炎时损伤风险更高⁴¹⁴²⁴⁴。极早产儿的预后极差:一项对美国妊娠<27 周的 B 族链球菌感染婴儿的 19 年随访研究显示,近 80% 的患儿要么死亡,要么存活但伴中至重度神经发育障碍⁴⁵。
孕产妇感染
孕期 B 族链球菌感染可表现为无症状菌尿、尿路感染或肾盂肾炎。即使经规范治疗,发生上述感染的孕产妇在分娩时仍被认定为 B 族链球菌定植状态。孕产妇的侵袭性 B 族链球菌病发病率,高于 18~49 岁的普通成人人群(表 1)。全球范围内,孕产妇侵袭性感染的发生率约为 29 例 / 10 万分娩(95% 置信区间 15~47)⁷。美国疾控中心 1999-2005 年的监测数据显示,孕产妇 B 族链球菌感染中,半数病例合并菌血症;此外,还可从子宫、胎盘、羊水和腹腔液中分离出该菌,相关临床综合征包括脓毒症、子宫内膜炎、绒毛膜羊膜炎和肺炎⁴。自发性流产或死产病例中,可从母体或胎儿组织中分离出 B 族链球菌。死产的病因诊断往往不完整,但研究显示,全球每年约有 2 万至 10 万例死产由宫内 B 族链球菌感染所致⁷。
B 族链球菌定植与早产也存在相关性,但相关效应值的置信区间较宽,且多数研究存在未校正的混杂因素⁷⁴⁶。
表 2 侵袭性 B 族链球菌病的危险因素
| 人群及感染类型 | 危险因素 |
|---|---|
| 新生儿早发型感染(0~6 日龄) | 母体直肠阴道 B 族链球菌定植;孕期 B 族链球菌菌尿 / 尿路感染;早产(妊娠<37 周);产时母体发热≥38℃;胎膜早破时间延长;既往分娩婴儿患 B 族链球菌病 |
| 婴儿晚发型感染(7~89 日龄) | 母体直肠阴道 B 族链球菌定植;早产(妊娠<37 周) |
| 孕产妇 | 直肠阴道定植;产时 / 产后发热≥38℃ |
| 其他成人 | 年龄≥65 岁;肥胖;功能性 / 手术性脾切除;糖尿病;恶性肿瘤;慢性心血管、胃肠道、肝脏、神经系统或肾脏疾病;食用生淡水鱼 |
非妊娠成人感染
非妊娠成人可发生 B 族链球菌菌血症及器官特异性感染。全球非妊娠成人的侵袭性 B 族链球菌病发病率约为 3 例 / 10 万,存在地域和年龄差异:北美地区的总体发病率最高(5.9 例 / 10 万),65 岁以上人群的发病率最高(19.4 例 / 10 万)⁴⁷。表 1 为美国 19 岁及以上成人的 B 族链球菌病发病率。美国疾控中心 2008-2016 年的监测显示,非妊娠成人的 B 族链球菌病发病率呈上升趋势,且感染者的风险特征发生变化⁴⁸。2016 年,美国非妊娠成人的侵袭性感染年发病例数约为 2.8 万,男性发病率高于女性。95% 的病例存在基础疾病,其中肥胖和糖尿病各占约 50%,恶性肿瘤和心血管疾病各占约 15%。几乎所有患者均需住院治疗,83% 合并菌血症,27% 收入重症监护室,病死率为 5%~6%。临床综合征包括皮肤、软组织、骨骼和关节感染,隐匿性菌血症及肺炎⁴⁸。
老年人易发生侵袭性 B 族链球菌感染的原因尚未明确。65 岁以上成人与孕产妇的 B 族链球菌定植率相近(20%~25%),血清型分布也一致⁴⁹。多数老年人存在基础疾病,提示免疫防御功能下降(尤其是中性粒细胞功能)可能是其易感性增加的原因,而活动能力下降、皮肤完整性受损及口腔卫生状况不佳也可能促进感染发生⁴⁹。
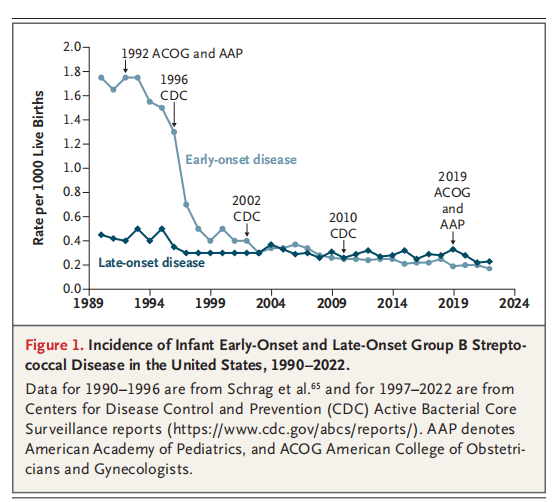
图1. 1990-2022年美国婴儿早期发病与晚期发病B组链球菌病发病率
B 族链球菌病的治疗与预防
治疗
B 族链球菌对 β- 内酰胺类抗生素几乎均敏感。2015-2017 年美国收集的 6340 株侵袭性 B 族链球菌分离株中,携带青霉素耐药相关基因的菌株不足 1%⁵⁰。与之相反,56% 的分离株携带大环内酯类和林可酰胺类抗生素耐药相关基因;2022 年的监测数据显示,52% 的分离株对克林霉素耐药,62% 对红霉素耐药 ³⁵⁰。
B 族链球菌感染的首选治疗药物为青霉素 G,氨苄西林为可接受的替代药物。新生儿菌血症的静脉抗生素疗程为 10 天,无并发症脑膜炎的疗程为 14 天 ²⁸。合并复杂中枢神经系统感染或器官特异性感染时,疗程可能延长,且可能需要外科干预。新生儿严重脓毒症可能需要机械通气、血管活性药物支持、吸入一氧化氮治疗,或联合采用上述措施;常规治疗无效的足月儿,可采用体外膜肺氧合治疗。脑膜炎婴儿需监测癫痫发作情况,并根据指征使用抗癫痫药物。
尽管经规范抗生素治疗,B 族链球菌感染仍可能复发,复发与黏膜部位的持续性定植相关;感染后的免疫应答低下也可能促进定植,在早产儿和免疫功能低下的成人中尤为明显⁵¹⁻⁵³。在标准抗生素治疗的基础上联用利福平,无法持续清除婴儿黏膜部位的 B 族链球菌定植⁵¹。临床需向成人患者及感染婴儿的家属告知,疾病复发的风险约为 1%~5%。
新生儿早发型感染的预防
目前的预防措施主要为产时抗生素预防,以降低新生儿早发型 B 族链球菌病的发病风险。孕期对定植产妇口服抗生素,或对新生儿采用青霉素预防,均无法有效清除 B 族链球菌定植及预防新生儿感染⁴⁰;而产时静脉输注氨苄西林,可降低新生儿的定植率和感染率 ³³。
产时抗生素预防的最佳应用方案曾存在争议,1992 年美国妇产科学会(ACOG)和美国儿科学会(AAP)发布的推荐意见也存在差异⁵⁴⁵⁵。1996 年,美国疾控中心、妇产科学会和儿科学会联合发布共识指南,提出两种预防方案⁴⁰:其一,根据新生儿 B 族链球菌病的临床危险因素实施产时抗生素预防;其二,根据产前直肠阴道或尿液培养结果,对定植产妇实施产时抗生素预防。后续的主动监测研究显示,基于产前培养的预防方案效果更优;2002 年、2010 年及 2019-2020 年的预防指南修订版,均一致推荐采用基于产前培养的产时抗生素预防方案 ²⁸²⁹⁴⁰⁵⁶⁵⁷。
部分医疗机构在分娩时若未知产妇的 B 族链球菌定植状态,会采用产时快速核酸扩增检测 ²⁹。表 3 为当前的产时抗生素预防指征。
在美国,产时抗生素预防使新生儿早发型感染的发病率下降了 90%(图 1)。在新生儿风险评估的多变量模型和算法中,母体的 B 族链球菌定植状态及规范的产时抗生素预防是关键考量因素 ²⁸⁵⁸。产时抗生素预防对 B 族链球菌感染的预防效果,源于三个后续效应:直肠阴道菌群中可培养的 B 族链球菌数量减少;羊水中的 β- 内酰胺类抗生素达到有效浓度;β- 内酰胺类抗生素通过胎盘进入胎儿血液循环。静脉输注氨苄西林或青霉素后,上述效应可快速出现(给药后 1~2 小时),且脐血抗生素浓度可高于抑制 B 族链球菌感染的最低抑菌浓度 ²⁸³³。
对青霉素过敏的产妇,可选用头孢唑林、克林霉素或万古霉素作为替代药物,具体选择需结合临床情况。头孢唑林对 B 族链球菌的预防效果确切,而克林霉素和万古霉素对早发型感染的预防效果相对较差 ²⁸²⁹⁵⁹⁶⁰。由于多数自述青霉素过敏的产妇,并非存在严重的 IgE 介导的超敏反应,美国妇产科学会目前推荐,孕期对青霉素过敏者进行青霉素过敏检测,以明确是否需要使用替代抗生素 ²⁹。
围产期预防策略的局限性
产时抗生素预防作为新生儿 B 族链球菌病的预防策略,仍存在诸多争议,且在全球的应用情况存在差异。在中低收入国家,产时常规静脉输注抗生素缺乏可行性;部分高收入国家(如英国)则反对基于产前筛查的全民产时抗生素预防,认为该方案成本高、弊大于利⁶¹。
产时抗生素预防无法预防晚发型感染(图 1),也不能完全预防早发型感染:目前约 40% 的早发型感染病例,发生于产前培养阴性且无产时抗生素预防指征的产妇所分娩的婴儿 ³⁹。剖宫产手术部位感染的预防、羊膜内感染的抗生素预防,以及 B 族链球菌的产时抗生素预防,三者叠加导致美国约 50% 的新生儿在出生前暴露于抗生素⁸⁹。产时抗生素预防的目的是改变母婴间传递的菌群,研究显示,婴儿肠道菌群的改变可在出生后持续数周至数月⁶²。尽管现有证据表明,婴儿肠道菌群的发育与多种慢性疾病相关,但产时 B 族链球菌抗生素预防的长期影响仍不明确。一项对 223431 名儿童的回顾性队列研究显示,暴露于产时抗生素的儿童,其生长发育存在差异,儿童期肥胖的患病率升高,且该效应可持续至出生后 10 年⁸⁶³;而另一项对 14046 名儿童的队列研究则显示,产时 B 族链球菌抗生素预防与儿童哮喘、湿疹、食物过敏或过敏性鼻炎无相关性⁶⁴。
表 3 B 族链球菌产时抗生素预防指征 *
- 本次妊娠 B 族链球菌检测阳性,符合以下任一情况†:产前直肠 / 阴道培养阳性;菌尿(无症状或合并尿路感染);产时核酸扩增检测阳性。
- 本次妊娠 B 族链球菌定植状态未知,且存在以下任一情况:产时母体发热≥38℃;胎膜早破≥18 小时;早产临产(妊娠<37 周);早产胎膜早破(妊娠<37 周);既往妊娠 B 族链球菌检测阳性‡;既往分娩婴儿患 B 族链球菌病。
- 推荐意见改编自美国妇产科学会 ²⁹。† 对于 B 族链球菌定植阳性、计划择期剖宫产且分娩时未临产、胎膜完整的产妇,无论新生儿的胎龄如何,均无需进行 B 族链球菌抗生素预防。‡ 若既往妊娠存在 B 族链球菌定植,本次妊娠的定植风险会升高,产妇与医务人员可共同决策是否实施产时抗生素预防。
其他人群的感染预防
产时抗生素预防可降低孕产妇围产期 B 族链球菌病的发病率⁶⁵,但对婴儿晚发型感染的发病率无明显影响(图 1),这可能是因为该方案仅能暂时抑制母体直肠阴道的 B 族链球菌定植 ³³。许多晚发型感染病例的母亲,均接受过规范的产时抗生素预防 ³⁵。目前尚无预防新生儿晚发型感染的有效策略,也缺乏针对非妊娠成人 B 族链球菌病的特异性预防手段。
疫苗研发
荚膜血清型特异性抗体对 B 族链球菌的保护作用,推动了预防侵袭性感染的疫苗研发。母体免疫接种是指对孕产妇进行疫苗接种,诱导其产生 IgG 抗体,该抗体可通过胎盘传递给胎儿,进而为新生儿提供保护。该策略可在新生儿出生时及出生后(小婴儿无法有效接种疫苗的阶段)为其提供感染保护。目前,母体免疫接种已被推荐用于预防婴儿百日咳、破伤风、流感、2019 冠状病毒病(新冠肺炎),以及最新推荐的呼吸道合胞病毒(RSV)感染⁶⁶⁶⁷。
贝克等人的研究显示,对孕产妇接种 Ⅲ 型多糖疫苗后,诱导产生的抗体可通过胎盘传递;其新生儿在出生后 1 月龄和 2 月龄时的血清样本,对 Ⅲ 型 B 族链球菌具有调理杀伤活性⁶⁸。但该研究及后续研究均显示,多糖疫苗的整体免疫原性较差,因此研究重点转向了糖偶联疫苗 —— 将 B 族链球菌荚膜多糖分子与破伤风类毒素、白喉类毒素等蛋白偶联。后续在健康非妊娠成人、孕产妇及老年人中开展的 Ⅰ 期研究显示,糖偶联疫苗安全性良好,且诱导产生的抗体水平显著高于单纯多糖疫苗⁶⁹。
目前,世界卫生组织、美国疾控中心、盖茨基金会、制药企业及学术机构均从不同角度支持 B 族链球菌疫苗的研发。2019-2020 年,南非开展了一项六价糖偶联疫苗的随机、安慰剂对照 Ⅱ 期临床试验⁷⁰。该疫苗包含 6 种血清型的多糖成分,可覆盖全球 98% 的婴儿 B 族链球菌病致病菌。研究共纳入 360 名孕产妇,证实了疫苗的短期安全性,并确定了诱导抗体应答的最佳剂量。疫苗诱导的抗体经胎盘传递的比值(脐血抗体浓度 / 母体血抗体浓度)为 0.4~1.1,且随疫苗剂量和血清型不同而存在差异。
该疫苗研究团队还开展了一项纳入 17752 名孕产妇的血清流行病学研究,以估算预防婴儿感染所需的荚膜多糖抗体浓度。上述两项研究均采用了国际 B 族链球菌联盟制定的标准化多重免疫检测方法,对 IgG 抗体进行定量检测。研究共同确定了可使婴儿获得 75% 感染保护的抗体水平,并证实疫苗接种可使新生儿在出生时达到该保护性抗体水平,不同血清型的婴儿达标率存在差异⁷⁰。
B 族链球菌疫苗的进一步检测、监管审批及临床应用仍面临诸多挑战。针对孕产妇的疫苗接种,临床试验需确定孕期的最佳接种时间,以最大限度保护新生儿免受早发型和晚发型 B 族链球菌感染;同时,接种时间还需兼顾目前孕期推荐接种的其他疫苗,包括破伤风 – 白喉 – 无细胞百日咳疫苗、流感疫苗、新冠疫苗和呼吸道合胞病毒疫苗⁶⁶⁶⁷。疟疾、人类免疫缺陷病毒(HIV)感染等疾病可降低疫苗的免疫原性及胎盘的抗体传递效率,这一问题也需纳入考量⁷¹⁷²。
疫苗获批上市的最紧迫问题,是确定 Ⅲ 期临床试验的终点指标⁷³。尽管全球新生儿 B 族链球菌病的疾病负担沉重,但目前的发病率较低,若以临床疗效为主要终点,疫苗临床试验预计需要 4 万至 6 万名受试者⁷³。未来可考虑以疾病保护的血清学标志物为临床试验终点,疫苗获批后再开展强制性的有效性和安全性监测⁷³。此外,还需开展更多研究,验证近期六价疫苗 Ⅱ 期临床试验中确定的保护相关性标志物,是否可作为围产期 Ⅲ 期研究的合适替代终点⁷⁴;同时也需明确非妊娠成人的保护性抗体浓度。
核心要点
- B 族链球菌为人体胃肠道和泌尿生殖道常见定植菌,主要引发新生儿、小婴儿、孕产妇及合并基础疾病的 65 岁以上老年人的感染;
- 该菌是美国新生儿侵袭性感染最常见的单一致病菌,全球范围内每年约造成 40 万例婴儿感染、5 万至 10 万例婴儿死亡;
- B 族链球菌依据表面多糖结构分为 10 种血清型,针对这些荚膜多糖的血清型特异性抗体,可预防侵袭性感染;
- 美国目前采用产时抗生素预防方案降低孕产妇和新生儿的 B 族链球菌病发病风险,但尚无策略预防婴儿晚期发病及非妊娠成人感染;
- 由荚膜多糖与蛋白抗原偶联制成的多价糖偶联 B 族链球菌疫苗正处于研发阶段,或可为所有高危人群提供预防手段。
结论
B 族链球菌是一种人体机会致病菌,主要感染新生儿、小婴儿、孕产妇及老年人,其全球疾病负担沉重。目前唯一的预防策略,是对 B 族链球菌定植或存在新生儿感染传播高风险的产妇,在产时输注抗生素。该方案虽能有效降低围产期感染发病率,但导致大量新生儿在出生前暴露于抗生素,且在中低收入国家缺乏可行性,同时无法预防婴儿晚期感染。目前尚无预防成人 B 族链球菌病的有效策略。
B 族链球菌糖偶联疫苗已完成初步研发,后续需开展 Ⅲ 期临床试验,验证疫苗在各类高危人群中的有效性和安全性。
Hits: 19
