Contents
Canadian Adverse Events Following Immunization Surveillance System (CAEFISS)
有关接种疫苗后可能出现的副作用的信息,请咨询:
加拿大免疫接种后的不良事件
加拿大卫生部(HC)和加拿大公共卫生局(PHAC)共同监督加拿大疫苗的安全性。要求市场授权持有者向HC的加拿大警戒计划(CVP)报告免疫接种后的严重不良事件(AEFIs)。
加拿大免疫接种后不良事件监测系统(CAEFISS)是一个联邦、省和地区(FPT)公共卫生疫苗上市后安全监测系统。CAEFISS由PHAC管理,其独特之处在于它包括被动(来自FPTs的自发报告)和主动监测。
关于系统
凯菲斯:
- 持续监控加拿大上市疫苗的安全性
- 确定先前确定的疫苗相关反应的频率或严重程度的增加
- 识别以前未知的不良事件(PDF)可能与疫苗有关的免疫接种(意外的AEFI)
- 确定需要进一步调查和/或研究的领域
- 为在加拿大销售的疫苗提供及时的AEFI报告信息,有助于免疫相关决策
报告免疫接种后的不良事件
下图描述了AEFI报告如何从源头(疫苗接受者)流向PHAC。CAEFISS包括自发的、增强的和主动的AEFI报告流程,这些流程将在下面进一步描述。
图AEFIs到CAEFISS的公共卫生报告途径
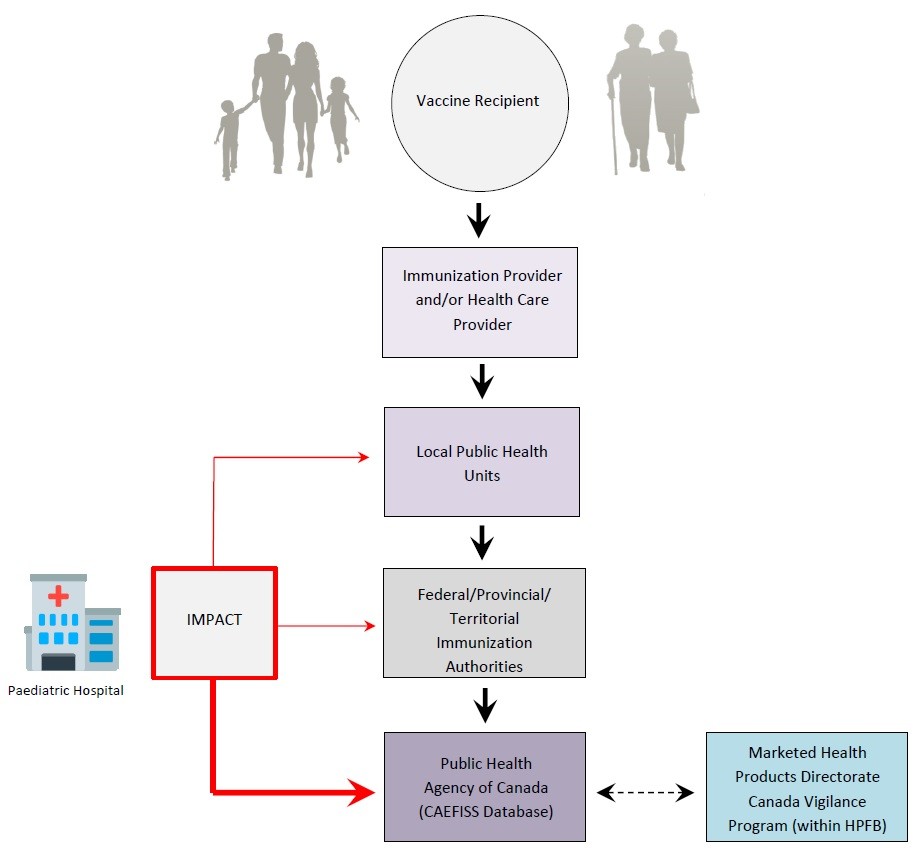
缩写:IMPACT,免疫监测方案正在实施;HPFB健康产品和食品处
文本等效-图1
提交的报告
CAEFISS报告由各省和地区的公共卫生当局提交,后者又从地方公共卫生单位接收报告。省和地区当局也从在其管辖范围内提供免疫接种的联邦当局收到报告,包括:
- 加拿大皇家骑警队
- 加拿大土著服务部
- 加拿大惩教署
这些报告中的大部分是由提供免疫接种或照顾AEFIs患者的护士、医生或药剂师生成的。国防部和加拿大武装部队收到的AEFIs直接向PHAC报告。
包括疫苗在内的所有药物的制造商都必须向营销健康产品局(MHPD)加拿大健康产品和食品部(HPFB)的加拿大警戒计划。
自1991年以来,IMPACT一直在进行积极的监测。IMPACT由PHAC通过与加拿大儿科学会的合同资助。该合同目前包括加拿大12个儿科中心,占该国所有儿科三级护理床位的90%以上。
IMPACT筛查住院患者的神经系统事件,例如:
- 发作
- 脑炎
- 血小板减少
- 接种部位脓肿/蜂窝组织炎
- 急性弛缓性麻痹(包括格林-巴利综合征和无菌性脑膜炎)
- 免疫接种后可能出现的其他并发症
任何被发现与免疫接种暂时相关但没有明确解释的都被报告为AEFI。影响报告被发送到PHAC,以输入CAEFISS,并发送到地方和省/地区卫生官员,以确保在个人层面采取适当的后续行动。
公共卫生行动
如图所示的AEFI报告流程使我们能够在流程中的每一步采取特定的措施。
AEFI管理,包括确定可能原因的适当调查,通常由报告免疫或卫生保健提供者进行。
个人公共卫生行动,如关于未来免疫接种的建议,在公共卫生单位或免疫接种提供者一级采取。
FPT卫生当局收集AEFI报告,作为正在进行的免疫规划评估的一部分。在人群层面,与AEFI报告相关的公共卫生行动可能包括免疫规划政策的变化。
PHAC在加拿大免疫接种后不良事件(CAEFI)数据库中整理AEFI报告,用于信号检测分析和报告。
如果发现潜在的信号,PHAC将与慧聪网的MHPD密切合作,讨论从CAEFISS和加拿大疫苗安全委员会提取的数据,以便采取与在加拿大上市的疫苗相关的监管措施。
因果关系评估
这因果关系评估咨询委员会是加拿大疫苗安全监测系统的一部分,也是疫苗安全监测的关键部分。ACCA审查通过国家监测收到的免疫接种后不良事件报告。委员会确定事件是否可能与特定疫苗有因果关系。ACCA使用基于世界卫生组织制定的标准化程序的流程进行因果关系评估。
因果关系评估结果
免疫接种后的新冠肺炎不良事件
我们定期更新此页面。
数据报告和出版物
年度报告
半年期报告
- 2019年1月1日至6月30日免疫接种后不良事件(AEFI)半年度报告
- 2018年7月1日至12月31日免疫接种后不良事件(AEFI)半年度报告
- 2018年1月1日至6月30日免疫接种后不良事件(AEFI)半年度报告
季度报告
2016
2015
2014
之前发布的疫苗安全性报告
对于未在线发布的报告副本,联系加拿大公共卫生局.
特定时间段内接种疫苗的AEFI摘要
- 加拿大免疫接种后不良事件监测系统(CAEFISS)的疫苗国家安全监测,2018-2019
- 加拿大免疫接种后不良事件监测系统(CAEFISS):2012年疫苗接种年度报告– CCDR:第40S-3卷,2014年12月4日
- 加拿大国家免疫报告:第5章-疫苗安全性:1992年至2004年免疫接种后不良事件的监测(已存档)
- 1998年关于免疫接种疫苗安全问题和监测的国家报告(中期)(1998年报告加上1993-1997年的趋势)。加拿大儿科学会杂志。1999年7月/8月第4卷:补编c
- 加拿大免疫报告:疫苗安全问题和监测的更新。加拿大儿科学会杂志。1998年3月/4月第3卷:补编b
- 1996年加拿大国家免疫报告:与疫苗接种暂时相关的不良事件监测。CCDR 1997年第23卷第4页(PDF,存档)
- 与疫苗暂时相关的不良事件- 1992年报告。CCDR 1995年第21-13卷:117-128页(PDF,存档)
- 与疫苗暂时相关的不良事件- 1991年报告。CCDR 1993年;19:168-78(不在线提供)
- 与疫苗暂时相关的不良事件- 1990年报告。Can Fam医师1993年;39:1907-13
关于特定疫苗的报告
- 2021-2022年接种季节性流感疫苗后加拿大疫苗安全性监测报告
- 加拿大卡介苗相关的严重不良事件。儿科传染病杂志2005;24:538-541
- 加拿大2001-2002年流感疫苗相关不良事件:被动监测结果。CCDR,2002年12月;第28-23卷:第189-196页(PDF,存档)
- 1987-2000年加拿大黄热病疫苗使用后不良事件回顾。CCDR,2002年1月;第28-2卷:第9-15页(PDF,存档)
- 影响疫苗安全出版物(PDF)
特定不良事件的报告
- mRNA新冠肺炎疫苗接种后心肌炎和/或心包炎风险:加拿大BNT162b2和mRNA-1273疫苗的头对头比较疫苗。2022年7月30日;40(32):4663-4671.
- 加拿大腺病毒载体新冠肺炎疫苗接种后血栓形成伴血小板减少综合征(TTS)。疫苗。2023年10月6日:S0264-410X(23)01159-3。
- 流感疫苗接种后的眼呼吸综合征:加拿大四个流感季节的上市后监测回顾。CCDR 2005年;第31-21卷:217-225页(PDF,存档)
- 与流感疫苗相关的眼呼吸综合征:加拿大,2000年10-11月(初步报告)。CCDR 2000年;第26-23卷:201页(PDF,存档)
相关链接
页面详细信息
- 修改日期:
Hits: 31
