LASSA END-TO-END
——一份支持公平获取未来拉沙热疫苗的区域计划
在本路线图中,公平获取指的是,无论支付能力如何,所需人群在需要时、在需要的地方都能优先获得适用的疫苗,以终止疫情暴发或遏制流行病蔓延,且这些疫苗能得到受影响国家的完全认可。
——西非卫生组织(WAHO)与流行病防范创新联盟(CEPI)
拉沙热是西非地区的重大健康问题。该疾病在该地区每年导致近4000人死亡,造成1.1亿美元的生产力损失。数十年来,拉沙热悄然夺走生命、破坏生计,并不断考验着我们卫生系统的韧性。正因如此,西非卫生组织与流行病防范创新联盟联合成立了拉沙热疫苗联盟。这是一个多方利益相关者合作伙伴关系,旨在推动和加速西非地区拉沙热疫苗的研发、准备工作及公平获取,支持各国将科学进展转化为实际的防范行动,并确保西非地区在构建拉沙热疫苗生态系统过程中发挥核心主导作用。
西非卫生组织的使命是推动拉沙热疫苗迈向获批上市,同时强化该地区疫苗研发、引进、广泛部署和使用所需的生态系统。我们的目标不仅是研发出安全、有效且高效的疫苗,更要确保疫苗能适配受影响国家的需求并便于获取。目前,在推进拉沙热疫苗研发以及强化区域能力以实现这一愿景方面,我们已取得重大进展。未来的机遇不仅在于科学领域的突破,更在于为公平获取奠定基础——确保当救命疫苗问世时,能送达该地区各国每一位有需求的人手中。
历史告诫我们,防范准备不足会付出沉重代价。这些教训促使我们坚定承诺,从疫苗研发到获取的各个环节,都要做好全面准备,并真正实现区域自主掌控。拉沙热是共同的威胁,需要各方携手制定针对性解决方案。当下做好规划,我们就能为疫苗的快速公平部署奠定基础,并为更广泛的防范工作筑牢根基。这些合作举措体现了我们的信念:公平获取并非偶然,而是通过深思熟虑的战略合作伙伴关系和前瞻性规划实现的。随着疫苗进入后期研发阶段,强有力的区域参与和稳固的合作伙伴关系依然至关重要。
我自豪地强调,西非卫生组织、各成员国、流行病防范创新联盟以及所有为这份路线图贡献力量、推动实现这一共同目标的利益相关者之间,建立了坚实的合作伙伴关系。该计划将疫苗研发、监管准入、需求、生产、交付到公平获取等全流程的防范准备工作整合到一个区域框架下,这表明西非地区已做好行动准备。我们要确保,当拉沙热疫苗准备就绪时,该地区也已做好迎接的准备。此外,对于目前寻求支持或投资拉沙热相关工作以及其他新发和再发传染病防控的合作伙伴而言,这份路线图提供了明确的切入点,能让他们的投入与这一以区域为主导、旨在实现公平获取的协调路线图保持一致。
这份路线图的首个版本仅仅是一个起点。西非卫生组织期待与更广泛的利益相关者合作,在未来几年不断完善这份路线图。
梅尔基奥尔·阿塔纳斯·若埃尔·C·艾西博士
西非卫生组织总干事
对公平获取的承诺已深深植根于流行病防范创新联盟的基因之中,是联盟愿景的核心——我们致力于打造一个流行病不再对人类构成威胁的世界。自成立以来,对公平获取的承诺就贯穿于联盟的各项工作之中。
公平获取始于为合适的疫苗产品提供资金支持,确保这些产品符合各国需求,并能服务于最需要的人群。迄今为止,流行病防范创新联盟已为五种拉沙热疫苗候选产品提供资金支持,其中两种仍在积极研发中。如今,确保这些疫苗获得批准上市至关重要,而这一阶段的工作,流行病防范创新联盟无法独自完成。
要全面实现公平获取并将疫苗送达有需要的人手中,需要国家和国际层面的各类合作伙伴形成合力,在“生态系统”内开展一系列广泛活动。作为研发资助机构,流行病防范创新联盟无法(也不应试图)独自完成这一任务。通过这份全程获取路线图,我们希望展示,通过与各国合作,我们需要将所有相关利益相关者聚集在一起,明确各自的优先事项和职责。流行病防范创新联盟的作用具有催化性——汇聚科学、政策和合作伙伴力量,推动集体进步。尽早规划这些重要的后续步骤,我们就能借助这些见解,最大限度地发挥对拉沙热防控投资的影响力。
我们与西非卫生组织的合作就体现了这一理念:区域主导、全球团结协作,共同承担防范责任。流行病防范创新联盟正通过由西非卫生组织牵头的拉沙热疫苗联盟,与各国政府和合作伙伴携手,支持西非地区开展一系列能力建设工作,涵盖临床、监管以及生产投资等多个领域。公平获取规划的起点和终点,都在于区域自主掌控,以及在研发早期与各国共同制定相关方案。我可以自豪地说,这份路线图从一开始就由西非卫生组织全权主导制定。就在几个月前,西非地区各国的部长们齐聚一堂,承诺将加速该地区拉沙热疫苗的研发和未来公平推广工作。
我们即将推出的“流行病防范创新联盟3.0战略”,重点是建设并展示支撑“100天任务”的各项能力,即在发现新威胁后的100天内,研发并交付安全、有效且可获取的疫苗。本路线图所阐述的工作,是该体系防范准备工作的关键组成部分,确保针对流行病威胁的疫苗能在西非地区得到公平研发、生产和交付。
我们希望这份初步路线图能成为一个蓝图,展示区域主导与全球合作如何共同实现公平获取,并为长期流行病防范奠定基础。在财政资源有限的大环境下,我们希望这份路线图能帮助所有利益相关者明确关键优先事项和存在的差距,避免工作重复,并在疫苗价值链中明确各方合作伙伴之间的关键衔接机制。随着拉沙热疫苗进入后期研发阶段,我们希望这份路线图能让大家看到,西非地区正为迎接拉沙热疫苗以及应对其他新发和再发传染病做好准备。同时,正如路线图所指出的,目前仍存在诸多差距。我们呼吁合作伙伴重新思考合作方式,投资并支持区域防范能力建设,最终实现公平获取。
理查德·哈切特博士
流行病防范创新联盟首席执行官
本路线图的制定基于案头研究以及与以下机构和利益相关者的多次咨询:
- 尼日利亚、塞拉利昂和利比里亚三国由部长级会议召集成立的拉沙热疫苗工作组
- 2025年在尼日利亚举办的一场详细研讨会,由尼日利亚疾病控制中心(NCDC)和国家食品药品监督管理局(NAFDAC)联合主办,来自尼日利亚的30多名专家参与,其中包括来自国家初级卫生保健发展局(NPHCDA)、国家健康保险局(NHIA)、总统解锁医疗保健价值链倡议(PVAC)、尼日利亚私营部门卫生联盟(PSHAN)、国家医学研究所(NIMR)的专家,以及诸如新型艾滋病疫苗和杀微生物剂倡导协会(NHVMAS)、妇女疫苗获取倡导组织(WAVA)等民间社会组织的代表
- 其他国家级组织,如尼日利亚药学会(PCN)以及多位专家,包括普雷cious·恩维科、阿尔法萨内·图雷博士(世界卫生组织几内亚办事处)、穆巴拉克·祖拜鲁博士(联合国儿童基金会尼日利亚办事处)、索里·孔德博士——国家卫生安全局(ANSS)总干事、蒂埃诺·哈米杜·巴尔德——几内亚科纳克里“非洲零贫困”组织执行主任、阿卜杜拉耶·图雷教授——国家公共卫生研究所总干事、塞库·西达特·西拉博士——达拉巴地区卫生局长、伊德里萨·迪亚洛博士——恩泽雷科雷地区区长兼地区卫生局长,以及布里特尼·M·瓦尔皮拉——利比里亚“最后一英里健康”组织国家主任
- 由西非卫生组织牵头的拉沙热政策研究议程区域技术工作组(由MMGH咨询公司协助开展),以及2025年拉沙热需求预测(由国际艾滋病疫苗倡议组织协助开展)
- 由拉沙热疫苗联盟秘书处合作伙伴(尼日利亚科罗纳管理系统公司、尼日利亚卫生观察组织和布鲁姆公共卫生组织)协助开展的咨询活动
- 2024年在加纳举办的拉沙热疫苗用例研讨会(由MMGH咨询公司协助开展)
- 与拉沙热疫苗研发商和生产商的讨论,包括国际艾滋病疫苗倡议组织(IAVI)、牛津大学(U.Oxford)和达喀尔巴斯德研究所(IPD)
- 区域和全球性组织,包括世界卫生组织非洲区域办事处(WHO AFRO)、免疫接种、疫苗和生物制品部门(IVB)、病毒性出血热部门(VHF)、非洲疫苗监管论坛(AVAREF)、全球疫苗免疫联盟(Gavi,市场塑造与疫苗投资战略团队)、非洲疾病控制与预防中心(Africa CDC)以及比尔及梅琳达·盖茨基金会(Gates Foundation)
本路线图由流行病防范创新联盟(沙尔瓦尼·萨拉夫、吉尔·梅森、艾玛·惠特利、卡特琳·拉姆绍尔博士和奥耶龙克·奥耶班吉)和西非卫生组织(维尔吉尔·夸西·洛科索博士和艾沙特·布科拉·乌斯曼博士)协调制定。
| 缩略语 | 英文全称 | 中文释义 |
| AFRO | WHO African Region | 世界卫生组织非洲区域办事处 |
| AVAREF | African Vaccine Regulatory Forum | 非洲疫苗监管论坛 |
| AMA | African Medicines Agency | 非洲药品管理局 |
| AVMA | African Vaccine Manufacturing Accelerator | 非洲疫苗生产加速器 |
| CEPI | Coalition for Epidemic Preparedness Innovation | 流行病防范创新联盟 |
| COGS | Cost of Goods Sold | 销售成本 |
| E2E ACCESS | End-to-End Access | 全程获取 |
| EA | Equitable Access | 公平获取 |
| EUL | WHO Emergency Use Listing | 世界卫生组织紧急使用清单 |
| EUA | Emergency Use Authorization | 紧急使用授权 |
| EAP | Expanded Access Program | 扩大使用项目 |
| ECOWAS | Economic Community of West African States | 西非国家经济共同体 |
| IPD | Institut Pasteur de Dakar | 达喀尔巴斯德研究所 |
| IAVI | International AIDS Vaccine Initiative | 国际艾滋病疫苗倡议组织 |
| LF VACCINES | Lassa Fever Vaccines | 拉沙热疫苗 |
| MAH | Marketing Authorization Holder | 上市许可持有人 |
| MCM | Medical Counter Measures | 医疗对策 |
| NCDC | Nigeria Centre for Disease Control and Prevention | 尼日利亚疾病控制与预防中心 |
| NAFDAC | National Agency for Food and Drug Administration and Control | (尼日利亚)国家食品药品监督管理局 |
| NITAG | WHO National Immunization Technical Advisory Group | 世界卫生组织国家免疫技术咨询小组 |
| NPHA | National Public Health Agencies | 国家公共卫生机构 |
| R&D | Research & Development | 研究与开发 |
| RITAG | WHO Regional Immunisation Technical Advisory Group | 世界卫生组织区域免疫技术咨询小组 |
| SAGE | The WHO Strategic Advisory Group of Experts on Immunization | 世界卫生组织免疫战略咨询专家组 |
| TPP | Target Product Profile | 目标产品特性 |
| 100 DM | 100 Days Mission | 100天任务 |
| U.Oxford | University of Oxford | 牛津大学 |
| VIS | Gavi Vaccine Investment Strategy | 全球疫苗免疫联盟疫苗投资战略 |
| WAHO | West African Health Organization | 西非卫生组织 |
| WHO | World Health Organization | 世界卫生组织 |
拉沙热全程(E2E)获取路线图勾勒出一条协同路径,以确保公平获取已获批的拉沙热疫苗。该路线图明确了实现最终减轻拉沙热负担所需开展的工作、实施主体及相关要求。
- 短期目标:明确公平获取的关键需求,提高整个生态系统的透明度,以便疫苗价值链上的各利益相关者能高效协同,填补这些空白。
- 中期目标:呼吁各国政府、行业、融资机构和捐赠方行动起来,在未来2-3年内为拉沙热疫苗公平获取所需的关键领域投入资源。
- 长期目标:促进全球卫生生态系统中各合作伙伴之间的顺畅衔接,减少获取差距,支持各国引进拉沙热疫苗。
为实现这一愿景,全程获取路线图将通过以下方式发挥作用:
- 明确为实现拉沙热疫苗(安全有效)的公平获取,拉沙热流行国家尤其需要开展哪些工作、在何时开展以及由谁来开展;
- 借鉴类似疫苗在应急响应中的应用经验,强化防范准备和交付工作;
- 确保(由流行病防范创新联盟或其他资助方提供的)研发投资从一开始就考虑下游的获取需求,从而使疫苗产品最终能满足目标国家的需求;
- 尽早让利益相关者参与进来,明确其在疫苗价值链中的角色和职责,推动合作伙伴之间的顺畅衔接,并规划协同主动的支持措施。
该路线图考虑了拉沙热疫苗全程获取路径中的公平获取需求,将早期研发到政策制定、生产、采购、交付及持续使用等各个环节的需求有机衔接起来。

图1:疫苗全程获取路径示意图
早期区域参与是实现最终公平获取成果的关键。为支持这一目标,流行病防范创新联盟与西非卫生组织联合制定了本路线图,并在疫苗获批上市前数年就启动了这一进程,以确保西非地区各国的观点能与全球范围内关注拉沙热的利益相关者的意见一同被纳入考量。该路线图具有动态性和迭代性,将根据不断变化的背景和假设,持续吸纳各类利益相关者的最新意见进行完善。
目前有多种拉沙热疫苗候选产品正在研发中。本路线图不局限于某一种拉沙热疫苗候选产品,而是以疾病为核心构建框架,并与最先进候选疫苗的研发时间表保持一致。
要实现拉沙热疫苗的公平获取,需回答三个关键问题:
- 谁将为疫苗后期临床试验和研发支持活动提供资金,将为多少种候选疫苗提供资金?
- 谁将负责疫苗的生产和商业化,以确保流行国家能够获取疫苗?
- 谁将为西非地区大规模部署疫苗提供资金和采购支持?
尽管在当前研发阶段,这些问题尚未完全得到解答,但目前正在开展的工作聚焦于确定相关利益相关者、支持其决策需求,并制定符合各国需求的拉沙热疫苗公平获取指导原则。以下是实现拉沙热疫苗公平获取的关键需求:
- 为疫苗后期研发和支持活动获取资金至关重要,这是确保受影响人群能够获得已获批拉沙热疫苗的前提。
- 疫苗设计必须符合西非地区目标人群的偏好(如路线图中所确定的);研发商应探索改进产品特性,各国应尽早开展社会行为研究和社区参与研究,为提高疫苗接受度奠定基础。
- 拉沙热在西非地区流行,各利益相关者强调,在该地区本土生产疫苗对于提高公平获取程度、强化供应链、建设本地能力以及维护全球卫生安全具有重要意义。要实现可负担且可持续的区域生产,还需进一步分析确定所需的激励措施、投资和合作伙伴关系。
- 拉沙热疫苗相关的政策和融资决策若要及时制定,就需要立即开展证据生成工作,例如在不同使用场景下评估疾病负担和疫苗的卫生经济影响,并以路线图中详细列出的一系列区域优先需求为指导。
- 目前拉沙热疫苗的融资渠道尚不明确,可能需要公共和私人资助方通过创新融资机制提供支持。需要尽早发出采购信号,使获取路径具有可预测性,从而制定合理计划,确保疫苗的可负担性和长期可持续供应。
- 拉沙热疫苗的长期可持续供应依赖于强有力的区域自主掌控和本地需求、全球与区域合作以及各国能力的提升。所有相关举措都应优先考虑这些核心要素。
- 早期社会参与和社区防范准备对于实现公平获取至关重要。各国强调,需要建立对疫苗的信任、应对错误信息,并借鉴其他疫苗引进过程中的经验教训。
为确保本路线图产生实际影响,我们诚挚邀请资助方、捐赠方、疫苗研发商、政策制定者、各国政府、区域机构、研究人员、执行合作伙伴和全球卫生行动方采取以下行动:
- 倡导并(或)投资于拉沙热疫苗已明确的关键缺口领域,尤其是以下方面:
a. 疫苗获批所需的后期临床试验和生产规模扩大
b. 为政策和融资决策提供支持的证据生成
c. 已获批拉沙热疫苗的剂量供应
d. 各国的社会行为研究、社区参与及沟通方法
e. 实现公平部署所需的国家准备和执行工作
- 确保在产品早期研发阶段就纳入各国对疫苗公平获取的需求
- 为路线图的下一次更新提供意见建议,支持路线图的持续完善和进展监测
- 将拉沙热及公平获取需求纳入国家获取计划,明确国内相关利益相关者的职责,承诺国内资金投入,动员社区参与,并监测进展情况
预计路线图中的高层见解将被转化为针对具体研发商的商业化和获取计划,以及各国的实施和获取计划,其中包括主要风险及风险缓解机制。路线图中确定的战略目标有望通过区域防范准备和获取仪表板,转化为各国可衡量的关键绩效指标(KPI),以便对进展情况进行监测。
预计将由西非卫生组织和流行病防范创新联盟牵头,组建一个拉沙热疫苗区域获取指导小组。该小组将吸纳来自拉沙热流行国家的关键获取专家、研发商、生产商及商业化合作伙伴,以及重要的区域和全球性组织的代表,包括政策制定者、潜在的拉沙热疫苗资助方、采购方和执行方。该小组的宗旨是共同解决路线图中确定的战略性公平获取需求,制定优先事项和时间表,并为填补缺口确定所需资金和资源。已针对具体活动组建了详细的技术工作组,并将在拉沙热联盟框架下继续开展工作。流行病防范创新联盟和西非卫生组织将共同负责监测各项活动的进展,并更新路线图。
拉沙热是西非地区的重大公共卫生问题,会引发季节性疫情。据估计,西非地区每年有数十万人受到拉沙热影响,该疾病每年在该地区导致近4000人死亡,造成1.1亿美元的生产力损失[2]。拉沙热症状多样,从轻微头痛到呕吐、面部肿胀,再到可能致命的全身性出血等都有可能出现。在康复患者中,听力损失的情况十分常见。建模研究[3]预测,受气候变化和人口增长影响,到2070年,可能有多达7亿人面临拉沙热感染风险,这意味着该疾病的潜在影响还将进一步加剧。各国的相关见解表明,在拉沙热季节性高发期间,医护人员往往会受到感染,因此拉沙热对常规医疗服务的提供产生了严重影响。由于监测和诊断能力存在不足,该疾病的实际负担可能被低估。目前,流行病防范创新联盟正在资助开展有史以来规模最大的拉沙热研究,以评估拉沙热的疾病负担;同时,还需要开展更多流行病学研究,以更好地了解该疾病的影响。
流行病防范创新联盟是拉沙热疫苗研发的最大资助方。迄今为止,该联盟已对五种疫苗候选产品进行了投资,其中两种仍在积极研发中[4]。国际艾滋病疫苗倡议组织(IAVI)研发的重组水疱性口炎病毒载体疫苗(rVSV)是目前最先进的候选疫苗,已进入2a期临床试验阶段。2024年4月,国际艾滋病疫苗倡议组织在尼日利亚启动了首个拉沙热疫苗II期临床试验,随后在加纳和利比里亚也开展了该试验[5]。牛津大学研发的ChAdOx候选疫苗目前正在英国进行1a期研究,预计将于2026年在加纳启动第二项1期研究[6]。此外,流行病防范创新联盟还在测试由SK生物科学公司研发的快速信使核糖核酸(mRNA)疫苗候选产品,该产品可用于预防拉沙热和X疾病。若研发成功,该疫苗可快速调整,以应对其他沙粒病毒属病毒。
图2:拉沙热疫苗组合——流行病防范创新联盟资助与非资助项目;来源:流行病防范创新联盟官网
| 研发阶段 | 临床前 | 1期 | 2期 | 注册 |
| 病毒载体 | 托马斯·杰斐逊大学、巴斯德研究所 | 牛津大学 | 国际艾滋病疫苗倡议组织 | – |
| mRNA | SK生物科学公司 | – | – | – |
| – | LASSARAB、MOPEVAC | LassaJ ChAdOx1 | rVSVΔG-LASV-GPC | – |
在这些候选疫苗中,有1-2种将在未来两年内在西非地区启动临床试验。
除了在疫情暴发情况下提供拉沙热疫苗的重要性之外,越来越多的数据支持在西非流行地区采取预防性接种策略。其中,世界卫生组织2022年发布的《目标产品特性》(TPP)[7]将预防性疫苗的使用列为优先事项;2024年流行病防范创新联盟在加纳举办的用例研讨会[8]也强调,各方希望在西非流行地区实施常规预防性接种;此外,多项建模研究也证实了预防性策略的初步价值。尽管还需要更多证据来支持有关这些疫苗使用场景的政策建议,但鉴于目前各方共识日益增强,本计划将重点关注流行情况下(预防性使用)的公平获取,同时兼顾流行病(应急性)使用场景下的疫苗获取。
针对各国拉沙热疫苗需求开展的初步预测显示,在多种情景下,每年的需求峰值在50万剂至1100万剂之间。这一预测既包括预防性需求(常规免疫接种和计划性活动),也包括应急疫情响应所需的储备需求。目前,各国、区域和全球专家正致力于完善这一预测,以确定主要情景,并将于2026年初发布最终结果。
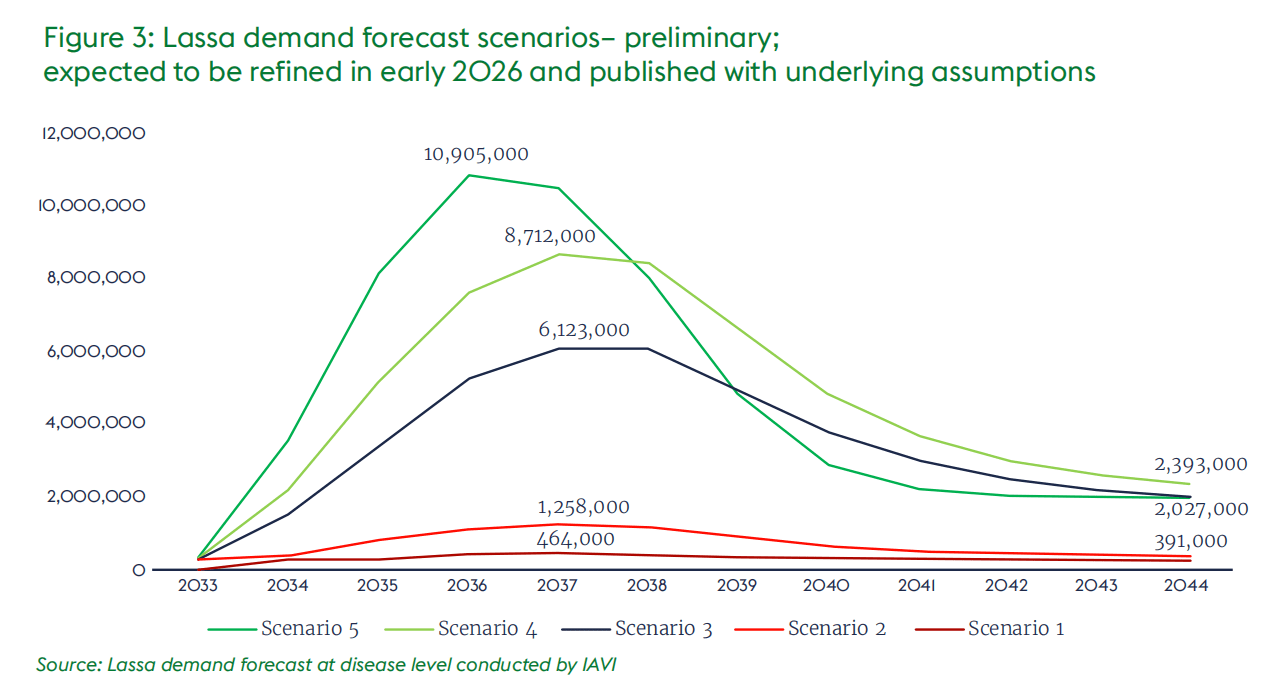 图3:拉沙热需求预测情景——初步结果;预计将于2026年初完善并发布,同时公布相关假设条件
图3:拉沙热需求预测情景——初步结果;预计将于2026年初完善并发布,同时公布相关假设条件
(图中纵轴为疫苗剂量,单位:剂;横轴为年份,从2033年到2044年;五条折线分别代表五种情景下的疫苗需求预测,具体数据如下:)
- 情景5(最雄心勃勃):2033年约125.8万剂,2034年约202.7万剂,2035年约39.1万剂,2036年约46.4万剂,2037年起需求大幅上升,2044年达到约1090.5万剂
- 情景4:需求整体呈上升趋势,2044年约871.2万剂
- 情景3:需求逐步增长,2044年约612.3万剂
- 情景2:2033-2036年需求较低,2037年后缓慢上升,2044年约239.3万剂
- 情景1(最保守):需求长期维持在较低水平,2044年仍不足50万剂
来源:国际艾滋病疫苗倡议组织开展的拉沙热疾病层面需求预测
这些情景的差异源于对地理目标范围(例如,情景1和情景2为针对性推广,情景3-5为全国推广)、接种率和目标人群(例如,情景1和情景2不将成人列为目标人群)等方面的假设,从保守到雄心勃勃不等。一旦根据各国意见最终确定相关假设,将于2026年初公布详细的假设清单。
拉沙热疫苗联盟是一个多方利益相关者合作伙伴关系,旨在推动和加速西非地区拉沙热疫苗的研发、防范准备和公平获取。该联盟由西非卫生组织(WAHO)召集,流行病防范创新联盟(CEPI)提供支持,汇聚了各国政府、区域机构、疫苗研发商、监管机构、学术界、执行合作伙伴和资助方,共同加强政治承诺、技术协调,并为拉沙热疫苗的研发和交付筹集资金。
拉沙热联盟作为一个平台,致力于协调区域优先事项与全球行动,衔接临床研究、伦理与监管强化、生产和政策防范准备等工作,同时将面临风险和受影响的社区置于工作核心,以确保工作成效。该联盟支持各国将科学进展转化为实际的防范准备行动,并确保西非地区在构建拉沙热疫苗生态系统过程中发挥核心主导作用。
尽管本路线图的许多内容旨在保障流行国家(尼日利亚、利比里亚、塞拉利昂、几内亚)公平获取拉沙热疫苗,但也已就其他高风险国家(如贝宁、布基纳法索、科特迪瓦、多哥、加纳、塞内加尔和马里南部)的需求展开探索,包括疫苗剂量需求、目标人群以及基于储备的应急策略等方面。随着气候变化带来的威胁不断加剧、人道主义危机频发以及疾病传播风险上升,拉沙热有可能蔓延至非洲中部、东部或其他地区[10]。本计划从宏观层面考虑了应对此类情况所需的干预措施,以实现快速公平的应对,例如监测和早期检测、快速监管和政策通道、应急生产能力投资,以及在研发商特定条款中为低收入和中等收入国家(LMIC)获取疫苗剂量提供便利等。
虽然拉沙热是一种已知疾病,但世界面临的威胁不断增加,一种与拉沙热相关的新病毒有可能出现并传染给人类(即“拉沙X”病毒)。在这种情况下,我们无法预知病毒的暴发地点、拉沙热疫苗候选产品是否对其他沙粒病毒属病毒有效,也无法确定哪些平台能够实现快速监管审批等。世界卫生组织研发蓝图团队已召集了一个涵盖所有病毒科的协作开放研究联盟(CORC),为此类情况制定公平的研发方法[11]。而针对“拉沙X”病毒的公平获取策略,预计将在流行病防范创新联盟的X疾病战略中明确,不在本文件讨论范围内。不过,上文提到的部分方法(如监测和早期检测、应急能力等)可为“拉沙X”病毒情景下的公平获取提供支持。
本路线图主要聚焦于疫苗获取需求,但要真正实现公平获取,还需要采取多管齐下的公共卫生应对措施,并投资于其他医疗对策,包括诊断和治疗方法。目前尚无专门用于治疗拉沙热的获批治疗方法。西非地区应对埃博拉和猴痘的实际经验表明,疫苗的公平获取在很大程度上依赖于体系防范准备——例如,确诊延迟以及诊断能力有限(尤其是在农村流行地区),会制约疫情的及时应对。此外,复杂的地形、部分地区的安全问题以及冷藏储存设施不足等物流挑战,也需要制定差异化的交付策略。各国拉沙热获取计划中,预计将纳入这些超出疫苗范畴的考量因素和需求。
拉沙热全程获取路线图围绕疫苗公平获取的10个关键组成部分展开,这些组成部分可分为以下三个层面:
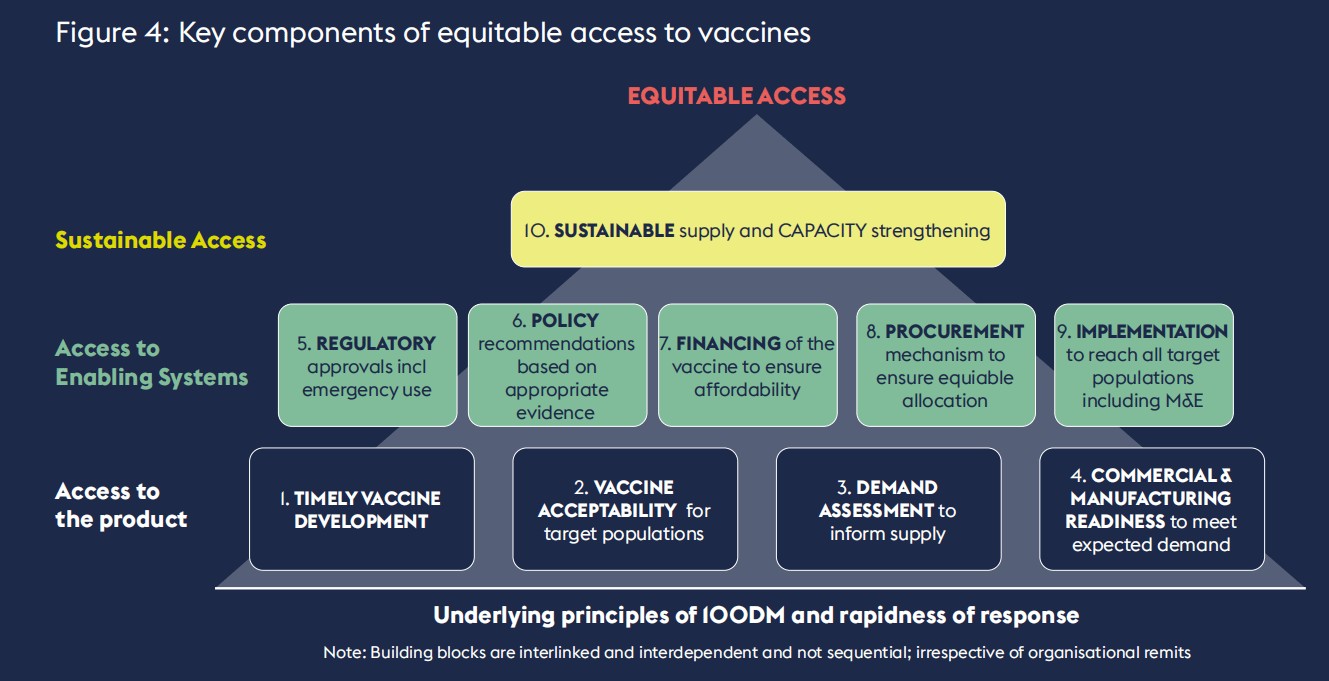 图4:疫苗公平获取的关键组成部分
图4:疫苗公平获取的关键组成部分
- 可持续获取
10. 可持续供应与能力建设
- 获取支持体系
5. 监管审批(包括紧急使用)
6. 基于适当证据的政策建议
7. 疫苗融资(确保可负担性)
8. 采购机制(确保公平分配)
9. 实施(覆盖所有目标人群,包括监测与评价)
- 产品获取
- 疫苗及时研发
- 目标人群对疫苗的可接受性
- 需求评估(为供应提供依据)
- 商业化与生产准备(满足预期需求)
注:“100天任务”的基本原则与快速响应要求
这些组成部分相互关联、相互依存,并非按先后顺序排列,且不受组织职责范围的限制。
为明确实现公平获取所需的干预措施,上述组成部分被归类为五个关键目标:
A. 疫苗的及时供应(1)与可接受性(2),确保合适疫苗的及时研发
B. 疫苗需求(3)、生产与供应(4),确保疫苗供应满足预期需求
C. 监管(5)与政策(6)需求,保障目标人群及时获取疫苗
D. 融资(7)与采购(8),确保目标人群可负担疫苗并实现公平分配
E. 可持续实施与能力建设(9和10),确保疫苗供应的持续可靠性
在每个部分中,我们都对实现公平获取的关键目标以及短期至长期内实现这些目标所需的干预措施进行了评估。
在已知情况下,文中注明了相关资金来源和牵头组织。对于流行病防范创新联盟(CEPI)而言,所列资金涵盖了其对国际艾滋病疫苗倡议组织(IAVI)和牛津大学(U.Oxford)拉沙热疫苗候选产品的资助,具体以内部治理和项目审查结果为准。对于其他合作伙伴,相关资金和资源承诺尚在落实中。图3展示了预期的大致时间表。
若没有疫苗产品,就无从谈及拉沙热疫苗的获取。已获批的拉沙热疫苗(包括紧急使用授权和全面授权)问世越早,就能越早遏制初发疫情。根据目前的项目时间预测,最乐观的预期是在2030年后提交疫苗注册申请,目前各方正探索加快进度的可能性。推动拉沙热疫苗候选产品进入后期研发阶段已成为当务之急,除流行病防范创新联盟的投资外,还需要额外资金支持和协同投资。西非地区各国对此项工作展现出了强烈的政治承诺[12]。同时,建立研究用应急储备库可作为阶段性获取里程碑,因为在疫情期间将研究用剂量用于临床试验,有助于为疫苗获批(或注册)积累证据。
在疫苗研发过程中,还需确保社区对疫苗的接受度。目前两种最先进的候选疫苗有望满足世界卫生组织(WHO)拉沙热疫苗目标产品特性(TPP)的最低标准[13],而各国初步咨询结果也为了解疫苗可接受性相关考量因素提供了参考。
各国反馈显示,国际艾滋病疫苗倡议组织研发的重组水疱性口炎病毒载体疫苗(rVSV)对超低温冷链的要求存在重大获取挑战。若不采取缓解措施,这一要求可能会影响疫苗接种率,并导致疫苗浪费率上升。目前,国际艾滋病疫苗倡议组织正努力提高该疫苗的热稳定性,包括探索在2-8°C条件下疫苗能否稳定保存1个月(这将有助于疫苗部署),同时还在采取其他措施提升热稳定性。冻干制剂或许能提高疫苗的热稳定性并延长保质期,但(若可行,相较于稳定的液体制剂而言)并非理想选择,因为在储存和交付过程中复溶疫苗存在物流挑战,且可能引发安全问题[14]。不过,医护人员已有使用其他冻干制剂疫苗的经验。牛津大学研发的ChAdOx候选疫苗无需超低温冷链运输,目前采用两剂接种方案。各国咨询指出,两剂接种方案存在问题,因其不太适合快速疫情应对,且首剂接种后,后续接种覆盖率可能会下降。为解决这一问题,牛津大学正在加纳评估该疫苗的单剂和两剂接种方案——这与其他基于ChAdOx平台的疫苗研究数据一致,即单剂接种可产生较强的免疫原性,而第二剂接种可进一步增强免疫效果。
在产品研发过程中,需要在速度、成本和可接受性之间进行多方面权衡。这些权衡需尽早明确,并经各国利益相关者验证。此外,理想情况下,应将社会行为研究和社区参与工作纳入疫苗研发过程,以了解并改善社区对潜在拉沙热疫苗的看法,从而使疫苗在推出后能更容易被社区接受。
- 关键获取成果:尽早实现拉沙热疫苗注册上市
- 阶段性获取成果:探索为高风险人群在疫情期间获取疫苗提供紧急使用授权(EUA)的条件,并建立研究用应急储备库,用于疫情期间的临床试验(或各国确定的其他场景)
| 干预措施 | 牵头方(L)与资助方(F) |
| 1. 获取各国监测数据和热点地区建模结果,为临床试验设计提供更好依据,并确定高风险人群和地区(2026年) | L:西非卫生组织(WAHO)、国家公共卫生机构(NPHA)、卫生部(MoH)、研发商<br>F:无特定标注 |
| 2. 探索加快整个疫苗组合注册时间表的途径(2026-2027年)——持续进行 | L:研发商、国家监管机构(NRAs)<br>F:流行病防范创新联盟(CEPI) |
| 3. 通过嵌入区域的投资案例,确定疫苗后期临床研发资金(2025-2026年)——持续进行 | L:西非卫生组织(WAHO)、流行病防范创新联盟(CEPI)、国际艾滋病疫苗倡议组织(IAVI)<br>F:无特定标注 |
| 4. 为后期研发提供资金并启动相关工作(国际艾滋病疫苗倡议组织计划于2026年前完成2b期准备工作) | L:研发商<br>F:待定(TBD) |
| 5. 准备好可用于疫情期间临床试验的研究用剂量,包括临床试验方案,并明确各利益相关者的职责(2027年) | L:研发商、国家监管机构(NRAs)、卫生部(MoH)<br>F:流行病防范创新联盟(CEPI)、世界卫生组织(WHO)沙粒病毒属协作开放研究联盟(CORC) |
| 6. 开展稳定性研究,探索提高热稳定性的方法,使疫苗可在2-8°C条件下储存;研究疫苗剂型的权衡因素(时间表待定) | L:研发商、商业化合作伙伴<br>F:流行病防范创新联盟(CEPI) |
| 7. 在临床试验中设置单剂接种组,对比分析单剂与两剂接种方案的有效性和免疫原性(2026年) | L:相关研发商<br>F:流行病防范创新联盟(CEPI) |
| 8. 开展社会行为研究和社区参与工作,尽早评估并提高疫苗可接受性——多项研究正在进行中并计划开展更多研究 | L:西非卫生组织(WAHO)、各国、研发商、拉沙热研究机构<br>F:待定(TBD) |
*注:每个部分中标记的内容为关键活动。蓝色框标注的活动目前已获得资金支持或已规划,具体以内部治理和项目审查结果为准。*时间表为大致参考,取决于各组织的资源情况和优先事项安排。
考虑到西非地区拉沙热的流行和流行特性,以及该疾病的季节性,拉沙热疫苗的需求预计具有可预测性,其中尼日利亚的需求预计将占大部分。由西非卫生组织牵头、关键技术专家参与的需求预测工作正在进行中,预计将于2026年初发布结果,初步估计如图2所示。随着资金、政策和供应相关假设逐渐明确,需对需求情景进行更新。明确需求预测对于深入了解拉沙热疫苗的预期定价、识别可负担性风险以及确定合适的市场塑造机制(包括所需的预先采购承诺)至关重要。
拉沙热疫苗需求的实现在很大程度上取决于疾病负担相关证据、公众对疫苗的信任度、对疾病风险的认知以及社区对新卫生干预措施的接受意愿。因此,需要通过其他部分中确定的干预措施(如证据生成、社区参与和沟通策略),与当地民众、医护人员和意见领袖共同创造需求。将定量需求预测与社会参与方法相结合,有助于确保预测更加准确,并为供应规划提供可靠依据。
在供应方面,各方更倾向于采用在非洲进行技术转让的生产策略,因为拉沙热疫苗作为一种区域性疫苗,理想情况下应能在区域内便捷获取。随着疫苗研发不断推进,制定商业化战略并确定上市许可持有人(MAH)将变得至关重要。目前,国际艾滋病疫苗倡议组织(IAVI)和牛津大学(U.Oxford)都在探索此类商业合作伙伴关系和技术转让事宜;国际艾滋病疫苗倡议组织已与达喀尔巴斯德研究所(IPD)签署协议,建立合作关系,重点关注重组水疱性口炎病毒(rVSV)平台[15]。尼日利亚的利益相关者表示,未来希望在尼日利亚本土生产疫苗,但还需进一步探索实现这一目标的可行性及所需激励措施,以确保生产的可持续性。
- 基于区域意见,尽早明确拉沙热疫苗的需求(无限制需求和有限制需求),为供应需求提供依据
- 拉沙热疫苗最好在非洲区域内生产
- 尽早确定上市许可持有人(MAH)并做好商业化准备
| 干预措施 | 牵头方(L)与资助方(F) |
| 1. 举办由区域主导的拉沙热疫苗用例研讨会并开展需求预测,以了解初步需求(2026年——持续进行);根据新假设,定期更新有限制需求情景(2027年及以后) | L:西非卫生组织(WAHO)、国际艾滋病疫苗倡议组织(IAVI)<br>F:流行病防范创新联盟(CEPI);需求更新(待定) |
| 2. 开展建模工作,为需求和用例提供支持(2025年——已完成[16]);根据需要定期更新 | L:牛津大学(U.Oxford)、伦敦大学学院(UCL);(更新工作待定)<br>F:流行病防范创新联盟(CEPI) |
| 3. 制定商业化战略,并确定拉沙热疫苗的上市许可持有人(MAH)(取决于具体产品——持续进行) | L:研发商、商业化合作伙伴<br>F:流行病防范创新联盟(CEPI)、国际艾滋病疫苗倡议组织(IAVI)/VaxSen及其他候选疫苗(待定) |
| 4. 向非洲生产商进行技术转让(取决于具体产品——最好在2030年前完成) | L:国际艾滋病疫苗倡议组织(IAVI)/达喀尔巴斯德研究所(IPD);其他候选疫苗的研发商和商业化合作伙伴<br>F:待定(TBD) |
| 5. 完成后期化学、制造和控制(CMC)工作,扩大生产规模并提升产能,以满足拉沙热疫苗需求,包括应对西非以外地区意外需求的应急产能(取决于具体产品——最好在2030年前完成) | L:生产合作伙伴<br>F:待定(TBD) |
| 6. 考虑将拉沙热疫苗纳入非洲疫苗生产加速器(AVMA)优先清单(仅当拉沙热疫苗获得全球疫苗免疫联盟疫苗投资战略(VIS)批准时);时间表待定 | L:生产合作伙伴<br>F:全球疫苗免疫联盟(Gavi) |
为支持监管流程,流行病防范创新联盟(CEPI)正在协调西非地区的监管强化工作——例如,西非国家经济共同体监管协调支持项目(ECOWAS RegECs Project)[17]。该项目是监管机构、伦理委员会与非洲疫苗监管论坛(AVAREF)之间的合作项目,通过让国家监管机构(NRAs)和伦理委员会(ECs)参与拉沙热疫苗评估工作,帮助它们为紧急使用批准做好准备,并简化常规注册流程。基于高风险国家的风险效益评估,还需进一步明确监管需求和条件,尤其是紧急或特殊获取相关的需求和条件。咨询结果显示,一旦获得临床数据,可通过多种机制实现快速监管审批,例如年度监管模拟演练(即“监管演习”)以及在流行国家间协调统一监管时间表。
关于拉沙热疫苗使用的政策建议,需基于疫苗获批后获得的证据制定。与此同时,需要及时生成恰当的证据,为相关决策提供支持。从基孔肯雅热等区域性疾病的经验来看,即便疫苗已可投入使用,若缺乏特定背景下与政策相关的研究,关键决策仍会延迟。为推动证据生成,流行病防范创新联盟和西非卫生组织(WAHO)于2025年制定了《政策研究议程》[18],该议程在四个类别下列出了13项关键研究优先事项,分别是:a)流行病学问题、b)疫苗临床试验、c)成本效益分析以及d)疫苗实施与接种率。目前需要在这些优先领域投入资源开展证据研究,以避免出现代价高昂的延误,并确保疫苗的公平推广。
如其他部分所述,监管和政策防范准备工作必须辅以清晰、透明且符合文化背景的沟通,以维护公众信任。西非地区以往应对流行病的经验表明,当监管决策公开透明,且当地专家和受信任人士参与对话时,社区更有可能接受新疫苗。此外,疾病的跨境传播特性也要求西非国家经济共同体(ECOWAS)各国协调统一政策,协同开展疫苗部署工作。
- 世界卫生组织(WHO)预认证(PQ)、非洲药品管理局(AMA)和非洲国家监管机构(NRAs)能够及时为疫苗的许可使用(以及适用情况下的紧急使用)提供审批
- 生成充足证据,确保区域免疫技术咨询小组(RITAGs)、国家免疫技术咨询小组(NITAGs)和免疫战略咨询专家组(SAGE)能够就拉沙热疫苗的使用(包括在证据支持情况下的预防性使用)提出恰当建议
| 干预措施 | 牵头方(L)与资助方(F) |
| 1. 明确高风险国家的监管路径,为其提供非洲监管支持和注册协助——持续进行 | L:研发商、国家监管机构(NRAs)<br>F:流行病防范创新联盟(CEPI) |
| 2. 加强西非地区的监管能力,以实现疫苗的及时注册;通过FRPath仪表板衡量进展——持续进行 | L:世界卫生组织(WHO)、西非卫生组织(WAHO)、保罗·埃尔利希研究所(PEI)、国家监管机构(NRAs)、非洲疫苗监管论坛(AVAREF)、非洲药品管理局(AMA)<br>F:流行病防范创新联盟(CEPI)、欧洲和发展中国家临床 Trials合作组织3(EDCTP3) |
| 3. 明确高风险国家的风险效益评估结果以及早期获取疫苗的条件,例如通过区域研讨会/监管模拟演练等方式(2026年) | L:西非卫生组织(WAHO)、国家监管机构(NRAs)、卫生部(MoH)、研发商<br>F:流行病防范创新联盟(CEPI) |
| 4. 制定政策研究议程,明确支持政策决策所需的关键证据生成优先事项——2025年(已完成[15]) | L:西非卫生组织技术工作组(WAHO Technical Working Group)<br>F:流行病防范创新联盟(CEPI) |
| 5. 通过在线仪表板跟踪器,协调统一区域证据生成工作,并监测《政策研究议程》的进展——2026年(持续进行) | L:西非卫生组织(WAHO)<br>F:流行病防范创新联盟(CEPI) |
| 6. 根据研究议程生成证据(如流行病学、成本效益、疫苗实施等方面)——2026-2029年 | L:西非卫生组织(WAHO)、研发商<br>F:待定(TBD) |
| 7. 将拉沙热纳入免疫战略咨询专家组(SAGE)/区域免疫技术咨询小组(RITAGs)/国家免疫技术咨询小组(NITAGs)的优先事项清单,并组建工作组监测进展和优先事项(2026年及以后);定期发布政策简报,汇总现有证据 | L:世界卫生组织非洲区域办事处(WHO AFRO)、西非卫生组织(WAHO)、区域免疫技术咨询小组(RITAGs)、国家免疫技术咨询小组(NITAGs)、免疫战略咨询专家组(SAGE)<br>F:待定(TBD) |
| 8. 为西非以外地区制定拉沙热快速监管和政策机制 | L:世界卫生组织非洲区域办事处-非洲药品管理局(AFRO-AMA)<br>F:无特定标注 |
疫苗获批后,需明确以下问题:谁将最终负责拉沙热疫苗的采购和资助?该疫苗对有需求的国家而言是否可负担?在没有捐赠资金的情况下,疫苗商业化合作伙伴能否可持续地开展疫苗研发工作?日益紧张的财政状况使得寻找可预测的融资途径更具挑战性,因此需要由区域主导制定融资解决方案。
全球疫苗免疫联盟(Gavi)开展的初步实时评估证实了拉沙热的疾病负担以及对拉沙热疫苗的需求,但同时强调需要更多证据来评估是否适合由全球疫苗免疫联盟提供资金支持。此外,还需在2027-2028年底前确定投资类型(即仅用于疫情/储备,还是同时包括预防性使用场景),以便将其纳入相应的疫苗投资战略(VIS)长名单流程。根据目前的估计,包括尼日利亚在内的所有拉沙热流行国家都有资格获得全球疫苗免疫联盟的支持(前提是拉沙热疫苗获得疫苗投资战略批准),但各国处于不同的过渡阶段。由于全球疫苗免疫联盟各国的疫苗预算压力日益增大,且疫苗投资战略的实施路径存在不确定性,建议探索全球疫苗免疫联盟之外的国内和区域资金来源,以便为高风险国家尽早发出采购信号,并通过预先市场承诺降低生产投资风险。
若拉沙热疫苗需通过国家免疫预算提供资金,则需了解各国的支付意愿。据估计,非洲区域办事处(AFRO)地区非全球疫苗免疫联盟资助的疫苗价格区间在每剂0.11美元(卡介苗,BCG)至22.8美元(人乳头瘤病毒疫苗2价,HPV2)之间[19]。目前正在确定拉沙热疫苗的销售成本(COGS)估计值,但考虑到财政限制,捐赠资金很可能需要用于补贴成本,以确保疫苗的广泛接种和可负担性。因此,需要探索公共和私人融资机制,并尽早发出相关信号,以便制定恰当计划,确保疫苗的可及性、可负担性和可持续性。
利益相关者表示,需要建立一个区域可获取的拉沙热疫苗储备库,并制定透明、公平的分配规则、补充参数和跨境应急调配机制。
- 确定拉沙热疫苗获批后的资金来源,包括全球、区域和国内层面的公共和私人捐赠资金
- 明确拉沙热疫苗的可负担性和可持续性战略(尤其是在没有捐赠补贴的情况下),包括尽早发出采购信号
- 确定获批疫苗储备的公平分配机制
| 干预措施 | 牵头方(L)与资助方(F) |
| 1. 持续评估并阐明拉沙热疫苗的优先性,向潜在资助方和各国政府发出信号 | L:西非卫生组织(WAHO)、各国<br>F:无特定标注 |
| 2. 生成支持决策所需的证据(如成本效益、卫生经济影响[20]等)——2026-2029年 | L:西非卫生组织(WAHO)、研发商<br>F:待定(TBD) |
| 2a. 开展销售成本(COGS)和定价分析,结合资助方的支付意愿,确保疫苗的可负担性;(2026-2027年) | L:研发商、商业化合作伙伴/上市许可持有人(MAH)<br>F:待定(TBD) |
| 3. 开展全面疫苗价值评估(FVVA)或类似分析,整合证据并为融资决策提供支持(2030-2031年) | L:世界卫生组织免疫接种、疫苗和生物制品部门(WHO IVB)(待定)<br>F:待定(TBD) |
| 4. 确定拉沙热疫苗获批后的资金来源 | L:无特定标注<br>F:待定(TBD)(全球/区域或国内资金) |
| 5. 确定并实施合适的市场塑造机制(如预先签约/市场承诺、联合采购等),以确保疫苗的可负担性(2028-2030年) | L:无特定标注<br>F:待定(TBD) |
| 6. 制定获批疫苗储备的分配机制(2029-2030年) | L:无特定标注<br>F:无特定标注 |
归根结底,公平获取的实现取决于疫苗在各国的可接受性以及预期需求的兑现。西非地区目前正在开展大量工作,以了解疫苗犹豫问题。本路线图认识到,需要尽早为拉沙热疫苗投入资源开展社区参与和社会行为改变工作,同时认识到社区卫生工作者在提高疫苗需求和可及性方面发挥的重要作用。这些工作将有助于确保社区了解相关信息、积极参与,并为拉沙热疫苗的引进做好准备。各国利益相关者强调,需要持续开展社会倾听、参与式规划,并让民间社会组织、社区团体和地方领导人参与进来,以便尽早识别并解决影响疫苗接种的社会决定因素,例如信任度、错误信息、性别动态以及当地对风险的认知等。通过将沟通和社区体系制度化,西非地区不仅能确保拉沙热疫苗的成功引进,还能强化更广泛的流行病防范体系。
目前,对拉沙热的投资不仅集中在疫苗研发方面,还包括西非地区的整体能力建设工作(如临床、监管、生产、获取等领域)。这些投资有助于增强区域自主掌控能力、提高信任度,并使这些投资在该地区更具可持续性。应充分利用这些投资来应对该地区的其他疫情和疫苗研发工作,以便在出现情况时能够快速、公平地做出响应。对于未来的疫苗试验,建议在更多拉沙热流行国家开展临床试验能力建设,以增强国家自主掌控能力并为疫苗推广提供支持。此外,两种拉沙热疫苗平台都基于已应用于其他病原体的技术(重组水疱性口炎病毒平台用于埃博拉病毒、苏丹病毒和马尔堡病毒,ChAdOx平台用于尼帕病毒、中东呼吸综合征冠状病毒、新冠病毒和裂谷热病毒)。这不仅有可能加快疫苗的注册进程,还有助于提高拉沙热疫苗研发和交付的商业可持续性。
- 拉沙热疫苗同时作为预防性(常规活动)和应急性(疫情应对)策略实施*
- 制定国家级拉沙热实施计划,明确需求和资源配置,例如冷链、诊断、疫苗需求等方面
- 拉沙热疫苗在整个生态系统中具有可持续性
*注:需以相关证据为依据
| 干预措施 | 牵头方(L)与资助方(F) |
| 1. 开发区域拉沙热防范准备和获取仪表板,通过可衡量指标监测各国拉沙热疫苗的防范准备情况(2026年及以后) | L:西非卫生组织(WAHO)、各国<br>F:流行病防范创新联盟(CEPI) |
| 2. 开展风险沟通和社区参与(RCCE)以及社会行为改变(SBC)活动,尽早动员社区,提高对疫苗的信任度,为疫苗推广做好准备(2026年及以后) | L:西非卫生组织(WAHO)、各国<br>F:待定(TBD) |
| 3. 在西非及其他国家建立早期检测和监测能力,以发现拉沙热向西非以外地区传播的潜在情况(2026年及以后) | L:西非卫生组织(WAHO)及包括西非以外国家在内的各国<br>F:待定(TBD) |
| 4. 拉沙热流行国家制定初步的拉沙热成本核算实施计划和资源配置计划,包括冷链要求、物流、医护人员培训、社区动员和药物警戒等方面(2027年及以后) | L:西非卫生组织(WAHO)、各国<br>F:待定(TBD) |
| 5. 制定计划,确保整个生态系统的可持续性,同时平衡低产量和可负担性之间的关系(即确保各国获得可靠供应,确保疫苗采购方和捐赠方能够负担,确保疫苗生产商具有可持续性),并充分利用生产平台投资和其他创新成果 | L:各国、研发商、生产商<br>F:流行病防范创新联盟(CEPI)+资助方+研发商+生产商+各国 |
| 研发阶段 | 临床前 | 1期 | 2a期 |
| 研发机构 | 韩国SK生物科学公司 | 英国牛津大学 | 美国国际艾滋病疫苗倡议组织 |
| 研发阶段 | 临床前 | 1期 | 2期 |
| 平台技术 | 信使核糖核酸(mRNA) | 复制缺陷型腺病毒载体(ChAdOx1) | 重组水疱性口炎病毒载体(rVSV) |
| 抗原 | 糖蛋白C(乔赛亚株)+核蛋白和原型拉沙热抗原(X疾病) | 糖蛋白C(乔赛亚株) | 糖蛋白C(乔赛亚株) |
| 接种方案 | 待定(TBD) | 2剂(第1天/第56天) | 1剂 |
| 目标适应症 | 预防性和主动免疫 | 预防性和主动免疫 | 预防性和主动免疫 |
| 目标人群 | 待定(TBD) | 儿童、成人,孕妇除外 | 儿童、成人,孕妇除外 |
| 临床试验地点 | 待定(TBD) | 英国和加纳(计划中) | 美国、利比里亚(1期);尼日利亚、利比里亚、加纳(2期) |
| (预期)储存条件与剂型 | 待定(TBD) | 在2-8°C条件下可储存2年;液体剂型,有单剂量或多剂量包装 | 超低温冷藏(在-70°C条件下可储存2年);或冻干剂型在2-8°C条件下可储存2年 |
流行病防范创新联盟(CEPI)在每份疫苗研发资助协议中都纳入了具有合同约束力的公平获取义务,将其作为实现公平获取的重要手段。流行病防范创新联盟支持的每种疫苗候选产品都旨在应对特定问题、服务特定人群或适用于特定环境,因此每份资助协议都会根据具体情况量身定制,而非采用“一刀切”的模式。流行病防范创新联盟《公平获取病原体原型框架》阐述了联盟如何通过定制化干预措施,应对每种病原体带来的不同公平获取挑战。
疫苗研发资助协议中包含的一些基本要素(并非专门针对拉沙热疫苗候选产品)如下:
- 数据获取
- 储备承诺
- 可负担且可持续的定价
- 防范准备和应对义务,如扩大生产规模和技术转让
- 持续使用权
由于保密原因,无法列出与特定产品相关的条款,但核心产品组合中疫苗的摘要包含了更多细节和以往协议的示例。
2024年,流行病防范创新联盟(CEPI)和西非国家经济共同体疾病控制中心(ECOWAS CDC)在加纳联合举办了一场用例研讨会,参与人员包括拉沙热疫苗研发和实施相关的利益相关者。与会者代表了各类国家卫生组织,如西非卫生组织(WAHO)、塞拉利昂和几内亚卫生部、加纳国家疫苗研究所、塞内加尔国际医疗行动联盟(ALIMA)、尼日利亚国家食品药品监督管理局(NAFDAC)和国家初级卫生保健发展局(NPHCDA);区域组织,如世界卫生组织非洲区域办事处区域免疫技术咨询小组(WHO AFRO RITAG)、联合国儿童基金会加纳办事处(UNICEF Ghana)、世界卫生组织非洲区域办事处(WHO AFRO)、加纳帕斯适宜卫生科技组织(PATH Ghana);全球性组织,如世界卫生组织病毒性出血热部门(WHO VHF)和国际诊断产品融资机制(FIND);以及来自伦敦卫生与热带医学院、利比里亚大学、尼日利亚拉各斯大学病毒学实验室、伊鲁阿专科教学医院、几内亚贾迈勒·阿卜杜勒·纳赛尔大学的传染病专家和其他独立专家。
本次研讨会旨在确定拉沙热疫苗的潜在实施策略和使用场景,并评估产品特性优化需求及在流行国家成功实施拉沙热疫苗所需的其他条件。
与会者绝大多数认为,在流行国家开展地方性、针对性的常规免疫接种是最有可能采用的策略。其次是在疫情地区开展全民免疫接种(即无论年龄或风险群体,对所有人进行接种),然后是在流行国家开展全国性、针对性的常规免疫接种。
在流行地区附近(包括与流行地区接壤的入境口岸以及动物宿主栖息地附近)开展针对性免疫接种的排名最低。
根据这些意见和讨论,确定了四种可能的实施策略,如图5所示。与会者一致认为,需要更好地界定流行地区/社区,为未来的实施工作提供指导。确定青少年、成人和/或儿童是否为目标人群,需要更多关于疾病流行病学和疫苗保护期的信息。疫苗是否需要定期接种和/或在流行季节前接种,也取决于疫苗的保护期。
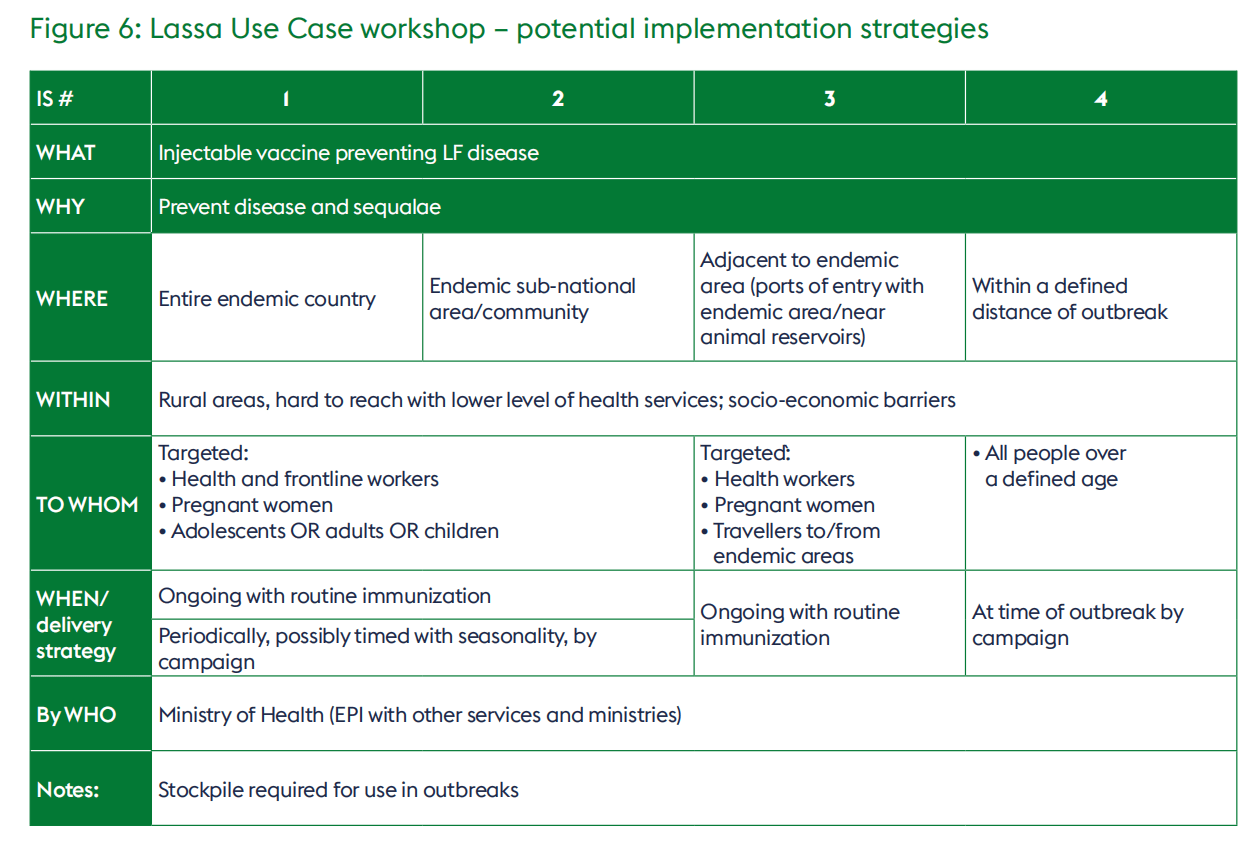 图6:拉沙热用例研讨会——潜在实施策略
图6:拉沙热用例研讨会——潜在实施策略
| 实施策略编号 | 1 | 2 | 3 | 4 |
| 疫苗类型 | 预防拉沙热的注射型疫苗 | – | – | – |
| 目的 | 预防疾病及其后遗症 | – | – | – |
| 实施地区 | 整个流行国家 | 流行地区/社区(地方性) | 流行地区附近(与流行地区接壤的入境口岸/动物宿主栖息地附近) | 疫情暴发点周边特定范围内 |
| 实施范围 | 农村地区、难以触及的地区,卫生服务水平较低;存在社会经济障碍 | – | – | – |
| 目标人群 | 针对性人群:<br>• 卫生工作者和一线工作者<br>• 孕妇<br>• 青少年或成人或儿童 | – | 针对性人群:<br>• 卫生工作者<br>• 孕妇<br>• 往返流行地区的旅行者 | • 特定年龄以上的所有人 |
| 实施时间/策略 | 通过常规免疫接种持续开展;<br>定期开展,可能结合流行季节安排活动 | – | 通过常规免疫接种持续开展 | 疫情暴发时通过活动开展 |
| 负责机构 | 卫生部(通过扩大免疫规划与其他部门和部委合作) | – | – | – |
| 备注 | 需要储备疫苗以应对疫情 | – | – | – |
与会者还受邀重新审视疫苗特性的工作假设,并讨论假设特性与使用场景之间是否存在不协调之处。讨论结果显示,需要考虑以下几点:
- 计划将适用年龄范围扩大到9个月及以上以及65岁以上人群,并将孕妇和有怀孕意愿的妇女纳入其中;
- 所描述的热稳定性特性无法支持若干预期的社区外展使用场景,应尽可能向其他扩大免疫规划(EPI)疫苗的热稳定性标准“看齐”;
- 疫苗应提供10剂以上包装规格,以便在疫情场景下使用;
- 疫苗能否与其他疫苗(尤其是针对青少年和儿童的疫苗以及该地区流行疾病的疫苗,特别是麻疹-风疹联合疫苗、黄热病疫苗、疟疾疫苗和人乳头瘤病毒疫苗)同时接种至关重要;
- 需要更多关于疫苗保护期的信息,以协助规划优先人群和交付策略。
- 会上还提到了研发针对拉沙热和其他未指明疾病的联合疫苗,以避免多次注射的想法。
随着有前景的疫苗候选产品有望在2030年前后投入使用,全球卫生界面临着一个有限的机遇窗口:若缺乏强有力的、特定背景下的研究为政策提供支持,疫苗部署工作可能会延迟或效果不佳。由流行病防范创新联盟(CEPI)资助、西非卫生组织(WAHO)牵头制定的一项研究议程,旨在指导并推动相关工作,及时生成相关且可操作的证据,为拉沙热疫苗引进和实施的政策制定与决策提供支持。该议程通过严格且包容的流程制定,采用了儿童健康与营养研究倡议(CHNRI)方法,在四个关键领域确定了13项优先研究问题:
- 疫苗接种率和接受度
- 流行病学认知
- 疫苗临床参数
- 经济影响
以下是每个领域内确定的优先研究问题:
 图7:政策研究议程的优先研究问题
图7:政策研究议程的优先研究问题
- 哪些沟通策略最能有效提高疫苗接受度和需求?
- 社区是否了解拉沙热及其后遗症?
- 不同年龄段人群对拉沙热预防性疫苗的接受度如何?
- 确定疫苗接种目标人群应考虑哪些适当因素?
- 是否存在特定合并症会增加患重症、出现后遗症和死亡的风险?
- 拉沙热再感染的风险因素(如有)是什么?
- 在高负担国家,拉沙热及其防控策略的经济影响是什么?
- 应急性和预防性疫苗接种策略的影响和成本效益如何?
- 实施拉沙热疫苗与其他预防性和治疗性干预措施相比,在健康和经济方面有哪些益处?
- 不同目标人群接种疫苗的风险与收益平衡情况如何?
- 疫苗在免疫功能低下或营养不良人群中的有效性如何?
- 该疫苗能否与常规儿童免疫接种中使用的其他疫苗或作为多抗原预防性活动的一部分同时接种?
- 该疫苗在不同年龄段人群中的有效性如何?
该研究议程由专门的政策研究工作组(PRWG)制定。该工作组由西非卫生组织(WAHO)作为拉沙热疫苗联盟的一部分召集成立,得到了流行病防范创新联盟(CEPI)和MMGH咨询公司的支持。政策研究工作组成员包括来自政府机构、区域卫生机构、学术界和免疫合作伙伴的代表,确保整个过程由区域主导并具有区域相关性。详细的方法学和更多信息可在此处获取。
[2] 来源:https://cepi.net/west-african-leaders-commit-advance-lassa-fever-vaccine-region
[3] 来源:https://www.nature.com/articles/s41467-022-33112-3
[4] 来源:流行病防范创新联盟拉沙热情况说明书
[6] 来源:《首位志愿者接种牛津大学突破性拉沙热疫苗》(First volunteer receives Lassa fever vaccine in cutting-edge Oxford trial)
[7] 来源:世界卫生组织拉沙热疫苗目标产品特性(WHO Lassa TPP)
[8] 来源:附件C中包含关于用例研讨会见解的更多详细信息
[9] 来源:https://www.wahooas.org/web-ooas/en/actualites/meeting-lassa-fever-coalition-governing-entity-lge
[10] 来源:《拉沙病毒流行地区未来几十年可能大幅扩大》(Lassa virus endemic area may expand dramatically in coming decades | Scripps Research)
[12] 来源:https://cepi.net/west-african-leaders-commit-advance-lassa-fever-vaccine-region
[13] 来源:https://www.who.int/publications/m/item/who-target-product-profile-for-lassa-virus-vaccine
[14] 来源:https://doi.org/10.1016/j.vaccine.2016.01.001
[16] 来源:https://storymaps.arcgis.com/stories/a87af9084b3242bb837e8602396d07fd
[17] 来源:https://www.ecowasregecsproject.com/about
[18] 来源:https://www.wahooas.org/web-ooas/en/node/2610
[19] 来源:获取市场信息(MI4A)疫苗采购数据库
[20] 来源:https://www.nature.com/articles/s41591-024-03232-y
ACCESS ROADMAP
Hits: 28
